















































































































































Komposition:
Anwendung:
Wird bei der Behandlung verwendet:
Medizinisch geprüft von Militian Inessa Mesropovna, Apotheke Zuletzt aktualisiert am 26.06.2023

Achtung! Die Informationen auf der Seite sind nur für medizinisches Fachpersonal! Die Informationen werden in öffentlichen Quellen gesammelt und können aussagekräftige Fehler enthalten! Seien Sie vorsichtig und überprüfen Sie alle Informationen auf dieser Seite!
Tabletten
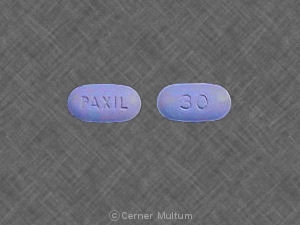
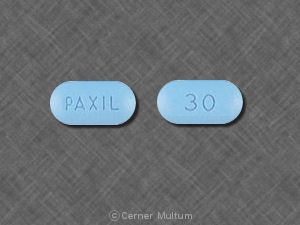
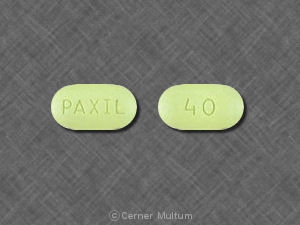
Filmtabletten, modifiziert-Ovale Tabletten wie folgt:
10 mg weiße Tabletten mit der Aufschrift TOPF 10 auf eine Seite. NDC 54766-201-01 Flaschen à 30
20 mg Dunkelorange Tabletten mit der Aufschrift POT 20 on einseitig. Die Tabletten sind auf beiden Seiten bewertet. NDC 54766-202-01 Flaschen à 30
30 mg gelbe Tabletten mit der Aufschrift TOPF 30 auf einem Seite. NDC 54766-203-01 Flaschen à 30
40 mg rosentabletten mit der Aufschrift POT 40 auf einer Seite. NDC 54766-204-01 Flaschen à 30
vor Feuchtigkeit Schützen. Shop bei 25°C (77°F); Ausflüge bis 15 erlaubt°-30°C (59° und 86°F) (siehe USP-Kontrollierten Raum Temperatur)
Vertrieben von Sebela Pharmaceuticals Inc. 645 Hembree Parkway, Suite I Roswell, Georgia 30076. www.sebelapharma.com. Gebührenfrei 1-844-732-3521. Überarbeiten: Jan 2017
Schwere Depressive Störung
PEXEVA® (paroxetinmesylat) ist für die Behandlung von MDD.
Die Wirksamkeit von Paroxetin bei der Behandlung eines major depressive episode wurde im 6-Wochen-kontrollierten Studien von ambulanten Patienten deren Diagnosen am ehesten der DSM-III-Kategorie der MDD entsprachen (siehe KLINISCHE PHARMAKOLOGIE). Eine große depressive episode impliziert eine Prominente und relativ anhaltende depressive oder dysphorische Stimmung, die normalerweise stört tägliche Funktion (fast jeden Tag für mindestens 2 Wochen); es sollte enthalten bei mindestens 4 der folgenden 8 Symptome: appetitveränderung, schlafveränderung, Psychomotorische Unruhe oder Verzögerung, Verlust des Interesses an üblichen Aktivitäten oder Abnahme des Sexualtriebs, erhöhte Müdigkeit, Schuldgefühle oder Wertlosigkeit, verlangsamtes denken oder Konzentrationsstörungen und ein Selbstmordversuch oder Selbstmordgedanken.
Die Auswirkungen von Paroxetin bei hospitalisierten depressiven Patienten wurden nicht ausreichend untersucht.
Die Wirksamkeit von Paroxetin bei der Aufrechterhaltung einer Reaktion in MDD für bis zu 1 Jahr wurde in einer placebokontrollierten Studie nachgewiesen (siehe KLINISCHE PHARMAKOLOGIE). Dennoch, der Arzt, der wählt zu verwenden PEXEVA® (paroxetinmesylat) für längere Zeit sollte in regelmäßigen Abständen bewerten Sie die langfristige Nützlichkeit des Arzneimittels für den einzelnen Patienten neu.
Zwangsstörung
PEXEVA® (paroxetinmesylat) ist für die Behandlung von Obsessionen und Zwängen bei Patienten mit OCD wie definiert in der DSM-IV. die Obsessionen oder Zwänge verursachen ausgeprägte not, sind zeitaufwendig, oder erheblich stören soziale oder berufliche funktionieren.
Die Wirksamkeit von Paroxetin wurde in zwei 12-wöchigen Studien mit zwanghaften ambulanten Patienten, deren Diagnosen am meisten entsprachen eng an die DSM-IIIR Kategorie von OCD (siehe ) Studien).
OCD zeichnet sich durch wiederkehrende und anhaltende Beschwerden aus, Gedanken, Impulse oder Bilder (Obsessionen), die egodystonisch und/oder repetitive, zielgerichtete und absichtliche Verhaltensweisen (Zwänge), die sind von der person als übermäßig oder unvernünftig anerkannt.
Langfristige Aufrechterhaltung der Wirksamkeit wurde in einem 6-monatige rückfallpräventionsstudie. In dieser Studie wurden Patienten zugewiesen Paroxetin zeigte eine niedrigere Rückfallrate im Vergleich zu Patienten unter placebo (siehe Klinische Studien). Dennoch, der Arzt wer wählt pexeva zu verwenden® (paroxetinmesylat) für längere Zeit sollte periodisch die langfristige Nützlichkeit des Medikaments für den einzelnen neu bewerten patient (siehe DOSIERUNG und VERABREICHUNG).
Panikstörung
PEXEVA® (paroxetinmesylat) ist für die Behandlung von PD, mit oder ohne Agoraphobie, wie in DSM-IV definiert. PD ist gekennzeichnet durch das auftreten von unerwarteten Panikattacken und damit verbundenen Sorge über zusätzliche Angriffe, Sorge über die Auswirkungen oder Folgen der Angriffe und / oder eine signifikante Verhaltensänderung im Zusammenhang mit Angriff.
Die Wirksamkeit von Paroxetin wurde in drei 10-bis 12-wöchige Studien an PD-Patienten, deren Diagnosen dem DSM-IIIR entsprachen Kategorie der PD (siehe Klinische Studien).
max.
Langfristige Aufrechterhaltung der Wirksamkeit wurde in einem 3-monatige rückfallpräventionsstudie. In dieser Studie wurden Patienten mit PD zugewiesen Paroxetin zeigte eine niedrigere Rückfallrate im Vergleich zu Patienten unter placebo (siehe Klinische Studien). Nichtsdestoweniger, die Arzt, der pexeva verschreibt® (paroxetinmesylat) für längere Zeit sollte regelmäßig die langfristige Nützlichkeit des Medikaments für die einzelnen Patienten.
Generalisierte Angststörung
Paroxetin ist zur Behandlung von Generalisierten Angststörung (Gad), wie in DSM-IV definiert. Angst oder Spannung assoziiert mit dem stress des Alltags erfordert in der Regel keine Behandlung mit einem anxiolytisch.
Die Wirksamkeit von Paroxetin bei der Behandlung von GAD war etabliert in zwei 8-wöchigen placebokontrollierten Studien bei Erwachsenen mit GAD. Paroxetin wurde nicht bei Kindern oder Jugendlichen mit Generalisierten Angststörung (siehe Klinische Studien).
Generalisierte Angststörung (DSM-IV) ist gekennzeichnet durch übermäßige Angst und Sorge (besorgniserregende Erwartung), die hartnäckig ist für mindestens 6 Monate und die die person schwer zu kontrollieren findet. Es muss sein assoziiert mit mindestens 3 der folgenden 6 Symptome: Unruhe oder Gefühl keyed up oder on edge, wobei leicht ermüdet, Konzentrationsschwierigkeiten oder Geist leer gehen, Reizbarkeit, Muskelverspannungen, Schlafstörungen.
Die Wirksamkeit von Paroxetin bei der Aufrechterhaltung einer Reaktion in Patienten mit Generalisierter Angststörung, die während einer 8-wöchigen akute Behandlungsphase während der Einnahme von Paroxetin und wurden dann beobachtet für Rückfall während eines Zeitraums von bis zu 24 Wochen, wurde in einem placebokontrollierte Studie (siehe Klinische Studien). Dennoch wählt der Arzt, der Paroxetin für längere Zeit verwendet sollte regelmäßig die langfristige Nützlichkeit des Medikaments für die einzelpatient (siehe DOSIERUNG und VERABREICHUNG).
Schwere Depressive Störung
Übliche Anfangsdosis
PEXEVA® (paroxetinmesylat) sollte als tägliche Einzeldosis mit oder ohne Nahrung, normalerweise morgens. Die empfohlene Anfangsdosis beträgt 20 mg / Tag. Die Patienten wurden in einem Bereich von 20 bis 50 mg/Tag dosiert in die klinischen Studien, die die Wirksamkeit von Paroxetin in der Behandlung von MDD. Wie bei allen Medikamenten, die bei der Behandlung von MDD wirksam sind, ist die volle Wirkung kann verzögert werden. Einige Patienten, die nicht auf eine 20-mg-Dosis ansprechen, können davon profitieren von dosiserhöhungen in Schritten von 10 mg/Tag bis zu maximal 50 mg/Tag. Dosisänderungen sollten in Abständen von mindestens 1 Woche auftreten.
Erhaltungstherapie
Es liegen keine Beweise für die Beantwortung der Frage, wie lange der mit Paroxetin behandelte patient darauf bleiben sollte. Es wird allgemein vereinbart, dass akute MDD-Episoden mehrere Monate benötigen oder länger anhaltende pharmakologische Therapie. Ob die Dosis benötigt, um zu induzieren die remission ist identisch mit der Dosis, die zur Aufrechterhaltung und/oder Aufrechterhaltung der euthymie erforderlich ist ist unbekannt.
Systematische Bewertung der Wirksamkeit von Paroxetin hat gezeigt, dass die Wirksamkeit für Zeiträume von bis zu 1 Jahr mit Dosen aufrechterhalten wird, die durchschnittlich etwa 30 mg.
Zwangsstörung
Übliche Anfangsdosis
PEXEVA® (paroxetinmesylat) sollte als tägliche Einzeldosis mit oder ohne Nahrung, normalerweise morgens. Die empfohlene die Dosis von Paroxetin bei der Behandlung von Zwangsstörungen beträgt 40 mg täglich. Patienten sollten sein begonnen mit 20 mg / Tag und die Dosis kann in Schritten von 10 mg/Tag erhöht werden. Dosisänderungen sollten in Abständen von mindestens 1 Woche auftreten. Patienten wurden dosiert in einem Bereich von 20 bis 60 mg/Tag in den klinischen Studien, die die Wirksamkeit von Paroxetin bei der Behandlung von OCD. Die maximale Dosierung sollte 60 mg/Tag nicht überschreiten.
Erhaltungstherapie
Langfristige Aufrechterhaltung der Wirksamkeit wurde in einem 6-monatige rückfallpräventionsstudie. In dieser Studie Patienten mit OCD zugewiesen Paroxetin zeigte eine niedrigere Rückfallrate im Vergleich zu Patienten unter placebo (siehe KLINISCHE PHARMAKOLOGIE). OCD ist eine chronische Erkrankung, und es ist vernünftig, eine Fortsetzung für einen ansprechenden Patienten in Betracht zu ziehen. Dosierung Anpassungen sollten vorgenommen werden, um den Patienten auf dem niedrigsten effektiv zu halten Dosierung und Patienten sollten regelmäßig neu bewertet werden, um den Bedarf zu bestimmen für die fortgesetzte Behandlung.
Panikstörung
Übliche Anfangsdosis
PEXEVA® (paroxetinmesylat) sollte als tägliche Einzeldosis mit oder ohne Nahrung, normalerweise morgens. Die zieldosis von Paroxetin bei der Behandlung von PD beträgt 40 mg / Tag. Patienten sollten begonnen werden auf 10 mg/Tag. Dosisänderungen sollten in Schritten von 10 mg/Tag und bei auftreten Abständen von mindestens 1 Woche. Die Patienten wurden in einem Bereich von 10 bis 60 mg/Tag dosiert in den klinischen Studien, die die Wirksamkeit von Paroxetin belegen. Der die maximale Dosierung sollte 60 mg/Tag nicht überschreiten.
Erhaltungstherapie
Langfristige Aufrechterhaltung der Wirksamkeit wurde in einem 3-monatige rückfallpräventionsstudie. In dieser Studie wurden Patienten mit PD zugewiesen Paroxetin zeigte eine niedrigere Rückfallrate im Vergleich zu Patienten unter placebo (siehe KLINISCHE PHARMAKOLOGIE). Morbus Parkinson ist eine chronische Erkrankung, und es ist vernünftig, eine Fortsetzung für einen ansprechenden Patienten in Betracht zu ziehen. Dosierung Anpassungen sollten vorgenommen werden, um den Patienten auf dem niedrigsten effektiv zu halten Dosierung und Patienten sollten regelmäßig neu bewertet werden, um den Bedarf zu bestimmen für die fortgesetzte Behandlung.
Generalisierte Angststörung
Übliche Anfangsdosis
PEXEVA® (paroxetinmesylat) sollte als tägliche Einzeldosis mit oder ohne Nahrung, normalerweise morgens. In der klinischen Studien die Wirksamkeit von Paroxetin wurde bei Patienten nachgewiesen, die in einem Bereich von 20 bis 50 mg/Tag. Die empfohlene Anfangsdosis und die etablierte effektive Dosierung beträgt 20 mg / Tag. Es gibt nicht genügend Beweise für eine größerer nutzen für Dosen höher als 20 mg / Tag. Dosisänderungen sollten in 10 auftreten mg / Tag in Schritten und in Intervallen von mindestens 1 Woche.
Erhaltungstherapie
Systematische Bewertung von fortgesetztem Paroxetin für Perioden von bis zu 24 Wochen bei Patienten mit GAD, die während der Einnahme angesprochen hatten Paroxetin während einer 8-wöchigen akuten Behandlungsphase hat einen Vorteil von gezeigt eine solche Wartung (siehe Klinische Studien). Dennoch sollten die Patienten regelmäßig neu bewertet werden, um den Bedarf festzustellen für wartungsbehandlung.
Besondere Populationen
Behandlung Schwangerer Frauen Im Dritten Trimester
Neugeborene, die Paroxetin und anderen SSRIs oder SNRIs ausgesetzt sind spät im Dritten trimester haben Komplikationen entwickelt, die verlängert werden müssen Krankenhausaufenthalt, Atemunterstützung und röhrenfütterung (siehe VORSICHTSMAßNAHMEN). Bei der Behandlung schwangerer Frauen mit Paroxetin während des Dritten Trimesters ist die Arzt sollte sorgfältig die potenziellen Risiken und Vorteile von Behandlung.
Dosierung für ältere Oder Geschwächte Und Patienten mit Schweren Nieren-Oder Leberfunktionsstörung
Die empfohlene Anfangsdosis beträgt 10 mg / Tag für ältere Menschen Patienten, geschwächte Patienten und / oder Patienten mit schweren Nieren-oder Lebererkrankungen Wertminderung. Erhöhungen können vorgenommen werden, wenn angegeben. Dosierung sollte 40 nicht überschreiten mg/Tag.
Umschalten eines Patienten Zu oder Von einer Monoaminoxidase Inhibitor (MAOI) Zur Behandlung Psychiatrischer Störungen
Zwischen dem absetzen von ein MAOI zur Behandlung psychiatrischer Störungen und Einleitung der Therapie mit PEXEVA®. Umgekehrt sollten nach dem absetzen von PEXEVA® mindestens 14 Tage erlaubt sein; vor Beginn eines MAOI zur Behandlung psychiatrischer Störungen (siehe GEGENANZEIGEN).
Verwendung von PEXEVA® Mit Anderen MAOIs, Wie Linezolid Oder Methylen Blau
Beginnen Sie nicht PEXEVA® bei einem Patienten, der behandelt wird mit linezolid oder intravenösem Methylenblau, da ein erhöhtes Risiko für serotonin-Syndrom. Bei einem Patienten, der eine dringendere Behandlung eines psychiatrischer Zustand, andere Interventionen, einschließlich Krankenhausaufenthalt, sollten berücksichtigt werden (siehe KONTRAINDIKATIONEN).
In einigen Fällen erhält ein patient bereits PEXEVA® die Therapie kann eine dringende Behandlung mit linezolid oder intravenösem Methylen erfordern blau. Wenn akzeptable alternativen zu linezolid oder intravenösem Methylenblau Behandlung sind nicht verfügbar und die potenziellen Vorteile von linezolid oder intravenöse methylenblaubehandlung wird als überwiegen der Risiken von serotonin-Syndrom BEI einem bestimmten Patienten, pexeva & reg; sollte sofort gestoppt werden, und linezolid oder intravenöses Methylenblau kann verabreicht werden. Patient sollte für 2 Wochen oder bis 24 auf Symptome des serotonin-Syndroms überwacht werden Stunden nach der letzten Dosis von linezolid oder intravenösem Methylenblau, je nachdem, welcher kommt zuerst. Die Therapie mit PEXEVA & reg; kann 24 Stunden nach der letzten Dosis wieder aufgenommen werden von linezolid oder intravenösem Methylenblau (siehe WARNHINWEISE).
Das Risiko der Verabreichung von Methylenblau durch nicht intravenöse Wege (wie orale Tabletten oder durch lokale Injektion) oder in intravenöse Dosen viel niedriger als 1 mg/kg mit PEXEVA®, ist unklar. Der Kliniker sollten sich dennoch der Möglichkeit eines emergenten bewusst sein Symptome des serotoninsyndroms bei einer solchen Anwendung (siehe WARNUNGEN).
Abbruch der Behandlung mit PEXEVA® (Paroxetin mesylate)
Symptome im Zusammenhang mit dem absetzen von Paroxetin wurden berichtet (siehe VORSICHTSMAßNAHMEN). Patienten sollten überwacht werden für diese Symptome bei absetzen der Behandlung, unabhängig von der Indikation für welches Paroxetin wird verschrieben? Eine allmähliche Verringerung der Dosis. als abrupte Beendigung wird empfohlen, Wann immer möglich. Wenn unerträgliche Symptome treten nach einer Abnahme der Dosis oder nach absetzen der Behandlung auf, dann kann die Wiederaufnahme der zuvor verschriebenen Dosis in Betracht gezogen werden. Anschließend, der Arzt kann die Dosis weiter verringern, jedoch schrittweise.
Die Verwendung von MAOIs zur Behandlung psychiatrischer Störungen mit PEXEVA® oder innerhalb von 14 Tagen nach Beendigung der Behandlung mit PEXEVA® ist kontraindiziert wegen eines erhöhten Risikos für serotoninsyndrom. Die Verwendung von PEXEVA® innerhalb 14 Tage nach dem absetzen eines MAOI zur Behandlung von psychiatrischen es ist auch kontraindiziert (siehe WARNUNGEN und DOSIERUNG UND ADMINISTRATION).
Ab PEXEVA® bei einem Patienten, der behandelt wird, mit MAOIs wie linezolid oder intravenöses Methylenblau sind ebenfalls kontraindiziert wegen eines erhöhten Risikos für serotoninsyndrom (siehe WARNUNGEN und DOSIERUNG Und VERWALTUNG).
Gleichzeitige Anwendung bei Patienten, die Thioridazin einnehmen, ist kontraindiziert (siehe WARNHINWEISE und VORSICHTSMAßNAHMEN).
Gleichzeitige Anwendung bei Patienten, die pimozid einnehmen, ist kontraindiziert (siehe VORSICHTSMAßNAHMEN).
Pexeva® (paroxetinmesylat) Tabletten sind kontraindiziert bei Patienten mit einer überempfindlichkeit gegen Paroxetin oder eine der inaktiven Zutaten in PEXEVA® (paroxetinmesylat) Tabletten.
WARNHINWEISE
Klinische Verschlechterung Und Suizidrisiko
Patienten mit schwerer depressiver Störung (MDD), beide Erwachsene und pädiatrisch, kann eine Verschlechterung Ihrer depression und/oder der Entstehung von Suizidgedanken und-Verhalten (Suizidalität) oder ungewöhnliche Veränderungen in Verhalten, ob Sie Antidepressiva einnehmen oder nicht, und dies das Risiko kann bestehen bleiben, bis eine signifikante remission Auftritt. Selbstmord ist ein bekanntes Risiko von depression und bestimmte andere psychiatrische Störungen und diese Störungen Sie selbst sind die stärksten Prädiktoren für Selbstmord. Es gab eine langjährige Bedenken jedoch, dass Antidepressiva eine Rolle bei der depression und die Entstehung von Suizidalität bei bestimmten Patienten während der frühe Phasen der Behandlung. Gepoolte Analysen von kurzfristigen placebokontrollierten Studien mit Antidepressiva (SSRIs und anderen) zeigten, dass diese Medikamente erhöhen Sie das Risiko von Selbstmordgedanken und-Verhalten (Suizidalität) bei Kindern, Jugendliche und junge Erwachsene (Alter 18-24) mit schwerer depressiver Störung (MDD) und andere psychiatrische Störungen. Kurzzeitstudien zeigten keinen Anstieg der das suizidalitätsrisiko bei Antidepressiva im Vergleich zu placebo bei Erwachsenen Alter 24; es gab eine Reduktion mit Antidepressiva im Vergleich zu placebo bei Erwachsenen ab 65 Jahren.
Die gepoolten Analysen von placebokontrollierten Studien in Kinder und Jugendliche mit MDD, Zwangsstörung (OCD) oder andere psychiatrische Störungen umfassten insgesamt 24 Kurzzeitstudien mit 9 Antidepressiva bei über 4400 Patienten. Die gepoolten Analysen von placebokontrollierte Studien bei Erwachsenen mit MDD oder anderen psychiatrischen Störungen umfasste insgesamt 295 kurzzeitversuche (mittlere Dauer von 2 Monaten) von 11 Antidepressiva bei über 77000 Patienten. Es gab erhebliche Unterschiede in Risiko der Suizidalität unter Drogen, aber eine Tendenz zu einer Zunahme der jüngere Patienten für fast alle untersuchten Medikamente. Es gab Unterschiede in der absolutes Suizidrisiko über die verschiedenen Indikationen hinweg mit dem höchsten Inzidenz bei MDD. Die risikounterschiede (Medikament gegen placebo) waren jedoch relativ stabil innerhalb der Altersschichten und über Indikationen hinweg. Diese risikounterschiede (drug-placebo Unterschied in der Anzahl der Fälle von Suizidalität pro 1000 behandelte Patienten) sind in Tabelle 1 aufgeführt.
TABELLE 1
Keine Selbstmorde in einem der Pädiatrische Studien. Es gab Selbstmorde in den erwachsenenversuchen, aber die Zahl war nicht ausreichend, um eine Schlussfolgerung über die Wirkung von Drogen auf Selbstmord zu ziehen.
Es ist nicht bekannt, ob die das suizidalitätsrisiko erstreckt sich auf eine längerfristige Anwendung, dh über mehrere Monate hinaus. Jedoch, es gibt erhebliche Beweise aus placebokontrollierten erhaltungsstudien in Erwachsene mit Depressionen, dass die Verwendung von Antidepressiva das Wiederauftreten verzögern kann von Depressionen.
alle behandelten Patienten mit Antidepressiva für jede Indikation sollte angemessen überwacht werden und eng beobachtet für klinische Verschlechterung, Suizidalität und ungewöhnliche Veränderungen in Verhalten, insbesondere in den ersten Monaten einer medikamentösen Therapie, oder zu Zeiten von dosisänderungen, entweder erhöht oder verringert.
Die folgenden Symptome, Angst, Unruhe, Panik Angriffe, Schlaflosigkeit, Reizbarkeit, Feindseligkeit, Aggressivität, Impulsivität, Akathisie (Psychomotorische Unruhe), Hypomanie und Manie wurden berichtet bei Erwachsenen und pädiatrischen Patienten, die mit Antidepressiva für major behandelt werden depressive Störung sowie für andere Indikationen, sowohl psychiatrische und nonpsychiatric. Obwohl ein ursächlicher Zusammenhang zwischen der Entstehung solcher Symptome und entweder die Verschlechterung der depression und/oder die Entstehung von suizidalen Impulse wurde nicht festgestellt, gibt es Bedenken, dass solche Symptome können stellen Vorläufer für aufkommende Suizidalität dar.
Es sollte überlegt werden, das therapeutische zu ändern Regime, einschließlich möglicherweise absetzen der Medikamente, bei Patienten, deren depression ist hartnäckig schlimmer, oder wer erlebt emergente Suizidalität oder Symptome, die Vorläufer für eine Verschlechterung der depression oder Suizidalität sein könnten, besonders wenn diese Symptome schwerwiegend sind, abrupt auftreten oder nicht Teil von der patient zeigt Symptome.
Wenn die Entscheidung getroffen wurde, die Behandlung abzubrechen, Medikamente sollten so schnell wie möglich eingenommen werden, aber mit Anerkennung dieses abrupte absetzen kann mit bestimmten Symptomen verbunden sein (siehe VORSICHTSMAßNAHMEN und DOSIERUNG und VERABREICHUNG - Absetzen von Behandlung mit PEXEVA® (paroxetinmesylat), für eine Beschreibung der Risiken von absetzen von PEXEVA® (paroxetinmesylat)).
Familien und Betreuer von Patienten, die mit Antidepressiva für schwere depressive Störungen oder andere Indikationen, beide psychiatrische und nichtpsychiatrische, sollte über die Notwendigkeit zu überwachen alarmiert werden Patienten für die Entstehung von Unruhe, Reizbarkeit, ungewöhnliche Veränderungen in Verhalten, und die anderen oben beschriebenen Symptome, sowie die Entstehung von Suizidalität und solche Symptome sofort an Gesundheitsdienstleister zu melden. Eine solche überwachung sollte die tägliche Beobachtung durch Familien und Betreuer umfassen. Rezept für PEXEVA® (paroxetinmesylat) sollte für die kleinste Menge geschrieben werden von Tabletten im Einklang mit einem guten Patientenmanagement, um das Risiko zu reduzieren von überdosierung.
Screening von Patienten Auf Bipolare Störung
Eine große depressive episode kann die Initiale sein Präsentation der bipolaren Störung. Es wird allgemein angenommen (wenn auch nicht in kontrollierten Studien festgestellt), dass die Behandlung einer solchen episode mit einem Antidepressivum allein kann die Wahrscheinlichkeit einer Ausfällung eines gemischte / manische episode bei Patienten mit einem Risiko für eine bipolare Störung. Ob einer von die oben beschriebenen Symptome stellen eine solche Umwandlung dar, die unbekannt ist. Jedoch, vor Beginn der Behandlung mit einem Antidepressivum, Patienten mit depressiven Symptome sollten angemessen gescreent werden, um festzustellen, ob Sie gefährdet sind für bipolare Störung; ein solches screening sollte eine detaillierte psychiatrische Anamnese enthalten, einschließlich einer Familiengeschichte von Selbstmord, bipolarer Störung und depression. Es ist zu beachten, dass PEXEVA® (paroxetinmesylat) ist nicht für die Verwendung in Behandlung der bipolaren depression.
Serotonin Syndrom
Die Entwicklung eines potenziell lebensbedrohlichen serotonin-Syndrom wurde mit SNRIs und SSRIs berichtet, einschließlich PEXEVA®, allein, aber besonders bei gleichzeitiger Anwendung anderer serotonergika (einschließlich Triptane, trizyklische Antidepressiva, fentanyl, lithium, tramadol, tryptophan, Buspiron, Amphetamine und Johanniskraut) und mit Drogen, die Beeinträchtigung des Metabolismus von serotonin (insbesondere MAOIs, die beide dazu bestimmt sind, behandeln Sie psychiatrische Störungen und auch andere, wie linezolid und intravenös Methylenblau).
Serotonin-Syndrom Symptome können psychischen status umfassen Veränderungen (Z. B. Erregung, Halluzinationen, delirium und Koma), autonom Instabilität (Z. B. Tachykardie, labiler Blutdruck, Schwindel, Diaphorese, Spülung, Hyperthermie), neuromuskuläre Symptome (Z. B. tremor, Steifigkeit, Myoklonus, Hyperreflexie, Koordinationsstörungen), Krampfanfälle und / oder Magen-Darm-Erkrankungen Symptome (Z. B. übelkeit, Erbrechen, Durchfall). Patienten sollten überwacht werden für die Entstehung des serotonin-Syndroms.
Die gleichzeitige Verwendung von PEXEVA® mit MAOIs soll Behandlung psychiatrischer Störungen ist kontraindiziert. PEXEVA® sollte auch nicht sein begonnen bei einem Patienten, der mit MAOIs wie linezolid behandelt wird oder intravenöses Methylenblau. Alle Berichte mit Methylenblau die zur Verfügung gestellt Informationen über den verabreichungsweg und die intravenöse Verabreichung im Dosisbereich von 1 mg/kg bis 8 mg/kg. Keine Berichte bei der Verwaltung Methylenblau auf anderen wegen (Z. B. orale Tabletten oder lokale gewebeinjektion) oder bei niedrigeren Dosen. Es kann Umstände geben, wenn es notwendig ist, zu initiieren Behandlung mit einem MAOI wie linezolid oder intravenösem Methylenblau in einem patient unter PEXEVA®. PEXEVA® sollte vor der Einleitung abgebrochen werden Behandlung mit dem MAOI (siehe KONTRAINDIKATIONEN und DOSIERUNG UND VERWALTUNG).
Bei gleichzeitiger Anwendung von PEXEVA® mit anderen serotonergen Medikamente einschließlich Triptane, trizyklische Antidepressiva, fentanyl, lithium, tramadol, Buspiron, tryptophan, Amphetamine und Johanniskraut ist klinisch ein potenziell erhöhtes Risiko für das serotonin-Syndrom, besonders während der behandlungseinleitung und dosiserhöhungen.
Behandlung mit PEXEVA® und jede begleitende serotonergic Agenten sollten sofort abgebrochen werden, wenn die oben genannten Ereignisse auftreten und unterstützende symptomatische Behandlung sollte eingeleitet werden.
Winkelverschlussglaukom
Die pupillendilatation, die nach der Verwendung von vielen Auftritt Antidepressiva, einschließlich Pexeva, können bei einem patient mit anatomisch schmalen Winkeln, der keine patent-iridektomie hat.
Mögliche Wechselwirkung mit Thioridazin
Thioridazin Verabreichung allein produziert Verlängerung des QTc-Intervalls, die mit schweren ventrikulären verbunden ist Arrhythmien wie Arrhythmien vom Typ torsade de pointes und plötzlicher Tod. Dieser Effekt scheint dosisabhängig zu sein.
eine in vivo Studie legt nahe, dass Medikamente, die hemmen CYP2D6, wie Paroxetin, erhöht die Plasmaspiegel von Thioridazin. Daher wird empfohlen, Paroxetin nicht in Kombination mit Thioridazin (siehe KONTRAINDIKATIONEN und VORSICHTSMAßNAHMEN).
Verwendung In der Schwangerschaft
Teratogene Wirkungen
Epidemiologische Studien haben gezeigt, dass Säuglinge ausgesetzt zu Paroxetin im ersten Trimester der Schwangerschaft haben ein erhöhtes Risiko von angeborene Fehlbildungen, insbesondere kardiovaskuläre Fehlbildungen. Der die Ergebnisse dieser Studien sind nachfolgend zusammengefasst:
- eine Studie, die auf schwedischen nationalen registerdaten basiert gezeigt, dass Säuglinge, die während der Schwangerschaft Paroxetin ausgesetzt waren (n = 815), hatten ein erhöhtes Risiko für kardiovaskuläre Fehlbildungen (2% Risiko in Paroxetin-exponierte Säuglinge) im Vergleich zur gesamten registrierungspopulation (1% Risiko), für ein odds ratio (ODER) von 1.8 (95% Konfidenzintervall 1.1 bis 2.8). Nein ein Anstieg des Risikos für angeborene Fehlbildungen insgesamt wurde in der Paroxetin-exponierte Säuglinge. Die herzfehlbildungen im Paroxetin-exponierten Säuglinge waren in Erster Linie ventrikuläre septumdefekte (VSDs) und vorhofseptumdefekte Mängel (ASDs). Septumdefekte liegen im Schweregrad von denen, die sich auflösen spontan zu denen, die operiert werden müssen.
- Einer separaten retrospektiven Kohortenstudie aus den Vereinigten USA (United Healthcare data) ausgewertet 5.956 Säuglinge von Müttern verzichtet Antidepressiva während des ersten Trimesters (n = 815 für Paroxetin). Diese Studie zeigte einen trend zu einem erhöhten Risiko für kardiovaskuläre Fehlbildungen für Paroxetin (Risiko von 1.5%) im Vergleich zu anderen Antidepressiva (Risiko von 1%), für ein ODER von 1.5 (95% Konfidenzintervall 0.8 zu 2.9). Von den 12 Paroxetin-exponierten Säuglinge mit kardiovaskulären Missbildungen, 9 hatten VSDs. Diese Studie auch deutete auf ein erhöhtes Risiko für insgesamt schwerwiegende angeborene Fehlbildungen hin, einschließlich Herz-Kreislauf-defekte bei Paroxetin (4% Risiko) im Vergleich zu anderen (2% Risiko) Antidepressiva (ODER 1.8; 95% Konfidenzintervall 1.2 bis 2.8).
- Zwei große Fall-Kontroll-Studien mit separaten Datenbanken, jeder mit > 9,000 Geburtsfehler Fällen und > 4.000 Kontrollen, gefunden, dass mütterliche Anwendung von Paroxetin während des ersten Trimesters der Schwangerschaft war verbunden mit einem 2-bis 3-Fach erhöhten Risiko eines rechtsventrikulären Abflusses. Behinderung. In einer Studie war das OR 2.5 (95% Konfidenzintervall, 1.0 bis 6.0, 7 exponierten Säuglingen) und in der anderen Studie war der OR 3.3 (95% - Konfidenzintervall Intervall, 1.3 bis 8.8, 6 exponierte Säuglinge).
- Andere Studien haben unterschiedliche Ergebnisse darüber gefunden, ob es wurde ein erhöhtes Risiko für Gesamt -, Herz-Kreislauf-oder bestimmten angeborenen Missbildung. Eine Metaanalyse epidemiologischer Daten über einen Zeitraum von 16 Jahren (1992 bis 2008) umfasste insgesamt 20 verschiedene Studien: 11 Studien (einschließlich die oben genannten Studien) berichteten über Schätzungen sowohl für kardiovaskuläre defekte als auch insgesamt angeborene Fehlbildungen, 3 Studien berichteten Schätzungen nur für Herz-Kreislauf-defekte und 6 Studien berichteten Schätzungen nur für insgesamt angeborene Fehlbildungen. Diese Metaanalyse unterliegt zwar Einschränkungen deutete auf ein erhöhtes auftreten kardiovaskulärer Fehlbildungen hin (Prävalenz odds ratio [POR] 1.5; 95% Konfidenzintervall 1.2 zu 1.9) und insgesamt Fehlbildungen (POR 1.2; 95% Konfidenzintervall 1.1 zu 1.4) mit Paroxetin verwenden während des ersten Trimesters. Es war in dieser Metaanalyse nicht möglich, bestimmen Sie, inwieweit kardiovaskuläre Fehlbildungen auftreten können trug zu gesamtfehlbildungen bei, noch war es möglich festzustellen, ob alle spezifischen Arten von kardiovaskulären Fehlbildungen trugen zu allen bei kardiovaskuläre Fehlbildungen.
- Wenn eine Patientin während der Einnahme von Paroxetin Schwanger wird, Sie sollte über den möglichen Schaden für den Fötus informiert werden. Es sei denn, die Vorteile von Paroxetin an die Mutter rechtfertigen die Fortsetzung der Behandlung, sollte entweder absetzen der Paroxetin-Therapie oder Umschalten auf eine andere gegeben werden Antidepressivum (siehe VORSICHTSMAßNAHMEN - Abbruch der Behandlung Mit PEXEVA®). Für Frauen, die Schwanger werden wollen oder in Ihrem ersten trimester der Schwangerschaft sollte Paroxetin nur nach Rücksichtnahme eingeleitet werden von den anderen verfügbaren Behandlungsmöglichkeiten.
Tierische Befunde
Reproduktionsstudien wurden in Dosen bis zu 50 durchgeführt mg / kg / Tag bei Ratten und 6 mg/kg/Tag bei Kaninchen, die während der Organogenese verabreicht werden. Diese Dosen sind ungefähr 8 (Ratte) und 2 (Kaninchen) mal die MRHD auf einem mg / m & sup2; Grundlage. Diese Studien haben keine Hinweise auf teratogene Wirkungen ergeben. Jedoch, bei Ratten gab es einen Anstieg der pup-Todesfälle während der ersten 4 Tage von Laktation bei der Dosierung trat während des letzten Trimesters der Schwangerschaft und Fortsetzung während der gesamten Laktation. Dieser Effekt trat bei einer Dosis von 1 mg/kg/Tag oder ungefähr ein Sechstel der MRHD auf mg / m² - basis. Die Dosis ohne Wirkung für Ratte pup Mortalität wurde nicht bestimmt. Die Ursache dieser Todesfälle ist nicht bekannt.
Nichtteratogene Wirkungen
Neugeborene, die PEXEVA® und anderen SSRIs oder serotonin ausgesetzt sind und Norepinephrin-Wiederaufnahmehemmer (SNRIs), spät im Dritten trimester haben Komplikationen entwickelt, die einen längeren Krankenhausaufenthalt erfordern, respiratorisch Unterstützung und sondennahrung. Solche Komplikationen können sofort nach auftreten Lieferung. Gemeldete klinische Befunde haben Atemnot enthalten, Zyanose, Apnoe, Krampfanfälle, temperaturinstabilität, fütterungsschwierigkeiten, Erbrechen, Hypoglykämie, Hypotonie, Hypertonie, Hyperreflexie, tremor, Nervosität, Reizbarkeit und ständiges Weinen. Diese Funktionen sind konsistent entweder mit einer direkten toxischen Wirkung von SSRIs und SNRIs oder möglicherweise einem Medikament Abbruch-Syndrom. Es sollte beachtet werden, dass in einigen Fällen die klinische das Bild stimmt mit dem serotonin-Syndrom überein (siehe WARNUNGEN: Serotonin Syndrom).
Säuglinge, die in der Schwangerschaft SSRIs ausgesetzt sind, können eine erhöhtes Risiko für anhaltende pulmonale Hypertonie des Neugeborenen (PPHN). PPHN tritt bei 1 - 2 pro 1.000 Lebendgeburten in der Allgemeinbevölkerung auf und ist assoziiert mit erheblicher neugeborenenmorbidität und Mortalität. Mehrere aktuelle epidemiologische Studien legen einen positiven statistischen Zusammenhang zwischen SSRI nahe Verwendung (einschließlich PEXEVA®) in der Schwangerschaft und PPHN. Andere Studien zeigen keine signifikante statistische Assoziation.
Ärzte sollten auch die Ergebnisse einer prospektiven Längsschnittstudie von 201 schwangeren Frauen mit einer Geschichte von schweren Depressionen, die entweder Antidepressiva Einnahmen oder Antidepressiva von weniger als 12 erhalten hatten Wochen vor Ihrer letzten Regelblutung und waren in remission. Frauen, die abgesetzte Antidepressiva während der Schwangerschaft zeigten eine signifikante Zunahme des Rückfalls Ihrer schweren depression im Vergleich zu jenen Frauen, die blieb während der Schwangerschaft auf Antidepressiva.
Bei der Behandlung einer schwangeren Frau mit PEXEVA®, die Arzt sollte sorgfältig prüfen, sowohl die potenziellen Risiken der Einnahme eines SSRI, zusammen mit den etablierten Vorteilen der Behandlung von Depressionen mit einem Antidepressivum. Diese Entscheidung kann nur von Fall zu Fall getroffen werden (siehe DOSIERUNG Und VERABREICHUNG und NEBENWIRKUNGEN, Postmarketing-Berichte).
VORSICHTSMAßNAHMEN
allgemein
Aktivierung von Manie / Hypomanie
Während des premarketing-Tests traten Hypomanie oder Manie auf bei etwa 1,0% der mit Paroxetin behandelten unipolaren Patienten im Vergleich zu 1,1% der aktiven Kontrolle und 0,3% der placebo-behandelten unipolaren Patienten. In einer Teilmenge von Patienten klassifiziert als bipolar, die rate der manischen Episoden Betrug 2,2% für Paroxetin und 11,6% für die kombinierten aktiven Kontrollgruppen. Wie bei allen Drogen wirksam bei der Behandlung von MDD sollte Paroxetin vorsichtig angewendet werden in Patienten mit einer Geschichte von Manie.
Anfälle
Während der premarketing-Tests traten bei 0,1% der Paroxetin-behandelte Patienten, eine ähnliche rate wie bei anderen Medikamenten wirksam bei der Behandlung von MDD. Paroxetin sollte vorsichtig angewendet werden in Patienten mit Anfällen in der Vorgeschichte. Es sollte bei jedem Patienten abgesetzt werden wer entwickelt Anfälle.
Abbruch der Behandlung mit PEXEVA® (Paroxetin mesylate)
Aktuelle klinische Studien zur Unterstützung der verschiedenen zugelassenen Indikationen für Paroxetin sind ein taper-phase-Regime, anstatt ein abruptes absetzen der Behandlung. Das in GAD verwendete taper-phase-Regime und Klinische PTSD-Studien beinhalteten eine inkrementelle Abnahme der Tagesdosis um 10 mg/Tag in wöchentlichen Abständen. Wenn eine tägliche Dosis von 20 mg/Tag erreicht wurde, die Patienten wurden 1 Woche lang mit dieser Dosis fortgesetzt, bevor die Behandlung abgebrochen wurde.
Mit diesem Regime in diesen Studien die folgenden unerwünschten Ereignisse wurden bei einer Inzidenz von 2% oder mehr für Paroxetin bei einem Inzidenz mindestens doppelt so hoch wie bei placebo: abnormale Träume, Parästhesien und Schwindel. Bei den meisten Patienten waren diese Ereignisse mild zu moderieren und waren selbstlimitierend und erforderten keinen medizinischen Eingriff.
Während der Vermarktung von Paroxetin und anderen SSRIs und SNRIs (serotonin-und Norepinephrin-Wiederaufnahmehemmer), es gab spontane Berichte über unerwünschte Ereignisse, die beim absetzen dieser Arzneimittel auftreten (besonders wenn abrupt), einschließlich der folgenden: dysphorische Stimmung, Reizbarkeit, Erregung, Schwindel, sensorische Störungen (zB Parästhesien) als elektrische Schock Empfindungen und tinnitus), Angst, Verwirrung, Kopfschmerzen, Lethargie, emotionale Labilität, Schlaflosigkeit und Hypomanie. Während diese Ereignisse sind im Allgemeinen selbstlimitierend, es gab Berichte über ein ernstes absetzen Problembeschreibung.
Patienten sollten auf diese Symptome überwacht werden, wenn Abbruch der Behandlung mit Paroxetin. Eine allmähliche Verringerung der Dosis, anstatt abrupte Beendigung, wird empfohlen, Wann immer möglich. Wenn unerträglich Symptome treten nach einer Abnahme der Dosis oder nach absetzen von die Behandlung und dann die Wiederaufnahme der zuvor verschriebenen Dosis können in Betracht gezogen werden. Anschließend kann der Arzt die Dosis weiter verringern, jedoch zu einem späteren Zeitpunkt schrittweise rate (siehe DOSIERUNG und VERABREICHUNG).
Siehe auch VORSICHTSMAßNAHMEN - Pädiatrische Anwendung für unerwünschte Ereignisse, die nach absetzen der Behandlung mit Paroxetin in der pädiatrischen Patienten.
Tamoxifen
Einige Studien haben gezeigt, dass die Wirksamkeit von tamoxifen, wie durch das Risiko von Brustkrebs Rückfall/Mortalität gemessen, kann reduziert werden, wenn co-verschrieben mit Paroxetin als Folge der irreversiblen Paroxetin Hemmung von CYP2D6 (siehe ARZNEIMITTELWECHSELWIRKUNGEN). Andere Studien haben ein solches Risiko nicht nachgewiesen. Es ist ungewiss, ob die die gleichzeitige Verabreichung von Paroxetin und tamoxifen hat eine signifikante nachteilige Wirkung zur Wirksamkeit von tamoxifen. Wenn tamoxifen zur Behandlung verwendet wird oder Prävention von Brustkrebs, sollten verschreibende ärzte eine alternative in Betracht ziehen Antidepressivum mit wenig oder keiner CYP2D6-Hemmung.
Akathisia
Die Verwendung von Paroxetin oder anderen SSRIs wurde assoziiert mit der Entwicklung der Akathisie, die sich durch einen inneren Sinn für Unruhe und Psychomotorische Unruhe wie Unfähigkeit zu sitzen oder zu stehen immer noch in der Regel mit subjektiver Belastung verbunden. Dies ist am wahrscheinlichsten innerhalb der ersten Wochen der Behandlung.
Hyponatriämie
Hyponatriämie kann als Folge der Behandlung mit SSRIs und SNRIs, einschließlich PEXEVA® (paroxetinmesylat). In vielen Fällen ist dies Hyponatriämie scheint das Ergebnis des Syndroms der unangemessenen zu sein antidiuretische Hormonsekretion (SIADH). Fälle mit serumnatrium unter 110 mmol / L wurden berichtet. Ältere Patienten haben möglicherweise ein höheres Risiko für Entwicklung von Hyponatriämie mit SSRIs und SNRIs. Auch Patienten, die Diuretika einnehmen oder wer sonst Volumen erschöpft ist, kann einem höheren Risiko ausgesetzt sein (siehe Geriatrie Verwenden). Absetzen von PEXEVA® (paroxetinmesylat) sollte in Betracht gezogen werden bei Patienten mit symptomatischer Hyponatriämie und entsprechender medizinischer intervention sollte eingeleitet werden.
Anzeichen und Symptome einer Hyponatriämie sind Kopfschmerzen, Konzentrationsschwierigkeiten, Gedächtnisstörungen, Verwirrung, Schwäche und Unruhe, die zu stürzen führen kann. Anzeichen und Symptome im Zusammenhang mit mehr schwere und / oder akute Fälle umfassen Halluzination, Synkope, Krampfanfälle, Koma, Atemstillstand und Tod.
Abnormale Blutung
SSRIs und SNRIs, einschließlich PEXEVA® (paroxetinmesylat), kann das Risiko von blutungsereignissen erhöhen. Die gleichzeitige Anwendung von aspirin, nichtsteroidale entzündungshemmende Medikamente, warfarin und andere gerinnungshemmende Mittel können fügen Sie zu diesem Risiko hinzu. Fallberichte und epidemiologische Studien (fallkontrolle und kohortendesign) haben einen Zusammenhang zwischen Drogenkonsum und stören Sie die serotonin-Wiederaufnahme und das auftreten von Magen-Darm-Erkrankungen Blutung. Blutungsereignisse im Zusammenhang mit SSRIs und SNRIs Verwendung reichten von ekchymosen, Hämatome, epistaxis und Petechien lebensbedrohlich Blutung.
Patienten sollten vor dem Blutungsrisiko gewarnt werden im Zusammenhang mit der gleichzeitigen Anwendung von PEXEVA® (paroxetine mesylate) und NSAIDs, aspirin oder andere Medikamente, die die Gerinnung beeinflussen.
Knochenbruch
Epidemiologische Studien zum knochenbruchrisiko nach Exposition gegenüber einigen Antidepressiva, einschließlich SSRIs, haben einen Zusammenhang gemeldet zwischen antidepressiver Behandlung und Frakturen. Es sind mehrere möglich Ursachen für diese Beobachtung und es ist nicht bekannt, inwieweit das Frakturrisiko ist direkt auf SSRI-Behandlung zurückzuführen. Die Möglichkeit eines pathologischen Fraktur, dh eine Fraktur, die durch ein minimales trauma bei einem Patienten mit verminderte Knochenmineraldichte, sollte bei Patienten in Betracht gezogen werden, die mit Paroxetin, das mit ungeklärten Knochenschmerzen, punktspannen, Schwellungen Auftritt, oder Blutergüsse.
Anwendung Bei Patienten Mit Begleiterkrankungen
Klinische Erfahrung mit Paroxetin bei Patienten mit bestimmte begleitende systemische Erkrankungen sind begrenzt. Vorsicht ist ratsam bei der Verwendung Paroxetin bei Patienten mit Erkrankungen oder Zuständen, die den Stoffwechsel beeinflussen könnten oder hämodynamische Reaktionen.
Paroxetin wurde weder bewertet noch angewendet nennenswertes Ausmaß bei Patienten mit einer kürzlichen Geschichte von Myokardinfarkt oder instabile Herzkrankheit. Patienten mit diesen Diagnosen wurden ausgeschlossen von klinische Studien während des premarket-Tests des Produkts. Bewertung von Elektrokardiogramme von 682 Patienten, die Paroxetin in doppelblind erhielten, placebokontrollierte Studien zeigten jedoch nicht, dass Paroxetin verbunden mit der Entwicklung signifikanter EKG-Anomalien. Ähnlich, Paroxetin verursacht keine klinisch wichtigen Veränderungen der Herzfrequenz oder Blutdruck.
Erhöhte Plasmakonzentrationen von Paroxetin treten auf in Patienten mit schwerer Nierenfunktionsstörung (Kreatinin-clearance < 30 ml/min) oder schwere leberfunktionsstörung. Bei solchen Patienten sollte eine niedrigere Anfangsdosis angewendet werden (siehe DOSIERUNG und VERABREICHUNG).
Informationen für Patienten
PEXEVA® (paroxetinmesylat) sollte nicht gekaut werden oder zerkleinert und sollte ganz geschluckt werden.
Patienten sollten vor dem Risiko von serotonin gewarnt werden Syndrom bei gleichzeitiger Anwendung von Paroxetin und triptanen, tramadol oder andere serotonerge Mittel.
Patienten sollten darauf hingewiesen werden, dass die Einnahme von Pexeva verursachen kann milde pupillendilatation, die bei anfälligen Individuen zu einer episode von winkelverschluss Glaukom. Vorbestehendes Glaukom ist fast immer Offenwinkelglaukom weil winkelverschlussglaukom, wenn diagnostiziert, kann behandelt werden definitiv mit iridektomie. Offenwinkelglaukom ist kein Risikofaktor für winkelverschluss Glaukom. Patienten können untersucht werden, um festzustellen, ob Sie sind anfällig für winkelverschlüsse und haben ein prophylaktisches Verfahren (Z., iridektomie), wenn Sie anfällig sind.
Verschreibende ärzte oder andere Angehörige der Gesundheitsberufe sollten informieren Patienten, Ihre Familien und Ihre Betreuer über die Vorteile und Risiken verbunden mit der Behandlung mit PEXEVA® (paroxetinmesylat) und sollte beraten Sie in Ihrer angemessenen Verwendung. Ein patient Medikation Guide über “Antidepressivum Medikamente, Depressionen und andere Schwere psychische Erkrankungen und Selbstmordgedanken oder Aktionen” ist verfügbar für PEXEVA® (paroxetinmesylat). Der verschreibende oder Angehörige der Gesundheitsberufe sollten Patienten, Ihre Familien und Ihre Betreuer, die den Medikamentenleitfaden Lesen und Ihnen beim Verständnis helfen sollten sein Inhalt. Patienten sollten die Möglichkeit gegeben werden, die Inhalte zu diskutieren der Medication Guide und um Antworten auf alle Fragen zu erhalten, die Sie haben können. Der vollständige text des Medikationsleitfadens wird am Ende dieses Artikels nachgedruckt Dokument.
Patienten sollten über folgende Probleme informiert werden und gebeten, Ihren verschreibenden Arzt zu alarmieren, wenn diese auftreten, während der Einnahme von PEXEVA® (Paroxetin mesylat).
Klinische Verschlechterung Und Suizidrisiko
Patienten, Ihre Familien und Ihre Betreuer sollten ermutigt, wachsam zu sein, um die Entstehung von Angst, Unruhe, Panikattacken, Schlaflosigkeit, Reizbarkeit, Feindseligkeit, Aggressivität, Impulsivität, Akathisie (Psychomotorische Unruhe), Hypomanie, Manie, andere ungewöhnliche Veränderungen im Verhalten, Verschlechterung der depression und Suizidgedanken, besonders früh während der Antidepressiven Behandlung und wenn die Dosis nach oben oder unten eingestellt wird. Familien und Pflegepersonen von Patienten sollten geraten werden, nach der Entstehung zu suchen von solchen Symptomen auf einer Tag-zu-Tag-basis, da änderungen abrupt sein können. Wie die Symptome sollten dem verschreibenden Arzt oder der medizinischen Fachkraft des Patienten gemeldet werden, vor allem, wenn Sie schwerwiegend sind, abrupt einsetzen oder nicht Teil der Symptome des Patienten. Symptome wie diese können mit einem erhöhtes Risiko für suizidales denken und Verhalten und weisen auf ein Bedürfnis nach sehr enge überwachung und möglicherweise änderungen der Medikation.
Medikamente, die die Hämostase Stören (NSAIDs, Aspirin, Warfarin, etc.)
Patienten sollten vor der gleichzeitigen Anwendung von Paroxetin mit NSAIDs, aspirin oder anderen Medikamenten, die die Gerinnung beeinflussen. die kombinierte Verwendung von Psychopharmaka, die die serotonin-Wiederaufnahme stören und diese Mittel wurden mit einem erhöhten Blutungsrisiko in Verbindung gebracht.
Störung der Kognitiven und Motorischen Leistungsfähigkeit
Jede psychoaktive Droge kann das Urteilsvermögen beeinträchtigen, denken, oder Motorik. Obwohl in kontrollierten Studien Paroxetin nicht gezeigt wurde Beeinträchtigung der psychomotorischen Leistung, Patienten sollten vor dem Betrieb gewarnt werden gefährliche Maschinen, einschließlich AUTOMOBILE, bis Sie vernünftigerweise sicher sind dass die paroxetintherapie Ihre Fähigkeit, sich an solchen Aktivitäten zu beteiligen, nicht beeinträchtigt.
Therapieverlauf Abschließen
Während Patienten eine Verbesserung mit Paroxetin bemerken können Therapie in 1 bis 4 Wochen sollten Sie geraten werden, die Therapie fortzusetzen als gerichtete.
Begleitmedikation
Patienten sollten geraten werden, Ihren Arzt zu informieren, wenn Sie nehmen oder planen, verschreibungspflichtige oder rezeptfreie Medikamente einzunehmen, da gibt es ein Potenzial für Interaktionen.
Alkohol
Obwohl Paroxetin nicht gezeigt wurde, um die Beeinträchtigung der geistigen und motorischen Fähigkeiten durch Alkohol, Patienten sollten sein empfohlen, Alkohol zu vermeiden, während der Einnahme von PEXEVA® (paroxetinmesylat).
Schwangerschaft
Patienten sollten geraten werden, Ihren Arzt zu Benachrichtigen, wenn Sie werden Schwanger oder beabsichtigen, während der Therapie Schwanger zu werden (siehe WARNHINWEISE - Anwendung in der Schwangerschaft: Teratogen und nicht Teratogen Effekte).
Pflege
Patienten sollten geraten werden, Ihren Arzt zu Benachrichtigen, wenn Sie stillen ein Kind (siehe VORSICHTSMAßNAHMEN - Stillende Mütter).
Labortests
Es werden keine spezifischen Labortests empfohlen.
Paxil® (paroxetinhydrochlorid)
Paroxetin, der Wirkstoff in PEXEVA® (Paroxetin mesylate), ist auch der Wirkstoff von Paxil®. Somit sind diese beiden Agenten sollte nicht mitregistriert werden.
Karzinogenese, Mutagenese, Beeinträchtigung Der Fruchtbarkeit
Karzinogenese
Zweijährige karzinogenitätsstudien wurden in Nagetiere gegeben Paroxetin in der Ernährung bei 1, 5 und 25 mg / kg / Tag (Mäuse) und 1, 5, und 20 mg/kg/Tag (Ratten). Diese Dosen sind bis zu 2.4 (Maus) und 3.9 (Ratte) - mal die empfohlene höchstdosis am Menschen (MRHD) für MDD und GAD auf mg / m & sup2; basis. Weil die MRHD für MDD etwas geringer ist als die FÜR OCD (50 mg vs 60 mg), die in diesen karzinogenitätsstudien verwendeten Dosen betrugen nur 2.0 (Maus) und 3.2 (Ratte) mal die MRHD für OCD. Es gab eine deutlich größere Anzahl von männlichen Ratten in der hochdosierten Gruppe mit Retikulum-Zell-Sarkomen (1/100, 0/50, 0/50, und 4/50 für Kontroll -, niedrig-, Mittel-und hochdosisgruppen) bzw. signifikant erhöhter linearer Trend über Gruppen hinweg für das auftreten von lymphoretikuläre Tumoren bei männlichen Ratten. Weibliche Ratten waren nicht betroffen. Obwohl es gab einen dosisbedingten Anstieg der Anzahl von Tumoren bei Mäusen, es gab keine drogenbedingter Anstieg der Anzahl von Mäusen mit Tumoren. Die Relevanz dieser Befunde für Menschen sind unbekannt.
Mutagenese
Paroxetin erzeugte keine genotoxischen Wirkungen in einer Batterie von 5 in vitro und 2 in vivo - assays, inklusive der folgenden: bakterielle mutation assay, Maus Lymphom mutation assay, außerplanmäßige DNA Synthese assay, und tests auf zytogenetische Aberrationen in vivo im mausknochenmark und in vitro in menschliche Lymphozyten und in einem dominanten tödlichen test bei Ratten.
Beeinträchtigung Der Fruchtbarkeit
Einige klinische Studien haben gezeigt, dass SSRIs (einschließlich Paroxetin) kann die Spermienqualität während der SSRI-Behandlung beeinflussen, was sich auf Fruchtbarkeit bei einigen Männern.
Eine reduzierte Schwangerschaftsrate wurde bei der Fortpflanzung gefunden Studien an Ratten in einer Dosis von Paroxetin von 15 mg / kg / Tag, die 2,9 mal die MRHD für MDD und GAD oder 2,4 mal die MRHD für OCD auf eine mg / m² basis. Irreversible Läsionen traten im fortpflanzungstrakt männlicher Ratten auf. Dosierung in toxizitätsstudien für 2 bis 52 Wochen. Diese Läsionen bestanden aus vakuolation des epididymalen tubulären Epithels bei 50 mg / kg / Tag und atrophisch Veränderungen in den samenkanälchen der Hoden mit festgenommenem spermatog
Nebenwirkungen
verbunden Mit Absetzen der Behandlung
Zwanzig Prozent (1199/6145) der Patienten mit Paroxetin in weltweiten klinischen Studien in MDD und 11,8% (64/542), 9,4% (44/469) und 10,7% (79/735) der mit Paroxetin behandelten Patienten weltweit Studien mit OCD, PD und GAD brachen die Behandlung aufgrund einer unerwünschtes Ereignis. Die häufigsten Ereignisse (≥ 1%) im Zusammenhang mit absetzen und als drogenbezogen angesehen (dh diese damit verbundenen Ereignisse mit dropout mit einer rate von etwa zweimal oder mehr für Paroxetin im Vergleich zu placebo) Folgendes enthalten:
| Altersgruppe | Drug-Placebo-Unterschied in der Anzahl der Fälle von Suizidalität pro 1000 Patienten Behandelt |
| Erhöht sich im Vergleich zu Placebo | |
| < 18 | 14 weitere Fälle |
| 18-24 | 5 weitere Fälle |
| Nimmt im Vergleich zu Placebo ab | |
| 25-64 | 1 weniger Fall |
| ≥ 65 | 6 weniger Fälle |
Häufig Beobachtete Unerwünschte Ereignisse
Schwere Depressive Störung
Die am häufigsten beobachteten unerwünschte Ereignisse im Zusammenhang mit der Anwendung von Paroxetin (Inzidenz von 5% oder mehr und Inzidenz für Paroxetin mindestens doppelt so hoch wie für placebo, abgeleitet aus Tabelle 2 unten) waren: Asthenie, Schwitzen, übelkeit, Appetitlosigkeit, Schläfrigkeit, Schwindel, Schlaflosigkeit, zittern, Nervosität, Ejakulationsstörungen, und andere männliche genitalstörungen.
Zwangsstörung
Die am häufigsten beobachteten unerwünschte Ereignisse im Zusammenhang mit der Anwendung von Paroxetin (Inzidenz von 5% oder höhere und Inzidenz für Paroxetin mindestens doppelt so hoch wie für placebo, abgeleitet aus Tabelle 3 unten) waren: übelkeit, trockener Mund, verminderter Appetit, Verstopfung, Schwindel, Schläfrigkeit, zittern, Schwitzen, Impotenz und abnormale Ejakulation.
Panikstörung
Die am häufigsten beobachteten unerwünschte Ereignisse im Zusammenhang mit der Anwendung von Paroxetin (Inzidenz von 5% oder mehr und Inzidenz für Paroxetin mindestens doppelt so hoch wie für placebo, abgeleitet aus Tabelle 3 unten) waren: Asthenie, Schwitzen, verminderter Appetit, libido verminderte, tremor, abnorme Ejakulation, weibliche genitalstörungen und Ohnmacht.
Generalisierte Angststörung
Die am häufigsten beobachteten unerwünschte Ereignisse im Zusammenhang mit der Anwendung von Paroxetin (Inzidenz von 5% oder mehr und Inzidenz für Paroxetin mindestens doppelt so hoch wie für placebo, abgeleitet aus Tabelle 4) waren: Asthenie, Infektion, Verstopfung, Appetitlosigkeit, trocken Mund, übelkeit, verminderte libido, Schläfrigkeit, zittern, Schwitzen und abnorme Ejakulation.
Inzidenz In Kontrollierten Klinischen Studien
Der Arzt sollte sich bewusst sein, dass die zahlen in der die folgenden Tabellen können nicht zur Vorhersage der Inzidenz von Nebenwirkungen in der Verlauf der üblichen medizinischen Praxis, wo patientenmerkmale und andere Faktoren unterscheiden sich von denen, die in den klinischen Studien vorherrschten. Ähnlich ist die zitierte Frequenzen können nicht mit zahlen anderer Kliniken verglichen werden Untersuchungen mit verschiedenen Behandlungen, Verwendungen und Ermittlern. Der zitierte zahlen liefern dem verschreibenden Arzt jedoch eine gewisse Grundlage zur Abschätzung des relativen Beitrags von Drogen-und nicht-Drogen-Faktoren zu den Nebenwirkung Häufigkeit in der Bevölkerung untersucht.
Schwere Depressive Störung
Tabelle 2 listet unerwünschte Ereignisse auf, die bei einem
Inzidenz von 1% oder mehr bei mit Paroxetin behandelten Patienten, die an
Kurzfristige (6-wöchige) placebokontrollierte Studien, in denen Patienten in einem
Bereich von 20 bis 50 mg/Tag. Gemeldete unerwünschte Ereignisse wurden unter Verwendung eines klassifiziert
standard COSTART-basierte Wörterbuch Terminologie.max.
2 Beinhaltet meistens “Klumpen im Hals” und “Engegefühl im Hals.”
3 Prozentsatz nach Geschlecht korrigiert.
4 Meistens “ejakulatorische Verzögerung.”
5 Enthält “orgasmusunfähigkeit” “erektile Schwierigkeiten” “verzögert
Ejakulation/Orgasmus” und “sexuelle Dysfunktion” und “Impotenz.”
6 Beinhaltet meistens “Schwierigkeit mit micturition” und “Harn -
Zögerlichkeit.”
7 ncludes meistens “Anorgasmie” und “Schwierigkeit zu erreichen
Höhepunkt/Orgasmus.”
Zwangsstörung Und Panikstörung
Tabelle 3 listet Nebenwirkungen auf
Ereignisse, die bei einer Häufigkeit von 2% oder mehr bei OCD-Patienten auftraten auf
Paroxetin, das an placebokontrollierten Studien mit einer Dauer von 12 Wochen teilnahm
in denen Patienten in einem Bereich von 20 bis 60 mg/Tag oder unter Patienten dosiert wurden
mit PD auf Paroxetin, die an placebokontrollierten Studien mit 10-bis
12-Wochen-Dauer, in der Patienten in einem Bereich von 10 bis 60 mg/Tag dosiert wurden.max. [PD]: abnorme Träume, Sehstörungen,
Brustschmerzen, Husten erhöht, depersonalisierung, depression, Dysmenorrhoe,
Dyspepsie, grippesyndrom, Kopfschmerzen, Infektion, Myalgie, Nervosität,
Herzklopfen, Parästhesien, pharyngitis, Hautausschlag, Atemwegserkrankungen, sinusitis,
Geschmack perversion, trauma, Wasserlassen beeinträchtigt, und Vasodilatation.
2 Prozentsatz nach Geschlecht korrigiert.
Generalisierte Angststörung
Tabelle 4 listet unerwünschte Ereignisse auf, die bei einem
Häufigkeit von 2% oder mehr BEI Gad-Patienten unter Paroxetin, die an
placebokontrollierte Studien von 8 Wochen Dauer, in denen Patienten in einem
Bereich von 10 mg / Tag bis 50 mg/Tag.max.
2 Prozentsatz nach Geschlecht korrigiert.
Dosisabhängigkeit Unerwünschter Ereignisse
max.0%
In einer festdosis-Studie. placebo und Paroxetin 20, 40 und 60 mg bei der Behandlung von Zwangsstörungen gab es keine klare Beziehung zwischen unerwünschten Ereignissen und der Dosis von Paroxetin, zu der Patienten wurden zugewiesen. Es wurden keine neuen unerwünschten Ereignisse im Paroxetin beobachtet 60 mg dosisgruppe im Vergleich zu einer der anderen Behandlungsgruppen.
In einer festdosis-Studie. placebo und Paroxetin 10, 20 und 40 mg bei der Behandlung von PD gab es keine klare Beziehung zwischen unerwünschten Ereignissen und der Dosis von Paroxetin, zu der Patienten wurden zugewiesen, außer Asthenie, trockener Mund, Angst, libido verminderte, tremor und abnorme Ejakulation. In Studien mit flexiblen Dosierungen keine neuen unerwünschte Ereignisse wurden bei Patienten beobachtet, die 60 mg Paroxetin erhielten. zu einer der anderen Behandlungsgruppen.
In einer festdosis-Studie. placebo und 20 und 40 mg Paroxetin bei der Behandlung von GAD, für die meisten der unerwünschte Ereignisse, es gab keine klare Beziehung zwischen unerwünschten Ereignissen und der Dosis von Paroxetin, der Patienten zugewiesen wurden, mit Ausnahme der folgenden unerwünschte Ereignisse: Asthenie, Verstopfung und abnormale Ejakulation.
In der flexiblen Dosis Studien, keine neue unerwünschte Ereignisse wurden bei Patienten beobachtet, die Paroxetin 60 mg erhielten im Vergleich zu allen anderen Behandlungsgruppen.
Anpassung an Bestimmte Unerwünschte Ereignisse: über einen Zeitraum von 4 bis 6 Wochen gab es Hinweise auf eine Anpassung zu einigen unerwünschten Ereignissen mit fortgesetzter Therapie (zB übelkeit und Schwindel), aber weniger zu anderen Effekten (zB Mundtrockenheit, Somnolenz und Asthenie).
Männliche und Weibliche Sexuelle Dysfunktion mit SSRIs: Obwohl Veränderungen des sexuellen Verlangens, der sexuellen Leistungsfähigkeit und sexuelle Befriedigung tritt Häufig als Manifestation einer psychiatrischen Störung auf, Sie können auch eine Folge der pharmakologischen Behandlung sein. Insbesondere einige Beweise deuten darauf hin, dass SSRIs solche ungeeigneten sexuellen Erfahrungen verursachen können.
Zuverlässige Schätzungen der Häufigkeit und schwere von ungeeigneten Erfahrungen mit sexuellem verlangen, Leistung und Zufriedenheit sind jedoch teilweise schwer zu erreichen, weil Patienten und ärzte zögern möglicherweise, Sie zu diskutieren. Dementsprechend, Schätzungen der Inzidenz von ungeeigneter sexueller Erfahrung und Leistung. bei der Produktkennzeichnung sind wahrscheinlich Ihre tatsächliche Inzidenz zu unterschätzen.
In placebokontrollierten klinischen Studien mit mehr als 3200 Patienten die Bereiche für die gemeldete Inzidenz von sexuellen Nebenwirkungen bei Männern und Frauen mit MDD, OCD, PD, soziale Angst Störung, GAD und posttraumatische Belastungsstörung (PTBS) werden in Tabelle 6 angezeigt.max
Es gibt keine angemessenen und gut kontrollierte Studien untersuchen sexuelle Dysfunktion mit Paroxetin-Behandlung.
Paroxetin-Behandlung wurde verbunden mit mehreren Fällen von Priapismus. In diesen Fällen mit einem bekannten Ergebnis, die Patienten erholten sich ohne Folgen.
Während es schwer zu wissen ist das genaue Risiko sexueller Dysfunktion im Zusammenhang mit der Verwendung von SSRIs, ärzte sollten sich routinemäßig nach solchen möglichen Nebenwirkungen erkundigen.
Gewicht und Vitalzeichen Änderungen: Signifikanter Gewichtsverlust kann ein unerwünschtes Ergebnis der Behandlung mit Paroxetin für einige Patienten, aber auf im Durchschnitt hatten Patienten in kontrollierten Studien einen minimalen Gewichtsverlust (etwa 1 Pfund) vs kleinere änderungen bei placebo und aktiver Kontrolle. Keine wesentlichen änderungen in Vitalfunktionen (systolischer und diastolischer Blutdruck, Puls und Temperatur) wurden bei Patienten beobachtet, die mit Paroxetin in kontrollierten klinischen Irrungen.
EKG Veränderungen: In einer Analyse von EKGs erhalten in 682 mit Paroxetin behandelte Patienten und 415 mit placebo behandelte Patienten in kontrollierte klinische Studien, keine klinisch signifikanten Veränderungen wurden in der EKGs beider Gruppen.
Leberfunktionstests: in placebokontrollierten klinische Studien, Patienten, die mit Paroxetin behandelt wurden, zeigten abnormale Werte auf leberfunktionstests mit nicht höherer rate als bei placebo-behandelten Patient. Insbesondere die Paroxetin vs placebo Vergleiche für alkalische phosphatase, SGOT, SGPT und bilirubin zeigten keine Unterschiede in der Prozentsatz der Patienten mit ausgeprägten Anomalien.
Halluzinationen: In gepoolten klinischen Studien paroxetinhydrochlorid mit sofortiger Freisetzung, Halluzinationen wurden bei 22 beobachtet von 9089 Patienten, die das Medikament erhielten, und 4 von 3187 Patienten, die placebo erhielten.
Sonstige Ereignisse, die Während der Vormarketing-Bewertung Von Paroxetine
Während seiner premarketing-Bewertung in MDD, mehrere Dosen von Paroxetin wurden 6145 Patienten in phase-2-und 3-Studien verabreicht. Der Bedingungen und Dauer der Exposition gegenüber Paroxetin variierten stark und beinhalteten (in überschneidenden Kategorien) offene und doppelblinde Studien, unkontrollierte und kontrollierte Studien, stationäre und ambulante Studien sowie festdosis-und titrationsstudien. Während premarketing klinische Studien in OCD, PD und GAD, 542, 469 und 735 Patienten erhielten jeweils mehrere Dosen von Paroxetin. Ungeeignete Ereignisse im Zusammenhang mit dieser Exposition wurden aufgezeichnet von klinische Forscher mit Terminologie Ihrer Wahl. Folglich, es ist nicht möglich, eine aussagekräftige Schätzung des Anteils von Personen, die unerwünschte Ereignisse erleben, ohne zuvor ähnliche Arten von untoward Ereignisse in eine kleinere Anzahl von standardisierten ereigniskategorien.
In den folgenden Tabellen berichtete unerwünschte Ereignisse wurden unter Verwendung einer standard-COSTART-basierten Wörterbuchterminologie klassifiziert. Der die vorgestellten Frequenzen stellen daher den Anteil der 9089 Patienten dar ausgesetzt mehreren Dosen Paroxetin, bei denen ein Ereignis des Typs auftrat zitiert mindestens einmal während der Einnahme von Paroxetin. Alle gemeldeten Ereignisse mit Ausnahme derjenigen, die bereits in den Tabellen 2 bis 4 aufgeführt sind , die in Begriffe, die so allgemein sind, dass Sie nicht informativ sind, und die Ereignisse, bei denen ein Medikament verursacht war fern.
Es ist wichtig zu betonen, dass, obwohl die Ereignisse Sie traten während der Behandlung mit Paroxetin auf und waren nicht unbedingt verursacht durch Sie.
Ereignisse werden weiter nach Körpersystem kategorisiert und aufgelistet in der Reihenfolge der abnehmenden
Schwangerschaftskategorie D (siehe WARNHINWEISE - ) in der Schwangerschaft: Teratogene und Nichtteratogene Wirkungen).
verbunden Mit Absetzen der Behandlung
Zwanzig Prozent (1199/6145) der Patienten mit Paroxetin in weltweiten klinischen Studien in MDD und 11,8% (64/542), 9,4% (44/469) und 10,7% (79/735) der mit Paroxetin behandelten Patienten weltweit Studien mit OCD, PD und GAD brachen die Behandlung aufgrund einer unerwünschtes Ereignis. Die häufigsten Ereignisse (≥ 1%) im Zusammenhang mit absetzen und als drogenbezogen angesehen (dh diese damit verbundenen Ereignisse mit dropout mit einer rate von etwa zweimal oder mehr für Paroxetin im Vergleich zu placebo) Folgendes enthalten:
| MDD | OCD | PD | GAD | |||||
| Paroxetin | Placebo | Paroxetin | Placebo | Paroxetin | Placebo | Paroxetin | Placebo | |
| CNS | ||||||||
| Somnolenz | 2.3% | 0.7% | - | - | 1.9% | 0.3% | 2.0% | 0.2% |
| Schlaflosigkeit | - | - | 1.7% | 0% | 1.3% | 0.3% | - | - |
| Bewegung | 1.1% | 0.5% | - | - | - | - | - | - |
| Tremor | 1.1% | 0.3% | - | |||||
| Schwindel | - | - | 1.5% | 0% | - | - | 1.0% | 0.2% |
| > | ||||||||
| Verstopfung | - | - | 1.1% | 0% | - | - | - | - |
| Übelkeit | 3.2% | 1.1% | 1.9% | 0% | 3.2% | 1.2% | 2.0% | 0.2% |
| Durchfall | 1.0% | 0.3% | - | - | - | - | - | - |
| Trockener Mund | 1.0% | 0.3% | - | - | - | - | - | - |
| Erbrechen | 1.0% | 0.3% | - | - | - | - | - | - |
| Sonstiges | ||||||||
| Schwäche | 1.6% | 0.4% | 1.9% | 0.4% | - | - | 1.8% | 0.2% |
| Abnorme | 1.6% | 0% | 2.1% | 0% | - | - | 2.5% | 0.5% |
| Ejakulation1 | ||||||||
| Schwitzen | 1.0% | 0.3% | - | - | - | - | 1.1% | 0.2% |
| Impotenz1 | - | - | 1.5% | 0% | - | - | - | - |
| Wo zahlen nicht angegeben sind, ist die Inzidenz der
Nebenwirkungen bei Patienten, die mit Paroxetin behandelt wurden, waren nicht > 1% oder war nicht
größer oder gleich der zweifachen Inzidenz von placebo. 1 Inzidenz nach Geschlecht korrigiert. |
||||||||
| 2.9% | 10.6% | 13.9% | 12.7% | |||||
| Dermatologie | ||||||||
| Schwitzen | 2.0% | 1.0% | 6.7% | 8.9% | 11.8% | |||
| > | ||||||||
| Verstopfung | 5.9% | 4.9% | 7.7% | 9.9% | 12.7% | |||
| Verminderter Appetit | 2.0% | 2.0% | 5.8% | 4.0% | 4.9% | |||
| Durchfall | 7.8% | 9.8% | 19.2% | 7.9% | 14.7% | |||
| Trockener Mund | 2.0% | 10.8% | 18.3% | 15.8% | 20.6% | |||
| Übelkeit | 13.7% | 14.7% | 26.9% | 34.7% | 36.3% | |||
| Nervensystem | ||||||||
| Angst | 0.0% | 2.0% | 5.8% | 5.9% | 5.9% | |||
| Schwindel | 3.9% | 6.9% | 6.7% | 8.9% | 12.7% | |||
| !Nervosität | 0.0% | 5.9% | 5.8% | 4.0% | 2.9% | |||
| Parästhesien | 0.0% | 2.9% | 1.0% | 5.0% | 5.9% | |||
| Somnolenz | 7.8% | 12.7% | 18.3% | 20.8% | 21.6% | |||
| Tremor | 0.0% | 0.0% | 7.7% | 7.9% | 14.7% | |||
| Spezielle Sinne | ||||||||
| Verschwommenes sehen | 2.0% | 2.9% | 2.9% | 2.0% | 7.8% | |||
| Urogenitalsystem | ||||||||
| Abnorme Ejakulation | 0.0% | 5.8% | 6.5% | 10.6% | 13.0% | |||
| Impotenz | 0.0% | 1.9% | 4.3% | 6.4% | 1.9% | |||
| Männliche Genitalstörungen | 0.0% | 3.8 | 8.7% | 6.4% | 3.7% | |||
| * Regel für die Einbeziehung von negativen Ereignisse in der Tabelle: Inzidenz mindestens 5% für eine der paroxetingruppen und ≥ zweimal die placebo-Inzidenz für mindestens eine Paroxetin-Gruppe. | ||||||||
Häufig Beobachtete Unerwünschte Ereignisse
Schwere Depressive Störung
Die am häufigsten beobachteten unerwünschte Ereignisse im Zusammenhang mit der Anwendung von Paroxetin (Inzidenz von 5% oder mehr und Inzidenz für Paroxetin mindestens doppelt so hoch wie für placebo, abgeleitet aus Tabelle 2 unten) waren: Asthenie, Schwitzen, übelkeit, Appetitlosigkeit, Schläfrigkeit, Schwindel, Schlaflosigkeit, zittern, Nervosität, Ejakulationsstörungen, und andere männliche genitalstörungen.
Zwangsstörung
Die am häufigsten beobachteten unerwünschte Ereignisse im Zusammenhang mit der Anwendung von Paroxetin (Inzidenz von 5% oder höhere und Inzidenz für Paroxetin mindestens doppelt so hoch wie für placebo, abgeleitet aus Tabelle 3 unten) waren: übelkeit, trockener Mund, verminderter Appetit, Verstopfung, Schwindel, Schläfrigkeit, zittern, Schwitzen, Impotenz und abnormale Ejakulation.
Panikstörung
Die am häufigsten beobachteten unerwünschte Ereignisse im Zusammenhang mit der Anwendung von Paroxetin (Inzidenz von 5% oder mehr und Inzidenz für Paroxetin mindestens doppelt so hoch wie für placebo, abgeleitet aus Tabelle 3 unten) waren: Asthenie, Schwitzen, verminderter Appetit, libido verminderte, tremor, abnorme Ejakulation, weibliche genitalstörungen und Ohnmacht.
Generalisierte Angststörung
Die am häufigsten beobachteten unerwünschte Ereignisse im Zusammenhang mit der Anwendung von Paroxetin (Inzidenz von 5% oder mehr und Inzidenz für Paroxetin mindestens doppelt so hoch wie für placebo, abgeleitet aus Tabelle 4) waren: Asthenie, Infektion, Verstopfung, Appetitlosigkeit, trocken Mund, übelkeit, verminderte libido, Schläfrigkeit, zittern, Schwitzen und abnorme Ejakulation.
Inzidenz In Kontrollierten Klinischen Studien
Der Arzt sollte sich bewusst sein, dass die zahlen in der die folgenden Tabellen können nicht zur Vorhersage der Inzidenz von Nebenwirkungen in der Verlauf der üblichen medizinischen Praxis, wo patientenmerkmale und andere Faktoren unterscheiden sich von denen, die in den klinischen Studien vorherrschten. Ähnlich ist die zitierte Frequenzen können nicht mit zahlen anderer Kliniken verglichen werden Untersuchungen mit verschiedenen Behandlungen, Verwendungen und Ermittlern. Der zitierte zahlen liefern dem verschreibenden Arzt jedoch eine gewisse Grundlage zur Abschätzung des relativen Beitrags von Drogen-und nicht-Drogen-Faktoren zu den Nebenwirkung Häufigkeit in der Bevölkerung untersucht.
Schwere Depressive Störung
Tabelle 2 listet unerwünschte Ereignisse auf, die bei einem
Inzidenz von 1% oder mehr bei mit Paroxetin behandelten Patienten, die an
Kurzfristige (6-wöchige) placebokontrollierte Studien, in denen Patienten in einem
Bereich von 20 bis 50 mg/Tag. Gemeldete unerwünschte Ereignisse wurden unter Verwendung eines klassifiziert
standard COSTART-basierte Wörterbuch Terminologie.max.
2 Beinhaltet meistens “Klumpen im Hals” und “Engegefühl im Hals.”
3 Prozentsatz nach Geschlecht korrigiert.
4 Meistens “ejakulatorische Verzögerung.”
5 Enthält “orgasmusunfähigkeit” “erektile Schwierigkeiten” “verzögert
Ejakulation/Orgasmus” und “sexuelle Dysfunktion” und “Impotenz.”
6 Beinhaltet meistens “Schwierigkeit mit micturition” und “Harn -
Zögerlichkeit.”
7 ncludes meistens “Anorgasmie” und “Schwierigkeit zu erreichen
Höhepunkt/Orgasmus.”
Zwangsstörung Und Panikstörung
Tabelle 3 listet Nebenwirkungen auf
Ereignisse, die bei einer Häufigkeit von 2% oder mehr bei OCD-Patienten auftraten auf
Paroxetin, das an placebokontrollierten Studien mit einer Dauer von 12 Wochen teilnahm
in denen Patienten in einem Bereich von 20 bis 60 mg/Tag oder unter Patienten dosiert wurden
mit PD auf Paroxetin, die an placebokontrollierten Studien mit 10-bis
12-Wochen-Dauer, in der Patienten in einem Bereich von 10 bis 60 mg/Tag dosiert wurden.max. [PD]: abnorme Träume, Sehstörungen,
Brustschmerzen, Husten erhöht, depersonalisierung, depression, Dysmenorrhoe,
Dyspepsie, grippesyndrom, Kopfschmerzen, Infektion, Myalgie, Nervosität,
Herzklopfen, Parästhesien, pharyngitis, Hautausschlag, Atemwegserkrankungen, sinusitis,
Geschmack perversion, trauma, Wasserlassen beeinträchtigt, und Vasodilatation.
2 Prozentsatz nach Geschlecht korrigiert.
Generalisierte Angststörung
Tabelle 4 listet unerwünschte Ereignisse auf, die bei einem
Häufigkeit von 2% oder mehr BEI Gad-Patienten unter Paroxetin, die an
placebokontrollierte Studien von 8 Wochen Dauer, in denen Patienten in einem
Bereich von 10 mg / Tag bis 50 mg/Tag.max.
2 Prozentsatz nach Geschlecht korrigiert.
Dosisabhängigkeit Unerwünschter Ereignisse
max.0%
In einer festdosis-Studie. placebo und Paroxetin 20, 40 und 60 mg bei der Behandlung von Zwangsstörungen gab es keine klare Beziehung zwischen unerwünschten Ereignissen und der Dosis von Paroxetin, zu der Patienten wurden zugewiesen. Es wurden keine neuen unerwünschten Ereignisse im Paroxetin beobachtet 60 mg dosisgruppe im Vergleich zu einer der anderen Behandlungsgruppen.
In einer festdosis-Studie. placebo und Paroxetin 10, 20 und 40 mg bei der Behandlung von PD gab es keine klare Beziehung zwischen unerwünschten Ereignissen und der Dosis von Paroxetin, zu der Patienten wurden zugewiesen, außer Asthenie, trockener Mund, Angst, libido verminderte, tremor und abnorme Ejakulation. In Studien mit flexiblen Dosierungen keine neuen unerwünschte Ereignisse wurden bei Patienten beobachtet, die 60 mg Paroxetin erhielten. zu einer der anderen Behandlungsgruppen.
In einer festdosis-Studie. placebo und 20 und 40 mg Paroxetin bei der Behandlung von GAD, für die meisten der unerwünschte Ereignisse, es gab keine klare Beziehung zwischen unerwünschten Ereignissen und der Dosis von Paroxetin, der Patienten zugewiesen wurden, mit Ausnahme der folgenden unerwünschte Ereignisse: Asthenie, Verstopfung und abnormale Ejakulation.
In der flexiblen Dosis Studien, keine neue unerwünschte Ereignisse wurden bei Patienten beobachtet, die Paroxetin 60 mg erhielten im Vergleich zu allen anderen Behandlungsgruppen.
Anpassung an Bestimmte Unerwünschte Ereignisse: über einen Zeitraum von 4 bis 6 Wochen gab es Hinweise auf eine Anpassung zu einigen unerwünschten Ereignissen mit fortgesetzter Therapie (zB übelkeit und Schwindel), aber weniger zu anderen Effekten (zB Mundtrockenheit, Somnolenz und Asthenie).
Männliche und Weibliche Sexuelle Dysfunktion mit SSRIs: Obwohl Veränderungen des sexuellen Verlangens, der sexuellen Leistungsfähigkeit und sexuelle Befriedigung tritt Häufig als Manifestation einer psychiatrischen Störung auf, Sie können auch eine Folge der pharmakologischen Behandlung sein. Insbesondere einige Beweise deuten darauf hin, dass SSRIs solche ungeeigneten sexuellen Erfahrungen verursachen können.
Zuverlässige Schätzungen der Häufigkeit und schwere von ungeeigneten Erfahrungen mit sexuellem verlangen, Leistung und Zufriedenheit sind jedoch teilweise schwer zu erreichen, weil Patienten und ärzte zögern möglicherweise, Sie zu diskutieren. Dementsprechend, Schätzungen der Inzidenz von ungeeigneter sexueller Erfahrung und Leistung. bei der Produktkennzeichnung sind wahrscheinlich Ihre tatsächliche Inzidenz zu unterschätzen.
In placebokontrollierten klinischen Studien mit mehr als 3200 Patienten die Bereiche für die gemeldete Inzidenz von sexuellen Nebenwirkungen bei Männern und Frauen mit MDD, OCD, PD, soziale Angst Störung, GAD und posttraumatische Belastungsstörung (PTBS) werden in Tabelle 6 angezeigt.max
Es gibt keine angemessenen und gut kontrollierte Studien untersuchen sexuelle Dysfunktion mit Paroxetin-Behandlung.
Paroxetin-Behandlung wurde verbunden mit mehreren Fällen von Priapismus. In diesen Fällen mit einem bekannten Ergebnis, die Patienten erholten sich ohne Folgen.
Während es schwer zu wissen ist das genaue Risiko sexueller Dysfunktion im Zusammenhang mit der Verwendung von SSRIs, ärzte sollten sich routinemäßig nach solchen möglichen Nebenwirkungen erkundigen.
Gewicht und Vitalzeichen Änderungen: Signifikanter Gewichtsverlust kann ein unerwünschtes Ergebnis der Behandlung mit Paroxetin für einige Patienten, aber auf im Durchschnitt hatten Patienten in kontrollierten Studien einen minimalen Gewichtsverlust (etwa 1 Pfund) vs kleinere änderungen bei placebo und aktiver Kontrolle. Keine wesentlichen änderungen in Vitalfunktionen (systolischer und diastolischer Blutdruck, Puls und Temperatur) wurden bei Patienten beobachtet, die mit Paroxetin in kontrollierten klinischen Irrungen.
EKG Veränderungen: In einer Analyse von EKGs erhalten in 682 mit Paroxetin behandelte Patienten und 415 mit placebo behandelte Patienten in kontrollierte klinische Studien, keine klinisch signifikanten Veränderungen wurden in der EKGs beider Gruppen.
Leberfunktionstests: in placebokontrollierten klinische Studien, Patienten, die mit Paroxetin behandelt wurden, zeigten abnormale Werte auf leberfunktionstests mit nicht höherer rate als bei placebo-behandelten Patient. Insbesondere die Paroxetin vs placebo Vergleiche für alkalische phosphatase, SGOT, SGPT und bilirubin zeigten keine Unterschiede in der Prozentsatz der Patienten mit ausgeprägten Anomalien.
Halluzinationen: In gepoolten klinischen Studien paroxetinhydrochlorid mit sofortiger Freisetzung, Halluzinationen wurden bei 22 beobachtet von 9089 Patienten, die das Medikament erhielten, und 4 von 3187 Patienten, die placebo erhielten.
Sonstige Ereignisse, die Während der Vormarketing-Bewertung Von Paroxetine
Während seiner premarketing-Bewertung in MDD, mehrere Dosen von Paroxetin wurden 6145 Patienten in phase-2-und 3-Studien verabreicht. Der Bedingungen und Dauer der Exposition gegenüber Paroxetin variierten stark und beinhalteten (in überschneidenden Kategorien) offene und doppelblinde Studien, unkontrollierte und kontrollierte Studien, stationäre und ambulante Studien sowie festdosis-und titrationsstudien. Während premarketing klinische Studien in OCD, PD und GAD, 542, 469 und 735 Patienten erhielten jeweils mehrere Dosen von Paroxetin. Ungeeignete Ereignisse im Zusammenhang mit dieser Exposition wurden aufgezeichnet von klinische Forscher mit Terminologie Ihrer Wahl. Folglich, es ist nicht möglich, eine aussagekräftige Schätzung des Anteils von Personen, die unerwünschte Ereignisse erleben, ohne zuvor ähnliche Arten von untoward Ereignisse in eine kleinere Anzahl von standardisierten ereigniskategorien.
In den folgenden Tabellen berichtete unerwünschte Ereignisse wurden unter Verwendung einer standard-COSTART-basierten Wörterbuchterminologie klassifiziert. Der die vorgestellten Frequenzen stellen daher den Anteil der 9089 Patienten dar ausgesetzt mehreren Dosen Paroxetin, bei denen ein Ereignis des Typs auftrat zitiert mindestens einmal während der Einnahme von Paroxetin. Alle gemeldeten Ereignisse mit Ausnahme derjenigen, die bereits in den Tabellen 2 bis 4 aufgeführt sind , die in Begriffe, die so allgemein sind, dass Sie nicht informativ sind, und die Ereignisse, bei denen ein Medikament verursacht war fern.
Es ist wichtig zu betonen, dass, obwohl die Ereignisse Sie traten während der Behandlung mit Paroxetin auf und waren nicht unbedingt verursacht durch Sie.
Ereignisse werden weiter nach Körpersystem kategorisiert und aufgelistet in der Reihenfolge der abnehmenden Frequenz nach
Menschliche Erfahrung
Seit der Einführung von Paroxetin in den USA, 342 spontane Fälle von vorsätzlicher oder versehentlicher überdosierung während Paroxetin die Behandlung wurde weltweit berichtet (circa 1999). Dazu gehören überdosierungen mit Paroxetin allein und in Kombination mit anderen Substanzen. Von diesen 48 die Fälle waren tödlich und von den Todesfällen Schienen 17 Paroxetin zu beinhalten allein. Acht tödliche Fälle, in denen die aufgenommene paroxetinmenge dokumentiert wurde wurden im Allgemeinen durch die Einnahme anderer Drogen oder Alkohol oder die Vorhandensein von signifikanten komorbiden Zuständen. Von 145 nicht tödlichen Fällen mit bekannten Ergebnis, die meisten erholten sich ohne Folgen. Die größte bekannte Einnahme beteiligt 2000 mg Paroxetin (33-fache der maximal empfohlenen Tagesdosis) in a patient, der sich erholt hat.
Häufig berichtete unerwünschte Ereignisse im Zusammenhang mit Paroxetin überdosierung umfassen Somnolenz, Koma, übelkeit, zittern, Tachykardie, Verwirrung, Erbrechen und Schwindel. Andere Bemerkenswerte Anzeichen und Symptome beobachtet bei überdosierungen mit Paroxetin (allein oder mit anderen Substanzen) gehören mydriasis, Krämpfe (einschließlich status epilepticus), ventrikuläre dysrhythmien (einschließlich torsade de pointes), Hypertonie, aggressive Reaktionen, Synkope, Hypotonie, stupor, Bradykardie, Dystonie, Rhabdomyolyse, Symptome einer leberfunktionsstörung (einschließlich Leberversagen, lebernekrose, Gelbsucht, hepatitis und Leber Steatose), serotonin-Syndrom, manische Reaktionen, Myoklonus, akute renale Versagen und Harnverhalt.
Überdosierung-Management
Es sind keine spezifischen Gegenmittel für Paroxetin bekannt. Behandlung sollte aus diesen Allgemeinen Maßnahmen bestehen, die bei der Verwaltung von überdosierung mit Medikamenten, die bei der Behandlung von MDD wirksam sind.
Sorgen Sie für eine ausreichende Atemwege, Sauerstoffversorgung und Belüftung. Überwachen Sie den Herzrhythmus und die Vitalfunktionen. Allgemein unterstützend und symptomatisch Maßnahmen werden ebenfalls empfohlen. Die Induktion von emesis wird nicht empfohlen.
Aufgrund des großen verteilungsvolumens dieses Medikaments, erzwungene Diurese, Dialyse, hämoperfusion und Austauschtransfusion sind unwahrscheinlich um von nutzen zu sein.
Eine spezifische Vorsicht betrifft Patienten, die einnehmen oder haben kürzlich Paroxetin eingenommen, das übermäßige Mengen eines trizyklisches Antidepressivum. In einem solchen Fall Akkumulation des elterntrizyklischen und/oder ein aktiver Metabolit kann die Möglichkeit einer klinisch signifikanten Folgen und verlängern die Zeit, die für eine enge medizinische Beobachtung benötigt wird (siehe Drogen Metabolisiert durch Cytochrom CYP2D6 unter VORSICHTSMAßNAHMEN).
Berücksichtigen Sie bei der Behandlung von überdosierungen die Möglichkeit von mehrfache drogenbeteiligung. Der Arzt sollte in Betracht ziehen, ein Gift zu Kontaktieren Kontrollzentrum für zusätzliche Informationen zur Behandlung einer überdosierung. Telefonnummern für zertifizierte giftkontrollstellen sind in den Arztpraxen aufgeführt. Desk Reference (PDR).
Die Wirksamkeit von Paroxetin bei der Behandlung von MDD, OCD, Panikstörung (PD) und generalisierte Angststörung (GAD) wird vermutet verbunden mit der Potenzierung der serotonergen Aktivität im Zentralnervensystem resultierend aus der Hemmung der neuronalen Wiederaufnahme von serotonin (5-Hydroxytryptamin, 5-HT). Studien zu klinisch relevanten Dosen beim Menschen haben gezeigt, dass Paroxetin die Aufnahme von serotonin in den Menschen blockiert Blutpl. in vitro Studien an Tieren legen auch nahe, dass Paroxetin ein potenter und hochselektiver inhibitor der neuronalen serotonin-Wiederaufnahme und hat nur sehr schwache Auswirkungen auf die neuronale Wiederaufnahme von Noradrenalin und Dopamin. In vitro radioligand bindungsstudien zeigen, dass Paroxetin wenig Affinität zu muskarin hat alpha1-, alpha2-, beta-adrenergen-, Dopamin - (D2)-, 5-HT1-, 5-HT2-und Histamin (H1)-Rezeptoren; Antagonismus von muskarinischen, histaminergen und alpha1-adrenerge Rezeptoren wurde mit verschiedenen anticholinergen assoziiert, sedative und kardiovaskuläre Wirkungen für andere Psychopharmaka.
Weil die relativen Potenzen von paroxetins major Metaboliten sind höchstens 1/50 der Stammverbindung, Sie sind im wesentlichen inaktiv.
Paroxetinmesylat wird nach oraler Verabreichung vollständig resorbiert die Dosierung der mesylate salt. In einer Studie, in der normale männliche Probanden (n=25) erhielt Paroxetin 30 mg Tabletten täglich für 24 Tage, steady-state-Paroxetin die Konzentrationen wurden bei den meisten Probanden um ungefähr 13 Tage erreicht, obwohl es bei einem gelegentlichen Patienten wesentlich länger dauern kann. Bei Konstanten Zustand, Mittelwerte von Cmax, Tmax, Cmin, und T½ waren 81.3 ng/ml (CV-41%), 8.1 Personalabteilung. (CV 56%), 43.2 ng/ml (CV 52%), und 33.2 hr. (+52%) bzw.. Der steady-state-Cmax - und Cmin-Werte waren etwa 7 - und 10-mal so hoch wie Ergebnisse aus einzeldosisstudien. Stationäre arzneimittelexposition basierend auf AUC0-24 war etwa 10-mal größer als aus Einzeldosis-Daten vorhergesagt worden wäre in diesen Fächern. Die überschüssige Akkumulation ist eine Folge der Tatsache, dass eines der Enzyme, das Paroxetin metabolisiert, ist leicht sättigend.
In Studien zur Proportionalität der stationären Dosis, an denen ältere und nicht Behinderte Patienten in Dosen von 20 bis 40 mg täglich für ältere Menschen und 20 bis 50 mg täglich für die nichtelderly, einige Nichtlinearität wurde beobachtet in beide Populationen spiegeln wiederum einen sättigenden Stoffwechselweg wider. Im Vergleich zu Cmin-Werten nach 20 mg täglich waren Werte nach 40 mg nur etwa 2 bis 3 mal größer als verdoppelt.
Die Auswirkungen von Lebensmitteln auf die Bioverfügbarkeit von Paroxetin wurden an Probanden untersucht, denen eine Einzeldosis mit und ohne Nahrung verabreicht wurde. AUC wurde nur geringfügig erhöht (6%), wenn Medikament mit Nahrung verabreicht wurde, aber die Cmax war 29% größer, während die Zeit bis zum erreichen der Plasmakonzentration abnahm von 6,4 Stunden nach der Dosierung bis 4,9 Stunden.
Paroxetin wird nach oraler Verabreichung weitgehend metabolisiert Verwaltung. Die hauptmetaboliten sind polare und konjugierte Produkte von oxidation und Methylierung, die leicht gelöscht. Konjugate mit Glucuronsäure und Sulfat überwiegen, und wichtige Metaboliten wurden isoliert und identifiziert. Daten zeigen, dass die Metaboliten nicht mehr als 1/50 die Wirksamkeit der Stammverbindung bei Hemmung der serotoninaufnahme. Der der Metabolismus von Paroxetin wird teilweise durch Cytochrom CYP2D6 erreicht. Die Sättigung dieses Enzyms in klinischen Dosen scheint für die Nichtlinearität der paroxetinkinetik mit Zunehmender Dosis und Zunehmender Dauer der Behandlung. Die Rolle dieses Enzyms im paroxetinstoffwechsel auch schlägt mögliche Wechselwirkungen zwischen Medikamenten vor (siehe VORSICHTSMAßNAHMEN).
Ungefähr 64% einer 30 mg oralen lösungsdosis von Paroxetin wurde im Urin mit 2% als Stammverbindung und 62% als ausgeschieden Metaboliten über einen Zeitraum von 10 Tagen nach der Dosierung. Etwa 36% wurde in der Fäkalien (wahrscheinlich über die Galle), meist als Metaboliten und weniger als 1% als die parent compound über den Zeitraum von 10 Tagen nach der Dosierung.
In einer Metaanalyse von Paroxetin aus 4 Studien in gesunde freiwillige nach mehrfacher Dosierung von 20 mg / Tag bis 40 mg/ Tag, Männer zeigte keine signifikant niedrigere Cmax oder AUC als Frauen.
Verteilung
Paroxetin verteilt sich im ganzen Körper, einschließlich der ZNS, wobei nur 1% im plasma verbleibt.
Proteinbindung
Ungefähr 95% und 93% von Paroxetin sind gebunden an Plasmaprotein bei 100 ng/ml bzw. 400 ng / ml. Unter klinisch Bedingungen, Paroxetin-Konzentrationen normalerweise weniger als 400 ng/ml. Paroxetin verändert nicht die in vitro proteinbindung von phenytoin oder warfarin.
Nieren-und Lebererkrankungen
Erhöhte Plasmakonzentrationen von Paroxetin treten auf in Probanden mit Nieren-und leberfunktionsstörung. Die mittleren Plasmakonzentrationen in Patienten mit Kreatinin-clearance unter 30 ml / min war etwa 4 mal größer als bei normalen Freiwilligen. Patienten mit Kreatinin-clearance von 30 bis 60 ml / min und Patienten mit leberfunktionsstörung hatten etwa ein 2-facher Anstieg der Plasmakonzentrationen (AUC, Cmax).
Die Anfangsdosis sollte daher reduziert werden in Patienten mit schwerer Nieren-oder leberfunktionsstörung und Titration nach oben, wenn notwendig, sollte in erhöhten Intervallen erfolgen (siehe DOSIERUNG und VERABREICHUNG).
Ältere Patienten
In einer mehrfachdosis-Studie bei älteren Menschen bei täglich Paroxetin-Dosen von 20, 30 und 40 mg, cmin-Konzentrationen waren etwa 70% bis 80% höher als die jeweiligen Cmin-Konzentrationen bei nicht-Behinderten Probanden. Daher sollte die Anfangsdosis bei älteren Menschen reduziert werden (siehe DOSIERUNG Und VERWALTUNG).
Verfügbar in Ländern
| MDD | OCD | PD | GAD | |||||
| Paroxetin | Placebo | Paroxetin | Placebo | Paroxetin | Placebo | Paroxetin | Placebo | |
| CNS | ||||||||
| Somnolenz | 2.3% | 0.7% | - | - | 1.9% | 0.3% | 2.0% | 0.2% |
| Schlaflosigkeit | - | - | 1.7% | 0% | 1.3% | 0.3% | - | - |
| Bewegung | 1.1% | 0.5% | - | - | - | - | - | - |
| Tremor | 1.1% | 0.3% | - | |||||
| Schwindel | - | - | 1.5% | 0% | - | - | 1.0% | 0.2% |
| > | ||||||||
| Verstopfung | - | - | 1.1% | 0% | - | - | - | - |
| Übelkeit | 3.2% | 1.1% | 1.9% | 0% | 3.2% | 1.2% | 2.0% | 0.2% |
| Durchfall | 1.0% | 0.3% | - | - | - | - | - | - |
| Trockener Mund | 1.0% | 0.3% | - | - | - | - | - | - |
| Erbrechen | 1.0% | 0.3% | - | - | - | - | - | - |
| Sonstiges | ||||||||
| Schwäche | 1.6% | 0.4% | 1.9% | 0.4% | - | - | 1.8% | 0.2% |
| Abnorme | 1.6% | 0% | 2.1% | 0% | - | - | 2.5% | 0.5% |
| Ejakulation1 | ||||||||
| Schwitzen | 1.0% | 0.3% | - | - | - | - | 1.1% | 0.2% |
| Impotenz1 | - | - | 1.5% | 0% | - | - | - | - |
| Wo zahlen nicht angegeben sind, ist die Inzidenz der
Nebenwirkungen bei Patienten, die mit Paroxetin behandelt wurden, waren nicht > 1% oder war nicht
größer oder gleich der zweifachen Inzidenz von placebo. 1 Inzidenz nach Geschlecht korrigiert. |
||||||||
| 2.9% | 10.6% | 13.9% | 12.7% | |||||
| Dermatologie | ||||||||
| Schwitzen | 2.0% | 1.0% | 6.7% | 8.9% | 11.8% | |||
| > | ||||||||
| Verstopfung | 5.9% | 4.9% | 7.7% | 9.9% | 12.7% | |||
| Verminderter Appetit | 2.0% | 2.0% | 5.8% | 4.0% | 4.9% | |||
| Durchfall | 7.8% | 9.8% | 19.2% | 7.9% | 14.7% | |||
| Trockener Mund | 2.0% | 10.8% | 18.3% | 15.8% | 20.6% | |||
| Übelkeit | 13.7% | 14.7% | 26.9% | 34.7% | 36.3% | |||
| Nervensystem | ||||||||
| Angst | 0.0% | 2.0% | 5.8% | 5.9% | 5.9% | |||
| Schwindel | 3.9% | 6.9% | 6.7% | 8.9% | 12.7% | |||
| !Nervosität | 0.0% | 5.9% | 5.8% | 4.0% | 2.9% | |||
| Parästhesien | 0.0% | 2.9% | 1.0% | 5.0% | 5.9% | |||
| Somnolenz | 7.8% | 12.7% | 18.3% | 20.8% | 21.6% | |||
| Tremor | 0.0% | 0.0% | 7.7% | 7.9% | 14.7% | |||
| Spezielle Sinne | ||||||||
| Verschwommenes sehen | 2.0% | 2.9% | 2.9% | 2.0% | 7.8% | |||
| Urogenitalsystem | ||||||||
| Abnorme Ejakulation | 0.0% | 5.8% | 6.5% | 10.6% | 13.0% | |||
| Impotenz | 0.0% | 1.9% | 4.3% | 6.4% | 1.9% | |||
| Männliche Genitalstörungen | 0.0% | 3.8 | 8.7% | 6.4% | 3.7% | |||
| * Regel für die Einbeziehung von negativen Ereignisse in der Tabelle: Inzidenz mindestens 5% für eine der paroxetingruppen und ≥ zweimal die placebo-Inzidenz für mindestens eine Paroxetin-Gruppe. | ||||||||


