
Componentes:
Opção de tratamento:
Medicamente revisado por Kovalenko Svetlana Olegovna, Farmácia Última atualização em 26.03.2022

Atenção! As informações na página são apenas para profissionais de saúde! As informações são coletadas em fontes abertas e podem conter erros significativos! Tenha cuidado e verifique novamente todas as informações desta página!
20 principais medicamentos com os mesmos componentes:

Daypro Alta

Apresentações E Dosagens
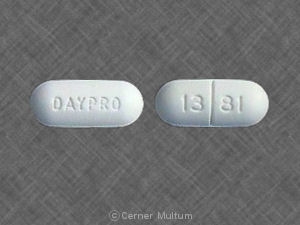
Comprimidos de DAYPRO ALTA (oxaprozina potássio): comprimidos de 600 mg, azuis, em forma de cápsula, revestidos por película, com Searle 1391 impresso numa das faces.
Armazenagem E Manuseamento
Os comprimidos de DAYPRO ALTA 600 mg são azuis, em forma de cápsula, revestidos por película, com Searle 1391 impresso numa das faces.
| Número NDC | Tamanhofrance. KGM |
| 0025-5500-01 | fiasco de 100 |
| 0025-5500-03 | fiasco de 500 |
| 0025-5500-02 | cartonagem de 100 dose unitária |
Conservar à temperatura ambiente de 20 ° C A 25 ° C( 68 ° F A 77 ° F), excursões Permitidas entre 15 ° C a 30 ° C (59 ° F A 86 ° F) (Ver temperatura ambiente controlada pela USP). Administrar num recipiente bem fechado. Proteger da humidade.
Fabricação na qual: Pfizer Inc., 235 East 42nd Street, New York, NY, 10017. Revisto Em Maio De 2016

DAYPRO ALTA está indicado:
- Para alívio dos sinais e sintomas da osteoartrite
- Para alívio dos sinais e sintomas da arte reumatóide

Instruções Gerais De Dosagem
Considere cuidadosamente os potenciais benefícios e riscos do DAYPRO ALTA e outras opções de tratamento antes de decidir utilizar o DAYPRO ALTA. Utilize a dose eficaz mais baixa durante o menor período de tempo consistente com os objectivos individuais de tratamento do doente.
Após observar a resposta à terapêutica inicial com DAYPRO ALTA, a dose e a frequência devem ser ajustadas de acordo com as necessidades de cada doente.
Pode tentar-se a administração de doses divididas em doentes que não conseguem tolerar doses únicas. Para doentes com osteoartrite de baixo peso corporal ou com doença mais ligeira, pode ser adequada uma dose inicial de um comprimido de 600 mg uma vez por dia. A dose diária total máxima é de 1200 mg.
Artrose
Para OA, a dose é de 1200 mg (dois comprimidos de 600 mg) administrados por via oral uma vez por dia.
Artrite Reumatóide
Para ar, a dose é de 1200 mg (dois comprimidos de 600 mg) administrados por via oral uma vez por dia.

DAYPRO ALTA está contra-indicado nos seguintes doentes::
- Hibersensibilidadconhecida (por ex., reacções anafiláticas e reacções cutâneas graves) à oxaprozina potássio ou a questquer componentes do medicamento
- Antecedentes de asma, urticária ou outras reacções do tipo clínico só tomar aspirina ou outros AINEs. Nestes doentes foram notificadas reacções anafilácticas graves, por labirintos fatais, aos AINEs.
- No contexto da cirurgia de bypass da arte coronária (CABG)

AVISO
Incluído como parte da "PRECAUCAO" Seccao
PRECAUCAO
Acontecimentos Trombóticos Cardiovasculares
Os ensaios clínicos com vários AINEs selectivos e não selectivos da COX-2 com uma duração até três anos demonstraram um risco aumentado de acontecimentos trombóticos cardiovasculares graves, incluindo enfarte do miocárdio (em) e acidente vascular cerebral, que podem ser fatais. . Com base nos dados disponíveis, não é claro que o risco para acontecimentos trombóticos CV é semelhante para todos os AINEs. . O aumento relativo de acontecimentos trombóticos CV graves ao longo do início conferido pela utilização de AINE parece ser semelhante nos que apresentam e sem doença CV conhecida ou factores de risco para a doença CV. No entanto, os doentes com doença CV conhecida ou factores de risco tiveram uma incidência absoluta mais elevada de acontecimentos trombóticos cardiovasculares graves em excesso, devido ao aumento da taxa inicial. Alguns estudos observacionais revelaram que este aumento do risco de acontecimentos trombóticos CV graves começou logo nas primeiras semanas de tratamento.. O aumento do risco trombótico CV foi observado de forma mais consistente com doses mais elevadas
Para minimizar o risco potencial de ocorrência de um evento CV adverso em doentes tratados com AINEs, utilize a dose eficaz mais baixa durante o menor período possível. Os médicos e os doentes devem permanecer alerta para o desenvolvimento destes acontecimentos, durante todo o ciclo de tratamento, mesmo na ausência de sintomas CV anteriores. Os doentes devem ser informados sobre os sintomas de acontecimentos CV graves e as medidas a tomar no caso de ocorrerem.
Não há evidência consistente de que o uso concomitante de aspirina reduz o risco aumentado de acontecimentos trombóticos CV graves associados ao uso de AINE. O uso concomitante de aspirina e um AINE, como a oxaprozina, aumenta o risco de acontecimentos gastrointestinais graves.
Estado pós-cirurgia de Bypass arterial coronário (CABG)
Dois grandes ensaios clínicos controlados de um AINE selectivo da COX-2 para o tratamento da dor nos primeiros 10-14 dias após cirurgia de bypass da artéria coronária revelaram um aumento da incidência de enfarte do miocárdio e acidente vascular cerebral. Os AINEs estão contra-indicados na configuração da CABG.
Doentes pós-em
Estudos observacionais realizados em dinamarquês Nacional de Registro demonstraram que os pacientes tratados com Aines no pós-MI período foram em maior risco de reinfarction, CV-relacionada com a morte, e todas as causas de mortalidade início na primeira semana de tratamento. Neste mesmo grupo, a incidência de morte no primeiro ano após o enfarte do miocárdio foi de 20 por 100 pessoas / ano em doentes tratados com AINEs, em comparação com 12 por 100 pessoas / ano em doentes não expostos a a AINEs. Embora a taxa absoluta de mortalidade tenha diminuído ligeiramente após o primeiro ano após o enfarte do miocárdio, o aumento do risco relativo de morte nos utilizadores de AINE persistiu durante, pelo menos, os próximos quatro anos de seguimento.
Evitar a utilização de DAYPRO ALTA em doentes com EM recente, a menos que se preveja que os benefícios sejam superiores ao risco de acontecimentos trombóticos CV recorrentes. Se o DAYPRO ALTA for utilizado em doentes com enfarte do miocárdio recente, deve monitorizar-se os doentes quanto a sinais de isquemia cardíaca.
Hemorragia Gastrointestinal, Ulceração E Perfuração
Os AINEs, incluindo o DAYPRO ALTA, causam efeitos adversos gastrointestinais graves, incluindo inflamação, hemorragia, ulceração e perfuração do esófago, estômago, intestino delgado ou intestino grosso, que podem ser fatais.. Estes acontecimentos adversos graves podem ocorrer a qualquer momento, com ou sem sintomas de alerta, em doentes tratados com AINEs.. Apenas um em cada cinco doentes que desenvolvem um acontecimento adverso GI superior grave na terapêutica com AINEs é sintomático. Úlceras GI superiores, hemorragia bruta ou perfuração causada por AINEs ocorreram em aproximadamente 1% dos doentes tratados durante 3-6 meses, e em cerca de 2% - 4% dos doentes tratados durante um ano.. No entanto, mesmo a terapêutica a curto prazo com AINEs não é isenta de risco
Factores de risco para hemorragia gastrointestinal, ulceração e Perfuração
Doentes com antecedentes de úlcera péptica e / ou hemorragia gastrointestinal que utilizaram AINEs tiveram um risco aumentado superior a 10 vezes para o desenvolvimento de hemorragia gastrointestinal comparativamente com doentes sem estes factores de risco.. Outros fatores que aumentam o risco de hemorragia GI em doentes tratados com Aines incluem a longa duração da terapia com AINES, o uso concomitante de corticosteróides orais, aspirina, anticoagulantes ou inibidores seletivos de serotonina (SSRIs), tabagismo, uso de álcool, idade mais avançada, e pobre estado de saúde geral. A maioria das notificações pós-comercialização de acontecimentos GI fatais ocorreram em doentes idosos ou debilitados. Adicionalmente, os doentes com doença hepática avançada e / ou coagulopatia têm um risco aumentado de hemorragia gastrointestinal.
Estratégias para minimizar os riscos GI em doentes tratados com AINEs:
- Utilizar uma dose eficaz mais baixa durante o período período possível.
- Evitar a administração de mais de um AINE de Dada vez.
- Evitar a utilização em dias de maior risco, a menos que se preveja que os benefícios compensem o risco aumentado de hemorragia. Para estes doentes, bem como para os doentes com hemorragia GI activa, devem considerar-se outras terapeuticas alternativas para além dos bovinos.
- Mantenha-se alerta para sinais e sintomas de ulceração GI e hemorragia durante a terapêutica com AINEs.
- Caso se suspeite de um acontecimento adverso GI grave, iniciar imediatamente a avaliação e o tratamento e interromper o tratamento com DAYPRO ALTA até se excluir um acontecimento adverso GI-túmulo.
- No contexto do uso concomitante de uma dose baixa de aspirina para profilaxia cardíaca, os doentes devem ser monitorizados mais de perto quanto à evidência de hemorragia gastrointestinal.
Hepatotoxicidade
Em ensaios clínicos, foram notificados aumentos da ALT ou AST (três ou mais vezes o limite superior do normal [LSN]) em aproximadamente 1% dos doentes tratados com AINEs. Adicionalmente, foram notificados casos raros, por vezes fatais, de lesão hepática grave, incluindo hepatite fulminante, necrose hepática e insuficiência hepática.
Podem ocorrer elevações da ALT ou AST (menos de três vezes o LSN) em até 15% dos doentes tratados com AINEs, incluindo oxaprozina potássio.
Informe os doentes dos sinais de aviso e sintomas de hepatotoxicidade (por exemplo, náuseas, fadiga, letargia, diarreia, prurido, icterícia, sensibilidade no quadrante superior direito e sintomas de tipo gripal). Se se desenvolverem sinais e sintomas clínicos consistentes com a doença hepática, ou se ocorrerem manifestações sistémicas (por ex., eosinofilia, erupção cutânea, etc.).), interromper imediatamente o tratamento com DAYPRO ALTA e efectuar uma avaliação clínica do doente.
Hipertensao
Os AINEs, incluindo a DAYPRO ALTA, podem levar a um novo início de hipertensão ou a um agravamento da hipertensão pré-existente, qualquer das quais pode contribuir para o aumento da incidência de acontecimentos CV. Os doentes a tomar inibidores da enzima de conversão da angiotensina (ECA), diuréticos tiazídicos ou diuréticos da ansa podem ter dificuldade em responder a estas terapêuticas quando estão a tomar AINEs.
Monitorizar a pressão Arterial (BP) durante o início do tratamento com AINEs e durante o curso da terapêutica.
Insuficiência Cardíaca E Edema
A meta-análise de colaboração dos Trialistas do Coxib e dos AINEs tradicionais de ensaios controlados aleatorizados demonstrou um aumento de aproximadamente duas vezes nas hospitalizações por insuficiência cardíaca em doentes tratados com COX-2 selectivos e em doentes não selectivos tratados com AINEs comparativamente aos doentes tratados com placebo. Num estudo do registo nacional dinamarquês de doentes com insuficiência cardíaca, o uso de AINE aumentou o risco de em, hospitalização por insuficiência cardíaca e morte.
Adicionalmente, foram observadas retenção de líquidos e edema em alguns doentes tratados com AINEs. A utilização de oxaprozina pode atenuar os efeitos CV de vários fármacos terapêuticos utilizados no tratamento destas situações clínicas (ex. diuréticos, inibidores da ECA ou bloqueadores dos receptores da angiotensina [ARBs]).
Evite a utilização de DAYPRO ALTA em doentes com insuficiência cardíaca grave, a menos que se preveja que os benefícios sejam superiores ao risco de agravamento da insuficiência cardíaca. Se DAYPRO ALTA for utilizado em doentes com insuficiência cardíaca grave, monitorizar os doentes quanto a sinais de agravamento da insuficiência cardíaca.
Toxicidade Renal E Hipercaliemia
Toxicidade Renal
A administração a longo prazo de AINEs resultou em necrose papilar renal e outra lesão renal. Também foi observada toxicidade Renal em doentes nos quais as prostaglandinas renais têm um papel compensatório na manutenção da perfusão renal.. Nestes doentes, a administração de um AINE pode causar uma redução dose-dependente na formação de prostaglandinas e, secundariamente, no fluxo sanguíneo renal, o que pode precipitar uma descompensação renal excessiva.. Os doentes com maior risco desta reacção são os que apresentam compromisso da função renal, desidratação, hipovolemia, insuficiência cardíaca, disfunção hepática, os que tomam diuréticos e inibidores da ECA ou ARBs, e os idosos. A interrupção da terapêutica com AINEs é geralmente seguida por recuperação no estado pré-tratamento
Não está disponível informação de estudos clínicos controlados sobre a utilização de DAYPRO ALTA em doentes com doença renal avançada. Os efeitos renais do DAYPRO ALTA podem acelerar a progressão da disfunção renal em doentes com doença renal pré-existente.
Estado correcto do volume em doentes desidratados ou hipovolémicos antes do início do DAYPRO ALTA. Monitorizar a função renal em doentes com insuficiência renal ou hepática, insuficiência cardíaca, desidratação ou hipovolemia durante o uso de DAYPRO ALTA. Evite a utilização de DAYPRO ALTA em doentes com doença renal avançada, a menos que se preveja que os benefícios sejam superiores ao risco de agravamento da função renal. Se DAYPRO ALTA for utilizado em doentes com doença renal avançada, deve monitorizar-se os doentes quanto a sinais de agravamento da função renal.
Hipercaliemia
Foram notificados aumentos na concentração sérica de potássio, incluindo hipercaliemia, com a utilização de AINEs, mesmo em alguns doentes sem compromisso renal. Em doentes com função renal normal, estes efeitos foram atribuídos a um estado hiporeninémico-hipoaldosteronismo.
Reacções Anafilácticas
O potássio oxaprozina tem sido associado a reacções anafilácticas em doentes com e sem hipersensibilidade conhecida à oxaprozina e em doentes com asma sensível à aspirina.
Procure ajuda de emergência se ocorrer uma reacção anafiláctica.
Exacerbação Da Asma Relacionada Com A Sensibilidade À Aspirina
Uma subpopulação de doentes com asma pode ter asma sensível à aspirina que pode incluir rinossinusite crónica complicada por pólipos nasais, broncospasmo grave, potencialmente fatal, e/ou intolerância à aspirina e a outros AINEs. Uma vez que foi notificada reactividade cruzada entre a aspirina e outros AINEs em doentes sensíveis à aspirina, a DAYPRO ALTA está contra-indicada em doentes com esta forma de sensibilidade à aspirina. Quando o DAYPRO ALTA é utilizado em doentes com asma pré-existente (sem sensibilidade conhecida à aspirina), monitorize os doentes quanto a alterações nos sinais e sintomas da asma.
Reacções Cutâneas Graves
Os AINEs, incluindo o potássio oxaprozina, podem causar reacções adversas cutâneas graves, tais como dermatite esfoliativa, síndrome de Stevens-Johnson (SJS) e necrólise epidérmica tóxica (TEN), que podem ser fatais. Estes acontecimentos graves podem ocorrer sem aviso prévio. Informe os doentes sobre os sinais e sintomas de reacções cutâneas graves e interrompa o uso de DAYPRO ALTA no primeiro aparecimento de erupção cutânea ou qualquer outro sinal de hipersensibilidade. DAYPRO ALTA está contra-indicado em doentes com reacções cutâneas graves anteriores aos AINEs.
Encerramento Prematuro Do Canal Arterial Fetal
A oxaprozina pode causar um encerramento prematuro do canal arterial fetal. Evitar a utilização de AINEs, incluindo o DAYPRO ALTA, em mulheres grávidas a partir das 30 semanas de gestação (terceiro trimestre).
Toxicidade Hematológica
Ocorreu Anemia em doentes tratados com AINEs. Isto pode ser devido a perda de sangue oculta ou bruta, retenção de líquidos ou um efeito incompletamente descrito na eritropoiese. Se um doente tratado com DAYPRO ALTA tiver quaisquer sinais ou sintomas de anemia, monitorize a hemoglobina ou o hematócrito.
Os AINEs, incluindo o DAYPRO ALTA, podem aumentar o risco de episódios hemorrágicos. As condições de co-morbilidade tais como alterações da coagulação ou o uso concomitante de varfarina, outros anticoagulantes, antiplaquetários (por exemplo, aspirina), inibidores da recaptação da serotonina (ISRSs) e inibidores da recaptação da serotonina norepinefrina (Isrns) podem aumentar este risco. Monitorize estes doentes quanto a sinais de hemorragia.
Mascaramento Da Inflamação E Da Febre
A actividade farmacológica do DAYPRO ALTA na redução da inflamação, e possivelmente da febre, pode diminuir a utilidade dos sinais diagnósticos na detecção de infecções.
Monitorização Laboratorial
Uma vez que podem ocorrer hemorragias GI graves, hepatotoxicidade e lesões renais sem sintomas de aviso ou sinais, considere a monitorização periódica de doentes em tratamento a longo prazo com AINEs e um perfil químico.
Fotossensibilidade
A oxaprozina tem sido associada a erupção cutânea e / ou fotossensibilidade ligeira nos testes dermatológicos. Nos ensaios clínicos, observou-se um aumento da incidência de erupção cutânea na pele exposta ao sol em alguns doentes.
Informação Do Aconselhamento Do Doente
Aconselhe o paciente a ler a rotulagem aprovada pela FDA do paciente (Guia de medicação) que acompanha cada prescrição dispensada. Informe os doentes, as famílias ou os seus prestadores de cuidados sobre as seguintes informações antes de iniciar a terapêutica com DAYPRO ALTA e periodicamente durante o curso da terapêutica em curso.
Acontecimentos Trombóticos Cardiovasculares
Aconselhe os doentes a estarem alerta para os sintomas de acontecimentos trombóticos cardiovasculares, incluindo dor torácica, falta de ar, fraqueza ou redução da fala, e a comunicarem imediatamente qualquer um destes sintomas ao seu prestador de cuidados de saúde.
Hemorragia Gastrointestinal, Ulceração E Perfuração
Aconselhe os doentes a comunicar ao seu médico os sintomas de ulcerações e hemorragias, incluindo dor epigástrica, dispepsia, melena e hematémese. No contexto do uso concomitante de uma dose baixa de aspirina para profilaxia cardíaca, informe os doentes do aumento do risco e dos sinais e sintomas de hemorragia gastrointestinal.
Hepatotoxicidade
Informe os doentes dos sinais de aviso e sintomas de hepatotoxicidade (por exemplo, náuseas, fadiga, letargia, prurido, diarreia, icterícia, sensibilidade no quadrante superior direito e sintomas de tipo gripal). Se estes ocorrerem, instrua os doentes a pararem o DAYPRO ALTA e a procurarem uma terapêutica médica imediata.
Insuficiência Cardíaca E Edema
Aconselhe os doentes a estarem alerta para os sintomas de insuficiência cardíaca congestiva, incluindo falta de ar, aumento de peso inexplicável ou edema, e a contactarem o seu médico caso ocorram tais sintomas.
Reacções Anafilácticas
Informe os doentes sobre os sinais de reacção anafiláctica (por ex. dificuldade em respirar, inchaço da face ou garganta). Instrua os doentes a procurarem ajuda de emergência imediata caso estas ocorram.
Reacções Cutâneas Graves
Aconselhe os doentes a parar o DAYPRO ALTA imediatamente se desenvolverem qualquer tipo de erupção cutânea e a contactar o seu prestador de cuidados de saúde o mais rapidamente possível.
Fertilidade Feminina
Informe as mulheres com potencial reprodutor que desejam engravidar que os AINEs, incluindo o DAYPRO ALTA, possam estar associados a um atraso reversível na ovulação.
Toxicidade Fetal
Informe as mulheres grávidas para evitar a utilização de DAYPRO ALTA e outros AINEs a partir das 30 semanas de gestação devido ao risco de encerramento prematuro do canal arterial fetal.
Evitar A Utilização Concomitante De AINEs
Informe os doentes que a utilização concomitante de DAYPRO ALTA com outros AINEs ou salicilatos (p.ex., diflunisal, salsalato) não é recomendada devido ao aumento do risco de toxicidade gastrointestinal, e pouco ou nenhum aumento na eficácia. Alerte os pacientes que os AINEs podem estar presentes em" over the counter " medicamentos para o tratamento de constipações, febre, ou insônia.
Uso de AINEs e aspirina em dose baixa
Informe os doentes a não tomarem doses baixas de aspirina concomitantemente com DAYPRO ALTA até falarem com o seu profissional de saúde.
Toxicologia Não Clínica
Carcinogénese, Mutagénese, Diminuição Da Fertilidade
Carcinogénese
Em estudos de carcinogenicidade em ratos e camundongos, oxaprozin de administração de 2 anos foi associado com a piora das neoplasias do fígado (hepática adenomas e carcinomas) no sexo masculino CD ratos, mas não em fêmeas de CD camundongos ou ratos tratados com até 216 mg/kg de peso através da dieta (de 1,2 vezes a máxima dose diária humana recomendada de 1800 mg com base na superfície corporal. Desconhece-se o Significado desta descoberta específica para o homem.
Mutagénese
A oxaprozina não genotóxica no teste de Ames, mutação para a frente em células de ovário de levedura e hamster chinês (CHO), testes de reparação de ADN em células CHO, testes de micronúcleos na medula óssea de ratinho, testes de aberração cromossómica em linfócitos humanos ou testes de transformação celular em fibroblastos de ratinho.
Diminuição Da Fertilidade
Oxaprozin administração não foi associada com diminuição da fertilidade em ratos machos e fêmeas em doses orais de até 200 mg/kg/dia (1.1-vezes a máxima dose diária humana recomendada [MRHD] de 1800 mg com base na área de superfície corporal de comparação). No entanto, observou-se degeneração testicular em cães beagle tratados com 37, 5 mg/kg/dia (0, 7 vezes a DMRH com base na área de superfície corporal) de oxaprozina durante 42 dias ou 6 meses, uma constatação não confirmada noutras espécies. Desconhece-se a relevância clínica deste resultado.
Utilização Em Populações Específicas
Gravidez
Resumo Do Risco
A utilização de AINEs, incluindo DAYPRO ALTA, durante o terceiro trimestre de gravidez aumenta o risco de encerramento prematuro do canal arterial fetal. Evitar a utilização de AINEs, incluindo o DAYPRO ALTA, em mulheres grávidas a partir das 30 semanas de gestação (terceiro trimestre).
Não existem estudos adequados e bem controlados com DAYPRO ALTA em mulheres grávidas.
Os dados de estudos observacionais relativos aos potenciais riscos embriofetais da utilização de AINE em mulheres no primeiro ou segundo trimestres de gravidez são inconclusivos.. No geral U.S. a população, todas as gravidezes clinicamente reconhecidas, independentemente da exposição ao fármaco, apresentam uma taxa de antecedentes de 2-4% de malformações major e de 15-20% de perda de gravidez.. Em estudos de reprodução em animais, administração oral de oxaprozina a coelhas grávidas em doses 0.1-vezes a dose humana diária máxima (com base na área de superfície corporal) resultou em evidência de teratogenicidade, no entanto, a administração oral de oxaprozin para grávidas camundongos e ratos durante a organogénese em doses equivalentes à dose humana máxima recomendada não revelaram qualquer evidência de teratogenicidade ou embryotoxicity. Em estudos de reprodução em ratos nos quais a oxaprozina foi administrada na fase final da gestação, não se verificou o parto e observou-se uma redução no índice de nascimentos vivos com doses equivalentes à dose máxima recomendada no ser humano.. Com base em dados em animais, as prostaglandinas demonstraram ter um papel importante na permeabilidade vascular endometrial, implantação de blastocist e decidualização.. Em estudos em animais, a administração de inibidores da síntese das prostaglandinas, tais como o potássio oxaprozina, resultou num aumento da perda pré e pós - implantação.
Considerações Clínicas
Trabalho ou entrega
Não existem estudos sobre os efeitos do DAYPRO ALTA durante o parto ou parto. Em estudos em animais, os AINEs, incluindo o potássio oxaprozina, inibem a síntese das prostaglandinas, causam atraso no parto e aumentam a incidência de nados-mortos.
Dado
Animal
Teratologia estudos com oxaprozin de potássio foram realizados em camundongos, ratos e coelhos fêmeas gestantes administrado via oral em doses de até 200 mg/kg/dia, 200 mg/kg/dia, e 30 mg/kg/dia, respectivamente, durante o período de organogénese. Em coelhos, observaram-se malformações com doses superiores ou iguais a 7.5 mg/kg/dia de oxaprozina (0.1 vezes a dose diária máxima recomendada em seres humanos de 1800 mg, com base na área de superfície corporal). No entanto, em ratinhos e ratos, não foram observadas alterações no desenvolvimento relacionadas com o fármaco ou toxicidade embrionária e fetal com doses até 50 e 200 mg/kg/dia de oxaprozina, respectivamente (0.1-vezes e 1.1 vezes o MRHD baseado na área de superfície corporal, respectivamente)
Em fertilidade/reprodutiva, estudos em ratos, a 200 mg/kg/dia oxaprozin foi administrada por via oral a ratas durante os 14 dias prévios ao acasalamento, através de lactação dia (LD) 2, ou a partir do dia de gestação (DG) 15 LD 2 e as fêmeas eram de acasalar com machos tratados com 200 mg/kg/dia oxaprozin para 60 dias antes do acasalamento. A administração de oxaprozina resultou na falência do parto e numa redução do Índice de nascimentos vivos de 200 mg/kg/dia (1, 1 vezes o MRHD com base na comparação da área de superfície corporal).
Lactacao
Resumo Do Risco
Lactação não foram realizados estudos com Daypro Alta. Desconhece-se se o Daypro Alta é excretado no leite humano. Daypro Alta só deve ser administrado a mulheres lactantes se claramente indicado. Os benefícios para o desenvolvimento e a saúde da amamentação devem ser considerados juntamente com a necessidade clínica da mãe de DAYPRO ALTA e quaisquer potenciais efeitos adversos para o lactente amamentado a partir do DAYPRO ALTA ou da condição materna subjacente.
Mulheres E Homens Com Potencial Reprodutor
Infertilidade
Mulher
Com base no mecanismo de acção, a utilização de AINEs mediados pela prostaglandina, incluindo o DAYPRO ALTA, pode atrasar ou prevenir a ruptura dos folículos ováricos, que tem sido associada a infertilidade reversível em algumas mulheres. Estudos em animais publicados demonstraram que a administração de inibidores da síntese das prostaglandinas tem o potencial de perturbar a ruptura folicular mediada pela prostaglandina necessária para a ovulação. Pequenos estudos em mulheres tratadas com AINEs demonstraram também um atraso reversível na ovulação. Considerar a retirada dos AINEs, incluindo DAYPRO ALTA, em mulheres que têm dificuldades em conceber ou que estão a ser submetidas a investigação de infertilidade.
Homem
Observou-se degeneração Testicular em cães beagle tratados com 37, 5 mg/kg/dia (0, 7 vezes a dose diária máxima recomendada no ser humano, com base na área de superfície corporal) de oxaprozina durante 42 dias ou 6 meses.
Uso Pediátrico
O DAYPRO ALTA não foi investigado em doentes com menos de 16 anos de idade. A segurança e eficácia do DAYPRO ALTA em doentes pediátricos não foram estabelecidas.
Uso Geriátrico
Os doentes idosos, em comparação com os doentes mais jovens, apresentam maior risco de reacções adversas cardiovasculares, gastrointestinais e/ou renais graves associadas a a AINEs. Se os benefícios previstos para o doente idoso superarem estes potenciais riscos, inicie a administração na extremidade inferior do intervalo posológico e monitorize os doentes quanto aos efeitos adversos.
A idade não demonstrou ter um efeito na farmacocinética do DAYPRO ALTA após 600, 1200 e 1800 doses de tapete ou na incidência de reacções adversas notificadas. Num ensaio clínico controlado de 6 meses com 803 doentes (322 dos quais receberam DAYPRO ALTA), cerca de 40% dos quais eram idosos, não foi detectada basicamente qualquer diferença em termos do número total de indivíduos que notificaram acontecimentos adversos relativamente à idade. Tal como com qualquer AINE, é provável que os idosos tolerem menos bem as reacções adversas do que os doentes mais jovens. Deve ter-se precaução no tratamento de idosos (com idade igual ou superior a 65 anos) e deve ter-se um cuidado extra quando se escolhe uma dose.
A oxaprozina é substancialmente excretada pelos rins, e o risco de reacções tóxicas ao DAYPRO ALTA pode ser maior em doentes com compromisso da função renal. Uma vez que é mais provável que os doentes idosos tenham uma função renal diminuída, deve ter-se cuidado na selecção da dose, e pode ser útil monitorizar a função renal.

SECUNDARIO
As seguintes reacções adversas são discutidas em maior detalhe noutras secções da rotulagem:
- Contactos Trombóticos Cardiovasculares
- Hemorragia gastrointestinal, ulceração e Perfuração
- Hepatotoxicidade
- Hipertensao
- Insuficiência cardíaca e Edema
- Toxidade Renal e hipercaliemia
- Reacções Anafiláticas
- Reactões Cutâneas Graves
- Toxicidade Hematológica
Experiência Em Ensaios Clínicos
Uma vez que os ensaios clínicos são realizados em condições muito variáveis, as taxas de reacções adversas observadas nos ensaios clínicos de um fármaco não podem ser directamente comparadas com as taxas dos ensaios clínicos de outro fármaco e podem não reflectir as taxas observadas na prática.
Em doentes a tomar DAYPRO ALTA (comprimidos de potássio de oxaprozina), oxaprozina ou outros AINEs, as seguintes reacções adversas notificadas mais frequentemente ocorreram em aproximadamente 1-10% dos doentes: :
Experiências gastrintestinais, incluindo: dor abdominal, anorexia, obstipação, diarreia, dispepsia, flatulência, hemorragia/perfuração gastrointestinal grosseira, úlceras GI (gástrica/duodenal), azia, náuseas, vómitos.
Experiências não gastrintestinais, incluindo: função renal anormal, anemia, confusão, depressão, perturbação do sono, tonturas, disúria ou frequência, edema, elevação das enzimas hepáticas, dores de cabeça, aumento do tempo de hemorragia, prurido, erupções cutâneas, sedação, sonolência, zumbido.
Reacções Adversas Adicionais Notificadas Em Menos De 1% Dos Doentes:
Corpo como um todo: reacções anafilácticas, alterações do apetite, morte, febre, infecção, sépsis, doença do soro.
Sistema Cardiovascular: arritmia, alterações da pressão arterial, insuficiência cardíaca congestiva, hipertensão, hipotensão, enfarte do miocárdio, palpitações, síncope, taquicardia, vasculite.
Sistema digestivo: Alteração do paladar, boca seca, eructação, esofagite, gastrite, glossite, hematémese, hemorragia hemoidal ou rectal, hepatite, icterícia, falência hepática, pancreatite, estomatite.
Doenças do sangue e do sistema linfático: agranulocitose, anemia aplástica, equimoses, eosinofilia, anemia hemolítica, leucopenia, linfadenopatia, melena, pancitopenia, púrpura, trombocitopenia.
Metabolismo e nutrição: hiperglicemia, alterações de peso.
Nervosocity in Italy: ansiedade, astenia, coma, convulsões, anomalias dos sonhos, sonolência, alucinações, insónia, mal-estar, meningite, nervosismo, parestesia, tremores, vertigens, fraqueza.
Sistema respiratório: asma, dispneia, pneumonia, infecções pulmonares, depressão respiratória, sinusite, sintomas de infecção do tracto respiratório superior.
Pelé e anexos: alopecia. angioedema, aumento da sudação, fotossensibilidade, pseudoporfiria, dermatite exfoliativa, eritema multiforme, Síndrome de Stevens-Johnson, necrólise epidérmica tóxica (lyell'Syndrome), urticária.
Sentidos especiais: visão turva, conjuntivite, diminuição da audição.
Sistema Urogenital: aguda, nefrite intersticial, insuficiência renal aguda, cistite, diminuição do fluxo menstrual, hematúria, aumento do fluxo menstrual, síndrome nefrótica, oligúria/poliúria, proteinúria, insuficiência renal.
INTERACCAO
Ver Tabela 1 para interacções medicamentosas clinicamente significativas com oxaprozina potássio.
Tabela 1: intervenções médicas clinicamente significativas com Oxaprozina potássio
| Medicamentos que interferem com a hemostase | |
| Impacto Clínico: |
|
| Intervencao: | Monitorar os dentes com o uso concomitante de DAYPRO ALTA com anticoagulantes (p.ex. varfarina), antiplaquetários (p.ex. aspirina), inibidores selectivos da recaptação da serotonina (ISRSs) e inibidores selectivos da recaptação da serotonina norepinefrina (Isrns) para sinais de hemorragia. |
| Aspirina | |
| Impacto Clínico: | Estudos clínicos controlados mostraram que o uso concomitante de AINEs e doses analgésicas de aspirina não produz qualquer efeito terapêutico superior ao uso de AINEs em monoterapia. Num estudo clínico, o uso concomitante de um AINE e aspirina foi associado a um aumento significativo da incidência de reacções adversas GI em comparação com o uso do Aine em monoterapia. |
| Intervencao: | O uso concomitante de DAYPRO ALTA e doses analgésicas de aspirina não é geralmente recomendado devido ao aumento do risco de hemorragia. O DAYPRO ALTA não é um substituto da aspirina de dose baixa para a protecção cardiovascular. |
| Inibidores da ECA, bloqueadores dos receptores da angiotensina e beta-bloqueadores | |
| Impacto Clínico: |
|
| Intervencao: |
|
| Diuréticos | |
| Impacto Clínico: | Estudos clínicos, bem como observações pós-comercialização, demonstram que os AINEs refutiram o efeito natriurético dos diuréticos da ansa (por ex., furosemida) e dos diuréticos tiazídicos em alguns doentes. Este efeito foi atribuído à aquisição dos bovinos da Suécia das prostaglandinas renais. |
| Intervencao: | Durante a utilização concomitante de DAYPRO ALTA com diuréticos, os doentes observam sinais de agravamento da função renal, para além de assegurarem uma eficácia diurética, incluindo efeitos anti-hipertensores. |
| Digoxina | |
| Impacto Clínico: | Foi notificado o uso concomitante de oxaprozina potássio com digoxina para aumentar a concentração sérica e prolongar uma semi-vida da digoxina. |
| Intervencao: | Durante a utilização concomitante de DAYPRO ALTA e digoxina, monitorar os níveis sírios de digoxina. |
| Litio | |
| Impacto Clínico: | Os bovinos produzem quantidades nos niveismáticos de leite e reduções na depuração renal do leite. A concentração mínima média de leite aumentou 15% e a diminuição renal diminuiu aproximadamente 20%. Este efeito foi atribuído à aquisição dos bovinos da Suécia das prostaglandinas renais. |
| Intervencao: | Durante a utilização concomitante de DAYPRO ALTA e láctio, os doentes devem monitorar os sinais de toxicidade pelo lítio. |
| Metotrexato | |
| Impacto Clínico: | A utilização concomitante de AINEs e metotrexato pode aumentar o risco de toxicidade do metotrexato (p.ex. neutropenia, trombocitopenia, disfunção renal) porque a administração de AINEs pode resultar num aumento dos níveis plasmáticos fazer metotrexato, especialmente em doentes a receber doses elevadas de metotrexato. |
| Intervencao: | Durante a utilização concomitante de DAYPRO ALTA e metotrexato, os doentes devem monitorar a toxicidade do metotrexato. |
| Ciclosporina | |
| Impacto Clínico: | O uso concomitante de DAYPRO ALTA e ciclosporina pode aumentar a nefrotoxicidade da ciclosporina. |
| Intervencao: | Durante a utilização concomitante de DAYPRO ALTA e ciclosporina, os doentes devem ser monitorizados relativamente a sinais de agravamento da função renal. |
| AINEs e salicilatos | |
| Impacto Clínico: | O uso concomitante de oxaprozina potássio com outros AINEs ou salicilatos (por ex., diflunisal, salsalato) aumenta o risco de toxicidade GI, com um pequeno ou nenhum aumento na eficácia. |
| Intervencao: | Não se recomenda o uso concomitante de oxaprozina potássio com outros AINEs ou salicilatos. |
| Pemetrexedo | |
| Impacto Clínico: | A utilização concomitante de DAYPRO ALTA e pemetrexedo pode aumentar o risco de mielossupressão associada uma pemetrexedo, toxicidade renal e GASTROINTESTINAL (ver informação sobre prescrição de pemetrexedo). |
| Intervencao: | Durante a utilização concomitante de DAYPRO ALTA e pemetrexedo, em doentes com insuficiência renal, cuja depuração da creatinina varia entre 45 e 79 mL/min, deve monitorizar-se a mielossupressão e a toxicidade renal e GASTROINTESTINAL. Os AINEs com semi-vidas de eliminação curtas (por exemplo, diclofenaco, indometacina) devem ser evitados durante um período de dois dias antes, no dia e dois dias após a administração de pemetrexedo. Na ausência de dados relativos à potencial interacção entre o pemetrexedo e os AINEs com meias-vidas mais longas (por exemplo, meloxicam, nabumetona), os doentes a tomar estes AINEs devem interromper a administração durante, pelo menos, cinco dias antes, no dia e dois dias após a administração de pemetrexedo. |
| Corticoides | |
| Impacto Clínico: | O uso concomitante de corticosteroides com DAYPRO ALTA pode aumentar o risco de ulceração ou hemorragia gastrointestinal. |
| Intervencao: | Monitorar os doentes com utilização concomitante de DAYPRO ALTA com corticosteróides para sinais de hemorragia. |
| Gliburida | |
| Impacto Clínico: | Embora um oxaprozina altere a farmacocinética da gliburida, uma co-administração da oxaprozina um diabéticos tipo II não dependem de insulina não afetou a área sob a curva de concentração de glicose nem a magnitude uo duração fazer o controlo. |
| Intervencao | Durante a utilização concomitante de DAYPRO ALTA e gliburida, monitorizar a glucose sanguínea dos dentes na fase inicial da coterapia. |
Interacções Nos Ensaios Laboratoriais
Foram notificados testes de imunoensaio falsos positivos para detecção de benzodiazepinas na urina em doentes a tomar oxaprozina. Isto deve-se à falta de especificidade dos testes de rastreio. Podem esperar-se resultados falsos-positivos durante vários dias após a interrupção da terapêutica com oxaprozina. Testes de confirmação, tais como cromatografia gasosa/espectrometria de massa, Irão distinguir a oxaprozina das benzodiazepinas.

Resumo Do Risco
A utilização de AINEs, incluindo DAYPRO ALTA, durante o terceiro trimestre de gravidez aumenta o risco de encerramento prematuro do canal arterial fetal. Evitar a utilização de AINEs, incluindo o DAYPRO ALTA, em mulheres grávidas a partir das 30 semanas de gestação (terceiro trimestre).
Não existem estudos adequados e bem controlados com DAYPRO ALTA em mulheres grávidas.
Os dados de estudos observacionais relativos aos potenciais riscos embriofetais da utilização de AINE em mulheres no primeiro ou segundo trimestres de gravidez são inconclusivos.. No geral U.S. a população, todas as gravidezes clinicamente reconhecidas, independentemente da exposição ao fármaco, apresentam uma taxa de antecedentes de 2-4% de malformações major e de 15-20% de perda de gravidez.. Em estudos de reprodução em animais, administração oral de oxaprozina a coelhas grávidas em doses 0.1-vezes a dose humana diária máxima (com base na área de superfície corporal) resultou em evidência de teratogenicidade, no entanto, a administração oral de oxaprozin para grávidas camundongos e ratos durante a organogénese em doses equivalentes à dose humana máxima recomendada não revelaram qualquer evidência de teratogenicidade ou embryotoxicity. Em estudos de reprodução em ratos nos quais a oxaprozina foi administrada na fase final da gestação, não se verificou o parto e observou-se uma redução no índice de nascimentos vivos com doses equivalentes à dose máxima recomendada no ser humano.. Com base em dados em animais, as prostaglandinas demonstraram ter um papel importante na permeabilidade vascular endometrial, implantação de blastocist e decidualização.. Em estudos em animais, a administração de inibidores da síntese das prostaglandinas, tais como o potássio oxaprozina, resultou num aumento da perda pré e pós - implantação.
Considerações Clínicas
Trabalho ou entrega
Não existem estudos sobre os efeitos do DAYPRO ALTA durante o parto ou parto. Em estudos em animais, os AINEs, incluindo o potássio oxaprozina, inibem a síntese das prostaglandinas, causam atraso no parto e aumentam a incidência de nados-mortos.
Dado
Animal
Teratologia estudos com oxaprozin de potássio foram realizados em camundongos, ratos e coelhos fêmeas gestantes administrado via oral em doses de até 200 mg/kg/dia, 200 mg/kg/dia, e 30 mg/kg/dia, respectivamente, durante o período de organogénese. Em coelhos, observaram-se malformações com doses superiores ou iguais a 7.5 mg/kg/dia de oxaprozina (0.1 vezes a dose diária máxima recomendada em seres humanos de 1800 mg, com base na área de superfície corporal). No entanto, em ratinhos e ratos, não foram observadas alterações no desenvolvimento relacionadas com o fármaco ou toxicidade embrionária e fetal com doses até 50 e 200 mg/kg/dia de oxaprozina, respectivamente (0.1-vezes e 1.1 vezes o MRHD baseado na área de superfície corporal, respectivamente)
Em fertilidade/reprodutiva, estudos em ratos, a 200 mg/kg/dia oxaprozin foi administrada por via oral a ratas durante os 14 dias prévios ao acasalamento, através de lactação dia (LD) 2, ou a partir do dia de gestação (DG) 15 LD 2 e as fêmeas eram de acasalar com machos tratados com 200 mg/kg/dia oxaprozin para 60 dias antes do acasalamento. A administração de oxaprozina resultou na falência do parto e numa redução do Índice de nascimentos vivos de 200 mg/kg/dia (1, 1 vezes o MRHD com base na comparação da área de superfície corporal).

As seguintes reacções adversas são discutidas em maior detalhe noutras secções da rotulagem:
- Contactos Trombóticos Cardiovasculares
- Hemorragia gastrointestinal, ulceração e Perfuração
- Hepatotoxicidade
- Hipertensao
- Insuficiência cardíaca e Edema
- Toxidade Renal e hipercaliemia
- Reacções Anafiláticas
- Reactões Cutâneas Graves
- Toxicidade Hematológica
Experiência Em Ensaios Clínicos
Uma vez que os ensaios clínicos são realizados em condições muito variáveis, as taxas de reacções adversas observadas nos ensaios clínicos de um fármaco não podem ser directamente comparadas com as taxas dos ensaios clínicos de outro fármaco e podem não reflectir as taxas observadas na prática.
Em doentes a tomar DAYPRO ALTA (comprimidos de potássio de oxaprozina), oxaprozina ou outros AINEs, as seguintes reacções adversas notificadas mais frequentemente ocorreram em aproximadamente 1-10% dos doentes: :
Experiências gastrintestinais, incluindo: dor abdominal, anorexia, obstipação, diarreia, dispepsia, flatulência, hemorragia/perfuração gastrointestinal grosseira, úlceras GI (gástrica/duodenal), azia, náuseas, vómitos.
Experiências não gastrintestinais, incluindo: função renal anormal, anemia, confusão, depressão, perturbação do sono, tonturas, disúria ou frequência, edema, elevação das enzimas hepáticas, dores de cabeça, aumento do tempo de hemorragia, prurido, erupções cutâneas, sedação, sonolência, zumbido.
Reacções Adversas Adicionais Notificadas Em Menos De 1% Dos Doentes:
Corpo como um todo: reacções anafilácticas, alterações do apetite, morte, febre, infecção, sépsis, doença do soro.
Sistema Cardiovascular: arritmia, alterações da pressão arterial, insuficiência cardíaca congestiva, hipertensão, hipotensão, enfarte do miocárdio, palpitações, síncope, taquicardia, vasculite.
Sistema digestivo: Alteração do paladar, boca seca, eructação, esofagite, gastrite, glossite, hematémese, hemorragia hemoidal ou rectal, hepatite, icterícia, falência hepática, pancreatite, estomatite.
Doenças do sangue e do sistema linfático: agranulocitose, anemia aplástica, equimoses, eosinofilia, anemia hemolítica, leucopenia, linfadenopatia, melena, pancitopenia, púrpura, trombocitopenia.
Metabolismo e nutrição: hiperglicemia, alterações de peso.
Nervosocity in Italy: ansiedade, astenia, coma, convulsões, anomalias dos sonhos, sonolência, alucinações, insónia, mal-estar, meningite, nervosismo, parestesia, tremores, vertigens, fraqueza.
Sistema respiratório: asma, dispneia, pneumonia, infecções pulmonares, depressão respiratória, sinusite, sintomas de infecção do tracto respiratório superior.
Pelé e anexos: alopecia. angioedema, aumento da sudação, fotossensibilidade, pseudoporfiria, dermatite exfoliativa, eritema multiforme, Síndrome de Stevens-Johnson, necrólise epidérmica tóxica (lyell'Syndrome), urticária.
Sentidos especiais: visão turva, conjuntivite, diminuição da audição.
Sistema Urogenital: aguda, nefrite intersticial, insuficiência renal aguda, cistite, diminuição do fluxo menstrual, hematúria, aumento do fluxo menstrual, síndrome nefrótica, oligúria/poliúria, proteinúria, insuficiência renal.

Os sintomas após sobredosagens agudas de AINEs têm sido tipicamente limitados à letargia, sonolência, náuseas, vómitos e dor epigástrica, que têm sido geralmente reversíveis com cuidados de suporte. Ocorreu hemorragia Gastrointestinal. Ocorreram hipertensão, insuficiência renal aguda, depressão respiratória e coma, mas foram raros.
Controlar os doentes com cuidados sintomáticos e de suporte após uma sobredosagem com AINEs. Não há antídotos específicos. Considerar emese e/ou carvão activado (60 a 100 gramas em adultos, 1 a 2 gramas por kg de peso corporal em doentes pediátricos) e / ou catártico osmótico em doentes sintomáticos observados nas quatro horas seguintes à ingestão ou em doentes com sobredosagem grave (5 a 10 vezes a dose recomendada). Diurese forçada, alcalinização da urina, hemodiálise ou hemoperfusão pode não ser útil devido à alta ligação às proteínas.
Para mais informações sobre o tratamento de sobredosagem, contacte um centro de controlo de venenos (1-800-2221222).

Características Farmacocinéticas Gerais
Em estudos de proporcionalidade de dose utilizando doses de 600, 1200 e 1800 mg, a farmacocinética da oxaprozina em indivíduos saudáveis demonstrou cinética não linear do fármaco total e não ligado em direcções opostas, i.e., aumento relacionado com a exposição à dose na depuração total do fármaco e diminuição na depuração do fármaco não ligado. As alterações dependentes da concentração na ligação às proteínas também resultaram em alterações no volume de distribuição da oxaprozina, que aumentou para o fármaco total, mas diminuiu para o fármaco não ligado. . Os parâmetros farmacocinéticos da oxaprozina em indivíduos saudáveis a receber uma dose única ou doses múltiplas de 1200 mg uma vez por dia são apresentados no quadro 2.
Quadro 2. Parâmetros farmacocinéticos da oxaprozina com administração de DAYPRO ALTA (1200 mg) [média (%CV)]
| Adultos saudáveis (18-42 anos, N = 12-24) | ||||
| Total Droga | Droga Não Ligada | |||
| Unico | Varia | Unico | Varia | |
| Tmaximo (hora) | 1.67 (65) | 2.13 (64) | 1.71 (63) | 1.59 (38) |
| Depuração Oral (L / hr / 70 kg)))) | 0.125 (15) | 0.289 (17) | 123 (20) | 86.7 (33) |
| Volume de distribuição aparentemente no estado Diário (Vd/F, L / 70 kg)) | 10.14 (11) | 16.24 (38) | 7741 (18) | 2067 (38) |
| Eliminação) | 57.0 (15) | 38.0 (29) | 44.8 (23) | 16.4 (11) |
| Tmaximo = tempo para atingir a concentração plasmática máxima de oxaprozina. |
Absorcao
Após administração oral, a DAYPRO ALTA dissocia-se em oxaprozina livre, que é 95% absorvida. A concentração plasmática máxima ocorre cerca de 1 hora e 45 minutos após a administração de uma dose única (Ver Tabela 2). Quando o DAYPRO ALTA é administrado com alimentos, a concentração máxima de oxaprozina é retardada em cerca de 45 minutos, mas a extensão da absorção mantém-se inalterada. Os antiácidos não afectam significativamente a extensão e a taxa de absorção da oxaprozina.
Distribuicao
O volume de distribuição aparente (Vd/F) da oxaprozina total é de aproximadamente 10-16 L/70 kg.. Oxaprozina o potássio liga-se 99% às proteínas plasmáticas, principalmente à albumina. Em concentrações terapêuticas do fármaco, a ligação da oxaprozina às proteínas plasmáticas é saturável, resultando numa proporção mais elevada do fármaco livre à medida que a concentração total do fármaco é aumentada.. Com o aumento de doses únicas ou após doses diárias repetitivas, o volume aparente de distribuição e depuração do fármaco total aumentou, enquanto que o fármaco não ligado diminuiu devido aos efeitos da ligação às proteínas não lineares.. Prevê-se que a oxaprozina seja excretada no leite humano com base nas suas propriedades físico-químicas, no entanto, a quantidade de oxaprozina excretada no leite materno não foi avaliada.
Metabolismo
Considera-se que vários metabolitos da oxaprozina excretados na urina humana ou nas fezes não têm actividade farmacológica significativa. A oxaprozina é principalmente metabolizada pelo fígado, por oxidação microssómica (65%) e conjugação do ácido glucurónico (35%). Éster e éter glucuronidos são os principais metabolitos conjugados da oxaprozina. Produz-se uma pequena quantidade (<5%) de metabolitos fenólicos activos, mas a contribuição para a actividade global é limitada.
Excrecao
Sessenta e cinco por cento (65%) da dose é excretada na urina e 35% nas fezes como metabolitos. A eliminação Renal dos metabolitos da oxaprozina é uma das principais vias de eliminação. A excreção biliar da oxaprozina inalterada é uma via menor. Depois de várias doses de DAYPRO ALTA (1200 mg QD), pós-estado estacionário significa a eliminação meia-vida de total oxaprozin e proteína independente oxaprozin foram 38.0 e 16,4 horas, respectivamente (ver Tabela 2).
However, we will provide data for each active ingredient


