

Kompozisyon:
Tedavide kullanılır:
Oliinyk Elizabeth Ivanovna tarafından tıbbi olarak gözden geçirilmiştir, Eczane Son güncelleme: 10.04.2022

Dikkat! Sayfadaki bilgiler sadece sağlık profesyonelleri içindir! Bilgi kamu kaynaklarında toplanır ve anlamlı hatalar içerebilir! Dikkatli olun ve bu sayfadaki tüm bilgileri tekrar kontrol edin!


Dozaj Formları ve Güçlü Yönleri
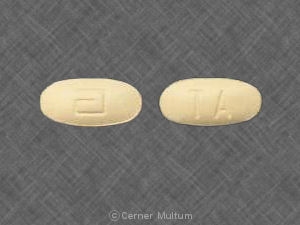
- 54 mg sarı tablet, “a” logosu ve kod tanımlama harfleri "TA" ile basılmıştır.
- 160 mg beyaz tablet, “a” logosu ve kod tanımlama harfleri "TC" ile basılmıştır.
Depolama ve Taşıma
TRICOR® (fenofibrat tabletleri) iki güçte mevcuttur:
54 mg "a" logosu ve kod tanımlama harfleri "TA" ile basılmış sarı tabletler, 90'lık şişelerde mevcuttur (NDC 0074-4009-90).
160 mg 90 (3) şişelerde bulunan “a” logosu ve kod tanımlama harfleri "TC" ile basılmış beyaz tabletlerNDC 0074-4013-90).
Depolama
25 ° C'de (77 ° F) saklayın; 15-30 ° C'ye (59-86 ° F) izin verilen geziler.
Çocukların ulaşabileceği yerlerden uzak tutun. Nemden koruyun.
Üretici: Laboratoires Fournier, S.A., 21300 Chenôve, Fransa. Revize: Ocak 2017.

Primer Hiperkolesterolemi veya Karışık Dislipidemi
TRICOR, yüksek düşük yoğunluklu lipoprotein kolesterolü (LDL-C), toplam kolesterol (Total-C), Trigliseritler ve apolipoprotein B'yi (Apo B) azaltmak ve yüksek yoğunluklu lipoprotein kolesterolü (HDL- C) primer hiperkolesterolemi veya karışık dislipidemili yetişkin hastalarda.
Şiddetli Hipertrigliseridemi
TRICOR ayrıca şiddetli hipertrigliseridemi olan yetişkin hastaların tedavisi için diyete yardımcı tedavi olarak endikedir. Açlık şilomikronemi gösteren diyabetik hastalarda glisemik kontrolün iyileştirilmesi genellikle farmakolojik müdahale ihtiyacını ortadan kaldıracaktır.
Belirgin derecede yüksek serum trigliseritleri (ör. > 2.000 mg / dL) pankreatit gelişme riskini artırabilir. Fenofibrat tedavisinin bu riski azaltma üzerindeki etkisi yeterince araştırılmamıştır.
Önemli Kullanım Sınırlamaları
160 mg TRICOR'a eşdeğer bir dozda fenofibratın, tip 2 diyabetes mellituslu hastaların büyük, randomize kontrollü bir çalışmasında koroner kalp hastalığı morbiditesini ve mortalitesini azalttığı gösterilmemiştir.

Genel Düşünceler
TRICOR almadan önce hastalar uygun bir lipit düşürücü diyete konulmalı ve TRICOR ile tedavi sırasında bu diyete devam etmelidir. TRICOR tabletleri yemeklerle birlikte verilmeli, böylece ilacın biyoyararlanımını optimize etmelidir.
Dislipidemi için ilk tedavi, lipoprotein anormallik tipine özgü diyet tedavisidir. Aşırı vücut ağırlığı ve aşırı alkolik alım hipertrigliseridemide önemli faktörler olabilir ve herhangi bir ilaç tedavisinden önce ele alınmalıdır. Fiziksel egzersiz önemli bir yardımcı önlem olabilir. Hipotiroidizm veya diabetes mellitus gibi hiperlipidemiye katkıda bulunan hastalıklar aranmalı ve yeterince tedavi edilmelidir. Östrojen tedavisi, tiazid diüretikleri ve beta-blokerler bazen plazma trigliseritlerinde, özellikle ailesel hipertrigliseridemisi olan hastalarda büyük artışlarla ilişkilidir. Bu gibi durumlarda, spesifik etiyolojik ajanın kesilmesi, hipertrigliserideminin spesifik ilaç tedavisi ihtiyacını ortadan kaldırabilir.
Lipid seviyeleri periyodik olarak izlenmeli ve lipit seviyeleri hedeflenen aralığın önemli ölçüde altına düşerse TRICOR dozunun azaltılmasına dikkat edilmelidir.
İki aylık tedaviden sonra günde bir kez önerilen maksimum 160 mg doz ile yeterli yanıtı olmayan hastalarda tedavi geri çekilmelidir.
Primer Hiperkolesterolemi veya Karışık Dislipidemi
TRICOR'un başlangıç dozu günde bir kez 160 mg'dır.
Şiddetli Hipertrigliseridemi
Başlangıç dozu günde 54 ila 160 mg'dır. Dozaj hasta yanıtına göre kişiselleştirilmeli ve gerekirse 4 ila 8 haftalık aralıklarla tekrarlanan lipit tespitlerinden sonra ayarlanmalıdır. Maksimum doz günde bir kez 160 mg'dır.
Bozulmuş Böbrek Fonksiyonu
TRICOR ile tedavi, hafif ila orta derecede bozulmuş böbrek fonksiyonuna sahip hastalarda günde 54 mg'lık bir dozda başlatılmalı ve sadece bu dozda böbrek fonksiyonu ve lipit seviyeleri üzerindeki etkilerin değerlendirilmesinden sonra arttırılmalıdır. Şiddetli böbrek yetmezliği olan hastalarda TRICOR kullanımından kaçınılmalıdır.
Geriatrik Hastalar
Yaşlılar için doz seçimi böbrek fonksiyonu temelinde yapılmalıdır.

TRICOR kontrendikedir:
- diyaliz alanlar da dahil olmak üzere ciddi böbrek yetmezliği olan hastalar.
- primer biliyer sirozlu olanlar da dahil olmak üzere aktif karaciğer hastalığı olan hastalar ve açıklanamayan kalıcı karaciğer fonksiyon anormallikleri.
- önceden var olan safra kesesi hastalığı olan hastalar.
- emziren anneler
- fenofibrat veya fenofibrik aside aşırı duyarlılığı olduğu bilinen hastalar.

UYARILAR
Bir parçası olarak dahil "KORUMALAR" Bölüm
ÖNLEMLER
Ölüm ve Koroner Kalp Hastalığı Morbidite
TRICOR'un koroner kalp hastalığı morbiditesi ve mortalitesi ve kardiyovasküler olmayan mortalite üzerindeki etkisi belirlenmemiştir.
Diyabet Lipidinde Kardiyovasküler Riski Kontrol Etme Eylemi (ACCORD Lipid) çalışması, fenofibrat ile tedavi edilen arka plan statin tedavisi üzerine tip 2 diabetes mellituslu 5518 hastanın randomize plasebo kontrollü bir çalışmasıydı. Ortalama takip süresi 4.7 yıldı. Fenofibrat artı statin kombinasyon tedavisi, ölümcül olmayan miyokard enfarktüsü, ölümcül olmayan inme ve kardiyovasküler hastalık ölümünün bir bileşimi olan majör advers kardiyovasküler olayların (MACE) birincil sonucunda anlamlı olmayan% 8 göreceli risk azalması gösterdi (tehlike oranı [ HR ] 0.92,% 95 CI 0.79-1.08) (p = = 0). Cinsiyet alt grup analizinde, statin monoterapisine karşı kombinasyon tedavisi alan erkeklerde MACE için tehlike oranı 0.82 (% 95 CI 0.69-0.99) ve statin monoterapisine karşı kombinasyon tedavisi alan kadınlarda MACE için tehlike oranı 1.38 (% 95 CI) idi. 0.98-1.94) (etkileşim p = 0.01). Bu alt grup bulgusunun klinik önemi belirsizdir.
Diyabette Fenofibrat Müdahalesi ve Olay Düşürme (FIELD) çalışması, fenofibrat ile tedavi edilen tip 2 diyabetes mellituslu 9795 hastanın 5 yıllık randomize, plasebo kontrollü bir çalışmasıydı. Fenofibrat, koroner kalp hastalığı olaylarının birincil sonucunda anlamlı olmayan% 11 göreceli azalma (tehlike oranı [HR] 0.89,% 95 CI 0.75-1.05, p = 0.16) ve toplamın ikincil sonucunda% 11 oranında önemli bir azalma gösterdi. kardiyovasküler hastalık olayları (HR 0.89 [0.80-0). Toplam ve koroner kalp hastalığı mortalitesinde sırasıyla% 11 (HR 1.11 [0.95, 1.29], p = 0.18) ve% 19 (HR 1.19 [0.90, 1.57], p = 0.22) artış vardı. plaseboya kıyasla fenofibrat.
TRICOR (fenofibrat tabletleri), klofibrat ve gemfibrozil arasındaki kimyasal, farmakolojik ve klinik benzerlikler nedeniyle, bu diğer fibrat ilaçlarla yapılan 4 büyük randomize, plasebo kontrollü klinik çalışmada olumsuz bulgular TRICOR için de geçerli olabilir
Klofibrat ile 5 yıl tedavi edilen hastaların miyokard enfarktüsü sonrası büyük bir çalışma olan Koroner İlaç Projesi'nde, klofibrat grubu ile plasebo grubu arasında mortalite farkı görülmemiştir. Bununla birlikte, iki grup arasında ameliyat gerektiren kolelitiaz ve kolesistit oranında bir fark vardı (% 3.0'a karşı. % 1.8).
Dünya Sağlık Örgütü (WHO) tarafından yapılan bir çalışmada, bilinen koroner arter hastalığı olmayan 5000 denek 5 yıl boyunca plasebo veya klofibrat ile tedavi edildi ve bir yıl daha takip edildi. Klofibrat grubunda plasebo grubuna kıyasla istatistiksel olarak anlamlı, daha yüksek yaş ayarlı tüm nedenlere bağlı mortalite vardı (% 5.70'e karşı. % 3.96, p = <0.01). Aşırı mortalite, malignite, kolesistektomi sonrası komplikasyonlar ve pankreatit dahil olmak üzere kardiyovasküler olmayan nedenlerde% 33'lük bir artışa bağlıydı. Bu, Koroner İlaç Projesi'nde incelenen klofibrat ile tedavi edilen hastalarda görülen safra kesesi hastalığı riskinin daha yüksek olduğunu doğruladı.
Helsinki Kalp Çalışması, koroner arter hastalığı öyküsü olmayan orta yaşlı erkeklerin büyük (n = 4081) bir çalışmasıydı. Deneklere 5 yıl boyunca plasebo veya gemfibrozil verildi ve daha sonra 3.5 yıl açık uzatma yapıldı. Toplam mortalite gemfibrozil randomizasyon grubunda sayısal olarak daha yüksekti, ancak istatistiksel anlamlılık elde etmedi (p = 0.19, göreceli risk G için% 95 güven aralığı: P = .91-1.64). Gemfibrozil grubunda kanser ölümleri daha yüksek eğilim göstermesine rağmen (p = 0.11), kanserlere (bazal hücreli karsinom hariç) her iki çalışma grubunda da eşit sıklıkta teşhis konuldu. Çalışmanın sınırlı boyutu nedeniyle, herhangi bir nedenden kaynaklanan göreceli ölüm riskinin, Dünya Sağlık Örgütü çalışmasının 9 yıllık takip verilerinde (RR = 1.29) görülenden farklı olmadığı gösterilmiştir.
Helsinki Kalp Çalışması'nın ikincil bir önleme bileşeni, bilinen veya şüphelenilen koroner kalp hastalığı nedeniyle birincil önleme çalışmasından hariç tutulan orta yaşlı erkekleri kaydetti. Deneklere 5 yıl boyunca gemfibrozil veya plasebo verildi. Gemfibrozil grubunda kardiyak ölümler daha yüksek eğilim göstermesine rağmen, bu istatistiksel olarak anlamlı değildi (tehlike oranı 2.2,% 95 güven aralığı: 0.94-5.05). Safra kesesi cerrahisi oranı çalışma grupları arasında istatistiksel olarak anlamlı değildi, ancak gemfibrozil grubunda daha yüksek bir eğilim gösterdi (% 1.9'a karşı. % 0.3, p = 0.07).
İskelet Kası
Fibratlar miyopati riskini arttırır ve rabdomiyoliz ile ilişkilendirilir. Ciddi kas toksisitesi riski yaşlı hastalarda ve diyabet, böbrek yetmezliği veya hipotiroidizmli hastalarda artmaktadır.
Yaygın miyaljileri, kas hassasiyeti veya zayıflığı ve / veya belirgin kreatin fosfokinaz (CPK) seviyeleri olan herhangi bir hastada miyopati düşünülmelidir.
Hastalara, özellikle halsizlik veya ateş eşlik ediyorsa, açıklanamayan kas ağrısı, hassasiyet veya halsizlik bildirmeleri tavsiye edilmelidir. Bu semptomları bildiren hastalarda CPK seviyeleri değerlendirilmeli ve belirgin derecede yüksek CPK seviyeleri ortaya çıkarsa veya miyopati / miyozit şüphesi varsa veya teşhis edilirse TRICOR tedavisi kesilmelidir.
Gözlemsel çalışmalardan elde edilen veriler, fibratlar, özellikle gemfibrozil, bir HMG-CoA redüktaz inhibitörü (statin) ile birlikte uygulandığında rabdomiyoliz riskinin arttığını göstermektedir. Lipid seviyelerindeki daha fazla değişikliğin yararının, bu ilaç kombinasyonunun artan riskinden daha ağır basması muhtemel değilse, kombinasyondan kaçınılmalıdır.
Rabdomiyoliz dahil miyopati vakaları, kolşisin ile birlikte uygulanan fenofibratlarla bildirilmiştir ve fenofibratın kolşisin ile reçete edilirken dikkatli olunmalıdır.
Karaciğer Fonksiyonu
Günde 107 mg ila 160 mg TRICOR'a eşdeğer dozlarda fenofibrat, serum transaminazlarındaki [AST (SGOT) veya ALT (SGPT)] artışlarla ilişkilendirilmiştir. 10 plasebo kontrollü çalışmanın birleştirilmiş analizinde, fenofibrat alan hastaların% 5.3'ünde plasebo ile tedavi edilen hastaların% 1.1'inde normalin üst sınırının> 3 katına yükselir.
Transaminaz tayinleri, tedavinin kesilmesinden sonra veya tedavinin devamı sırasında takip edildiğinde, genellikle normal sınırlara geri dönüş gözlenmiştir. Fenofibrat tedavisine bağlı transaminazlardaki artış insidansı doza bağlı görünmektedir. 8 haftalık doz aralıklı bir çalışmada, günde 107 mg ila 160 mg TRICOR'a eşdeğer dozaj alan hastalarda ALT veya AST yükselmelerinin normalin üst sınırının en az üç katına çıkması% 13 idi ve 54 mg veya daha az TRICOR'a eşdeğer dozaj alanlarda% 0 idi. gün, veya plasebo. Fenofibrat tedavisi ile ilişkili hepatosellüler, kronik aktif ve kolestatik hepatit, haftalar ila birkaç yıl maruziyetten sonra bildirilmiştir. Çok nadir durumlarda, kronik aktif hepatit ile ilişkili siroz bildirilmiştir.
TRICOR ile tedavi süresince serum ALT (SGPT) dahil olmak üzere karaciğer fonksiyonunun temel ve düzenli periyodik olarak izlenmesi ve enzim seviyeleri normal sınırın üç katının üzerinde kalırsa tedavi kesilmelidir.
Serum Kreatinin
Fenofibrat hastalarında serum kreatinininde artış bildirilmiştir. Bu yükselmeler fenofibratın kesilmesinden sonra taban çizgisine dönme eğilimindedir. Bu gözlemlerin klinik önemi bilinmemektedir. TRICOR alan böbrek yetmezliği olan hastalarda böbrek fonksiyonlarını izleyin. TRICOR alan hastalar için yaşlılar ve diyabetli hastalar gibi böbrek yetmezliği riski taşıyan hastalar için böbrek izleme de düşünülmelidir.
Kolelitiazis
Klofibrat ve gemfibrozil gibi fenofibrat, safraya kolesterol atılımını artırabilir ve kolelitiazise yol açabilir. Kolelitiaziden şüpheleniliyorsa, safra kesesi çalışmaları endikedir. Safra taşı bulunursa TRICOR tedavisi kesilmelidir.
Kumarin Antikoagülanları
Protrombin Süresi / Uluslararası Normalleştirilmiş Oranın (PT / INR) uzamasında kumarin tipi antikoagülan etkilerin güçlendirilmesi nedeniyle kumarin antikoagülanları TRICOR ile birlikte verildiğinde dikkatli olunmalıdır. Kanama komplikasyonlarını önlemek için, PT / INR'nin sık izlenmesi ve antikoagülanın doz ayarlaması PT / INR stabilize olana kadar önerilir.
Pankreatit
Fenofibrat, gemfibrozil ve klofibrat alan hastalarda pankreatit bildirilmiştir. Bu olay, şiddetli hipertrigliseridemi, doğrudan ilaç etkisi veya safra yolu taşı veya ortak safra kanalının tıkanmasıyla çamur oluşumu ile aracılık eden ikincil bir fenomen olan hastalarda etkinlik başarısızlığını temsil edebilir.
Hematolojik Değişiklikler
Fenofibrat tedavisine başlandıktan sonra hastalarda hafif ila orta şiddette hemoglobin, hematokrit ve beyaz kan hücresi azalması gözlenmiştir. Bununla birlikte, bu seviyeler uzun süreli uygulama sırasında stabilize olur. Fenofibrat ile tedavi edilen bireylerde trombositopeni ve agranülositoz bildirilmiştir. TRICOR uygulamasının ilk 12 ayında kırmızı ve beyaz kan hücresi sayımlarının periyodik olarak izlenmesi önerilir.
Aşırı duyarlılık Reaksiyonları
Fenofibratlarla tedavi edilen bireylerde Stevens-Johnson sendromu ve hastanın hastaneye yatırılmasını ve steroidlerle tedaviyi gerektiren toksik epidermal nekroliz gibi akut aşırı duyarlılık reaksiyonları bildirilmiştir. Ürtiker 1.1'e karşı görüldü. % 0 ve 1.4'e karşı döküntü. Kontrollü çalışmalarda fenofibrat ve plasebo hastalarının sırasıyla% 0.8'i.
Venotromboembolik Hastalık
FIELD çalışmasında, fenofibratta plasebo ile tedavi edilen gruptan daha yüksek oranlarda pulmoner embolus (PE) ve derin ven trombozu (DVT) gözlenmiştir. FIELD'e kayıtlı 9.795 hastanın plasebo grubunda 4.900 ve fenofibrat grubunda 4.895 vardı. DVT için plasebo grubunda 48 (% 1) ve fenofibrat grubunda 67 (% 1) (p = 0.074); ve PE için plasebo grubunda 32 (% 0.7) ve fenofibrat grubunda 53 (% 1) olay vardı (p = 0.022).
Koroner İlaç Projesi'nde, klofibrat grubunun daha yüksek bir oranı, plasebo grubundan kesin veya şüpheli ölümcül veya ölümcül olmayan pulmoner emboli veya tromboflebit yaşadı (% 5.2'ye karşı. Beş yılda% 3.3; p <0.01).
HDL Kolesterol Seviyelerinde Paradoksal Düşüşler
Fibrat tedavisi ile başlatılan diyabetik ve diyabetik olmayan hastalarda meydana gelen HDL kolesterol düzeylerinde (2 mg / dL kadar düşük) ciddi düşüşlerin pazarlama sonrası ve klinik çalışma raporları vardır. HDL-C'deki azalma, apolipoprotein A1'deki bir azalma ile yansıtılır. Bu azalmanın fibrat tedavisine başlandıktan sonraki 2 hafta ila yıl içinde meydana geldiği bildirilmiştir. HDL-C seviyeleri fibrat tedavisi geri çekilinceye kadar depresyonda kalır; fibrat tedavisinin geri çekilmesine verilen yanıt hızlı ve süreklidir. HDL-C'deki bu azalmanın klinik önemi bilinmemektedir. Fibrat tedavisine başlandıktan sonraki ilk birkaç ay içinde HDL-C seviyelerinin kontrol edilmesi önerilir. Şiddetli depresif bir HDL-C seviyesi tespit edilirse, fibrat tedavisi geri çekilmeli ve HDL-C seviyesi taban çizgisine dönene kadar izlenmeli ve fibrat tedavisi yeniden başlatılmamalıdır.
Klinik Olmayan Toksikoloji
Kanserojenez ve Mutajenez ve Doğurganlığın Bozukluğu
Fenofibratlı sıçanlarda iki diyet karsinojenisite çalışması yapılmıştır. İlk 24 aylık çalışmada, Wistar sıçanlarına, vücut yüzey alanı karşılaştırmalarına (mg) göre önerilen maksimum insan dozunun (MRHD) yaklaşık 0.3, 1 ve 6 katı olan 10, 45 ve 200 mg / kg / gün fenofibrat verildi. / m2). 200 mg / kg / gün dozunda (MRHD'nin 6 katında), her iki cinsiyette de karaciğer karsinomu insidansı önemli ölçüde artmıştır. MRHD'nin 1 ve 6 katında erkeklerde pankreas karsinomlarında istatistiksel olarak anlamlı bir artış gözlenmiştir; erkeklerde MRHD'nin 6 katında pankreas adenomlarında ve iyi huylu testis interstisyel hücre tümörlerinde bir artış gözlenmiştir. Farklı bir sıçan suşunda 24 aylık ikinci bir sıçan karsinojenisite çalışmasında (Sprague-Dawley) 10 ve 60 mg / kg / gün dozları (MRHD'nin 0.3 ve 2 katı) her iki cinsiyette pankreas asinar adenom insidansında önemli artışlar ve MRHD'nin 2 katında erkeklerde testis interstisyel hücre tümörlerinde artışlar üretti
Üç ilacı karşılaştıran sıçanlarda 117 haftalık bir karsinojenisite çalışması yapıldı: fenofibrat 10 ve 60 mg / kg / gün (MHD'nin 0.3 ve 2 katı), klofibrat (400 mg / kg / gün; insan dozunun 2 katı) ve gemfibrozil (250 mg / kg / gün; mg'ye göre insan dozunun 2 katı2 yüzey alanı). Fenofibrat, her iki cinsiyette pankreas asinar adenomlarını arttırdı. Klofibrat erkeklerde hepatosellüler karsinom ve pankreas asinar adenomlarını ve kadınlarda hepatik neoplastik nodülleri arttırdı. Gemfibrozil, erkeklerde ve kadınlarda hepatik neoplastik nodülleri arttırırken, üç ilacın hepsi erkeklerde testis interstisyel hücre tümörlerini arttırdı.
CF-1 farelerinde yapılan 21 aylık bir çalışmada, fenofibrat 10, 45 ve 200 mg / kg / gün (mg / m temelinde MRHD'nin yaklaşık 0.2, 1 ve 3 katı)2 yüzey alanı) MRHD'nin 3 katında her iki cinsiyette karaciğer karsinomlarını önemli ölçüde artırdı. 10, 60 ve 200 mg / kg / gün'de yapılan 18 aylık ikinci bir çalışmada fenofibrat, erkek farelerde karaciğer karsinomlarını ve dişi farelerde karaciğer adenomlarını MRHD'nin 3 katında önemli ölçüde artırdı
Elektron mikroskopisi çalışmaları, sıçanlara fenofibrat uygulanmasını takiben peroksizomal proliferasyon göstermiştir. İnsanlarda peroksizom proliferasyonunu test etmek için yeterli bir çalışma yapılmamıştır, ancak karaciğer biyopsileri aynı kişide tedaviden önce ve sonra karşılaştırıldığında fibrat sınıfının diğer üyeleriyle tedaviden sonra insanlarda peroksizom morfolojisi ve sayılarında değişiklikler gözlenmiştir.
Mutajenez
Fenofibratın aşağıdaki testlerde mutajenik potansiyelden yoksun olduğu gösterilmiştir: Ames, fare lenfoma, kromozomal sapma ve primer sıçan hepatositlerinde planlanmamış DNA sentezi.
Doğurganlığın Bozukluğu
Doğurganlık çalışmalarında sıçanlara oral diyet fenofibrat dozları verildi, erkekler çiftleşmeden 61 gün önce ve dişiler sütten kesilmeden 15 gün önce alındı, bu da 300 mg / kg / gün'e kadar olan dozlarda doğurganlık üzerinde olumsuz bir etkiye neden olmadı (~ 10 kez) MRHD, mg / m'ye göre2 yüzey alanı karşılaştırmaları).
Belirli Popülasyonlarda Kullanın
Gebelik
Gebelik Kategorisi C
Gebe kadınlarda güvenlik belirlenmemiştir. Gebe kadınlarda yeterli ve iyi kontrol edilen fenofibrat çalışması yoktur. Fenofibrat hamilelik sırasında sadece potansiyel fayda fetusun potansiyel riskini haklı çıkarsa kullanılmalıdır.
Sütten kesilmeden 15 gün önce 15, 75 ve 300 mg / kg / gün fenofibrat oral diyet dozları verilen dişi sıçanlarda, vücut yüzey alanı karşılaştırmalarına dayanarak MRHD'nin 0.3 katında maternal toksisite gözlenmiştir; mg / m2.
Organogenez döneminde gebelik gününden 6-15 gün sonra 14, 127 ve 361 mg / kg / gün oral diyet dozları verilen gebe sıçanlarda, 14 mg / kg / gün'de (1 kattan az) olumsuz gelişimsel bulgular gözlenmemiştir. vücut yüzey alanı karşılaştırmalarına dayanan MRHD; mg / m2). İnsan dozlarının daha yüksek katlarında maternal toksisite kanıtı gözlenmiştir.
Organogenez döneminde 618 gebelik gününden itibaren 15, 150 ve 300 mg / kg / gün oral gavaj dozları verilen ve doğumuna izin verilen hamile tavşanlarda, 150 mg / kg / gün (MRHD'nin 10 katı) durdurulmuş çöpler gözlendi. , vücut yüzey alanı karşılaştırmalarına dayanarak: mg / m2). 15 mg / kg / gün (vücut yüzey alanı karşılaştırmalarına dayanarak MRHD'nin 1 katından az; mg / m) hiçbir gelişimsel bulgu gözlenmemiştir2).
Gebelik gününden 21. emzirme gününe (sütten kesme) kadar 15, 75 ve 300 mg / kg / gün oral diyet dozları verilen gebe sıçanlarda, maternal toksisite, önerilen maksimum insan dozunun (MRHD) 1 katından daha az bir oranda gözlenmiştir. vücut yüzey alanı karşılaştırmaları; mg / m2.
Hemşirelik Anneler
Fenofibrat emziren annelerde kullanılmamalıdır. İlacın anneye önemi dikkate alınarak hemşireliğin kesilmesine veya ilacın kesilmesine karar verilmelidir.
Pediatrik Kullanım
Pediyatrik hastalarda güvenlik ve etkinlik belirlenmemiştir.
Geriatrik Kullanım
Fenofibrik asidin böbrek tarafından önemli ölçüde atıldığı bilinmektedir ve böbrek fonksiyon bozukluğu olan hastalarda bu ilaca olumsuz reaksiyon riski daha büyük olabilir. Fenofibrik asit maruziyeti yaştan etkilenmez. Yaşlı hastalar böbrek yetmezliği insidansına sahip olduğundan, yaşlılar için doz seçimi böbrek fonksiyonu temelinde yapılmalıdır. Böbrek fonksiyonu normal olan yaşlı hastalar doz modifikasyonu gerektirmemelidir. TRICOR alan yaşlı hastalarda böbrek fonksiyonlarını izlemeyi düşünün
Böbrek Bozukluğu
Şiddetli böbrek yetmezliği olan hastalarda TRICOR kullanımından kaçınılmalıdır. Hafif ila orta derecede böbrek yetmezliği olan hastalarda dozun azaltılması gerekir. Böbrek yetmezliği olan hastalarda böbrek fonksiyonunun izlenmesi önerilir.
Karaciğer yetmezliği
TRICOR kullanımı karaciğer yetmezliği olan hastalarda değerlendirilmemiştir.

YAN ETKİLER
Klinik Araştırmalar Deneyimi
Klinik çalışmalar çok çeşitli koşullar altında yapıldığından, bir ilacın klinik çalışmalarında gözlenen advers reaksiyon oranları, başka bir ilacın klinik çalışmalarındaki oranlarla doğrudan karşılaştırılamaz ve uygulamada gözlemlenen oranları yansıtmayabilir.
Nedensellikten bağımsız olarak çift kör, plasebo kontrollü çalışmalar sırasında fenofibrat (ve plasebodan daha büyük) ile tedavi edilen hastaların% 2 veya daha fazlası tarafından bildirilen advers olaylar aşağıdaki Tablo 1'de listelenmiştir. Olumsuz olaylar fenofibrat ile tedavi edilen hastaların% 5.0'ında ve plasebo ile tedavi edilen% 3.0'ında tedavinin kesilmesine yol açtı. Karaciğer fonksiyon testlerindeki artışlar en sık görülen olaylardı ve çift kör çalışmalarda hastaların% 1.6'sında fenofibrat tedavisinin kesilmesine neden oldu.
Tablo 1. Çift Kör, Plasebo Kontrollü Çalışmalar sırasında Fenofibrat ile Tedavi Edilen ve Plasebodan Daha Büyük Hastaların% 2 veya Daha Fazlası Tarafından Bildirilen Olumsuz Reaksiyonlar
| VÜCUT SİSTEMİ Olumsuz Reaksiyon |
Fenofibrat * | Plasebo |
| (N = 439) | (N = 439) | |
| BÜTÜN OLARAK VÜCUT | ||
| Karın Ağrısı | % 4.6 | % 4.4 |
| Sırt ağrısı | % 3.4 | % 2.5 |
| Baş ağrısı | % 3.2 | % 2.7 |
| DİJESTİF | ||
| Bulantı | % 2.3 | % 1.9 |
| Kabızlık | % 2.1 | % 1.4 |
| METABOLİK VE BESLENME BOZUKLUKLARI | ||
| Anormal Karaciğer Fonksiyon Testleri | % 7.5 ** | % 1.4 |
| Artan ALT | % 3.0 | % 1.6 |
| Artan CPK | % 3.0 | % 1.4 |
| Artan AST | % 3.4 ** | % 0.5 |
| YANIT | ||
| Solunum Bozukluğu | % 6.2 | % 5.5 |
| Rinit | % 2.3 | % 1.1 |
| * 160 mg TRICOR'a eşdeğer dozaj . ** Plasebo'dan önemli ölçüde farklı. |
||
Pazarlama Sonrası Deneyim
Fenofibratın onay sonrası kullanımı sırasında aşağıdaki advers reaksiyonlar tanımlanmıştır: miyalji, rabdomiyoliz, pankreatit, akut böbrek yetmezliği, kas spazmı, hepatit, siroz, anemi, artralji, hemoglobinde azalma, hematokritte azalma, beyaz kan hücresi azalması, asteni ve ciddi depresif HDL-kolesterol seviyeleri. Bu reaksiyonlar, belirsiz büyüklükteki bir popülasyondan gönüllü olarak bildirildiğinden, sıklıklarını güvenilir bir şekilde tahmin etmek veya ilaca maruz kalma ile nedensel bir ilişki kurmak her zaman mümkün değildir.
İLAÇ ETKİLEŞİMLERİ
Kumarin Antikoagülanları
PT / INR uzaması ile kumarin tipi antikoagülan etkilerin güçlendiği gözlenmiştir
Kumarin antikoagülanları TRICOR ile birlikte verildiğinde dikkatli olunmalıdır. Kanama komplikasyonlarını önlemek için PT / INR'yi istenen seviyede tutmak için antikoagülanların dozu azaltılmalıdır. PT / INR'nin stabilize olduğu kesin olarak belirlenene kadar sık PT / INR belirlemeleri tavsiye edilir.
İmmünsüpresanlar
Siklosporin ve takrolimus gibi immünosupsanslar, kreatinin klerensindeki düşüşler ve serum kreatininindeki artışlarla nefrotoksisite üretebilir ve böbrek atılımı, TRICOR dahil olmak üzere fibrat ilaçlarının birincil eliminasyon yolu olduğundan, bir etkileşimin böbrek fonksiyonunun bozulmasına yol açma riski vardır. . İmmünsüpresanlar ve diğer potansiyel olarak nefrotoksik ajanlarla TRICOR (fenofibrat tabletleri) kullanmanın yararları ve riskleri dikkatle düşünülmeli ve kullanılan en düşük etkili doz ve böbrek fonksiyonu izlenmelidir.
Safra Asidi Bağlama Reçineleri
Safra asidi bağlanma reçineleri aynı anda verilen diğer ilaçları bağlayabileceğinden, hastalar emilimini engellememek için safra asidi bağlanma reçinesinden en az 1 saat önce veya 4 ila 6 saat sonra TRICOR almalıdır.
Kolşisin
Rabdomiyoliz dahil miyopati vakaları, kolşisin ile birlikte uygulanan fenofibratlarla bildirilmiştir ve fenofibratın kolşisin ile reçete edilirken dikkatli olunmalıdır.

Gebelik Kategorisi C
Gebe kadınlarda güvenlik belirlenmemiştir. Gebe kadınlarda yeterli ve iyi kontrol edilen fenofibrat çalışması yoktur. Fenofibrat hamilelik sırasında sadece potansiyel fayda fetusun potansiyel riskini haklı çıkarsa kullanılmalıdır.
Sütten kesilmeden 15 gün önce 15, 75 ve 300 mg / kg / gün fenofibrat oral diyet dozları verilen dişi sıçanlarda, vücut yüzey alanı karşılaştırmalarına dayanarak MRHD'nin 0.3 katında maternal toksisite gözlenmiştir; mg / m2.
Organogenez döneminde gebelik gününden 6-15 gün sonra 14, 127 ve 361 mg / kg / gün oral diyet dozları verilen gebe sıçanlarda, 14 mg / kg / gün'de (1 kattan az) olumsuz gelişimsel bulgular gözlenmemiştir. vücut yüzey alanı karşılaştırmalarına dayanan MRHD; mg / m2). İnsan dozlarının daha yüksek katlarında maternal toksisite kanıtı gözlenmiştir.
Organogenez döneminde 618 gebelik gününden itibaren 15, 150 ve 300 mg / kg / gün oral gavaj dozları verilen ve doğumuna izin verilen hamile tavşanlarda, 150 mg / kg / gün (MRHD'nin 10 katı) durdurulmuş çöpler gözlendi. , vücut yüzey alanı karşılaştırmalarına dayanarak: mg / m2). 15 mg / kg / gün (vücut yüzey alanı karşılaştırmalarına dayanarak MRHD'nin 1 katından az; mg / m) hiçbir gelişimsel bulgu gözlenmemiştir2).
Gebelik gününden 21. emzirme gününe (sütten kesme) kadar 15, 75 ve 300 mg / kg / gün oral diyet dozları verilen gebe sıçanlarda, maternal toksisite, önerilen maksimum insan dozunun (MRHD) 1 katından daha az bir oranda gözlenmiştir. vücut yüzey alanı karşılaştırmaları; mg / m2.

Klinik Araştırmalar Deneyimi
Klinik çalışmalar çok çeşitli koşullar altında yapıldığından, bir ilacın klinik çalışmalarında gözlenen advers reaksiyon oranları, başka bir ilacın klinik çalışmalarındaki oranlarla doğrudan karşılaştırılamaz ve uygulamada gözlemlenen oranları yansıtmayabilir.
Nedensellikten bağımsız olarak çift kör, plasebo kontrollü çalışmalar sırasında fenofibrat (ve plasebodan daha büyük) ile tedavi edilen hastaların% 2 veya daha fazlası tarafından bildirilen advers olaylar aşağıdaki Tablo 1'de listelenmiştir. Olumsuz olaylar fenofibrat ile tedavi edilen hastaların% 5.0'ında ve plasebo ile tedavi edilen% 3.0'ında tedavinin kesilmesine yol açtı. Karaciğer fonksiyon testlerindeki artışlar en sık görülen olaylardı ve çift kör çalışmalarda hastaların% 1.6'sında fenofibrat tedavisinin kesilmesine neden oldu.
Tablo 1. Çift Kör, Plasebo Kontrollü Çalışmalar sırasında Fenofibrat ile Tedavi Edilen ve Plasebodan Daha Büyük Hastaların% 2 veya Daha Fazlası Tarafından Bildirilen Olumsuz Reaksiyonlar
| VÜCUT SİSTEMİ Olumsuz Reaksiyon |
Fenofibrat * | Plasebo |
| (N = 439) | (N = 439) | |
| BÜTÜN OLARAK VÜCUT | ||
| Karın Ağrısı | % 4.6 | % 4.4 |
| Sırt ağrısı | % 3.4 | % 2.5 |
| Baş ağrısı | % 3.2 | % 2.7 |
| DİJESTİF | ||
| Bulantı | % 2.3 | % 1.9 |
| Kabızlık | % 2.1 | % 1.4 |
| METABOLİK VE BESLENME BOZUKLUKLARI | ||
| Anormal Karaciğer Fonksiyon Testleri | % 7.5 ** | % 1.4 |
| Artan ALT | % 3.0 | % 1.6 |
| Artan CPK | % 3.0 | % 1.4 |
| Artan AST | % 3.4 ** | % 0.5 |
| YANIT | ||
| Solunum Bozukluğu | % 6.2 | % 5.5 |
| Rinit | % 2.3 | % 1.1 |
| * 160 mg TRICOR'a eşdeğer dozaj . ** Plasebo'dan önemli ölçüde farklı. |
||
Pazarlama Sonrası Deneyim
Fenofibratın onay sonrası kullanımı sırasında aşağıdaki advers reaksiyonlar tanımlanmıştır: miyalji, rabdomiyoliz, pankreatit, akut böbrek yetmezliği, kas spazmı, hepatit, siroz, anemi, artralji, hemoglobinde azalma, hematokritte azalma, beyaz kan hücresi azalması, asteni ve ciddi depresif HDL-kolesterol seviyeleri. Bu reaksiyonlar, belirsiz büyüklükteki bir popülasyondan gönüllü olarak bildirildiğinden, sıklıklarını güvenilir bir şekilde tahmin etmek veya ilaca maruz kalma ile nedensel bir ilişki kurmak her zaman mümkün değildir.

TRICOR ile aşırı doz için spesifik bir tedavi yoktur. Aşırı doz meydana gelirse, hayati belirtilerin izlenmesi ve klinik durumun gözlemlenmesi de dahil olmak üzere hastanın genel destekleyici bakımı endikedir. Belirtilirse, emilmemiş ilacın ortadan kaldırılması kusma veya mide lavajı ile sağlanmalıdır; hava yolunu korumak için olağan önlemler alınmalıdır. Fenofibrik asit plazma proteinlerine yüksek oranda bağlı olduğundan, hemodiyaliz düşünülmemelidir.

Çeşitli klinik çalışmalar, bir LDL membran kompleksi olan yüksek total-C, LDL-C ve apo B seviyelerinin insan aterosklerozu ile ilişkili olduğunu göstermiştir. Benzer şekilde, HDL-C seviyelerinin azalması ve taşıma kompleksi, apolipoprotein A (apo AI ve apo AII) ilişkilidir ateroskleroz gelişimi ile. Epidemiyolojik araştırmalar, kardiyovasküler morbidite ve mortalitenin doğrudan total-C, LDL-C ve TG seviyesine ve ters olarak HDL-C seviyesine göre değiştiğini ortaya koymuştur. HDL-C'yi yükseltmenin veya trigliseritleri (TG) düşürmenin kardiyovasküler morbidite ve mortalite riski üzerindeki bağımsız etkisi belirlenmemiştir.
Fenofibratın aktif metaboliti olan fenofibrik asit, tedavi edilen hastalarda toplam kolesterol, LDL kolesterol, apolipoprotein B, total trigliseritler ve trigliserit bakımından zengin lipoproteinde (VLDL) azalma sağlar. Ek olarak, fenofibrat ile tedavi, yüksek yoğunluklu lipoprotein (HDL) ve apolipoproteinlerde apoAI ve apoAII artışlarına neden olur

Fenofibrat, aktif kimyasal parça fenofibrik asidin bir ön ilacıdır. Fenofibrat, vücuttaki ester hidrolizi ile dolaşımda ölçülebilen aktif bileşen olan fenofibrik aside dönüştürülür.
Emilim
Fenofibratın mutlak biyoyararlanımı, bileşik enjeksiyon için uygun sulu ortamda neredeyse çözünmez olduğu için belirlenemez. Bununla birlikte, fenofibrat gastrointestinal sistemden iyi emilir. Sağlıklı gönüllülerde oral uygulamayı takiben, tek bir doz radyoaktif işaretli fenofibratın yaklaşık% 60'ı idrarda, öncelikle fenofibrik asit ve glukuronat konjugatı olarak ortaya çıktı ve% 25'i dışkıya atıldı. Fenofibrik asidin pik plazma seviyeleri, uygulamadan sonraki 6 ila 8 saat içinde ortaya çıkar.
Fenofibrat emilimi, gıda ile uygulandığında artar. Fenofibrat tabletlerde, emilim derecesi, oruç koşullarına kıyasla beslenen altında yaklaşık% 35 oranında artırılır.
Dağıtım
Fenofibratın çoklu dozlaması üzerine, fenofibrik asit kararlı durumu 5 gün içinde elde edilir. Kararlı durumda fenofibrik asidin plazma konsantrasyonları, tek bir dozu takip edenlerin yaklaşık iki katıdır. Serum proteinlerine bağlanma normal ve hiperlipidemik hastalarda yaklaşık% 99 idi.
Metabolizma
Oral uygulamayı takiben fenofibrat, aktif metabolit fenofibrik aside esterazlarla hızla hidrolize edilir; plazmada değişmemiş fenofibrat tespit edilmez.
Fenofibrik asit öncelikle glukuronik asit ile konjüge edilir ve daha sonra idrarla atılır. Az miktarda fenofibrik asit, karbonil parçasında, glukuronik asit ile konjüge edilen ve idrarla atılan bir benzhidrol metabolitine indirgenir.
İn vivo metabolizma verileri, ne fenofibratın ne de fenofibrik asidin oksidatif metabolizmaya uğramadığını gösterir (ör.sitokrom P450) önemli ölçüde.
Eliminasyon
Emiliminden sonra fenofibrat esas olarak idrarda, öncelikle fenofibrik asit ve fenofibrik asit glukuronid olmak üzere metabolitler şeklinde atılır. Radyoaktif işaretli fenofibrat uygulandıktan sonra, dozun yaklaşık% 60'ı idrarda ve% 25'i dışkıda atılmıştır.
Fenofibrik asit, günde bir kez dozlamaya izin vererek 20 saatlik bir yarılanma ömrü ile elimine edilir.

However, we will provide data for each active ingredient







