





































コンポーネント:
治療オプション:
Fedorchenko Olga Valeryevna 、薬局による医学的評価、 最終更新日:26.06.2023

アテンション! そのこのページの情報は医療専門家のみを対象としています! その情報が収集したオープン源を含めることが可能である重大な誤差! 注意して、このページ上のすべての情報を再確認してください!

アキュテイン

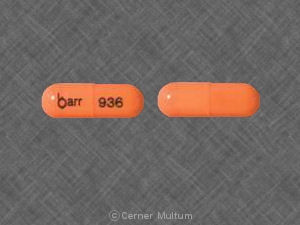
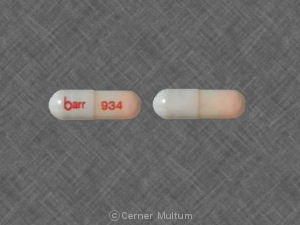
ソフトソラチンカプセル、10mg (ライトピンク)、インプリント %薬用イソトレチノイン10ローション 100包入り10包入り10包入り (NDC 0004-0155-49).
ソフトソラチンカプセル、20mg イソトレチノイン(イソトレチノイン)、イソトレチノイン(イソトレチノイン)) ロッシュ20 100包入り10包入り10包入り (NDC 0004-0169-49).
ソフトソラチンカプセル、40mg イソトレチノイン(イソトレチノイン)、インプリント(イソトレチノイン)) 40ロシュ 100包入り10包入り10包入り (NDC 0004-0156-49).
ストレージ
管理された室温(59°への86°F、15°への30°C)で貯えて下さい。 光から保護する。
参考文献
1. Peck GL,Olsen TG,Yoder FW,et al. 長期の寛解 13-cis-レチノイン酸を有する嚢胞性および塊状のにきびのうち。 N Engl J Med300:329-333, 1979.
2. ポチペ、シャリタAR、シュトラウスJS、ウェブスター SB。 のレポート アクネの分類の一致の会議。 J Amアカデミーデルマトール24:495-500, 1991.
3. ファレルLN、シュトラウスJS、ストラニエリアム。 13-cis-レチノイン酸による重度の嚢胞性座瘡の治療:皮脂産生の評価および 複数回投与試験における臨床応答。 J Am Acad Dermatol3:602-611,1980.
4. ジョーンズH、ブランD、カンリフWJ。 13-シスレチノイン酸とにきび。 ランセット2:1048-1049,1980.
8. シュトラウスJS,Rapini RP,Shalita AR,et al. イソトレチノイン療法 にきびの場合:多施設用量反応研究の結果。 J Am Acad Dermatol10:490-496, 1984.
販売元:株式会社ロシュ研究所,340キングスランドストリート,ナットリー,ニュージャージー州07110-1199. PI改訂:月2010.

-

激しい反抗的な結節性のアクネ
%medicine_name%(isotretinoin)は厳しく反抗的なふしのアクネの処置のために示されます。 結節は、直径5mm以上の炎症性病変である。 ノジュール 化膿性または出血性になることがあります。 "厳しい"という定義によって,2 "いくつかまたはいくつかの"結節とは対照的に、"多くの"を意味します。 使用と関連付けられる重要な悪影響のために%medicine_name%(isotretinoin)はべきです 全身の抗生物質を含む慣習的な療法に応答しない厳しいふしのアクネを持つ患者のために予約されて下さい。 また、%medicine_name%(イソトレチノイン)が示されています 妊娠していないそれらの女性の患者のためにだけ、%medicine_name%(isotretinoin)が引き起こすことができるので 重度の先天性欠損症( 箱入り禁忌および 警告).
15から20週のための療法の単一のコースは完全で起因するために示されていました そして、多くの患者における疾患の長期寛解。1,3,4 第二の場合 治療のコースが必要であり、少なくとも8週間まで開始すべきではありません 最初のコースの完了後、経験が示しているので、患者 これらの薬を服用することはできません。 Retreatmentの前の最適間隔 骨格成長を完了していない患者のために定義されていない(参照 警告:骨格:骨ミネラル密度、骨過多症, そして早期の骨端閉鎖).

%medicine_name%(イソトレチノイン)は食事と一緒に投与する必要があります(参照 患者さん 情報).
%Medicine_name%(isotretinoin)のための推薦された適量の範囲は与えられる0.5から1.0mg/kg/dayです 15-20週間の食品と二分割用量。 0.1を比較した研究では、0.5, および1.0mg/kg/日,8 すべての適量が最初に提供したことが分りました 病気のクリアが、より低いとの再治療のためのより大きな必要性があった 適量. 処置の間に、線量は応答に従っての調節されるかもしれません 疾患および/または臨床的副作用の出現—そのうちのいくつかは be線量関連. 病気が傷つくことと非常に厳しいまたはである成人患者 主に体幹に現れるのは、2までの用量調整が必要な場合があります.0 許容されるように、mg/kg/日. 食物と一緒に%medicine_name%(イソトレチノイン)を服用しないと、有意になります 吸収を減らす. 上向きの線量の調節がなされる前に、患者はべきです 食品の指示への準拠について疑問視される
%Medicine_name%(isotretinoin)との一度毎日の投薬の安全は確立されませんでした。 一度 毎日の投薬はお勧めしません。
完了する前に総結節の数が70%以上減ったら 処置の15から20週は、薬剤中止されるかもしれません. の期間の後 治療オフ2ヶ月以上、および永続的または定期的な重度によって保証されている場合 結節性にきびは、治療の第二のコースを開始することができます. 最適な間隔 再治療が完了していない患者のために定義されていない前に 骨格の成長. %Medicine_name%(イソトレチノイン)の長期使用は、低用量であっても、されていませんでした 勉強し、推奨されていません. それは%medicine_name%(isotretinoin)がで与えられること重要です 推薦された持続期間よりもはやのための推薦された線量. の効果 骨の損失に対する%medicine_name%の長期使用は不明である(参照 警告: Γ:γミネラル濃度、骨過多および骨の上皮性Γ).
避妊措置は、その後の治療コースのために従わなければならない (参照 注意事項).
表4:%medicine_name%(イヨトレチノイン)体重による人(人に基づく
食べ物と一緒に)
| 体重 | 総mg/日 | |||
| キログラム | ポンド | 0.5mg/kg | 1mg/kg | 2mg/kg* |
| 40 | 88 | 20 | 40 | 80 |
| 50 | 110 | 25 | 50 | 100 |
| 60 | 132 | 30 | 60 | 120 |
| 70 | 154 | 35 | 70 | 140 |
| 80 | 176 | 40 | 80 | 160 |
| 90 | 198 | 45 | 90 | 180 |
| 100 | 220 | 50 | 100 | 200 |
| *参照 適量および管理:この された適量の範囲は0.5から1.0mg/kg/dayです。 |
薬剤師のための情報
インターネット経由でiPLEDGEシステムにアクセス(www.ipledgeprogram.com)または電話 (1-866495-0654)許可を得るために、"に分配しないでください "日付"の後の患者。 %medicine_name%(イソトレチノイン)は、a以下でのみ分配されなければなりません 30日間の供給。
リフィルには、食しい処方食とpledgeからの食しい食が必要です システム。
%Medicine_name%(isotretinoin)投薬ガイドは、%medicine_name%(isotretinoin)毎に患者に与えられなければなりません) 法律によって要求されるように、分配される。 この%medicine_name%(イソトレチノイン)投薬ガイドは重要です 患者のためのリスク管理プログラムの一部。

妊娠
カテゴリーxを参照 箱入り禁忌および警告.
アレルギー反応
%medicine_name%(イソトレチノイン)は、この薬に過敏である患者には禁忌である またはその構成要素のいずれかに。 %medicine_name%(isotretinoin)はある患者に与えられるべきではないです ゼラチンカプセルの防腐剤として使用されるパラベンに敏感 (参照 注意事項:過敏症).

警告
精神疾患
%medicine_name%(イソトレチノイン、うつ病、精神病、まれに自殺念慮を引き起こす可能性があります, 自殺未遂、自殺、および積極的および/または暴力的な行動。 メカニズムなし これらのイベントに対して作用が確立されている(有害を参照 リアクション:精神医学)。 パンフレットを読む, 認識 青少年および若年成人における精神障害:処方者のためのガイド イソトレチノインの 処方者は、精神科の警告兆候に注意する必要があります 彼らが必要とする助けを受けるために患者を導く障害. したがって、事前に %medicine_name%(イソトレチノイン)療法の開始には、患者および家族が尋ねられるべきである 精神疾患の病歴について、および治療中の各訪問時に 患者は不況、気分妨害、精神病の徴候のために査定されるべきです, またはさらなる評価が必要かどうかを判断するための攻撃性. サインおよび パンフレットに記載されているように、うつ病の症状("精神医学の認識 青少年および若年成人における障害")、悲しい気分、絶望を含む, 罪悪感、無価値または無力感、喜びまたは関心の喪失 活動において、疲労、集中力の低下、睡眠パターンの変化、変化 体重または食欲、自殺思考または試み、落ち着きのなさ、過敏性, 危険な衝動に作用し、永続的な身体症状が応答しない 治療に. 患者は%medicine_name%(isotretinoin)および患者または薬を飲むべきです 速やかに連絡をとり触った場合、患者のうつ病の開発, 気分障害、精神病、または攻撃性、次の訪問まで待たずに. %Medicine_name%(イソトレチノイン)療法の中断性は不十分であるかもしれません、さらなる人 必要かもしれません. られたモニタリングするのに役立つかもしれないで検出されないすべて リスクのある患者. 患者は精神衛生上の問題か家族歴を報告するかもしれない 精神疾患の. これらのレポートは患者と論議されるべきです および/または患者の家族. メンタルヘルスプロフェッショナルへの紹介 必要であること. 薬は、%medicine_name%(イヒトレチノイン)療法が適切であるかどうかを問う必要があります この設定では、何かの患者のためには%medicine_name%(isotretinoin)の要点を上回るかもしれません) セラピー.
脳脊髄液減少症
%medicine_name%(isotretinoin)の使用は私のいくつかのケースと関連付けられました (良性頭蓋内高血圧症)、そのうちのいくつかは、の併用を伴いました テトラサイクリン. したがって、テトラサイクリンとの併用治療は 避けられる. 偽腫瘍脳の初期徴候および症状には、乳頭浮腫が含まれる, 頭痛、吐き気および嘔吐、および視覚障害. これらの患者 症状は乳頭浮腫のためにスクリーニングされるべきであり、存在する場合、それらは すぐに%medicine_name%(イソトレチノイン)を中止し、神経科医に相談するように言われました さらなる診断およびケア(有害反応を参照: 神経).
深刻な皮膚反応
多形性紅斑および重度の皮膚の市販後の報告がありました 反応[例えば、スティーブンス-ジョンソン症候群(SJS)、毒性表皮壊死症(TEN)] イソトレチノインの使用と関連付けられる。 これらのイベントは深刻であり、結果として 死亡、生命を脅かすイベント、入院、または障害。 患者はすべきです 厳しい皮の反作用のために密接に監視されて下さい、および%のmedicine_name%(isotretinoin)の中断) 保証されれば考慮されるべきです。
膵炎
急性膵炎 上昇したどちらかの患者で報告されています または正常な血清のトリグリセリドのレベル。 まれに致命的な出血が起こります 膵炎が報告されている。 %medicine_name%(isotretinoin)は高トリグリセリド血症場合停止する必要があります 許容可能なレベルで制御することはできませんまたは膵炎の症状が発生した場合。
脂質
800mg/dLを超える血清トリグリセリドの上昇が報告されている %medicine_name%(イソトレチノイン)で治療された患者において). 血清トリグリセリドの著しい上昇 臨床の%medicine_name%(isotretinoin)を受け取っている患者のおよそ25%で報告されました トライアル. さらに、約15%が高密度リポタンパク質の減少を示し、約7%がコレステロールレベルの増加を示した. 臨床において 試験、トリグリセリド、HDLおよびコレステロールに対する効果はリバーシブルでした %(イソトレチノイン)療法の中止について. 何人かの患者はトリグリセリドを逆転できました 重量の減少、食餌療法の脂肪およびアルコールの制限による上昇、および イソトレチノイン(イソトレチノイン)を継続しながら用量を減少させる)5
血の脂質の決定は%medicine_name%(isotretinoin)が与えられる前に行われるべきです 次に、%medicine_name%(イソトレチノイン)に対する脂質応答が確立されるまでの間隔で、 通常4週間以内に発生します. 特に慎重に検討する必要があります %medicine_name%(isotretinoin)療法の間に危険度が高いにあるかもしれない患者のために危険にさらすか、または寄与するため (糖尿病、肥満、アルコール摂取量の増加、脂質代謝のある患者 脂質代謝障害の障害または家族歴). If%medicine_name%(イソトレチノイン)療法 脂質および/または血液の血清値のより頻繁なチェックが制定されています 砂糖は推奨されています(参照 注意:実験室テスト).
高トリグリセリド血症による心血管障害(イソトレチノイン)に対する影響について) 不明です。 動物実験:イソトレチノインの8または32mg/kg/日を与えられたラットで (1.3~5.推奨臨床用量の3倍の1.正常化後0mg/kg/日 総体表面積のために)18か月またはより長く、心筋の焦点石灰化、線維症および発火の発生、石灰化の 冠動脈、肺および腸間膜動脈、および転移性石灰化の 胃粘膜は同様の年齢の対照ラットよりも大きかった. 焦点心内膜 および冠動脈の石灰化に関連する心筋石灰化 動脈は、治療の約6-7ヶ月後に二つの犬で観察されました 60から120mg/kg/日(推薦される30から60回)の適量のisotretinoinを使って 臨床用量1.合計の正規化後、それぞれ0mg/kg/日 体表面積)
聴覚障害
聴覚障害は、いくつかのケースでは、%medicine_name%(イソトレチノイン)を服用している患者で報告されています, 聴覚障害は、治療が中止された後も持続することが報告されている。 このイベントのメカニズムと因果関係は確立されていません。 患者さん 耳鳴りまたは聴覚障害を経験する人は、%medicine_name%(イソトレチノイン)治療を中止する必要があります するための専門的なケアのための更なる評価を参照 不利 リアクション:特別な感覚).
肝毒性
おそらく、またはおそらく%medicine_name%(イソトレチノイン)に関連すると考えられる臨床肝炎) 治療が報告されている。 さらに、レバー酵素の高度を緩和する穏やかの間に扱われた個人のおよそ15%で観察されました 臨床試験,そのうちのいくつかは、投与量の減少と正規化または継続 薬物の投与。 正常化が容易に起こらない場合、または肝炎の場合 %medicine_name%(イソトレチノイン)による治療中に疑われる場合は、薬剤を中止する必要があります そして病因はさらに調査された。
炎症性腸疾患
%medicine_name%(isotretinoin)は炎症性腸疾患と関連付けられました(を含む地方 腸の無秩序の前の歴史のない患者のileitis)。 いくつかの 例、徴候は%medicine_name%(isotretinoin)の処置の後で持続するために報告されました持っています 停止された。 腹部の苦痛、直腸の出血または厳しい経験している患者 下痢はすぐに%medicine_name%を中止する必要があります(参照 不利 反応:胃腸).
骨格
骨のミネラル密度
発達中の筋骨格系に対する%medicine_name%(イソトレチノイン)の複数のコースの影響 不明です. 長期、高用量、または複数のコースがあるという証拠があります イソトレチノインによる治療の単一のコースよりも効果の多くを持っています 筋骨格系の治療. オープンラベル臨床試験において(N=217) 重度の反抗性結節性ざ瘡に対する%medicine_name%(イソトレチノイン)による単一の治療コースのうち、いくつかの骨格部位での骨密度の測定は有意ではなかった 減少した(腰椎の変化>-4%および総股関節変化>-5%)またはあった 患者の大半で増加しました. ある患者は腰椎の減少を有していた 未調整のデータに基づく脊柱の骨のミネラル密度>4%. 十六(7).9%)の患者さん 腰椎の骨のミネラル密度>4%の減少を持っていた、そして他のすべて 患者(92%)は有意な減少を有していなかったか、または増加を有していた(調整 ボディマスの索引のため). ナイン患者さん(4.5%)総股関節骨の減少がありました 未調整データに基づく鉱物密度>5%. トゥエンティワン(10.6%)の患者さん 総股関節骨のミネラル密度の減少が>5%、および他のすべての患者を持っていました (89%)有意な減少がなかったか、または増加があった(ボディのために調節される 質量指数). フォローアップの調査は減らされるの患者の8で行いました その後11ヶ月までの骨ミネラル密度が増加することを示した 腰椎の5人の患者の骨密度、他の3人の患者は持っていたが ベースライン値以下の腰椎の骨密度の測定. 総ヒップの骨 鉱物密度はベースライン(範囲-1.6%~-7%.6%)で5の8患者 (62.5%)
10人の患者の別のオープンラベル拡張研究では、年齢13-18年, 最初のコースから4ヶ月後に%medicine_name%(イソトレチノイン)の第二のコースを開始した人、二つ 患者は3.25まで平均腰椎の骨のミネラル密度の減少を示しました% (参照 注意:小児科の使用).
骨粗鬆症、骨減少症、骨折、および遅延の自発的な報告 骨折の治癒は、%medicine_name%(イソトレチノイン)集団で見られている。 因果関係がありながら %medicine_name%(イソトレチノイン)が確立されていないため、効果を排除することはできません。 より長い 用語効果は研究されていない。 これは、%medicine_name%(イソトレチノイン)がで与えられることが重要です 推薦された持続期間よりもはやのための推薦された線量。
骨粗しょう症
骨格過形成症の高い有病率は臨床試験でのための注意されました 2.24mg/kg/日の平均用量による角質化の障害。 さらに, 骨格過形成症は前向き調査の6の8人の患者での注意されました 角質化の障害。6 最小限の骨格過形成症および石灰化 靭帯および腱のまた前向き調査のx線によって観察されました 推薦されるで療法の単一のコースと扱われる結節性のアクネの患者の 線量。 アクネのための多数の%のmedicine_name%(isotretinoin)の処置のコースの骨格の効果 不明です。
重度の217人の小児患者(12歳から17歳)の臨床研究において 反抗的な結節性ざ瘡、骨過多症は16-20週間後に観察されなかった 約1mg/kg/日の治療の%medicine_name%(イソトレチノイン)を割った二つで与えられた 線量。 骨過多症が表示されるより長い時間枠が必要な場合があります。 クリニカル コースと意義は不明のままです。
早期骨端閉鎖
アクネの患者の早期のepiphyseal閉鎖の自発のレポートがあります %medicine_name%(isotretinoin)の推薦された線量を受け取ります。 イソトレチノイン)の複数コースの効果) 骨端閉鎖については不明である。
視力障害
視覚的な問題は慎重に監視する必要があります。 すべての%medicine_name%(イソトレチノイン)患者が経験している 視覚障害は、%medicine_name%(イソトレチノイン)治療を中止し、眼科を持っている必要があります 検査( 副作用:特別な感覚).
角膜混濁
アクネのための%のmedicine_name%(isotretinoin)を受け取っている患者でCorneal opacitiesは起こりました 障害のある患者でより高い薬物投与量が使用された場合、より頻繁に ケラチン化の。 臨床で観察されている角膜の不透明度 %medicine_name%(イソトレチノイン)で治療された試験患者は、完全に解決されたか、またはそうであった 薬物中止後6-7週間後のフォローアップ時に解決する(参照 不利 リアクション:特別な感覚).
減らされた夜間視力
減らされた夜間視力は%medicine_name%(isotretinoin)療法の間にそしていくつかで報告されました 治療が中止された後もイベントは持続しています。 何人かの患者の手始めが突然だったので、患者はこの潜在性の助言されるべきです 問題および夜に車を運転するか、または作動させるとき注意深いように警告されて。
注意事項
%medicine_name%(イソトレチノイン)は、登録および活性化された処方者によってのみ処方されなければならない iPLEDGEプログラムで。 %medicine_name%(イソトレチノイン)は、登録された薬局によってのみ調剤されなければなりません そしてiPLEDGEと活動化させ、登録されている患者にだけ分配されなければなりません そしてipledgeのすべての条件を満たして下さい。 登録および活性化された薬局 ipledgeに登録されている卸売業者からのみ%medicine_name%(イソトレチノイン)を受け取る必要があります。
卸売業者、処方者、および薬剤師のためのiPLEDGEプログラム要件 以下に記載されています:
卸売業者
IPLEDGEプログラムの目的のために、卸売業者という用語は卸売業者を指します, 代理店、および/またはチェーン薬局の販売代理店。 %医薬品(イソトレチノイン)を配布するために、卸売業者 iPLEDGEに登録する必要があり、すべてのiPLEDGE要件を満たすことに同意する必要があります isotretinoinプロダクトの卸し売り配分のため。 卸売業者は登録する必要があります ipledgeの卸し業者の一致に署名し、戻ることによるiPLEDGEを使ってそれ それらがisotretinoinの配分のためのすべてのiPLEDGEの条件に従うことを断言します。 これらには、:
- イソトレチノインを配布する前に登録し、毎年再登録します その後
- FDA社のイヤトレチノイン製品のみを配信する
- イソトレチノインのみを出荷する
- 前の日による同窓を得てpledgeプログラムに締められた被験者 メーカーから、または
- Ipledgeでライセンスを取得し、ipledgeで活性化された! プログラム
- 非登録のイソトレチノインメーカー(または代理人)に通知する および/または注文しようとする非活性化薬局または未登録の卸売業者 イソトレチノイン
- コンプライアンスの確認のための卸業者の記録の点検に従うこと イソトレチノインメーカー(またはデリゲート)によるipledgeプログラムで)
- 配布済みの製品があれば、製造元(または代理人)に戻ります 登録は製造業者によってまたは卸し業者がに選んだら取り消されます 毎年再登録しない
プロセッサー
イソトレチノインを処方するには、処方者を登録して活性化する必要があります 妊娠リスク管理プログラムiPLEDGEで。 処方者は登録できます 記入した登録フォームに署名して返すことによって。 処方者のみができます 要件を満たしていることを確認して登録を有効にします 以下の点を証明することにより、すべてのiPLEDGE要件に準拠します:
- 私はイソトレチノインからの胎児の傷害/生まれつきの欠陥の危険そして重大度を知っている。
- 私は計画外妊娠の危険因子と効果的な対策を知っています 計画外妊娠の回避のため。
- 私は患者に詳細な妊娠予防を提供する専門知識を持っています カウンセリングについて一言触れたいと思いま彼女の専門家のためにこのような個人カウンセリングの返還 メーカーによる。
- 私は小さな子供に記録されているipledgeプログラムの概要を教えてください タイトル Ipledgeプログラムとipledgeのためのベストプラクティスへのガイド プログラム処方避妊カウンセリングガイド
- 妊娠可能性女性患者の治療を開始する前に イソトレチノインを使用して、毎月、患者は以下のことを相談されます 同時かつ継続的に避妊の二つの形態を使用して妊娠を避ける イソトレチノイン療法の一ヶ月前、中、および一ヶ月後、しない限り 患者は継続的な禁欲にコミットします。
- 私は妊娠中の女性患者にイソトレチノインを処方しません 彼女は否定的なスクリーニング妊娠検査を持っていることを確認する マンスリー-ネガティブ-クリア認定(臨床検査改善改正)) 妊娠検査薬 患者は完了時に妊娠検査を受けるべきです イソトレチノインの全コースと1ヶ月後の別の妊娠検査。
- 女性ながら気づいた妊娠事例をレポートしていきます 患者はイソトレチノインまたは妊娠への最後の投与後1ヶ月である レジストリ。
イソトレチノインを処方するには、処方者はipledgeシステムにアクセスする必要があります インターネット(www.ipledgeprogram.com)または電話(1-866-495-0654)へ:
- IPLEDGEプログラムに各者を押します。
- 確認の月額をそれぞれの患者を受けた相談及び教育を行う。
- のために 出産可能性のある女性患者:
- 毎月の避妊の患者の二つの選択された形態を入力してください。
- CLIA定定所実施からの結果を入力してください テスト。
イソトレチノインは、知られていない女性患者にのみ処方されなければならない 否定的なCLIA証明された実験室によって行なわれた妊娠によって確認されるように妊娠 テスト。
Isotretinoinは登録され、活動化させる薬学によってだけ分配されなければならない 妊娠リスクマネジメントプログラムiPLEDGEとのみ登録されたとき 患者はiPLEDGEプログラムのすべての要件を満たしています。 要件を満たす 妊娠可能な可能性の女性患者のためにその彼女を意味します:
- 持っている カウンセリングされ、患者情報に署名している/通知されている 先天性欠損症に関する同意(妊娠できる女性患者のための)フォーム それは胎児が潜在的な生まれつきの欠陥の危険についての警告を含んでいます イソトレチノインにさらされる。 患者はインフォームドコンセントフォームに 治療を開始する前に、患者のカウンセリ 時間および月単位のその後。
- 持っていました 感度を有する二つの陰性尿または血清妊娠検査
最新のイソトレチノインの決定を受け取る前の少なくとも25miu/mlの。
最初のテスト(スクリーニングテスト)は、決定時に処方者によって得られます
イソトレチノインに対する患者の資格を追求するために作られています。 二つ目は、
妊娠検査(確認検査、CLIA認定検査室で行わなければなりません。
2つのテストの間隔は少なくとも19日でなければなりません。
- 定期的な月経周期を有する患者のために、第二の妊娠検査 すぐに月経期間の最初の5日間に行う必要があります イソトレチノイン療法の開始に先立ち、患者の後 避妊の2つの形態を1か月の間使用しました。
- 無月経、不規則なサイクル、または避妊薬を使用している患者のために 離脱出血を排除する方法は、第二の妊娠検査がなければなりません イソトレチノイン療法の開始直前に行われ、 患者が2つの形態の避妊を1ヶ月間使用した後。
- 持っていました 尿または血清妊娠検査からの陰性の結果 イヤトレチノインのそれに続く各コースを受け取る前のCLIA明らかにされた実験。 妊娠検査はCLIA認定検査室で毎月繰り返さなければなりません, 各処方を受け取る女性患者の前に。
- 持っている 選択され、効果的な避妊の2形態を使用することを約束しています
同時に、患者がいない限り、少なくとも1つは主要な形態でなければならない
異性との接触、または患者からの継続的な禁欲にコミットします
子宮摘出術または両側卵巣摘出術を受けたか、または医学的に行われている
閉経後であることが確認されました. 患者は効果的な避妊の2形態を使用する必要があります
イソトレチノイン法の開始前の少なくとも1か月の間、イソトレチノインの間に
療法、およびイソトレチノイン療法を中止した後1ヶ月. カウンセリ
妊娠リスクの増加に関連する避妊と行動について
毎月繰り返される必要があります
患者がいつでも保護されていない異性の性交を持っている場合1ヶ月 治療の前、中、または1ヶ月後に、彼女は必要があります:- 治療中の場合は、すぐに%medicine_name%(イソトレチノイン)の服用を中止してください
- 保護されていない最後の行為の少なくとも19日後に妊娠検査を受けてください 異性愛者の性交
- 有効な避妊の2つの形態を同時に再度使用し始めて下さい %medicine_name%(イヒトレチノイン)療法を開始する前の1日
- 効果的な避妊の2つの形態を使用した後、第二の妊娠検査を持っています 彼女は定期的な月経を持っているかどうかに応じて、上記のように1ヶ月 またはない。
避妊の効果的な形態には、一次および二次の両方の形態が含まれる。 避妊:
| プライマリ形式 | 二次形式 |
|
バリア: |
|
|
| その他: | |
|
任意の避妊方法は失敗することができます. から妊娠の報告がありました 経口避妊薬を使用した女性の患者、またtransdermalパッチ/注射可能な/implantable/腟 リングホルモ 患者は%のmedicine_name%(isotretinoin)を取っていました). これらの報告は女性患者に&

副作用
臨床試験および市販後のサーベイランス
以下に示す副作用は、治験当時の経験を反映しています イソトレチノイン)の研究、および市販後の経験。 いくつかの関係 これらのイベントのうち、%medicine_name%(イソトレチノイン)療法は不明である。 副作用の多くと %medicine_name%(isotretinoin)を受けている患者で見られる不利な反作用は記述されているそれらに類似しています 非常に高用量のビタミンA(皮膚および粘液の乾燥)を服用している患者では 膜、例えば、唇、鼻の通路、および目の)。
線量関係
Cheilitisおよび高トリグリセリド血症は通常関連しています線量です。 ほとんどの副作用 しかし、臨床試験で報告された治療が中止されたときに可逆的であった, いくつかは、治療の中止後に持続した(参照 警告 そして不利な反作用).
ボディ全体として
アレルギー反応,血管炎を含みます,全身過敏症(参照してください 注意事項: 過敏症)、浮腫、疲労、リンパ節腫脹、体重減少
心血管
動悸、頻脈、血管血栓性疾患、脳卒中
内分泌-代謝
高トリグリセリド血症( 警告:脂質), 血糖値の変化( 注意事項: 検査室テスト)
胃腸
炎症性腸疾患( 警告:炎症性 腸の病気)、肝炎( 警告: 肝毒性)、膵炎( 警告: 脂質)、歯茎の出血および炎症、大腸炎、食道炎/食道潰瘍形成、回腸炎、吐き気、その他の非特異的な胃腸症状
血液学
アレルギー反応( 注意事項:過敏症), 貧血、血小板減少症、neut球減少症、無ran粒球症のまれな報告(参照 患者情報). 見る 注意事項: 検査室テスト 他の血液学的パラメータのために。
筋骨格
骨格過形成症、腱および靭帯の石灰化、早期骨端 閉鎖、骨のミネラル密度の減少(見て下さい 警告: 骨格)、背中の痛みを含む筋骨格症状(時には重度), 筋肉痛、関節痛( 患者情報), 胸の一時的な痛み(参照 患者情報 )、関節炎、腱炎、その他の骨の異常、隆起 CPKの/横紋筋融解症のまれなレポート(参照 注意事項: 検査室テスト).
神経
脳脊髄液減少症( 警告:疑似腫瘍 セレブリ)、めまい、眠気、頭痛、不眠、無気力、倦怠感, 緊張、感覚異常、発作、脳卒中、失神、脱力感
精神科
自殺念慮、自殺未遂、自殺、うつ病、精神病、侵略, 暴力的な行動( 警告:精神科 障害)、情緒不安定
患者の報告、うつ病、一部の報告によると、うつ病後退 治療の中止および治療の再導入により再発した。
生殖システム
異常月経
呼吸器
気管支痙攣(喘息の病歴の有無にかかわらず)、呼吸器感染症, 声の変化
皮膚および付属物
にきび劇症、脱毛症(場合によっては持続する)、挫傷、cheilitis (乾燥した唇)、乾燥した口、乾燥した鼻、乾燥肌、鼻出血、噴火のxanthomas,7 多形性紅斑、紅潮、皮膚のもろさ、髪の異常、多毛症, 色素沈着過多および色素沈着低下、感染症(播種性ヘルペスを含む シンプレックス)、爪ジストロフィー、爪周囲炎、手のひらと足の裏の剥離、光アレルギー/光感受性 反応、掻痒、化膿性肉芽腫、発疹(顔面紅斑、脂漏症を含む, および湿疹)、スティーブンス-ジョンソン症候群、日焼け感受性が増加し、発汗, 毒性表皮壊死症、蕁麻疹、血管炎(ウェゲナー肉芽腫症を含む, 見る 注意事項:過敏症)、異常 創傷治癒(遅延治癒または痂皮を伴うあふれんばかりの肉芽組織, 見る 患者情報)
特別な感覚
ヒアリング - 聴覚障害( 警告: 聴覚障害)、耳鳴り。
ビジョン- 角膜混濁( 警告: 角膜混濁)、持続するかもしれない減らされた夜間視力(参照 警告: 減らされた夜間視力)、白内障、色覚障害、結膜炎, ドライアイ、眼瞼炎、角膜炎、視神経炎、羞明、視力障害、視力障害、視力障害、視力障害、視力障害 乱れ
Urinary器系
糸球体腎炎( 注意事項:過敏症), 非特異的なu生殖器所見(参照 注意事項: 検査室テスト その他の泌尿器科パラメータについて)
研究室
血しょうトリグリセリドの上昇(見て下さい 警告: 脂質)、血清高密度リポタンパク質(HDL)レベルの低下、上昇 治療中の血清コレステロールの
増加したアルカリホスファターゼ、SGOT(AST)、SGPT(ALT)、GGTPまたはLDH(参照 警告: 肝毒性)
空腹時血糖の上昇、CPKの上昇(を参照してください 注意事項: 検査室テスト)、高尿酸血症
赤血球パラメータの減少、白血球数の減少 (重度のneut球減少症および無ran粒球症のまれな報告を含む、参照 患者さん 情報)、沈降速度の上昇、血小板数の上昇, 血小板減少症
尿中の白血球、タンパク尿、顕微鏡的または肉眼的血尿
薬物相互作用
- ビタミンA:ビタミンに対する%medicine_name%(イヨトレチノイン)の関係のために 患者さんに対してビタミンサプリメントを含む 添加物の活性作用を避けるためにビタミンA。
- テトラサイクリン:イソトレチノインおよびテトラサイクリンによる併用療法 %medicine_name%(isotretinoin)の使用はいくつかのと関連付けられたので避けるべきです 偽腫瘍脳(良性頭蓋内圧亢進症)の症例、そのうちのいくつか テトラサイクリンの併用が関与している。
- マイクロ投与プロゲステロン製剤:マイクロドーズプロゲステロン 調製物(エストロゲンを含まない"ミニピル")は、 %medicine_name%(イソトレチノイン)療法の間に人の不十分な方法であって下さい。 しかし 他のホルモン避妊薬は非常に効果的ですが、報告がありました 併用経口避妊薬を使用した女性患者からの妊娠の, ホルモン性経皮パッチ/射出可能/植込み可能/腟リングと同様、 避妊グッズ. これらの報告は女性患者にとってより頻繁である 避妊の単一の方法だけを使用する人. それは知られていない場合ホルモン 薬は、%medicine_name%(イヒトレチノイン)と一緒に使用すると、その有効性が異なります)。 したがって, それは出産の潜在性の女性の患者のために非常に重要にです 選択し、同時に効果的な避妊の2形態を使用することをコミットします, 少なくとも1のでなければな一次形(覧 注意事項).
- ノルエチンドロン/エチニルエストラジオール:31の閉経前の研究では 重度の反抗性結晶性を有する患者は、orthonovum®を受ける 口口避妊薬として7/7/7の薬剤、%medicine_name%(イヒトレチノイン)が投与されています 1mg/kg/米の使用量は、生物動態学における本質的に関連する変化を誘導しなかった エチニルエストラジオールおよびノルエチンドロンのそしてプロゲステロンの血清のレベル, 胞ホルモン(fsh)および体形成ホルモン(lh)。 プロセッサー 付随して投与される薬物の添付文書に相談することをお勧めします ホルモン避妊薬では、いくつかの薬が有効性を低下させる可能性があるため これらの避妊製品の
- セントジョンズ 麦汁: %medicine_name%(isotretinoin)の使用は関連付けられます 一部の患者におけるうつ病(警告を参照: 精神疾患および有害反応:精神医学)。 患者はすべきです 前向きにハーブのサプリメントと自己薬で治療しないように警告される 可能な相互作用がホルモンと示唆されているため、セントジョンズワート 経口避妊薬における画期的な出血の報告に基づく避妊薬 セントジョンズワートを開始した直後。 妊娠はによって報告されています また、聖ヨハネのいくつかのフォームを使用した複合ホルモン避妊薬のユーザー 麦汁
- フェニトイン:%medicine_name%(isotretinoin)は生物学的態様を変えることが示されていません 七つの健康なボランティアの研究におけるフェニトインの。 これらの結果は一貫している を使って、 in vitro イソトレチノインもその代謝産物もないことを見出した CYP2C9ヒト肝臓P450酵素の活性を誘導または阻害する。 フェニトイン 骨軟化症を引き起こすことが知られている。 正式な臨床研究は行われていません フェニトイン間の骨の損失に対する相互作用の効果があるかどうか査定するため そして、%medicine_name%(イソトレチノイン)。 したがって、これらの薬物を使用するときは注意が必要です 一緒に。
- 全身性コルチコステロイド:全身性コルチコステロイドが知られている 骨粗鬆症を引き起こす。 評価するための正式な臨床研究は行われていません 全身の副腎皮質ホルモン間の骨の損失に対する相互効果があれば そして、%medicine_name%(イソトレチノイン)。 したがって、これらの薬物を使用するときは注意が必要です 一緒に。
検査室テスト
- 妊娠検査薬
- 妊娠可能性の女性患者は、二つの陰性を持っていたに違いありません 少なくとも25miu/mlの濃度を有する米または米検査 イントレチノイン)処を受け取る前に。 最初のテスト( スクリーニングテスト)は、決定が行われたときに処方者が得る %medicine_name%(イヒトレチノイン)のための患者の人を請求する。 第二の妊娠 テスト(テスト)はクリアランスにされた実験で行われなければなりません。 二つのテストの間隔は、少なくとも19日でなければなりません。
- 定期的な月経周期を有する患者のために、第二の妊娠検査 すぐに月経期間の最初の5日間に行われなければなりません %medicine_name%(isotretinoin)療法の開始に進行し、患者が持っていた後 2ヶ月間避妊の1形態を使用しました。
- 無月経、不規則なサイクル、または避妊薬を使用している患者のために 離脱出血を排除する方法は、第二の妊娠検査がなければなりません %medicine_name%(イヒトレチノイン)療法の開始直前および後に行われる 患者は2つの形態の避妊を1ヶ月間使用している。
- 毎月の治療では、患者は尿から否定的な結果を得なければなりません または血清妊娠検査。 妊娠検査は毎月繰り返されなければなりません, CLIA確定実証では、女性患者が受け取る前に 各処方。
- 脂質: 前処理およびフォローアップ血の脂質はあるべきです 断食条件下で得られる。 アルコールを摂取した後、少なくとも これらの決定が行われるまでに36時間が経過する必要があります。 それは推薦されます これらのテストは脂質までの週か隔週間隔で行われること %medicine_name%(isotretinoin)に対する応答が認められます。 高トリグリセリド血症の発生率 は1人の患者で4%の治療を行っています(参照)。 警告: 脂質).
- 肝機能検査: 肝臓の酵素の上昇があるので 臨床試験中に観察され、肝炎が報告されており、前処理 そしてフォローアップのレバー機能テストは週か隔週で行われるべきです %medicine_name%への応答が認められるまでの期間 警告: 肝毒性).
- グルコース: %Medicine_name%(isotretinoin)を受け取っている人かの患者は喜びました 彼らの血糖値の制御における問題。 さらに、糖尿病の新しいケース 薬果関係が%medicine_name%(isotretinoin)療法の間に判断されましたが、 が設立されました。
- CPK: 活発な身体活動を経ている何人かの患者は間、 %medicine_name%(イヒトレチノイン)療法では、CPKレベルの上昇を介していますが、標準的には 意義は不明です. 横紋筋融解症のまれな市販後の報告がありました, 激しい身体活動に関連するいくつかのもの. 217の臨床試験では 重度の反抗性結節性ざ瘡を有する小児患者(12歳から17歳), CPKの一時的な上昇はそれらを含む患者の12%で、起こされました 報告された筋骨格系に関連して激しい身体活動を受ける 腰痛、関節痛、四肢損傷、または筋肉の捻挫などの有害事象. これらの患者では、CPK上げの割合が正常に達した 2週間以内に半分は4週間以内に正常に戻りました. 横紋筋融解症の症例はない この裁判で報告されました
参考文献
7. ディッケン-CHコノリー-スマートフォン に関連する噴火性黄色腫 イソトレチノイン(13-シス-レチノイン酸)。 Arch Dermatol116:951-952,1980.

カテゴリーxを参照 箱入り禁忌および警告.

臨床試験および市販後のサーベイランス
以下に示す副作用は、治験当時の経験を反映しています イソトレチノイン)の研究、および市販後の経験。 いくつかの関係 これらのイベントのうち、%medicine_name%(イソトレチノイン)療法は不明である。 副作用の多くと %medicine_name%(isotretinoin)を受けている患者で見られる不利な反作用は記述されているそれらに類似しています 非常に高用量のビタミンA(皮膚および粘液の乾燥)を服用している患者では 膜、例えば、唇、鼻の通路、および目の)。
線量関係
Cheilitisおよび高トリグリセリド血症は通常関連しています線量です。 ほとんどの副作用 しかし、臨床試験で報告された治療が中止されたときに可逆的であった, いくつかは、治療の中止後に持続した(参照 警告 そして不利な反作用).
ボディ全体として
アレルギー反応,血管炎を含みます,全身過敏症(参照してください 注意事項: 過敏症)、浮腫、疲労、リンパ節腫脹、体重減少
心血管
動悸、頻脈、血管血栓性疾患、脳卒中
内分泌-代謝
高トリグリセリド血症( 警告:脂質), 血糖値の変化( 注意事項: 検査室テスト)
胃腸
炎症性腸疾患( 警告:炎症性 腸の病気)、肝炎( 警告: 肝毒性)、膵炎( 警告: 脂質)、歯茎の出血および炎症、大腸炎、食道炎/食道潰瘍形成、回腸炎、吐き気、その他の非特異的な胃腸症状
血液学
アレルギー反応( 注意事項:過敏症), 貧血、血小板減少症、neut球減少症、無ran粒球症のまれな報告(参照 患者情報). 見る 注意事項: 検査室テスト 他の血液学的パラメータのために。
筋骨格
骨格過形成症、腱および靭帯の石灰化、早期骨端 閉鎖、骨のミネラル密度の減少(見て下さい 警告: 骨格)、背中の痛みを含む筋骨格症状(時には重度), 筋肉痛、関節痛( 患者情報), 胸の一時的な痛み(参照 患者情報 )、関節炎、腱炎、その他の骨の異常、隆起 CPKの/横紋筋融解症のまれなレポート(参照 注意事項: 検査室テスト).
神経
脳脊髄液減少症( 警告:疑似腫瘍 セレブリ)、めまい、眠気、頭痛、不眠、無気力、倦怠感, 緊張、感覚異常、発作、脳卒中、失神、脱力感
精神科
自殺念慮、自殺未遂、自殺、うつ病、精神病、侵略, 暴力的な行動( 警告:精神科 障害)、情緒不安定
患者の報告、うつ病、一部の報告によると、うつ病後退 治療の中止および治療の再導入により再発した。
生殖システム
異常月経
呼吸器
気管支痙攣(喘息の病歴の有無にかかわらず)、呼吸器感染症, 声の変化
皮膚および付属物
にきび劇症、脱毛症(場合によっては持続する)、挫傷、cheilitis (乾燥した唇)、乾燥した口、乾燥した鼻、乾燥肌、鼻出血、噴火のxanthomas,7 多形性紅斑、紅潮、皮膚のもろさ、髪の異常、多毛症, 色素沈着過多および色素沈着低下、感染症(播種性ヘルペスを含む シンプレックス)、爪ジストロフィー、爪周囲炎、手のひらと足の裏の剥離、光アレルギー/光感受性 反応、掻痒、化膿性肉芽腫、発疹(顔面紅斑、脂漏症を含む, および湿疹)、スティーブンス-ジョンソン症候群、日焼け感受性が増加し、発汗, 毒性表皮壊死症、蕁麻疹、血管炎(ウェゲナー肉芽腫症を含む, 見る 注意事項:過敏症)、異常 創傷治癒(遅延治癒または痂皮を伴うあふれんばかりの肉芽組織, 見る 患者情報)
特別な感覚
ヒアリング - 聴覚障害( 警告: 聴覚障害)、耳鳴り。
ビジョン- 角膜混濁( 警告: 角膜混濁)、持続するかもしれない減らされた夜間視力(参照 警告: 減らされた夜間視力)、白内障、色覚障害、結膜炎, ドライアイ、眼瞼炎、角膜炎、視神経炎、羞明、視力障害、視力障害、視力障害、視力障害、視力障害 乱れ
Urinary器系
糸球体腎炎( 注意事項:過敏症), 非特異的なu生殖器所見(参照 注意事項: 検査室テスト その他の泌尿器科パラメータについて)
研究室
血しょうトリグリセリドの上昇(見て下さい 警告: 脂質)、血清高密度リポタンパク質(HDL)レベルの低下、上昇 治療中の血清コレステロールの
増加したアルカリホスファターゼ、SGOT(AST)、SGPT(ALT)、GGTPまたはLDH(参照 警告: 肝毒性)
空腹時血糖の上昇、CPKの上昇(を参照してください 注意事項: 検査室テスト)、高尿酸血症
赤血球パラメータの減少、白血球数の減少 (重度のneut球減少症および無ran粒球症のまれな報告を含む、参照 患者さん 情報)、沈降速度の上昇、血小板数の上昇, 血小板減少症
尿中の白血球、タンパク尿、顕微鏡的または肉眼的血尿

オーラルLD50 イソトレチノインのラットの4000mg/kgより大きいです およびマウス(推奨臨床用量の600倍以上の1.0mg/kg/日の後 総体表面積および>300回のためのラットの線量の正常化 推奨される臨床用量は、1.マウスの正常化後0mg/kg/日 総体表面積のための線量)およびウサギのおよそ1960mg/kgです (推奨臨床用量の653倍の1.正常化後0mg/kg/日 総ボディ表面積のため). 人間では、overdosageはと関連付けられました 嘔吐、顔面紅潮、口腔炎、腹痛、頭痛、めまい、および 運動失調. これらの徴候は明白な残りの効果なしですぐに解決
%medicine_name%(isotretinoin)はあらゆる適量で深刻な生まれつきの欠陥を引き起こします(見なさい 箱入り

吸収
高いlipophilicityが原因で、isotretinoinの口頭吸収は高められます 高脂肪の食事と与えられたとき. クロスオーバー研究では、74の健康な成人の被験者 単一を受け取りました80mgの経口用量(2x40mgのカプセル)%medicine_name%(isotretinoin)絶食させたの下で そして供給された条件. ピーク血しょう集中(Cmax)および総露出両方 イソトレチノインの(AUC)は、標準化された高脂肪に続いて倍増した以上であった 絶食させた条件の下で与えられる%medicine_name%(isotretinoin)と比較されたとき食事(表2を見て下さい). 観察された除去半減期は変化しなかった. この半減期の変化の欠如 食糧が変わらないでisotretinoinの生物学的利用能を高めることを提案します その処分. ピーク濃度までの時間(Tmax)もまた、以下のように増加した。 食糧はより長い吸収段階と関連し、かもしれません. したがって、%medicine_name%(イソトレチノイン)カプセル 常に食べ物と一緒に摂取する必要があります(参照 適量および管理). 臨床 調査はisotretinoinのpharmacokineticsに相違がないことを示しました 結節性ざ瘡を有する患者と正常な皮膚を有する健常者との間にある。
表2:イソトレチノイン平均の薬物動態パラメータ
(%CV)、N=74
| %medicine_name%2x40mgカプセル | AUC0-∞(ngÃ-hr/mL) | Cmax(ng/mL) | Tmax(hr) | t½(hr) |
| Fed* | 10,004 (22%) | 862 (22%) | 5.3 (77%) | 21 (39%) |
| 断食 | 3,703 (46%) | 301 (63%) | 3.2 (56%) | 21 (30%) |
| *標準化された高脂肪の食事を食べること |
配布
イソトレチノインは、血漿タンパク質、主にアルブミンに99.9%以上結合している。
代謝
イソトレチノインの経口投与に続いて、少なくとも三つの代謝産物は ヒト血漿中で同定されている:4-オキソ-イソトレチノイン、レチノイン酸(トレチノイン), そして4-オクソ-レチノイン酸(4-オキソトレチノイン)。 レチノイン酸と13-cis-レチノイン 酸は幾何異性体であり、可逆的な相互変換を示す。 行政のことなら 一方の異性体のうち、他方の異性体を生じさせる。 イソトレチノインも不可逆的である 4-オキソ-イソトレチノインに酸化され、その幾何異性体である4-オキソ-トレチノインを形成する。
単一の後80%medicine_name%のmgの口頭線量(isotretinoin)への74健康な大人の主題,同時 食物の投与は、すべての代謝産物の形成の程度を増加させた 絶食させた条件の下の形成の程度と比較されたとき血しょうで。
すべてのこれらの代謝産物を持ちretinoid活動の一部 in vitro 親イソトレチノインのそれより多くを模倣します。 しかし、臨床 これらのモデルの意義は不明である。 複数の経口投与後 大人の嚢胞性のアクネの患者(≥18年)へのisotretinoinの、露出の 絶食させられ、与えられた条件の下の定常状態の4オキソisotretinoinへの患者 イソトレチノインの約3.4倍であった。
In vitroの調査はisotretinoinにかかわる第一次P450アイソフォームがことを示します 代謝は2C8、2C9、3A4、および2B6である。 イソトレチノインおよびその代謝産物は さらにコンジュゲートに代謝され、尿および糞便中に排泄される。
排除
液体として80c-イソトレチノインの14mgの線量の経口投与の後で 懸濁液、血の14Cactivityは90時間の半減期と減りました. これは、 イソトレチノインおよび共役の代謝物質はで最終的に排泄されます 糞便および尿は比較的同等量(合計65%から83%)である%). シングルの後に 80mg経口投与量%medicine_name%(イソトレチノイン)へ74健康な成人被験者の条件下で供給されます。, イソトレチノインの平均±SD除去半減期(tβ)および 4-オキソ-イソトレチノインは21.0 ± 8.2時間と24.0 ± 5.3時間, それぞれ. 単一および多数の線量の後で、観察された蓄積 イソトレチノインの比率は0から及びました.90万円~5万円.嚢胞性にきびの患者で43

-

-

2010年一月


