










Composition:
Application:
Utilisé dans le traitement:
Examiné médicalement par Fedorchenko Olga Valeryevna, Pharmacie Dernière mise à jour le 22.03.2022

Attention! Information sur la page est réservée aux professionnels de la santé! Les informations sont collectées dans des sources ouvertes et peuvent contenir des erreurs significatives! Soyez prudent et revérifiez toutes les informations de cette page!


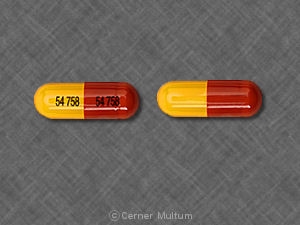
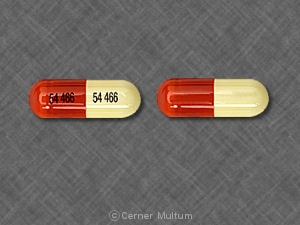
Capsules Tofranil-PM ™ (Imipramin pamoat)
Capsules 75 mg - corps de corail en relief en noir "M" et capuchon corallien imprimé en noir «Tofranil PM 75 mg».
Bouteilles de 30 ... € ... € ... ... € /.NDR 0406-9923-03
Capsules 100 mg - mais corps en relief en noir "M" et capuchon corallien imprimé en noir «Tofranil-PM 100 mg».
Bouteilles de 30 € / ... € /..........NDR 0406-9924-03
Capsules 125 mg - Corps ivoire en relief en noir "M" et capuchon corallien imprimé en noir «Tofranil-PM 125 mg».
Bouteilles de 30 € / ... € /..........NDR 0406-9925-03
Capsules 150 mg - corps de corail en relief en noir "M" et capuchon corallien imprimé en noir «Tofranil-PM 150 mg».
Bouteilles de 30 € / ... € /...........NDR 0406-9926-03
Conserver entre 20 ° et 25 ° C (68 ° et 77 ° F).
Dans un récipient hermétique (USP) avec une protection enfant Fermeture.
Réalisé par: Patheon Inc., Whitby, Ontario, Canada, L1N 5Z5. Conçu pour: Mallinckrodt Inc., Hazelwood, MO 63042 ÉTATS-UNIS. Révisé: 10/2012

pour soulager les symptômes de la dépression. Endogène La dépression est atténuée plutôt que d'autres conditions dépressives. Un aussi trois semaines de traitement peuvent être nécessaires avant d'obtenir des effets thérapeutiques optimaux évident.

Les doses recommandées suivantes pour Tofranil-PM devraient si nécessaire par la réponse clinique et toute preuve de Intolérance.
Posologie initiale pour les adultes
Patients ambulatoires
Le traitement doit être démarré avec 75 mg / jour. Le dosage peut l'être augmenté à 150 mg / jour, c'est-à-dire la dose à laquelle la réaction optimale est généralement reçu. Si nécessaire, la posologie peut être augmentée à 200 mg / jour.
Une posologie supérieure à 75 mg / jour peut également être administrée le une fois par jour après la détermination du dosage et de la tolérance optimaux. La posologie quotidienne peut être administrée avant le coucher. Chez certains patients, cela peut être nécessaire utiliser un schéma posologique partagé.
Comme pour tous les tricycliques, l'effet antidépresseur de L'imipramine peut ne pas être évidente chez certains patients pendant une à trois semaines.
Patients hospitalisés
La thérapie doit et peut être commencée avec 100 à 150 mg / jour être porté à 200 mg / jour. Si après deux semaines il n'y a pas de réaction, posologie doit être porté à 250 à 300 mg / jour.
Une posologie supérieure à 150 mg / jour peut également être administrée le une fois par jour après la détermination du dosage et de la tolérance optimaux. La posologie quotidienne peut être administrée avant le coucher. Chez certains patients, cela peut être nécessaire utiliser un schéma posologique partagé.
Comme pour tous les tricycliques, l'effet antidépresseur de L'imipramine peut ne pas être évidente chez certains patients pendant une à trois semaines.
Dose d'entretien pour les adultes
Après la rémission, les médicaments d'entretien peuvent être utilisés pendant une plus longue période au dose la plus faible qui maintient la rémission après laquelle le dosage doit être effectué être progressivement réduit.
La dose d'entretien habituelle est de 75 à 150 mg / jour. Globalement le dosage quotidien peut être administré une fois par jour, de préférence avant le coucher. Certains patients peuvent avoir besoin d'utiliser un schéma posologique partagé.
En cas de rechute due au retrait anticipé du Médicament, la posologie efficace de l'imipramine doit être restaurée.
Adolescents et patients gériatriques
La thérapie dans ces groupes d'âge doit être commencée Tofranil & trade;, marque de comprimés de chlorhydrate d'imipramine, en dose totale quotidienne de 25 à 50 mg car les gélules de Tofranil-PM n'y sont pas disponibles Force. La posologie peut être augmentée en fonction de la réaction et de la tolérance, mais c'est possible n'est généralement pas nécessaire pour dépasser 100 mg / jour chez ces patients. Tofranil PM Des capsules peuvent être utilisées si la dose quotidienne totale est fixée à 75 mg ou plus.
La dose quotidienne totale peut être administrée sur a une fois par jour, de préférence avant de se coucher. Chez certains patients, cela peut être nécessaire utiliser un schéma posologique partagé.
Comme pour tous les tricycliques, l'effet antidépresseur de L'imipramine peut ne pas être évidente chez certains patients pendant une à trois semaines.
Les adolescents et les patients gériatriques peuvent généralement l'être maintenu à des doses plus faibles. Après la rémission, les médicaments d'entretien peuvent l'être requis pour une période plus longue à la dose la plus faible maintenue rémission après laquelle la posologie doit être progressivement réduite.
La dose d'entretien quotidienne totale peut être administrée le une fois par jour, de préférence avant de se coucher. Chez certains patients, cela peut être nécessaire utiliser un schéma posologique partagé.
En cas de rechute due au retrait anticipé du Médicament, la posologie efficace de l'imipramine doit être restaurée.
Passez un patient vers ou depuis une monoamine oxydase Inhibiteur (IMAO) Pour le traitement des troubles psychiatriques
Entre l'arrêt de un IMAO pour le traitement des troubles psychiatriques et l'initiation d'un traitement par Tofranil-PM. À l'inverse, au moins 14 jours devraient être accordés après le sevrage Tofranil-PM avant de commencer un IMAO pour traiter les troubles psychiatriques (voir PRIX).
Utilisation de Tofranil-PM avec d'autres IMAO, comme Linezolid ou Bleu de méthylène
Ne commencez pas PM chez un patient d'Emil-PM qui traité avec du linezolide ou du bleu de méthylène intraveineux car il est augmenté Risque de syndrome sérotoninergique. Chez un patient, le traitement le plus urgent d'un état psychiatrique, autres interventions, y compris l'hospitalisation être pris en compte (voir CONTRAINDICATIONS).
Dans certains cas, un patient reçoit déjà Tofranil-PM le traitement peut nécessiter un traitement urgent avec du linézolide ou du méthylène intraveineux bleu. Si des alternatives acceptables au linézolide ou au bleu de méthylène intraveineux Le traitement n'est pas disponible et les avantages potentiels du linézolide ou un traitement intraveineux au bleu de méthylène est considéré comme l'emportant sur les risques de syndrome sérotoninergique chez un patient particulier, le tofranil PM doit être arrêté immédiatement et du bleu de méthylène linézolide ou intraveineux peut être administré. Le patient devrait être surveillé pour les symptômes du syndrome sérotoninergique pendant deux semaines ou jusqu'à 24 heures après la dernière dose de linézolide ou de bleu de méthylène intraveineux, selon la première éventualité d'abord. Le traitement par Tofranil-PM peut être redémarré 24 heures après la dernière dose de linezolid ou bleu de méthylène intraveineux (voir AVERTISSEMENTS).
Le risque d'administration de bleu de méthylène par voies non intraveineuses (telles que les comprimés oraux ou par injection locale) ou in les doses intraveineuses bien inférieures à 1 mg / kg avec le tofranil PM ne sont pas claires. Le Les cliniques doivent toujours être conscientes de la possibilité d'un émergent Symptômes du syndrome sérotoninergique avec une telle utilisation (voir AVERTISSEMENTS).

Inhibiteur de la monoamine oxydase (IMAO)
L'utilisation des IMAO pour traiter les troubles psychiatriques avec Tofranil-PM ou dans les 14 jours après l'arrêt du traitement par Tofranil-PM contre-indiqué en raison d'un risque accru de syndrome sérotoninergique. L'utilisation de Tofranil-PM dans les 14 jours suivant l'arrêt d'un IMAO pour le traitement des psychiatres il est également contre-indiqué (voir AVERTISSEMENTS et DOSAGE ET ADMINISTRATION).
De tofranil PM chez un patient traité avec des IMAO comme le linézolide ou le bleu de méthylène intraveineux est également contre-indiqué en raison d'un risque accru de syndrome sérotoninergique (voir AVERTISSEMENTS et DOSAGE et ADMINISTRATION).
Infarctus du myocarde
Le médicament est contre-indiqué pendant la récupération aiguë Période après un infarctus du myocarde.
Hypersensibilité aux antidépresseurs tricycliques
Patients présentant une hypersensibilité connue à ce composé le médicament ne doit pas être administré. La possibilité d'une sensibilité croisée aux autres les composés de la dibenzazépine doivent être pris en compte.

WARNHINWEISE
Klinische Verschlechterung und Suizidrisiko
Patienten mit schwerer depressiver Störung (MDD), beide Erwachsene und pädiatrisch, kann eine Verschlechterung Ihrer depression und/oder der Entstehung von Suizidgedanken und-Verhalten (Suizidalität) oder ungewöhnliche Veränderungen in Verhalten, ob Sie Antidepressiva einnehmen oder nicht, und dies das Risiko kann bestehen bleiben, bis eine signifikante remission Auftritt. Selbstmord ist ein bekanntes Risiko von depression und bestimmte andere psychiatrische Störungen und diese Störungen Sie selbst sind die stärksten Prädiktoren für Selbstmord. Es gab eine langjährige Bedenken jedoch, dass Antidepressiva eine Rolle bei der depression und die Entstehung von Suizidalität bei bestimmten Patienten während der frühe Phasen der Behandlung. Gepoolte Analysen von kurzfristigen placebokontrollierten Studien mit Antidepressiva (SSRIs und anderen) zeigten, dass diese Medikamente erhöhen Sie das Risiko von Selbstmordgedanken und-Verhalten (Suizidalität) bei Kindern, Jugendliche und junge Erwachsene (Alter 18-24) mit schwerer depressiver Störung (MDD) und andere psychiatrische Störungen. Kurzzeitstudien zeigten keinen Anstieg der das suizidalitätsrisiko bei Antidepressiva im Vergleich zu placebo bei Erwachsenen Alter 24; es gab eine Reduktion mit Antidepressiva im Vergleich zu placebo bei Erwachsenen ab 65 Jahren.
Die gepoolten Analysen von placebokontrollierten Studien in Kinder und Jugendliche mit MDD, Zwangsstörung (OCD) oder andere psychiatrische Störungen umfassten insgesamt 24 Kurzzeitstudien mit 9 Antidepressiva bei über 4400 Patienten. Die gepoolten Analysen von placebokontrollierte Studien bei Erwachsenen mit MDD oder anderen psychiatrischen Störungen enthalten insgesamt 295 Kurzzeitstudien (mittlere Dauer von 2 Monaten) mit 11 Antidepressiva Drogen bei über 77.000 Patienten. Es gab erhebliche Unterschiede im Suizidrisiko unter Drogen, aber eine Tendenz zu einer Zunahme der jüngeren Patienten für fast alle untersuchten Drogen. Es gab Unterschiede im absoluten Suizidrisiko über die verschiedenen Indikationen hinweg mit der höchsten Inzidenz bei MDD. Risiko Unterschiede (Medikament gegen placebo) waren jedoch im Alter relativ stabil Schichten und über Indikationen. Diese risikounterschiede (Drogen-placebo-Unterschied in der Anzahl der Fälle von Suizidalität pro 1000 behandelte Patienten) zur Verfügung gestellt in Tabelle 1.
Tabelle 1
In keinem der pädiatrischen Studien traten Selbstmorde auf. Es gab Selbstmorde in den erwachsenenversuchen, aber die Zahl reichte nicht aus, um erreichen Sie jede Schlussfolgerung über Drogen Wirkung auf Selbstmord.
Es ist nicht bekannt, ob sich das suizidalitätsrisiko auf längerfristige Nutzung, D. H. über mehrere Monate hinaus. Es gibt jedoch erhebliche Belege aus placebo-kontrollierten Wartungs-Studien bei Erwachsenen mit depression dass die Verwendung von Antidepressiva das Wiederauftreten von Depressionen verzögern kann.
Alle Patienten, die mit Antidepressiva behandelt werden für jede Indikation sollte angemessen überwacht und genau beobachtet werden für klinische Verschlechterung, Suizidalität und ungewöhnliche Verhaltensänderungen, insbesondere während der ersten paar Monate eines Kurses der medikamentösen Therapie oder zu Zeiten der Dosis änderungen, entweder erhöht oder verringert.
Die folgenden Symptome, Angst, Unruhe, Panik Angriffe, Schlaflosigkeit, Reizbarkeit, Feindseligkeit, Aggressivität, Impulsivität, Akathisie (Psychomotorische Unruhe), Hypomanie und Manie wurden berichtet bei Erwachsenen und pädiatrischen Patienten, die mit Antidepressiva für major behandelt werden depressive Störung sowie für andere Indikationen, sowohl psychiatrische und nonpsychiatric. Obwohl ein ursächlicher Zusammenhang zwischen der Entstehung solcher Symptome und entweder die Verschlechterung der depression und/oder die Entstehung von suizidalen Impulsen wurde nicht festgestellt, besteht die Sorge, dass solche Symptome Vorläufer darstellen können zur aufkommenden Suizidalität.
Es sollte überlegt werden, das therapeutische zu ändern Regime, einschließlich möglicherweise absetzen der Medikamente, bei Patienten, deren depression ist hartnäckig schlimmer, oder wer erlebt emergente Suizidalität oder Symptome, die Vorläufer für eine Verschlechterung der depression oder Suizidalität sein könnten, besonders wenn diese Symptome schwerwiegend sind, abrupt auftreten oder nicht Teil von der patient zeigt Symptome.
Familien und Betreuer von Patienten, die mit Antidepressiva für schwere depressive Störungen oder andere Indikationen, beide psychiatrische und nichtpsychiatrische, sollte über die Notwendigkeit zu überwachen alarmiert werden Patienten für die Entstehung von Unruhe, Reizbarkeit, ungewöhnliche Veränderungen in Verhalten, und die anderen oben beschriebenen Symptome, sowie die Entstehung von Suizidalität und solche Symptome sofort an Gesundheitsdienstleister zu melden. Eine solche überwachung sollte die tägliche Beobachtung durch Familien und Betreuer umfassen. Rezepte für Imipramin sollte pamoat für die kleinste Menge Kapseln geschrieben werden im Einklang mit einem guten Patientenmanagement, um das Risiko von Überdosierung.
Screening von Patienten auf Bipolare Störung
Eine große depressive episode kann die Initiale sein Präsentation der bipolaren Störung. Es wird allgemein angenommen (wenn auch nicht in kontrollierten Studien festgestellt), dass die Behandlung einer solchen episode mit einem Antidepressivum allein kann die Wahrscheinlichkeit einer Ausfällung eines gemischte / manische episode bei Patienten mit einem Risiko für eine bipolare Störung. Ob einer von die oben beschriebenen Symptome stellen eine solche Umwandlung dar, die unbekannt ist. Jedoch, vor Beginn der Behandlung mit einem Antidepressivum, Patienten mit depressiven Symptome sollten angemessen gescreent werden, um festzustellen, ob Sie gefährdet sind für bipolare Störung; ein solches screening sollte eine detaillierte psychiatrische Anamnese enthalten, einschließlich einer Familiengeschichte von Selbstmord, bipolarer Störung und depression. Es zu beachten ist, dass Imipramin pamoat nicht zur Anwendung bei der Behandlung zugelassen ist bipolare depression.
Äußerste Vorsicht ist geboten, wenn dieses Medikament verabreicht wird Patienten mit Herz-Kreislauf-Erkrankungen wegen der Möglichkeit der Leitung defekte, Arrhythmien, kongestive Herzinsuffizienz, Myokardinfarkt, Schlaganfälle, und Tachykardie. Diese Patienten benötigen überhaupt eine herzüberwachung. Ebenen des Medikaments; Patienten mit erhöhtem Augeninnendruck, Geschichte von Harnverhalt oder Anamnese eines engwinkelglaukoms aufgrund des Arzneimittels anticholinerge Eigenschaften; Hyperthyreose Patienten oder solche mit schilddrüsenmedikation wegen der Möglichkeit der kardiovaskulären Toxizität; Patienten mit einer Geschichte der anfallsstörung, weil gezeigt wurde, dass dieses Medikament den Anfall senkt Schwellenwert; Patienten, die guanethidin, Clonidin oder ähnliche Mittel erhalten, da Imipramin pamoat kann die pharmakologischen Wirkungen dieser Medikamente blockieren; Patienten empfangen von methylphenidathydrochlorid. Seit methylphenidathydrochlorid kann den Metabolismus von Imipramin pamoat hemmen, Dosisanpassung nach unten von Imipramin pamoat kann erforderlich sein, wenn es gleichzeitig mit Methylphenidat-Hydrochlorid.
Da Imipramin pamoat die geistige und / oder körperliche Fähigkeiten, die für die Ausführung potenziell gefährlicher Aufgaben erforderlich sind, wie der Betrieb eines Automobils oder einer Maschine sollte der patient gewarnt werden dementsprechend.
Tofranil-PM kann die ZNS-depressiven Wirkungen verstärken von Alkohol. Daher sollte berücksichtigt werden, dass die Gefahren, die einem Selbstmordversuch oder versehentliche überdosierung mit dem Medikament kann für die erhöht werden patient, der übermäßige Mengen an Alkohol verwendet (siehe VORSICHTSMAßNAHMEN).
Serotonin Syndrom
Die Entwicklung eines potenziell lebensbedrohlichen serotonin-Syndrom wurde mit SNRIs und SSRIs berichtet, einschließlich Tofranil-PM, allein, aber besonders bei gleichzeitiger Anwendung anderer serotonergika Drogen (einschließlich Triptane, trizyklische Antidepressiva, fentanyl, lithium, tramadol, tryptophan, Buspiron und Johanniskraut) und mit Drogen, die Beeinträchtigung des Metabolismus von serotonin (insbesondere MAOIs, die beide dazu bestimmt sind, behandeln Sie psychiatrische Störungen und auch andere, wie linezolid und intravenös Methylenblau).
Serotonin-Syndrom Symptome können psychischen status umfassen Veränderungen (Z. B. Erregung, Halluzinationen, delirium und Koma), autonom Instabilität (Z. B. Tachykardie, labiler Blutdruck, Schwindel, Diaphorese, Spülung, Hyperthermie), neuromuskuläre Veränderungen (Z. B. tremor, Steifigkeit, Myoklonus, Hyperreflexie, Koordinationsstörungen), Krampfanfälle und / oder Magen-Darm-Erkrankungen Symptome (Z. B. übelkeit, Erbrechen, Durchfall). Patienten sollten überwacht werden für die Entstehung des serotonin-Syndroms.
Die gleichzeitige Anwendung von Tofranil-PM mit MAOIs soll Behandlung psychiatrischer Störungen ist kontraindiziert. Tofranil-PM sollte auch nicht sein begonnen bei einem Patienten, der mit MAOIs wie linezolid behandelt wird oder intravenöses Methylenblau. Alle Berichte mit Methylenblau die zur Verfügung gestellt Informationen über den verabreichungsweg und die intravenöse Verabreichung im Dosisbereich von 1 mg/kg bis 8 mg/kg. Keine Berichte bei der Verwaltung Methylenblau auf anderen wegen (Z. B. orale Tabletten oder lokale gewebeinjektion) oder bei niedrigeren Dosen. Es kann Umstände geben, unter denen die Behandlung eingeleitet werden muss mit einem MAOI wie linezolid oder intravenösem Methylenblau bei einem Patienten, der Tofranil-PM. Tofranil-PM sollte vor Beginn der Behandlung abgebrochen werden mit dem MAOI (siehe KONTRAINDIKATIONEN und DOSIERUNG und VERABREICHUNG).
Bei gleichzeitiger Anwendung von Tofranil-PM mit anderen serotonergen Medikamente, einschließlich Triptane, trizyklische Antidepressiva, fentanyl, lithium, tramadol, Buspiron, tryptophan und Johanniskraut ist klinisch gerechtfertigt, Patienten sollten auf ein potenziell erhöhtes Risiko für serotonin aufmerksam gemacht werden Syndrom, insbesondere während der Einleitung der Behandlung und dosiserhöhungen.
Behandlung mit Tofranil-PM und jeder Begleitperson serotonerge Mittel sollten sofort abgesetzt werden, wenn die oben genannten Ereignisse eine wirksame und unterstützende symptomatische Behandlung sollte eingeleitet werden.
VORSICHTSMAßNAHMEN
allgemein
Eine EKG-Aufzeichnung sollte vor der Einleitung erfolgen von größeren als üblichen Dosen Imipramin-pamoat und in geeigneten Intervallen danach, bis steady-state erreicht ist. (Patienten mit jeglichen Anzeichen von Herz-Kreislauf-Erkrankungen erfordern eine herzüberwachung auf allen dosierungsstufen des Droge. Siehe WARNUNGEN.) Ältere Patienten und Patienten mit Herzerkrankungen oder eine Vorgeschichte von Herzerkrankungen sind einem besonderen Risiko der Entwicklung der herzanomalien im Zusammenhang mit der Verwendung von Imipramin pamoat. Es sollte beachten Sie, dass die Möglichkeit des Selbstmordes bei schwer depressiven Patienten ist der Krankheit inhärent und kann bestehen bleiben, bis eine signifikante remission Auftritt. Solche Patienten sollten während der frühen phase von sorgfältig überwacht werden Behandlung mit Imipramin pamoat und kann einen Krankenhausaufenthalt erfordern. Rezept sollte für den kleinsten möglichen Betrag geschrieben werden.
Hypomanische oder manische Episoden können auftreten, insbesondere bei Patienten mit zyklischen Störungen. Solche Reaktionen können ein absetzen erfordern der Droge. Bei Bedarf kann Imipramin pamoat in niedrigerer Dosierung wieder aufgenommen werden, wenn diese Episoden sind erleichtert.
Die Verabreichung eines Beruhigungsmittels kann nützlich sein bei Kontrolle solcher Episoden. Eine Aktivierung der Psychose kann gelegentlich sein beobachtet bei schizophrenen Patienten und kann eine Dosisreduktion erfordern und die Zugabe eines phenothiazins.
Gleichzeitige Verabreichung von Imipramin pamoat mit Elektroschocktherapie kann die Gefahren erhöhen: eine solche Behandlung sollte begrenzt sein für diejenigen Patienten, für die es wichtig ist, da es begrenzte klinische Erfahrung.
Patienten, die Imipramin pamoat einnehmen, sollten übermäßiges Exposition gegenüber Sonnenlicht, da es Berichte über Photosensibilisierung gab.
Sowohl die Erhöhung als auch die Senkung des Blutzuckerspiegels haben wurde mit Imipramin pamoat Verwendung berichtet.
Imipramin pamoat sollte mit Vorsicht angewendet werden bei Patienten mit signifikant eingeschränkter Nieren-oder Leberfunktion.
Patienten, die Fieber und Halsschmerzen entwickeln während die Therapie mit Imipramin pamoat sollte Leukozyten - und differentialblut haben Zählungen durchgeführt.
Imipramin pamoat sollte abgesetzt werden, wenn es Hinweise auf eine pathologische Neutrophile depression.
Vor der elektiven Operation sollte Imipramin pamoat sein so lange unterbrochen, wie es die klinische situation zulässt.
Informationen für Patienten
Verschreibende ärzte oder andere Angehörige der Gesundheitsberufe sollten informieren Patienten, Ihre Familien und Ihre Betreuer über die Vorteile und Risiken verbunden mit der Behandlung mit Imipramin pamoat und sollte Sie beraten in seine angemessene Verwendung. Ein patient Medikation Guide über “Antidepressivum Medikamente, Depressionen und andere Schwere psychische Erkrankungen und Selbstmordgedanken oder Aktionen” ist für Imipramin pamoat verfügbar. Der verschreibende Arzt oder die Gesundheit professional sollte Patienten, Ihre Familien und Ihre Betreuer anweisen, Lesen Sie den Medikationsleitfaden und sollte Ihnen helfen, seinen Inhalt zu verstehen. Patienten sollten die Möglichkeit gegeben werden, den Inhalt des Medikation Führer und Antworten auf alle Fragen zu erhalten, die Sie haben können. Der vollständiger text des Medikationsleitfadens wird am Ende dieses Dokuments nachgedruckt.
Patienten sollten über folgende Probleme informiert werden und gebeten, Ihren verschreibenden Arzt zu alarmieren, wenn diese während der Einnahme von Imipramin pamoat auftreten.
Klinische Verschlechterung und Suizidrisiko
Patienten, Ihre Familien und Ihre Betreuer sollten ermutigt, wachsam zu sein, um die Entstehung von Angst, Unruhe, Panikattacken, Schlaflosigkeit, Reizbarkeit, Feindseligkeit, Aggressivität, Impulsivität, Akathisie (Psychomotorische Unruhe), Hypomanie, Manie, andere ungewöhnliche Verhaltensänderungen, Verschlechterung der depression, und Suizidgedanken, besonders früh während der Antidepressiven Behandlung und wenn die Dosis wird nach oben oder unten angepasst. Familien und Betreuer von Patienten sollten beraten werden um das auftreten solcher Symptome auf einer täglichen basis zu suchen, da änderungen kann abrupt sein. Solche Symptome sollten dem verschreibenden Arzt des Patienten gemeldet werden oder Angehörige der Gesundheitsberufe, insbesondere wenn Sie schwerwiegend, abrupt auftreten oder waren nicht Teil der Symptome des Patienten. Symptome wie diese können sein verbunden mit einem erhöhten Risiko für suizidales denken und Verhalten und zeigen eine Notwendigkeit für eine sehr enge überwachung und möglicherweise änderungen in der Medikament.
Schwangerschaft
Tierexperimentelle Studien haben dabei nicht schlüssig Ergebnisse (siehe auch Tier-Pharmakologie & Toxikologie).
Es wurden keine gut kontrollierten Studien mit schwangere Frauen, um die Wirkung von Imipramin auf den Fötus zu bestimmen. Jedoch, es gab klinische Berichte über angeborene Fehlbildungen im Zusammenhang mit die Verwendung der Droge. Obwohl ein kausaler Zusammenhang zwischen diesen Effekten und das Medikament konnte nicht nachgewiesen werden, die Möglichkeit eines fetalen Risikos von der die mütterliche Einnahme von Imipramin kann nicht ausgeschlossen werden. Daher Imipramin sollte nur bei Frauen angewendet werden, die Schwanger sind oder werden könnten, wenn die klinische der Zustand rechtfertigt eindeutig ein potenzielles Risiko für den Fötus.
Stillende Mütter
Begrenzte Daten deuten darauf hin, dass Imipramin wahrscheinlich ist ausgeschieden in der menschlichen Muttermilch. In der Regel sollte eine Frau, die ein Medikament einnimmt, nicht notwendig, da die Möglichkeit besteht, dass das Medikament in der Brust ausgeschieden werden kann Milch und schädlich für das Kind sein.
Pädiatrische Anwendung
Sicherheit und Wirksamkeit in der pädiatrischen Bevölkerung haben nicht etabliert (siehe BOX WARNUNG und WARNUNGEN, ) Verschlechterung und Suizidrisiko).
Es wird allgemein empfohlen, dass Tofranil-PM nicht bei Kindern wegen des erhöhten Potenzials für akute überdosierung aufgrund von die hohe Potenz Einheit (75 mg, 100 mg, 125 mg und 150 mg). Jede Kapsel enthält imipramine pamoate entspricht 75 mg, 100 mg, 125 mg oder 150 mg imipraminhydrochlorid. Jeder, der die Verwendung von Imipramin pamoat in a in Betracht zieht Kinder oder Jugendliche müssen die potenziellen Risiken mit dem klinischen Bedarf abwägen.
Geriatrische Anwendung
In der Literatur gab es vier gut kontrolliert, randomisierte, doppelblinde, parallele gruppenvergleiche klinische Studien mit Tofranil & trade;, Marke von imipraminhydrochlorid-Tabletten, bei älteren Menschen Bevölkerung. Es wurde eine Gesamtzahl von 651 Fächern, die in diesen Studien. Diese Studien lieferten keinen Vergleich zu jüngeren Probanden. Es gab keine zusätzliche unerwünschte Erfahrungen bei älteren Menschen festgestellt.
Klinische Studien von Tofranil & trade;, Marke von Imipramin Hydrochlorid-Tabletten, in der ursprünglichen Anwendung enthalten nicht ausreichend Anzahl der Probanden ab 65 Jahren, um festzustellen, ob Sie Antworten anders als jüngere Probanden. Klinische Erfahrung nach dem Inverkehrbringen hat nicht identifizierte Unterschiede in den Reaktionen zwischen älteren und jüngeren Probanden. Im Allgemeinen sollte die dosisauswahl für ältere Menschen vorsichtig sein, normalerweise beginnend am unteren Ende des dosierbereichs, was eine größere Häufigkeit von verminderten Leber -, Nieren-oder Herzfunktion sowie von Begleiterkrankungen oder anderen Arzneimitteln Therapie. (siehe auch DOSIERUNG UND VERABREICHUNG bei Jugendlichen und Geriatrisch Patienten) (siehe auch VORSICHTSMAßNAHMEN, allgemein)
| Altersgruppe | Drug-Placebo-Unterschied in der Anzahl der Fälle von Suizidalität pro 1000 Patienten Behandelt |
| Erhöht sich im Vergleich zu Placebo | |
| < 18 | 14 weitere Fälle |
| 18-24 | 5 weitere Fälle |
| Nimmt im Vergleich zu Placebo ab | |
| 25-64 | 1 weniger Fall |
| ≥ 65 | 6 weniger Fälle |

Effets secondaires
Remarque: bien que la liste suivante en contienne Effets secondaires qui n'ont pas été signalés avec ce médicament spécifique nécessitent des similitudes pharmacologiques entre les antidépresseurs tricycliques que chacune des réactions est prise en compte lors de l'administration d'imipramine.
Cardiovasculaire
Hypotension orthostatique, hypertension, tachycardie, Palpitations, infarctus du myocarde, arythmies, bloc cardiaque, changements ECG, Symptômes d'insuffisance cardiaque congestive, accident vasculaire cérébral.
Psychiatrique
Conditions confuses (en particulier chez les personnes âgées) avec Hallucinations, désorientation, délires; Anxiété, agitation, agitation; Insomnie et cauchemars; Hypomanie; Aggravation de la psychose.
Neurologique
Surdité, picotements, paresthésie des extrémités; Coordination, ataxie, tremblements; neuropathie périphérique; extrapyramidal Symptômes; Convulsions, changements dans les schémas EEG; acouphènes.
Anticholinergique
Bouche sèche et adénite sublinguale rarement associée; voir flou, troubles de l'hébergement, mydriase; Constipation, iléus paralytique; Rétention urinaire, miction retardée, expansion du Tractus urinaires.
Allergique
Éruption cutanée, pétéchies, urticaire, démangeaisons , Photosensibilisation; œdème (gonflement général du visage et de la langue); fièvre liée à la drogue ; Sensibilité croisée à la désipramine.
Hématologique
Dépression de la moelle osseuse, y compris agranulocytose; Éosinophilie; purpura; Thrombocytopénie.
Tractus digestif
Nausées et vomissements, anorexie, stress épigastrique, Diarrhée; goût étrange, stomatite, crampes abdominales, langue noire.
Glande endocrinienne
Gynécomastie chez l'homme; Augmentation mammaire et Galactorrhée chez la femme; augmentation ou diminution de la libido, impuissance; gonflement des testicules; Augmentation ou dépression de la glycémie ; hormone antidiurétique inappropriée (ADH) - syndrome de sécrétion.
Autre
Jaunisse (simule obstructif); changement de foie Fonction; Gain ou perte de poids; Soudage; Rinçage; fréquence de durcissement; somnolence, étourdissements, faiblesse et fatigue; Mal de tête; gonflement parotide ; Alopécie; Tendance à tomber.
Symptômes de sevrage
Bien qu'il n'y ait aucune référence aux recherches, arrêtez brusquement le traitement après un traitement prolongé peut provoquer des nausées, des maux de tête et des malaises.
Interactions avec les MÉDICAMENTS
Médicaments métabolisés par P450 2d6
L'activité biochimique du médicament qui métabolise l'isozyme Le cytochrome P450 2D6 (débrisoquin hydroxylase) est réduit dans un sous-ensemble du Caucase Personnes (environ 7% à 10% des Caucasiens sont dits «mauvais métaboliseurs») estimations fiables de la prévalence de l'activité isozyme P450 2D6 réduite Les populations asiatiques, africaines et autres ne sont pas encore disponibles. Pauvre
les métaboliseurs ont un plasma plus élevé que prévu Concentrations d'antidépresseurs tricycliques (TCA) à des doses normales. Selon la fraction du médicament métabolisée par P450 2d6, l'augmentation la concentration plasmatique peut être faible ou assez importante (augmentation de 8 fois du plasma AUC du TCA).
De plus, certains médicaments inhibent leur activité isozyme et faire ressembler les métaboliseurs normaux à de mauvais métaboliseurs. Individuel si vous êtes stable à une dose donnée de TCA, vous pouvez devenir brusquement toxique si vous en obtenez un de ces médicaments inhibiteurs en tant que traitement concomitant. Les médicaments qui inhibent Le cytochrome P450 2D6 en comprend certains qui ne sont pas métabolisés par l'enzyme (Chinidine; Cimétidine) et beaucoup de substrats pour P450 2D6 (beaucoup d'autres Antidépresseurs, phénothiazines et propafénone antiarythmique de type 1C et flycaïnide). Alors que tous les inhibiteurs sélectifs du recaptage de la sérotonine (ISRS), par exemple., La fluoxétine, la sertraline et la paroxétine inhibent P450 2D6, elles peuvent varier dans la mesure de l'inhibition. Dans quelle mesure des interactions SSRI-TCA peuvent se produire les problèmes cliniques dépendent du degré d'inhibition et du Pharmacocinétique des ISRS impliqués. Cependant, la prudence est recommandée la co-administration des TCA avec l'un des ISRS et également lors de la conversion une classe à une autre. Un temps suffisant doit passer par une importance particulière avant de commencer le traitement par TCA chez un patient retiré de la fluoxétine compte tenu de la longue demi-vie du parent et du métabolite actif (au moins 5 semaines peut être nécessaire).
Utilisation simultanée d'antidépresseurs tricycliques avec des médicaments cela peut inhiber le cytochrome P450 2d6, nécessitant peut-être des doses plus faibles que la normale prescrit soit pour l'antidépresseur tricyclique, soit pour l'autre médicament. En outre, chaque fois que l'un de ces autres médicaments est retiré de la co-thérapie, une augmentation augmente Une dose d'antidépresseurs tricycliques peut être nécessaire. Il est souhaitable de surveiller Taux plasmatiques de TCA lorsqu'un TCA est administré avec un autre Médicament connu comme inhibiteur de P450 2D6.
La concentration plasmatique d'imipramine peut augmenter si le médicament est co-administré avec des inhibiteurs de l'enzyme hépatique (Z., Cimétidine, fluoxétine) et diminution due à l'administration simultanée avec le foie inducteurs d'enzymes (par ex. barbituriques, phénytoïne) et ajustement de la posologie L'imipramine peut donc être nécessaire.
Chez les patients parfois sensibles ou chez ceux qui Les anticholinergiques (y compris les agents antiparkinsoniens) sont également les Les effets de type atropine peuvent devenir plus prononcés (par ex. iléus paralytique). Fermer Une surveillance et un ajustement minutieux de la posologie sont nécessaires en cas d'imipramine le pamoate est administré simultanément avec des anticholinergiques.
Évitez d'utiliser des préparations telles que des agents et Anesthésiques locaux qui contiennent chaque amine sympathomimétique (par ex. épinéphrine, Norepinéphrine) car il a été signalé que les antidépresseurs tricycliques peuvent le faire potentialiser les effets des catécholamines.
La prudence s'impose lorsque l'imipramine est du pamoate utilisé avec des agents qui abaissent la pression artérielle. L'imipramine pamoat peut potentialiser les effets des dépresseurs du SNC.
Les patients doivent être avertis que l'imipramine peut pamoate augmenter les effets dépressifs de l'alcool sur le SNC (voir AVERTISSEMENTS).
Inhibiteur de la monoamine oxydase (IMAO)
(Voir CONTRAINDICATIONS, AVERTISSEMENTS et DOSAGE Et l'ADMINISTRATION.)
Médicaments sérotoninergiques
(Voir CONTRAINDICATIONS, AVERTISSEMENTS et DOSAGE et ADMINISTRATION.)

Les études animales ne sont pas concluantes Résultats (voir aussi Pharmacologie animale et toxicologie).
Il n'y avait aucune étude bien contrôlée avec femmes enceintes pour déterminer l'effet de l'imipramine sur le fœtus. Toutefois des rapports cliniques de malformations congénitales ont été rapportés l'utilisation du médicament. Bien qu'il s'agisse d'une relation causale entre ces effets et le médicament n'a pas pu être prouvé, la possibilité d'un risque fœtal de la l'apport maternel d'imipramine ne peut être exclu. D'où l'imipramine ne doit être utilisé que chez les femmes enceintes ou susceptibles de devenir enceintes si la clinique la condition justifie clairement un risque potentiel pour le fœtus.

Remarque: bien que la liste suivante en contienne Effets secondaires qui n'ont pas été signalés avec ce médicament spécifique nécessitent des similitudes pharmacologiques entre les antidépresseurs tricycliques que chacune des réactions est prise en compte lors de l'administration d'imipramine.
Cardiovasculaire
Hypotension orthostatique, hypertension, tachycardie, Palpitations, infarctus du myocarde, arythmies, bloc cardiaque, changements ECG, Symptômes d'insuffisance cardiaque congestive, accident vasculaire cérébral.
Psychiatrique
Conditions confuses (en particulier chez les personnes âgées) avec Hallucinations, désorientation, délires; Anxiété, agitation, agitation; Insomnie et cauchemars; Hypomanie; Aggravation de la psychose.
Neurologique
Surdité, picotements, paresthésie des extrémités; Coordination, ataxie, tremblements; neuropathie périphérique; extrapyramidal Symptômes; Convulsions, changements dans les schémas EEG; acouphènes.
Anticholinergique
Bouche sèche et adénite sublinguale rarement associée; voir flou, troubles de l'hébergement, mydriase; Constipation, iléus paralytique; Rétention urinaire, miction retardée, expansion du Tractus urinaires.
Allergique
Éruption cutanée, pétéchies, urticaire, démangeaisons , Photosensibilisation; œdème (gonflement général du visage et de la langue); fièvre liée à la drogue ; Sensibilité croisée à la désipramine.
Hématologique
Dépression de la moelle osseuse, y compris agranulocytose; Éosinophilie; purpura; Thrombocytopénie.
Tractus digestif
Nausées et vomissements, anorexie, stress épigastrique, Diarrhée; goût étrange, stomatite, crampes abdominales, langue noire.
Glande endocrinienne
Gynécomastie chez l'homme; Augmentation mammaire et Galactorrhée chez la femme; augmentation ou diminution de la libido, impuissance; gonflement des testicules; Augmentation ou dépression de la glycémie ; hormone antidiurétique inappropriée (ADH) - syndrome de sécrétion.
Autre
Jaunisse (simule obstructif); changement de foie Fonction; Gain ou perte de poids; Soudage; Rinçage; fréquence de durcissement; somnolence, étourdissements, faiblesse et fatigue; Mal de tête; gonflement parotide ; Alopécie; Tendance à tomber.
Symptômes de sevrage
Bien qu'il n'y ait aucune référence aux recherches, arrêtez brusquement le traitement après un traitement prolongé peut provoquer des nausées, des maux de tête et des malaises.

Des décès peuvent survenir en raison d'une surdose avec cette classe de Médicament. L'usage multiple de drogues (y compris l'alcool) est délibéré surdosage tricyclique. Étant donné que le complexe de gestion est et change, il l'est a recommandé au médecin de contacter un centre anti-poison pour les centres actuels Informations sur le traitement. Les signes et symptômes de toxicité se développent rapidement surdosage tricyclique. Une surveillance hospitalière est donc nécessaire dans les plus brefs délais.
Les enfants seraient plus sensibles que Adultes à une surdose aiguë de pamoate d'imipramine. Une surdose aiguë de tout le monde La quantité chez les nourrissons ou les jeunes enfants, en particulier, doit être considérée comme grave et potentiellement mortel.
Apparences
Ceux-ci peuvent varier en gravité en fonction de facteurs tels que la quantité de médicament absorbé, l'âge du patient et l'intervalle entre Prendre des médicaments et commencer le traitement. Manifestations critiques d'une surdose comprennent un rythme cardiaque irrégulier, une hypotension sévère, des crampes et du SNC dépression, y compris le coma. Changements dans l'électrocardiogramme, en particulier dans L'axe ou la largeur QRS sont des indicateurs cliniquement significatifs de la toxicité tricyclique.
D'autres manifestations du SNC peuvent inclure la somnolence, la stupeur Ataxie, agitation, agitation, réflexes hyperactifs, raideur musculaire, mouvements athétoïdes et choréiformes.
Les anomalies cardiaques peuvent inclure la tachycardie et les signes d'échec congestif. Dépression respiratoire, cyanose, choc, vomissements, une hyperpyrexie, une mydriase et une diaphorèse peuvent également être présentes.
Administration
Recevez un électrocardiogramme et lancez immédiatement votre cœur Surveillance. Protégez les voies respiratoires du patient, établissez une ligne intraveineuse et initier une décontamination de l'estomac. Au moins 6 heures d'observation avec surveillance et observation cardiaques des signes de SNC ou de dépression respiratoire L'hypotension, les arythmies cardiaques et / ou les blocages et les convulsions linéaires le sont nécessaire. Si des signes de toxicité se produisent à tout moment au cours de cette période, prolongés une surveillance est nécessaire. Il y a des rapports de cas de patients qui succombent à des dysrythmies mortelles tard après une surdose; ces patients avaient des signes cliniques d'intoxication importante avant la mort et la plupart ont reçu une décontamination gastro-intestinale insuffisante. La surveillance des taux plasmatiques de médicaments ne doit pas guider la gestion du patient.
Décontamination gastro-intestinale
Tous les patients soupçonnés d'être tricycliques surdosés doivent recevoir une décontamination gastro-intestinale. Cela devrait être de grand volume. Lavage gastrique suivi d'un charbon actif. Lorsque la conscience est altérée, les voies respiratoires doit être fixé avant le lavage. L'émèse est contre-indiquée.
Cardiovasculaire
Une durée maximale de QRS de plomb de membre ≥ 0,10 seconde peut être la meilleure indication du surdosage sévère. Sodium intraveineux Le bicarbonate doit être utilisé pour ajuster le pH sérique dans la plage de 7,45 à 7.55. Si la réponse au pH est insuffisante, une hyperventilation peut également être utilisée. L'utilisation simultanée d'hyperventilation et de bicarbonate de sodium doit être effectuée extrême prudence avec une surveillance fréquente du pH. Un pH> 7,60 ou un pCO2 <20 mmHg n'est pas souhaitable.
Les dysrythmies ne répondent pas au bicarbonate de sodium La thérapie / hyperventilation peut répondre à la lidocaïne, au brétylium ou à la phénytoïne. Les antiarythmiques de type 1A et 1C sont généralement contre-indiqués (par ex. quinidine , Disopyramide et procaïnamide).
Dans de rares cas, une hémoperfusion peut être bénéfique instabilité cardiovasculaire réfractaire aiguë chez les patients présentant une toxicité aiguë. Hémodialyse, dialyse péritonéale, transfusions d'échange et forcées La diurèse a généralement été jugée inefficace lors de l'intoxication tricyclique.
CNS
L'intubation précoce concerne les patients souffrant de dépression du SNC donner son avis sur la possibilité d'une détérioration brutale. Les saisies devraient l'être contrôlés avec des benzodiazépines ou s'ils sont inefficaces, d'autres Anticonvulsivants (par ex. phénobarbital, phénytoïne).
La physostigmine n'est pas recommandée, sauf pour le traitement des personnes potentiellement mortelles Symptômes qui n'ont pas répondu à d'autres thérapies, puis seulement à l'intérieur Conseils avec un centre de contrôle des cadeaux.
Prise en charge psychiatrique
Puisqu'un surdosage est souvent prévu, les patients le peuvent essayer le suicide par d'autres moyens pendant la phase de rétablissement. Renvoi psychiatrique peut être approprié.
Gestion pédiatrique
Les principes de gestion des surdoses d'enfants et d'adultes sont similaires. Il est fortement recommandé que le médecin contacte le poison local Centre de contrôle pour un traitement pédiatrique spécifique.

However, we will provide data for each active ingredient



