

コンポーネント:
治療オプション:
Oliinyk Elizabeth Ivanovna 、薬局による医学的評価、 最終更新日:10.04.2022

アテンション! そのこのページの情報は医療専門家のみを対象としています! その情報が収集したオープン源を含めることが可能である重大な誤差! 注意して、このページ上のすべての情報を再確認してください!


投薬形態と強さ。
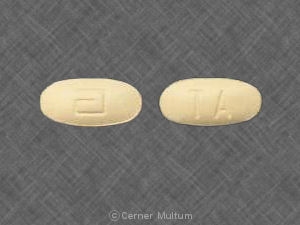
- 「a」ロゴとコード識別文字「TA」が刻印された54 mgの黄色の錠剤。.
- 「a」ロゴとコード識別文字「TC」が刻印された160 mgの白い錠剤。.
保管と取り扱い。
トリコール。® (フェノフィブラート錠)。 2つの強みで利用できます。
54 mg。 黄色のタブレット。「a」のロゴとコード識別文字「TA」が刻印されており、90本(。NDC。 0074-4009-90)。.
160 mg。 「a」のロゴとコード識別文字「TC」が刻印された白い錠剤。90本入り(。NDC。 0074-4013-90)。.
ストレージ。
25°C(77°F)で保管してください。 15-30°C(59-86°F)への遠足が許可されています。.
子供の手の届かないところに保管してください。. 水分から保護してください。.
製造元:Laboratoires Fournier、S.A.、21300Chen ⁇ ´ve、フランス。. 改訂:2017年1月。.

一次高コレステロール血症または混合型脂質血症。
TRICORは、低密度リポタンパク質コレステロール(LDL-C)の上昇、総コレステロール(Total-C)、トリグリセリドおよびアポリポタンパク質B(Apo B)の低下、および高密度リポタンパク質コレステロール(HDL- C)原発性高コレステロール血症または混合脂質異常症の成人患者。.
重度の高トリグリセリド血症。
TRICORは、重度の高トリグリセリド血症の成人患者の治療のための食事療法の補助療法としても示されています。. 空腹時カイロ血症を示す糖尿病患者の血糖コントロールを改善すると、通常、薬理学的介入の必要がなくなります。.
血清トリグリセリドのレベルが著しく上昇(例:. > 2,000 mg / dL)は、 ⁇ 炎を発症するリスクを高める可能性があります。. このリスクの低減に対するフェノフィブラート療法の効果は十分に研究されていません。.
使用の重要な制限。
160 mgのTRICORに相当する用量のフェノフィブラートは、2型糖尿病患者の大規模無作為化比較試験で冠状動脈性心臓病の ⁇ 患率と死亡率を下げることは示されていません。.

一般的な考慮事項。
患者は、TRICORを受ける前に適切な脂質低下食を摂るべきであり、TRICORによる治療中もこの食生活を継続する必要があります。 TRICOR錠剤は食事とともに投与し、それによって薬のバイオアベイラビリティを最適化する必要があります。.
ジスリピド血症の最初の治療は、リポタンパク質異常のタイプに固有の食事療法です。. 過剰な体重と過剰なアルコール摂取は、高トリグリセリド血症の重要な要因である可能性があり、薬物療法の前に対処する必要があります。. 身体運動は重要な付随的手段となります。. 甲状腺機能低下症や糖尿病などの高脂血症の原因となる疾患を探し、適切に治療する必要があります。. エストロゲン療法、チアジド系利尿薬、ベータ遮断薬は、特に家族性高トリグリセリド血症の被験者で、血漿トリグリセリドの大幅な上昇と関連していることがあります。. そのような場合、特定の病因剤の中止は、高トリグリセリド血症の特定の薬物療法の必要性を取り除く可能性があります。.
脂質レベルは定期的に監視する必要があり、脂質レベルが目標範囲を大幅に下回る場合は、TRICORの投与量を減らすことを考慮する必要があります。.
治療は、2か月の治療後に適切な反応が得られない患者で中止し、最大推奨用量は1日1回160 mgです。.
一次高コレステロール血症または混合型脂質血症。
TRICORの初期用量は1日1回160 mgです。.
重度の高トリグリセリド血症。
初期用量は1日あたり54〜160 mgです。. 投与量は患者の反応に応じて個別化する必要があり、4〜8週間間隔で脂質測定を繰り返した後、必要に応じて調整する必要があります。. 最大用量は1日1回160 mgです。.
腎機能障害。
TRICORによる治療は、軽度から中等度の腎機能障害のある患者では1日あたり54 mgの用量で開始し、この用量での腎機能と脂質レベルへの影響の評価後にのみ増加する必要があります。. TRICORの使用は、重度の腎機能障害のある患者では避ける必要があります。.
老人患者。
高齢者の用量選択は、腎機能に基づいて行われるべきです。.

TRICORは以下では禁 ⁇ です。
- 透析を受けている患者を含む、重度の腎機能障害のある患者。.
- 原発性胆 ⁇ 性肝硬変を含む活動性肝疾患の患者。 原因不明の持続的な肝機能異常。.
- 既存の胆 ⁇ 疾患の患者。.
- 授乳中の母親。
- フェノフィブラートまたはフェノフィブリン酸に対する過敏症が知られている患者。.

警告。
の一部として含まれています。 「注意」。 セクション。
注意。
死亡率と冠状動脈性心疾患 ⁇ 患率。
冠状動脈性心疾患の ⁇ 患率と死亡率および非心血管死亡率に対するTRICORの影響は確立されていません。.
糖尿病の心血管リスクを制御するためのアクション(ACCORD Lipid)試験は、フェノフィブラートで治療されたバックグラウンドスタチン療法に関する2型糖尿病患者5518人を対象とした無作為化プラセボ対照試験でした。. フォローアップの平均期間は4.7年でした。. フェノフィブラートとスタチンの併用療法は、主要な有害な心血管イベント(MACE)の主要転帰、非致死性心筋 ⁇ 塞、非致死的脳卒中、および心血管疾患による死亡(ハザード比[ HR] 0.92、95%CI 0.79-1.08)と比較したp = 0. 性別サブグループ分析では、併用療法とスタチン単剤療法を受けている男性のMACEのハザード比は0.82(95%CI 0.69-0.99)であり、併用療法を受けている女性のMACEとスタチン単剤療法のハザード比は1.38(95%CI 0.98-1.94)(相互作用p = 0.01)。. このサブグループの発見の臨床的意義は不明確です。.
糖尿病におけるフェノフィブラート介入とイベント低下(FIELD)研究は、フェノフィブラートで治療された2型糖尿病患者9795人を対象とした5年間の無作為化プラセボ対照研究でした。. フェノフィブラートは、冠状動脈性心臓病イベントの主要な結果(ハザード比[HR] 0.89、95%CI 0.75-1.05、p = 0.16)の有意ではない11%の相対的減少と、総心血管疾患イベント(HR 0.89 [0.80] p0). 有意ではない11%(HR 1.11 [0.95、1.29]、p = 0.18)および19%(HR 1.19 [0.90、1.57]、p = 0.22)の合計および冠状動脈性心疾患死亡率の増加、それぞれ、プラセボと比較してフェノフィブラート。.
TRICOR(フェノフィブラート錠)、クロフィブラート、およびゲムフィブロジルの間の化学的、薬理学的および臨床的類似性のため、これらの他のフィブラート薬を使用した4つの大規模な無作為化プラセボ対照臨床試験での有害所見は、TRICORにも適用される場合があります。
クロフィブラートで5年間治療された患者の心筋 ⁇ 塞後の大規模な研究である冠状動脈薬プロジェクトでは、クロフィブラート群とプラセボ群の間で死亡率に違いは見られませんでした。. しかし、2つのグループ間で手術を必要とする胆石症と胆 ⁇ 炎の割合には違いがありました。 (3.0%対. 1.8%)。.
世界保健機関(WHO)が実施した研究では、冠動脈疾患が知られていない5000人の被験者がプラセボまたはクロフィブラートで5年間治療され、その後さらに1年間追跡されました。. プラセボ群と比較して、クロフィブラート群では統計的に有意な、より高い年齢-調整された全原因死亡率がありました(5.70%vs. 3.96%、p = <0.01)。. 過剰な死亡率は、悪性腫瘍、胆 ⁇ 摘出術後の合併症、 ⁇ 炎などの非心血管系の原因が33%増加したためです。. これは、冠動脈薬プロジェクトで研究されたクロフィブラート治療患者で見られる胆 ⁇ 疾患の高いリスクを確認するように思われました。.
ヘルシンキ心臓研究は、冠動脈疾患の病歴のない中年男性を対象とした大規模な研究(n = 4081)でした。. 被験者はプラセボまたはゲムフィブロジルのいずれかを5年間投与され、その後3.5年の延長が開始されました。. ゲムフィブロジル無作為化群では総死亡率が数値的に高かったが、統計的有意性は達成されなかった(p = 0.19、相対リスクの95%信頼区間G:P = .91-1.64)。. ゲムフィブロジル群では癌による死亡率が高く(p = 0.11)、癌(基底細胞癌を除く)は両方の研究群で同頻度で診断されました。. 研究の規模が限られているため、何らかの原因による死亡の相対リスクは、世界保健機関の研究からの9年間の追跡データ(RR = 1.29)で見られたものと変わらないことが示されました。.
ヘルシンキ心臓研究の二次予防コンポーネントは、既知または疑われる冠状動脈性心臓病のために一次予防研究から除外された中年男性を登録しました。. 被験者はゲムフィブロジルまたはプラセボを5年間投与されました。. ゲムフィブロジル群では心臓の死亡率が高くなる傾向がありましたが、これは統計的に有意ではありませんでした(ハザード比2.2、95%信頼区間:0.94-5.05)。. 胆 ⁇ 手術の割合は研究グループ間で統計的に有意ではありませんでしたが、ゲムフィブロジルグループではより高い傾向を示しました(1.9%vs. 0.3%、p = 0.07)。.
骨格筋。
線維化はミオパシーのリスクを高め、横紋筋融解症と関連しています。. 深刻な筋肉毒性のリスクは、高齢の患者と糖尿病、腎不全、または甲状腺機能低下症の患者で増加しているようです。.
ミオパシーは、びまん性筋肉痛、筋肉の圧痛または脱力感、および/またはクレアチンホスホキナーゼ(CPK)レベルの著しい上昇のある患者で考慮する必要があります。.
特に ⁇ 怠感や発熱を伴う場合は、原因不明の筋肉痛、圧痛、脱力感を迅速に報告するよう患者にアドバイスする必要があります。. これらの症状を報告している患者ではCPKレベルを評価する必要があり、著しく上昇したCPKレベルが発生したり、ミオパシー/筋炎が疑われるか診断された場合は、TRICOR療法を中止する必要があります。.
観察研究のデータは、フィブラート、特にゲムフィブロジルがHMG-CoAレダクターゼ阻害剤(スタチン)と同時投与されると、横紋筋融解症のリスクが高まることを示しています。. 脂質レベルのさらなる変更の利点がこの薬物の組み合わせのリスクの増加を上回る可能性が高い場合を除き、この組み合わせは避けるべきです。.
横紋筋融解症を含むミオパシーの症例は、コルヒチンと同時投与されたフェノフィブラートで報告されており、コルヒチンとフェノフィブラートを処方するときは注意が必要です。.
肝機能。
1日あたり107 mg〜160 mg TRICORに相当する用量のフェノフィブラートは、血清トランスアミナーゼ[AST(SGOT)またはALT(SGPT)]の増加と関連しています。. 10件のプラセボ対照試験のプールされた分析では、フェノフィブラートを服用している患者の5.3%とプラセボで治療された患者の1.1%で、正常の上限の3倍を超える増加が発生しました。.
治療の中止後または継続治療中にトランスアミナーゼの測定が行われた場合、通常、正常限界への復帰が観察されました。. フェノフィブラート療法に関連するトランスアミナーゼの増加の発生率は、用量に関連しているようです。. 8週間の用量範囲研究。, ALTまたはASTの上昇の発生率が正常の上限の少なくとも3倍になったのは、1日あたり107 mg〜160 mg TRICORに相当する投与量を受けた患者では13%であり、54 mg以下のTRICORに相当する投与量を受けた患者では0%でした。 1日。, またはプラセボ。. フェノフィブラート療法に関連する肝細胞、慢性活動性および胆 ⁇ うっ滞性肝炎は、数週間の暴露後に数年に報告されています。. 非常にまれなケースでは、肝硬変は慢性活動性肝炎に関連して報告されています。.
TRICORによる治療期間中、血清ALT(SGPT)を含む肝機能のベースラインと定期的な定期的なモニタリングを実施し、酵素レベルが正常限界の3倍を超えて持続する場合は治療を中止する必要があります。.
血清クレアチニン。
血清クレアチニンの上昇は、フェノフィブラートの患者で報告されています。. これらの上昇は、フェノフィブラートの中止後にベースラインに戻る傾向があります。. これらの観察の臨床的意義は不明です。. TRICORを服用している腎障害のある患者の腎機能を監視します。高齢者や糖尿病患者など、腎不全のリスクがあるTRICORを服用している患者についても、腎モニタリングを検討する必要があります。.
コレリシア症。
クロフィブラートやゲムフィブロジルのようなフェノフィブラートは、胆 ⁇ へのコレステロール排 ⁇ を増加させ、胆石症を引き起こす可能性があります。. 胆 ⁇ 症が疑われる場合は、胆 ⁇ の研究が適応となります。. 胆石が見つかった場合は、TRICOR療法を中止する必要があります。.
クマリン抗凝固剤。
プロトロンビン時間/国際標準化比(PT / INR)の延長におけるクマリン型抗凝固効果の増強のため、クマリン抗凝固剤がTRICORと併用される場合は注意が必要です。. 出血合併症を防ぐために、PT / INRが安定するまで、PT / INRの頻繁なモニタリングと抗凝固剤の用量調整が推奨されます。.
⁇ 炎。
⁇ 炎は、フェノフィブラート、ゲムフィブロジル、およびクロフィブラートを服用している患者で報告されています。. この発生は、重度の高トリグリセリド血症、直接的な薬物効果、または胆管結石または一般的な胆管の閉塞を伴うスラッジ形成を介した二次現象の患者における有効性の失敗を表す可能性があります。.
血液学的変化。
フェノフィブラート療法の開始後の患者では、軽度から中程度のヘモグロビン、ヘマトクリット、および白血球の減少が観察されています。. ただし、これらのレベルは長期投与中に安定します。. 血小板減少症および無 ⁇ 粒球症は、フェノフィブラートで治療された個人で報告されています。. TRICOR投与の最初の12か月間は、赤血球数と白血球数の定期的なモニタリングが推奨されます。.
過敏反応。
スティーブンス・ジョンソン症候群などの急性過敏反応や、患者の入院とステロイドによる治療を必要とする中毒性表皮壊死症が、フェノフィブラートで治療された個人で報告されています。. じんましんは1.1対. 0%、1.4対発疹. 対照試験では、フェノフィブラートとプラセボ患者のそれぞれ0.8%。.
静脈血栓塞栓症。
FIELD試験では、肺塞栓症(PE)と深部静脈血栓症(DVT)が、フェノフィブラートでプラセボ治療群よりも高い率で観察されました。. FIELDに登録された9,795人の患者のうち、プラセボ群では4,900人、フェノフィブラート群では4,895人でした。. DVTの場合、プラセボ群で48のイベント(1%)、フェノフィブラート群で67(1%)(p = 0.074)がありました。 PEの場合、プラセボ群で32(0.7%)、フェノフィブラート群で53(1%)のイベントがありました(p = 0.022)。.
冠動脈薬プロジェクトでは、クロフィブラート群のより高い割合が、プラセボ群よりも確定的または疑わしい致命的または非致命的な肺塞栓症または血栓性静脈炎を経験しました(5.2%vs. 5年間で3.3%。 p <0.01)。.
HDLコレステロールレベルの逆説的な低下。
線維化療法で開始された糖尿病および非糖尿病患者で発生したHDLコレステロール値(2 mg / dLと低い)の深刻な減少の市販後および臨床試験の報告があります。. HDL-Cの減少は、アポリポタンパク質A1の減少に反映されています。. この減少は、フィブラート療法の開始後2週間から数年以内に発生すると報告されています。. HDL-Cレベルは、フィブラート療法が中止されるまで低下したままです。フィブラート療法の中止に対する反応は迅速で持続的です。. HDL-Cのこの減少の臨床的意義は不明です。. 線維化療法の開始後最初の数か月以内にHDL-Cレベルを確認することをお勧めします。. ひどく落ち込んでいるHDL-Cレベルが検出された場合は、フィブラート療法を中止し、HDL-Cレベルがベースラインに戻るまで監視し、フィブラート療法を再開しないでください。.
非臨床毒性学。
発がんと変異誘発と生殖能力の障害。
フェノフィブラートを含むラットで2つの食事発がん性試験が行われた。. 最初の24か月の研究では、体表面積の比較に基づいて、Wistarラットにフェノフィブラートを10、45、および200 mg / kg /日で投与しました。これは、推奨される最大ヒト用量(MRHD)の約0.3、1、および6倍です。 (mg / m。2)。. 200 mg / kg /日の用量(MRHDの6倍)で、肝癌の発生率は両性で有意に増加しました。. ⁇ 臓癌の統計的に有意な増加がMRHDの1倍と6倍の男性で観察されました。男性のMRHDの6倍で、 ⁇ 腺腫と良性精巣間質細胞腫瘍の増加が観察されました。. 別の系統のラットにおける2番目の24か月ラット発がん性試験。 (Sprague-Dawley。) 10および60 mg / kg /日の用量。 (MRHDの0.3および2倍。) MRHDの2倍で、両性の ⁇ 腺腺腫の発生率の大幅な増加と男性の精巣間質細胞腫瘍の増加が生じました。
117週間の発がん性試験が3つの薬物を比較するラットで行われた:フェノフィブラート10および60 mg / kg /日(MRHDの0.3および2倍)、クロフィブラート(400 mg / kg /日、ヒト用量の2倍)、およびゲムフィブロジル(250 mg / kg /日、ヒト用量の2倍、2 表面積)。. フェノフィブラートは、両性において ⁇ 腺腺腫を増加させた。. クロフィブラートは、男性の肝細胞癌と ⁇ 腺腺腫、女性の肝腫瘍性結節を増加させました。. ゲムフィブロジルは男性と女性の肝腫瘍性結節を増加させ、3つの薬物すべてが男性の精巣間質細胞腫瘍を増加させました。.
CF-1マウスを用いた21か月の研究では、フェノフィブラート10、45、および200 mg / kg /日(mg / mに基づいてMRHDの約0.2、1、および3倍)。2 表面積)は、MRHDの3倍で両性の肝癌を大幅に増加させました。 10、60、および200 mg / kg /日の2番目の18か月の研究では、フェノフィブラートは、MRHDの3倍で雄マウスの肝癌と雌マウスの肝腺腫を大幅に増加させました。
電子顕微鏡研究は、ラットへのフェノフィブラート投与後のペルオキシソーム増殖を実証しています。. ヒトのペルオキシソーム増殖をテストするための適切な研究は行われていませんが、ペルオキシソームの形態と数の変化は、同じ個人で治療の前後に肝生検を比較した場合、フィブラートクラスの他のメンバーによる治療後にヒトで観察されました。.
変異誘発。
フェノフィブラートは、次のテストで変異原性がないことが実証されています:エイムス、マウスリンパ腫、染色体異常、および原発性ラット肝細胞における予定外のDNA合成。.
不妊の障害。
生殖能力研究では、ラットにフェノフィブラートの経口食事投与量が与えられ、雄は交尾の61日前に、雌は離乳から交尾の15日前に投与され、300 mg / kg /日までの用量で生殖能力に悪影響はなかった(〜10倍) mg / mに基づくMRHD。2 表面積の比較)。.
特定の集団で使用します。
妊娠。
妊娠カテゴリーC
妊婦の安全は確立されていません。. 妊娠中の女性におけるフェノフィブラートの適切で十分に管理された研究はありません。. フェノフィブラートは、潜在的な利益が胎児への潜在的なリスクを正当化する場合にのみ、妊娠中に使用されるべきです。.
離乳による交配の15日前から15、75、300 mg / kg /日のフェノフィブラートの経口食事投与を受けた雌ラットでは、体表面積の比較に基づいて、MRHDの0.3倍で母体毒性が観察されました。 mg / m。2.
臓器形成期間中の妊娠6〜15日目から14、127、および361 mg / kg /日の経口食事投与を受けた妊娠中のラットでは、14 mg / kg /日で有害な発生所見は観察されなかった(1回未満)体表面積の比較に基づくMRHD; mg / m。2)。. より高い倍数のヒト用量で、母体毒性の証拠が観察された。.
妊娠中のウサギでは、器官形成の期間中、妊娠618日目から15、150、および300 mg / kg /日の経口強制飼養用量を投与し、出産を許可したところ、流産した同腹児が150 mg / kg /日(MRHDの10倍)で観察されました、体表面積の比較に基づく:mg / m。2)。. 15 mg / kg /日で発生所見は観察されませんでした(体表面積の比較に基づいて、MRHDの1倍未満、mg / m。2).
妊娠15日目から授乳21日目(離乳)までの15、75、300 mg / kg /日の経口食事投与を受けた妊娠中のラットでは、最大推奨ヒト用量(MRHD)の1倍未満で母体毒性が観察されました。体表面積の比較に基づく; mg / m。2.
授乳中の母親。
フェノフィブラートは授乳中の母親には使用しないでください。. 母親にとっての薬物の重要性を考慮して、看護を中止するか、薬物を中止するかを決定する必要があります。.
小児用。
小児患者では安全性と有効性は確立されていません。.
老人用。
フェノフィブリン酸は腎臓から実質的に排 ⁇ されることが知られており、この薬に対する副作用のリスクは腎機能障害のある患者で高くなる可能性があります。. フェノフィブリン酸への曝露は年齢の影響を受けません。. 高齢患者は腎障害の発生率が高いため、高齢者の用量選択は腎機能に基づいて行う必要があります。. 腎機能が正常な高齢患者は、用量の変更を必要としないはずです。. TRICORを服用している高齢患者の腎機能のモニタリングを検討してください。
腎障害。
TRICORの使用は、重度の腎機能障害のある患者では避ける必要があります。. 軽度から中等度の腎機能障害のある患者では、減量が必要です。. 腎機能障害のある患者の腎機能のモニタリングが推奨されます。.
肝障害。
TRICORの使用は、肝障害のある被験者では評価されていません。.

副作用。
臨床試験の経験。
臨床試験はさまざまな条件下で行われるため、薬物の臨床試験で観察された副作用率は、他の薬物の臨床試験の率と直接比較することはできず、実際に観察された率を反映しない場合があります。.
因果関係に関係なく、二重盲検プラセボ対照試験中にフェノフィブラート(およびプラセボより大きい)で治療された患者の2%以上が報告した有害事象を以下の表1に示します。. 有害事象により、フェノフィブラートで治療された患者の5.0%、プラセボで治療された患者の3.0%で治療が中止されました。. 肝機能検査の増加が最も頻繁なイベントであり、二重盲検試験で患者の1.6%でフェノフィブラート治療の中止を引き起こしました。.
表1。. 二重盲検プラセボ対照試験中にフェノフィブラートとプラセボより大きい患者で2%以上が報告した副作用。
| ボディシステム。 副作用。 |
フェノフィブラート*。 | プラセボ。 |
| (N = 439)。 | (N = 439)。 | |
| 全体としての体。 | ||
| 腹痛。 | 4.6%。 | 4.4%。 |
| 背中の痛み。 | 3.4%。 | 2.5%。 |
| 頭痛。 | 3.2%。 | 2.7%。 |
| DIGESTIVE。 | ||
| 吐き気。 | 2.3%。 | 1.9%。 |
| 便秘。 | 2.1%。 | 1.4%。 |
| 代謝および栄養障害。 | ||
| 異常な肝機能検査。 | 7.5%**。 | 1.4%。 |
| ALTの増加。 | 3.0%。 | 1.6%。 |
| CPKの増加。 | 3.0%。 | 1.4%。 |
| ASTの増加。 | 3.4%**。 | 0.5%。 |
| 呼吸。 | ||
| 呼吸器疾患。 | 6.2%。 | 5.5%。 |
| 鼻炎。 | 2.3%。 | 1.1%。 |
| * 160 mg TRICORに相当する投与量。 **プラセボとは大きく異なります。. |
||
市販後の経験。
フェノフィブラートの承認後の使用中に、以下の副作用が確認されています:筋肉痛、横紋筋融解症、 ⁇ 炎、急性腎不全、筋肉のけいれん、肝炎、肝硬変、貧血、関節痛、ヘモグロビンの減少、ヘマトクリットの減少、白血球の減少、無力症、そしてひどく落ち込んだHDLコレステロール値。. これらの反応は不確実なサイズの集団から自発的に報告されるため、その頻度を確実に推定したり、薬物曝露との因果関係を確立したりすることは常に可能ではありません。.
薬物相互作用。
クマリン抗凝固剤。
クマリン型抗凝固効果の増強は、PT / INRの延長とともに観察されています。
クマリン抗凝固剤をTRICORと組み合わせて投与する場合は注意が必要です。抗凝固剤の投与量を減らして、出血の合併症を防ぐためにPT / INRを望ましいレベルに維持する必要があります。. PT / INRが安定していることが明確に決定されるまで、PT / INRの頻繁な測定が推奨されます。.
免疫抑制剤。
シクロスポリンやタクロリムスなどの免疫抑制剤は、クレアチニンクリアランスの低下と血清クレアチニンの上昇を伴う腎毒性を生み出す可能性があり、腎排 ⁇ はTRICORを含む線維酸薬の主要な排 ⁇ 経路であるため、相互作用が腎機能の低下につながるリスクがあります。. TRICOR(フェノフィブラート錠)を免疫抑制剤やその他の潜在的に腎毒性のある薬剤と併用することの利点とリスクを慎重に検討し、最低有効量を採用し、腎機能を監視する必要があります。.
胆 ⁇ 酸結合樹脂。
胆 ⁇ 酸結合樹脂は同時に投与される他の薬物に結合する可能性があるため、患者は、吸収を妨げないように、胆 ⁇ 酸結合樹脂の少なくとも1時間前または4〜6時間後にTRICORを服用する必要があります。.
コルヒチン。
横紋筋融解症を含むミオパシーの症例は、コルヒチンと同時投与されたフェノフィブラートで報告されており、コルヒチンとフェノフィブラートを処方するときは注意が必要です。.

妊娠カテゴリーC
妊婦の安全は確立されていません。. 妊娠中の女性におけるフェノフィブラートの適切で十分に管理された研究はありません。. フェノフィブラートは、潜在的な利益が胎児への潜在的なリスクを正当化する場合にのみ、妊娠中に使用されるべきです。.
離乳による交配の15日前から15、75、300 mg / kg /日のフェノフィブラートの経口食事投与を受けた雌ラットでは、体表面積の比較に基づいて、MRHDの0.3倍で母体毒性が観察されました。 mg / m。2.
臓器形成期間中の妊娠6〜15日目から14、127、および361 mg / kg /日の経口食事投与を受けた妊娠中のラットでは、14 mg / kg /日で有害な発生所見は観察されなかった(1回未満)体表面積の比較に基づくMRHD; mg / m。2)。. より高い倍数のヒト用量で、母体毒性の証拠が観察された。.
妊娠中のウサギでは、器官形成の期間中、妊娠618日目から15、150、および300 mg / kg /日の経口強制飼養用量を投与し、出産を許可したところ、流産した同腹児が150 mg / kg /日(MRHDの10倍)で観察されました、体表面積の比較に基づく:mg / m。2)。. 15 mg / kg /日で発生所見は観察されませんでした(体表面積の比較に基づいて、MRHDの1倍未満、mg / m。2).
妊娠15日目から授乳21日目(離乳)までの15、75、300 mg / kg /日の経口食事投与を受けた妊娠中のラットでは、最大推奨ヒト用量(MRHD)の1倍未満で母体毒性が観察されました。体表面積の比較に基づく; mg / m。2.

臨床試験の経験。
臨床試験はさまざまな条件下で行われるため、薬物の臨床試験で観察された副作用率は、他の薬物の臨床試験の率と直接比較することはできず、実際に観察された率を反映しない場合があります。.
因果関係に関係なく、二重盲検プラセボ対照試験中にフェノフィブラート(およびプラセボより大きい)で治療された患者の2%以上が報告した有害事象を以下の表1に示します。. 有害事象により、フェノフィブラートで治療された患者の5.0%、プラセボで治療された患者の3.0%で治療が中止されました。. 肝機能検査の増加が最も頻繁なイベントであり、二重盲検試験で患者の1.6%でフェノフィブラート治療の中止を引き起こしました。.
表1。. 二重盲検プラセボ対照試験中にフェノフィブラートとプラセボより大きい患者で2%以上が報告した副作用。
| ボディシステム。 副作用。 |
フェノフィブラート*。 | プラセボ。 |
| (N = 439)。 | (N = 439)。 | |
| 全体としての体。 | ||
| 腹痛。 | 4.6%。 | 4.4%。 |
| 背中の痛み。 | 3.4%。 | 2.5%。 |
| 頭痛。 | 3.2%。 | 2.7%。 |
| DIGESTIVE。 | ||
| 吐き気。 | 2.3%。 | 1.9%。 |
| 便秘。 | 2.1%。 | 1.4%。 |
| 代謝および栄養障害。 | ||
| 異常な肝機能検査。 | 7.5%**。 | 1.4%。 |
| ALTの増加。 | 3.0%。 | 1.6%。 |
| CPKの増加。 | 3.0%。 | 1.4%。 |
| ASTの増加。 | 3.4%**。 | 0.5%。 |
| 呼吸。 | ||
| 呼吸器疾患。 | 6.2%。 | 5.5%。 |
| 鼻炎。 | 2.3%。 | 1.1%。 |
| * 160 mg TRICORに相当する投与量。 **プラセボとは大きく異なります。. |
||
市販後の経験。
フェノフィブラートの承認後の使用中に、以下の副作用が確認されています:筋肉痛、横紋筋融解症、 ⁇ 炎、急性腎不全、筋肉のけいれん、肝炎、肝硬変、貧血、関節痛、ヘモグロビンの減少、ヘマトクリットの減少、白血球の減少、無力症、そしてひどく落ち込んだHDLコレステロール値。. これらの反応は不確実なサイズの集団から自発的に報告されるため、その頻度を確実に推定したり、薬物曝露との因果関係を確立したりすることは常に可能ではありません。.

TRICORによる過剰摂取に対する特定の治療法はありません。過剰摂取が発生した場合に、バイタルサインのモニタリングや臨床状態の観察など、患者の一般的な支持療法が示されます。. 必要に応じて、吸収されない薬物の排除は、 ⁇ 吐または胃洗浄によって達成されるべきです。気道を維持するために通常の予防策を講じる必要があります。. フェノフィブリン酸は血漿タンパク質に強く結合しているため、血液透析は考慮すべきではありません。.

さまざまな臨床試験により、トータルC、LDL-C、およびLDL膜複合体であるapo Bのレベルが上昇すると、ヒトアテローム性動脈硬化症に関連していることが示されています。. 同様に、HDL-Cとその輸送複合体のレベルの低下、アポリポタンパク質A(アポAIとアポAII)が関連付けられています。 アテローム性動脈硬化症の発症を伴う。. 疫学調査により、心血管の ⁇ 患率と死亡率は、総C、LDL-C、およびTGのレベルによって直接異なり、逆にHDL-Cのレベルによって異なることが確立されています。心血管の ⁇ 患率と死亡率のリスクに対するHDL-Cの上昇またはトリグリセリド(TG)の低下の独立した影響は決定されていません。.
フェノフィブラートの活性代謝物であるフェノフィブリン酸は、治療を受けた患者の総コレステロール、LDLコレステロール、アポリポタンパク質B、総トリグリセリド、およびトリグリセリドリッチリポタンパク質(VLDL)の減少をもたらします。. さらに、フェノフィブラートによる治療は、高密度リポタンパク質(HDL)とアポリポタンパク質のapoAIとapoAIIの増加をもたらします。

フェノフィブラートは、活性化学部分フェノフィブリン酸のプロドラッグです。. フェノフィブラートは、体内のエステル加水分解によって、循環で測定可能な活性成分であるフェノフィブリン酸に変換されます。.
吸収。
化合物は注射に適した水性媒体で実質的に不溶性であるため、フェノフィブラートの絶対バイオアベイラビリティは決定できません。. しかし、フェノフィブラートは消化管からよく吸収されます。. 健康なボランティアでの経口投与後、放射性標識フェノフィブラートの単回投与の約60%が尿中に現れ、主にフェノフィブリン酸とそのグルクロネート抱合体として現れ、25%が ⁇ 便中に排 ⁇ されました。. フェノフィブリン酸のピーク血漿レベルは、投与後6〜8時間以内に発生します。.
フェノフィブラートの吸収は、食物と一緒に投与すると増加します。. フェノフィブラート錠を使用すると、空腹時と比較して、摂食時の吸収範囲が約35%増加します。.
分布。
フェノフィブラートを複数回投与すると、5日以内にフェノフィブリン酸の定常状態が達成されます。. 定常状態でのフェノフィブリン酸の血漿濃度は、単回投与後の濃度の約2倍です。. 血清タンパク質結合は、正常および高脂血症の被験者で約99%でした。.
代謝。
経口投与後、フェノフィブラートはエステラーゼによって活性代謝物であるフェノフィブリン酸に急速に加水分解されます。血漿中に変化しないフェノフィブラートは検出されません。.
フェノフィブリン酸は主にグルクロン酸と結合し、尿中に排 ⁇ されます。. 少量のフェノフィブリン酸は、カルボニル部分からベンズヒドロール代謝物まで還元され、ベンズヒドロール代謝物は、グルクロン酸と結合して尿中に排 ⁇ されます。.
生体内で。 代謝データは、フェノフィブラートもフェノフィブリン酸も酸化的代謝を受けないことを示しています(例:.、チトクロームP450)かなりの程度。.
除去。
吸収後、フェノフィブラートは主に代謝産物の形で尿中に排 ⁇ されます。主にフェノフィブリン酸とフェノフィブリン酸グルクロニドです。. 放射性標識フェノフィブラートの投与後、用量の約60%が尿中に現れ、25%が ⁇ 便中に排 ⁇ されました。.
フェノフィブリン酸は20時間の半減期で除去され、1日1回の投与が可能です。.

However, we will provide data for each active ingredient







