
Componentes:
Método de ação:
Opção de tratamento:
Medicamente revisado por Fedorchenko Olga Valeryevna, Farmácia Última atualização em 26.06.2023

Atenção! As informações na página são apenas para profissionais de saúde! As informações são coletadas em fontes abertas e podem conter erros significativos! Tenha cuidado e verifique novamente todas as informações desta página!
20 principais medicamentos com os mesmos componentes:
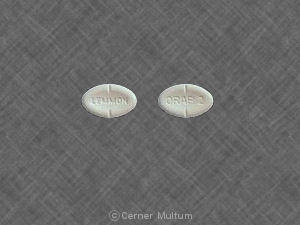
ORAP® (pimozida) 1 mg comprimidos são comprimidos brancos, ovais e pontilhados, com a gravação "ORAP 1". Eles estão disponíveis em frascos de 100 (NDC 57844-151-01).
ORAP® (pimozida) 2 mg comprimidos são comprimidos brancos, ovais e pontilhados, com a gravação "LEMMON" de um lado e "ORAP 2" do outro. Eles estão disponíveis em frascos de 100 (NDC 57844-187-01).
Armazenar a 25 ° C (77 ° F); excursões permitidas a 15 ° -30 ° C (59 ° -86 ° F) .
Dispense em um recipiente apertado e resistente à luz, conforme definido no compêndio oficial.
Farmacêutico: Dispensa em recipiente resistente a crianças.
Fabricado para: Gate Pharmaceuticals, Div. da Teva Pharmaceuticals USA Sellersville, PA 18960. Fabricado por: Teva Pharmaceuticals USA, Sellersville, PA 18960. Rev. Agosto de 2011
ORAP (pimozida) é indicado para a supressão de tiques motores e fônicos pacientes com Transtorno de Tourette que não responderam satisfatoriamente ao tratamento padrão. ORAP não se destina a ser um tratamento de primeira escolha nem se destina ao tratamento de tiques que são meramente irritantes ou cosmeticamente problemático. ORAP deve ser reservado para uso em pacientes com Transtorno de Tourette cujo desenvolvimento e / ou função da vida cotidiana é severamente comprometida pelo presença de tiques motores e fônicos.
Evidências que apóiam a aprovação da pimozida para uso no Transtorno de Tourette foram obtido em duas investigações clínicas controladas que incluíram pacientes entre eles com idades entre 8 e 53 anos. A maioria dos sujeitos nos dois ensaios tinha 12 anos ou mais.
Geral
A supressão de tiques pelo ORAP requer uma introdução lenta e gradual de a droga. A dose do paciente deve ser cuidadosamente ajustada a um ponto em que o a supressão de tiques e o alívio concedido são equilibrados contra os desagradáveis efeitos colaterais da droga.
Um ECG deve ser feito na linha de base e periodicamente a partir de então, especialmente durante o período de ajuste da dose (ver AVISO e PRECAUÇÕES – Laboratório Testes). Tentativas periódicas devem ser feitas para reduzir a dose de ORAP para veja se os tiques persistem ou não no nível e extensão identificados pela primeira vez. No tentativas de reduzir a dose de ORAP, deve-se considerar a possibilidade de que aumentos de intensidade e frequência tic possam representar um transitório fenômeno relacionado à retirada, em vez de um retorno dos sintomas da doença. Especificamente, uma a duas semanas deve decorrer antes de concluir que um aumento nas manifestações tic é uma função da síndrome da doença subjacente do que uma resposta à retirada de drogas. Uma retirada gradual é recomendada em qualquer caso.
Crianças
Dados confiáveis de resposta à dose para os efeitos do ORAP (pimozida) na manifestação tic no Tourette's Disorder pacientes com menos de doze anos de idade não estão disponíveis.
O tratamento deve ser iniciado na dose de 0,05 mg / kg, de preferência tomado uma vez na hora de dormir. A dose pode ser aumentada a cada três dias para um máximo de 0,2 mg / kg não exceder 10 mg / dia.
Em doses acima de 0,05 mg / kg / dia, deve ser realizada genotipagem do CYP 2D6. Em pobre Metabolizadores do CYP 2D6, doses de ORAP não devem exceder 0,05 mg / kg / dia e doses não deve ser aumentado antes de 14 dias (ver PRECAUÇÕES - Farmacogenômica).
Adultos
Em geral, o tratamento com ORAP deve ser iniciado com uma dose de 1 a 2 mg um dia em doses divididas. A dose pode ser aumentada posteriormente a cada dois dias. A maioria dos pacientes é mantida a menos de 0,2 mg / kg / dia ou 10 mg / dia, o que for é menos. Doses superiores a 0,2 mg / kg / dia ou 10 mg / dia não são recomendadas.
Em doses acima de 4 mg / dia, deve ser realizada genotipagem do CYP 2D6. No pobre CYP Metabolizadores 2D6, doses de ORAP não devem exceder 4 mg / dia e as doses não devem ser aumentado antes de 14 dias (ver PRECAUÇÕES - Farmacogenômica).
Farmacologia Animal
Um estudo crônico em cães indicou que a pimozida causou hiperplasia gengival quando administrado por vários meses a cerca de 5 vezes o máximo recomendado dose humana. Esta condição era reversível após a retirada.
- ORAP (pimozida) é contra-indicado no tratamento de tiques ou tiques simples que não sejam aqueles associados ao Transtorno de Tourette.
- ORAP não deve ser usado em pacientes que tomam medicamentos que podem, eles próprios, causar tiques motores e fônicos (por exemplo,., pemolina, metilfenidato e anfetaminas) até esses pacientes foram retirados desses medicamentos para determinar se ou não os medicamentos, em vez do distúrbio de Tourette, são responsáveis pelos tiques.
- Como o ORAP prolonga o intervalo QT do eletrocardiograma, ele é contra-indicado em pacientes com síndrome do QT longo congênito, pacientes com histórico cardíaco arritmias, pacientes que tomam outros medicamentos que prolongam o intervalo QT de o eletrocardiograma ou pacientes com hipocalemia ou hipomagnesemia conhecida (veja também PRECAUÇÕES: INTERAÇÕES DE DROGAS).
- ORAP está contra-indicado em pacientes com sistema nervoso central tóxico grave depressão ou estados em coma de qualquer causa.
- ORAP está contra-indicado em pacientes com hipersensibilidade a ele. Como é não se sabe se existe sensibilidade cruzada entre os antipsicóticos, a pimozida deve ser usado com a devida cautela em pacientes que demonstraram hipersensibilidade a outros medicamentos antipsicóticos.
- Arritmias ventriculares raramente foram associadas ao uso de macrólido antibióticos em pacientes com intervalos prolongados de QT, como pode ser produzido por ORAP. Especificamente, duas mortes repentinas foram relatadas quando a claritromicina foi adicionado à terapia contínua com pimozida. Além disso, algumas evidências sugerem essa pimozida é metabolizada em parte pelo sistema enzimático citocromo P450 3A4 (CYP 3A4). Os antibióticos macrólidos são inibidores do CYP 3A4 e, portanto, poderiam potencialmente impedir o metabolismo da pimozida. Por esses motivos, o ORAP é contra-indicado em pacientes que recebem antibióticos macrólidos claritromicina, eritromicina, azitromicina, diritromicina e troleandomicina.
- O uso concomitante em pacientes em uso de Celexa ou Lexapro é contra-indicado (VejoPRECAUÇÕES: INTERAÇÕES DE DROGAS - Pimozida e Celexa).
- Estudos de interação clínica com medicamentos demonstraram que a pimozida também é metabolizado pelo CYP 2D6. Uso concomitante de ORAP com paroxetina e outros inibidores fortes do CYP 2D6 são contra-indicados (verPRECAUÇÕES: DROGAS INTERAÇÕES).
- O uso concomitante de pimozida em pacientes em uso de sertralina é contra-indicado (VejoPRECAUÇÕES: INTERAÇÕES DE DROGAS).
Porque os agentes antifúngicos azólicos também são inibidores das enzimas CYP 3A4 e, portanto, também pode prejudicar o metabolismo da pimozida, o ORAP é contra-indicado pacientes que recebem os agentes antifúngicos azólicos itraconazol e cetoconazol.
Da mesma forma, os medicamentos inibidores da protease também são inibidores do CYP 3A4 e, portanto, ORAP está contra-indicado em pacientes que recebem inibidores de protease, como o ritonavir saquinovir, indinavir e nelfinavir. (VejoPRECAUÇÕES: INTERAÇÕES DE DROGAS.)
A nefazodona é um potente inibidor do CYP 3A4 e seu uso concomitante com ORAP também é contra-indicado.
Outros medicamentos que são inibidores relativamente menos potentes do CYP 3A4 também devem ser evitado, tendo em vista os riscos: p. zileuton, fluvoxamina.
AVISO
O uso de ORAP (pimozida) no tratamento do Transtorno de Tourette envolve considerações de risco / benefício diferentes das que quando medicamentos antipsicóticos são usados tratar outras condições. Consequentemente, uma decisão de usar o ORAP deve tomar em consideração o seguinte (veja também INFORMAÇÃO PATIENTE).
Discinesia tardia
Síndrome que consiste em potencialmente irreversível, involuntário, diskinético movimentos podem se desenvolver em pacientes tratados com medicamentos antipsicóticos. Apesar a prevalência da síndrome parece ser mais alta entre os idosos, especialmente mulheres idosas, é impossível confiar nas estimativas de prevalência para prever no início do tratamento antipsicótico, que os pacientes provavelmente desenvolverão a síndrome. Se os medicamentos antipsicóticos diferem em seu potencial causar discinesia tardia é desconhecido.
Tanto o risco de desenvolver discinesia tardia quanto a probabilidade de fazê-lo se tornam irreversíveis, acredita-se que aumentem como a duração do tratamento e a dose cumulativa total de medicamentos antipsicóticos administrados ao paciente aumentar. No entanto, a síndrome pode se desenvolver, embora muito menos comumente, depois períodos de tratamento relativamente breves em doses baixas.
Não existe tratamento conhecido para casos estabelecidos de discinesia tardia a síndrome pode remeter, parcial ou completamente, se o tratamento antipsicótico é retirado. O próprio tratamento antipsicótico, no entanto, pode suprimir (ou parcialmente suprimir) os sinais e sintomas da síndrome e, portanto, podem mascarar o processo subjacente. O efeito que a supressão sintomática tem sobre o o curso a longo prazo da síndrome é desconhecido.
Dadas essas considerações, os medicamentos antipsicóticos devem ser prescritos de maneira é mais provável que minimize a ocorrência de discinesia tardia. Crônico o tratamento antipsicótico deve geralmente ser reservado para pacientes que sofrem de uma doença crônica que, 1) é conhecida por responder a medicamentos antipsicóticos e 2) para quem alternativa, igualmente eficaz, mas potencialmente menos prejudicial tratamentos não estão disponíveis ou são adequados. Em pacientes que necessitam de crônica tratamento, a menor dose e a menor duração da produção do tratamento deve ser buscada uma resposta clínica satisfatória. A necessidade de tratamento continuado deve ser reavaliado periodicamente.
Se sinais e sintomas de discinesia tardia aparecerem em um paciente com antipsicóticos, a descontinuação do medicamento deve ser considerada. No entanto, alguns pacientes podem precisar tratamento apesar da presença da síndrome.
(Para mais informações sobre a descrição da discinesia tardia e sua detecção clínica, consulte REAÇÕES ADVERSAS e PRECAUÇÕES -Informações para pacientes.)
Síndrome Maligna Neuroléptica (SNM)
Um complexo de sintomas potencialmente fatal, às vezes chamado de maligno neuroléptico A síndrome (SNM) foi relatada em associação com medicamentos antipsicóticos. Clínico manifestações de SMN são hiperpirexia, rigidez muscular, estado mental alterado (incluindo sinais catatônicos) e evidência de instabilidade autonômica (irregular pressão arterial ou de pulso, taquicardia, diaforese e disritmias cardíacas). Sinais adicionais podem incluir creatina fosfoquinase elevada, mioglobinúria (rabdomiólise) e insuficiência renal aguda.
A avaliação diagnóstica de pacientes com essa síndrome é complicada. No chegando a um diagnóstico, é importante identificar os casos em que o clínico a apresentação inclui ambas as doenças médicas graves (por exemplo,., pneumonia, sistêmica infecção etc.) e sinais extrapiramidais não tratados ou inadequadamente tratados e sintomas (EPS). Outras considerações importantes no diagnóstico diferencial incluem toxicidade anticolinérgica central, insolação, febre do medicamento e primária patologia do sistema nervoso central (SNC).
O manejo da SMN deve incluir 1) descontinuação imediata do antipsicótico medicamentos e outros medicamentos não essenciais à terapia concomitante, 2) sintomáticos intensivos tratamento e monitoramento médico e 3) tratamento de qualquer grave concomitante problemas médicos para os quais estão disponíveis tratamentos específicos. Não há geral acordo sobre regimes específicos de tratamento farmacológico para não complicados NMS .
Se um paciente necessitar de tratamento antipsicótico após recuperação da SMN, a potencial reintrodução da terapia medicamentosa deve ser cuidadosamente considerada. O paciente deve ser cuidadosamente monitorado, uma vez que ocorreram recorrências de SMN relatado.
Hiperpirexia, não associada ao complexo de sintomas acima, foi relatada com outros medicamentos antipsicóticos.
De outros
De repente, mortes inesperadas ocorreram em estudos experimentais de condições além do transtorno de Tourette. Essas mortes ocorreram enquanto os pacientes estavam recebendo dosagens na faixa de 1 mg por kg. Um mecanismo possível para essas mortes é prolongamento do intervalo QT predispondo pacientes à arritmia ventricular. Um eletrocardiograma deve ser realizado antes do início do tratamento com ORAP e periodicamente depois, especialmente durante o período de ajuste da dose.
ORAP pode ter um potencial tumorigênico. Com base em estudos realizados em camundongos sabe-se que a pimozida pode produzir um aumento relacionado à dose nos tumores da hipófise. O significado total dessa descoberta não é conhecido, mas deve ser levado em consideração consideração nas decisões do médico e do paciente de usar este medicamento. Esse achado deve ser considerado especialmente quando o paciente é jovem e o uso crônico de pimozida é antecipado (ver PRECAUÇÕES -Carcinogênese, Mutagênese, Compromisso de Fertilidade).
PRECAUÇÕES
Leucopenia, Neutropenia e Agranulocitose
Efeito de classe: Em ensaios clínicos e / ou experiência pós-comercialização, eventos de leucopenia / neutropenia e agranulocitose foram relatadas temporalmente relacionados a agentes antipsicóticos.
Os possíveis fatores de risco para leucopenia / neutropenia incluem branco baixo preexistente contagem de células sanguíneas (leucócitos) e histórico de leucopenia / neutropenia induzida por drogas. Pacientes com histórico de baixa leucopenia / neutropenia induzida por medicamentos ou WBC clinicamente significativos deve ter seu hemograma completo (CBC) monitorado com frequência durante o primeiros meses de terapia e descontinuação do ORAP devem ser considerados ao primeiro sinal de um declínio clinicamente significativo no leucócitos na ausência de outros fatores causais.
Pacientes com neutropenia clinicamente significativa devem ser cuidadosamente monitorados para febre ou outros sintomas ou sinais de infecção e tratados prontamente, se houver sintomas ou sinais ocorrem. Pacientes com neutropenia grave (neutrófilos absolutos) count <1000 / mm³) deve interromper o ORAP e seguir o seu WBC até a recuperação.
Geral
ORAP (pimozida) pode prejudicar as habilidades mentais e / ou físicas necessárias o desempenho de tarefas potencialmente perigosas, como dirigir um carro ou operar máquinas, especialmente durante os primeiros dias de terapia.
ORAP produz efeitos colaterais anticolinérgicos e deve ser usado com cautela em indivíduos cujas condições podem ser agravadas pela atividade anticolinérgica.
ORAP deve ser administrado com cautela em pacientes com insuficiência hepática ou função renal, porque é metabolizada pelo fígado e excretada pelo rins.
Os antipsicóticos devem ser administrados com cautela em pacientes que recebem anticonvulsivante medicação, com histórico de convulsões ou com anormalidades de EEG, porque elas pode diminuir o limiar convulsivo. Se indicado, terapia anticonvulsivante adequada deve ser mantido concomitantemente.
Testes de laboratório
Um ECG deve ser feito na linha de base e periodicamente posteriormente durante todo o período de ajuste da dose. Qualquer indicação de prolongamento do intervalo QTc além um limite absoluto de 0,47 segundos (crianças) ou 0,52 segundos (adultos) ou mais 25% acima da linha de base original do paciente deve ser considerado uma base para interromper um aumento adicional da dose (ver CONTRA-INDICAÇÕES) e considerando uma dose mais baixa.
Desde que a hipocalemia tem sido associada a arritmias ventriculares, o potássio insuficiência secundária a diuréticos, diarréia ou outra causa deve ser corrigida antes do início da terapia com ORAP e manutenção normal do potássio durante o tratamento.
Carcinogênese, Mutagênese, Compromisso de Fertilidade
Estudos de carcinogenicidade foram realizados em camundongos e ratos. Em ratos, pimozida causa um aumento relacionado à dose nos tumores da hipófise e da mamária.
Quando os ratos foram tratados por até 18 meses com pimozida, a hipófise muda desenvolvido apenas em mulheres. Essas alterações foram caracterizadas como hiperplasia em doses que se aproximam da dose e do adenoma humanos em doses cerca de quinze vezes a dose máxima recomendada em humanos em mg por kg. O mecanismo para o a indução de tumores hipofisários em camundongos não é conhecida.
Os tumores da glândula mamária em camundongos fêmeas também aumentaram, mas esses tumores são esperado em roedores tratados com medicamentos antipsicóticos que elevam a prolactina níveis. A administração crônica de um antipsicótico também causa prolactina elevada níveis em humanos. Experimentos de cultura de tecidos indicam que aproximadamente um terço dos cânceres de mama humanos dependem da prolactina in vitro , um fator de importância potencial se a prescrição desses medicamentos for contemplada em a paciente com câncer de mama detectado anteriormente. Embora distúrbios como esse como galactorréia, amenorréia, ginecomastia e impotência foram relatadas com medicamentos antipsicóticos, o significado clínico da prolactina sérica elevada níveis é desconhecido para a maioria dos pacientes. Nem estudos clínicos nem epidemiológicos estudos realizados até o momento mostraram uma associação entre administração crônica desses medicamentos e tumorigênese mamária. A evidência disponível, no entanto, é considerado muito limitado para ser conclusivo no momento.
Em um estudo de carcinogenicidade de 24 meses em ratos, os animais receberam até 50 vezes a dose máxima recomendada para humanos. Não há incidência aumentada de tumores em geral ou tumores em qualquer local foram observados em ambos os sexos. Por causa do número limitado dos animais que sobrevivem a este estudo, o significado desses resultados não é claro.
A pimozida não teve atividade mutagênica no teste de Ames com quatro bactérias cepas de teste, no teste letal dominante do mouse ou no teste de micronúcleos em ratos.
Os estudos de reprodução em animais não foram adequados para avaliar todos os aspectos de fertilidade. No entanto, as ratos fêmeas administradas com pimozida prolongaram o estro ciclos, um efeito também produzido por outros medicamentos antipsicóticos.
Gravidez
Categoria C. Estudos de reprodução realizados em ratos e coelhos por via oral doses até 8 vezes a dose máxima humana não revelaram evidência de teratogenicidade. No rato, no entanto, esse múltiplo da dose humana resultou em diminuição da gravidez e no desenvolvimento retardado de fetos. Pensa-se que esses efeitos sejam devido a uma inibição ou atraso no implante, que também é observado em roedores administrou outros medicamentos antipsicóticos. No coelho, toxicidade materna, mortalidade diminuição do ganho de peso e embriotoxicidade, incluindo aumento de reabsorções relacionado à dose. Porque os estudos de reprodução animal nem sempre são preditivos da resposta humana, a pimozida deve ser dada a uma mulher grávida apenas se a os benefícios potenciais do tratamento superam claramente os riscos potenciais.
Efeitos não teratogênicos
Neonatos expostos a medicamentos antipsicóticos, durante o terceiro trimestre de gravidez estão em risco de sintomas extrapiramidais e / ou de abstinência após o parto. Houve relatos de agitação, hipertonia, hipotonia, tremor, sonolência dificuldade respiratória e distúrbio alimentar nesses neonatos. Essas complicações variaram em gravidade; enquanto em alguns casos os sintomas foram autolimitados em outros casos, os neonatos exigiram apoio da unidade de terapia intensiva e prolongaram-se hospitalização.
ORAP deve ser usado durante a gravidez apenas se o benefício potencial justificar o risco potencial para o feto.
Trabalho e entrega
Este medicamento não tem uso reconhecido em trabalho de parto ou parto.
Mães de enfermagem
Não se sabe se a pimozida é excretada no leite humano. Porque muitas drogas são excretados no leite humano e devido ao potencial de tumorigenicidade e efeitos cardiovasculares desconhecidos no bebê, deve-se tomar uma decisão sobre se interromper a amamentação ou interromper o medicamento, levando em consideração a importância da droga para a mãe.
Uso pediátrico
Embora o Transtorno de Tourette tenha mais frequentemente seu início entre as idades de 2 e 15 anos, informações sobre o uso e eficácia de ORAP em pacientes menores que 12 anos de idade é limitado. Um estudo aberto de 24 semanas em 36 crianças entre elas as idades de 2 e 12 demonstraram que a pimozida tem um perfil de segurança semelhante nessa faixa etária, como em pacientes mais velhos, e não houve achados de segurança impediria seu uso nessa faixa etária.
Porque seu uso e segurança não foram avaliados em outros distúrbios da infância ORAP não é recomendado para uso em nenhuma outra condição além do Transtorno de Tourette.
EFEITOS SECUNDÁRIOS
Geral
Reações extrapiramidais
Reações neuromusculares (extrapiramidais) durante a administração de ORAP® (pimozida) foram relatados com frequência, geralmente durante os primeiros dias de tratamento. Na maioria dos pacientes, essas reações envolviam sintomas semelhantes a Parkinson que, quando observados pela primeira vez, eram geralmente leves a moderadamente graves e geralmente reversível.
Outros tipos de reações neuromusculares (inquietação motora, distonia, acatisia, hiperreflexia, opistótonos, crises oculogíricas) foram relatadas muito menos frequentemente. Reações extrapiramidais graves foram relatadas para ocorrer relativamente doses baixas. Geralmente a ocorrência e gravidade da maioria dos sintomas extrapiramidais estão relacionados à dose, uma vez que ocorrem em doses relativamente altas e foram demonstrados desaparecer ou tornar-se menos grave quando a dose for reduzida. Administração de medicamentos antiparkinsonianos, como mesilato de benztropina ou cloridrato de trihexifenidil pode ser necessário para o controle de tais reações. Note-se que persistente reações extrapiramidais foram relatadas e que a droga pode ter que ser descontinuado nesses casos.
Retirada de sinais neurológicos emergentes
Geralmente, os pacientes que recebem terapia de curto prazo não apresentam problemas descontinuação abrupta de medicamentos antipsicóticos.
No entanto, alguns pacientes em tratamento de manutenção apresentam diskinética transitória sinais após retirada abrupta. Em alguns desses casos, os movimentos diskinéticos são indistinguíveis da síndrome descrita abaixo em “Tardive Discinesia ”, exceto por duração. Não se sabe se a retirada gradual de medicamentos antipsicóticos reduzirá a taxa de ocorrência de abstinência emergente sinais neurológicos, mas até que mais evidências se tornem disponíveis, parece razoável para retirar gradualmente o uso do ORAP
Discinesia tardia
O ORAP pode estar associado a discinesias persistentes. Discinesia tardia, uma síndrome consistindo em movimentos diskinéticos potencialmente irreversíveis, involuntários, podem aparecer em alguns pacientes em terapia prolongada ou pode ocorrer após terapia medicamentosa foi descontinuado. O risco parece ser maior em pacientes idosos terapia com altas doses, especialmente mulheres. Os sintomas são persistentes e em alguns os pacientes parecem irreversíveis. A síndrome é caracterizada por involuntário rítmico movimentos da língua, rosto, boca ou mandíbula (por exemplo,.protrusão da língua, inchando bochechas, franzindo a boca, mastigando movimentos). Às vezes, estes podem ser acompanhados por movimentos involuntários das extremidades e do tronco.
Não existe tratamento eficaz conhecido para discinesia tardia; antiparkinson os agentes geralmente não aliviam os sintomas dessa síndrome. É sugerido que todos os agentes antipsicóticos sejam descontinuados se esses sintomas aparecerem. Deveria é necessário restabelecer o tratamento ou aumentar a dose do agente ou mude para um agente antipsicótico diferente, essa síndrome pode ser mascarada.
Foi relatado que o movimento vermicular fino da língua pode ser um sinal precoce de discinesia tardia e se o medicamento for interrompido naquele momento a síndrome pode não se desenvolver.
Alterações eletrocardiográficas
Alterações eletrocardiográficas foram observadas em ensaios clínicos de ORAP no distúrbio de Tourette e na esquizofrenia. Estes incluíram prolongamento de o intervalo QT, achatamento, entalhe e inversão da onda T e a aparência de ondas U. De repente, mortes inesperadas e apreensão de grandes doenças ocorreram em doses acima de 20 mg / dia.
Síndrome maligna dos neurolépticos
A síndrome maligna dos neurolépticos (SNM) foi relatada com ORAP. (Veja AVISO para mais informações sobre o NMS.)
Hiperpirexia
Hiperpirexia foi relatada com outros medicamentos antipsicóticos.
Ensaios Clínicos
A seguinte tabulação de reação adversa foi derivada de 20 pacientes em a Ensaio clínico de ORAP, controlado por placebo, com 6 semanas de duração, em Tourette's Disorder.
| Sistema Corporal / Reação Adversa | Pimozide (N = 20) |
Placebo (N = 20) |
| Corpo como um todo | ||
| Dor de cabeça | 1 | 2 |
| Gastrointestinal | ||
| Boca seca | 5 | 1 |
| Diarréia | 1 | 0 |
| Náusea | 0 | 2 |
| Vômitos | 0 | 1 |
| Constipação | 4 | 2 |
| Erutações | 0 | 1 |
| Com sede | 1 | 0 |
| Aumento de apetite | 1 | 0 |
| Endócrino | ||
| Distúrbio menstrual | 0 | 1 |
| Secreções mamárias | 0 | 1 |
| Musculoesquelético | ||
| Cãibras musculares | 0 | 1 |
| Aperto muscular | 3 | 0 |
| Postura parada | 2 | 0 |
| CNS | ||
| Sonolência | 7 | 3 |
| Sedação | 14 | 5 |
| Insônia | 2 | 2 |
| Tontura | 0 | 1 |
| Akathisia | 8 | 0 |
| Rigidez | 2 | 0 |
| Distúrbio da fala | 2 | 0 |
| Mudança de caligrafia | 1 | 0 |
| Akinesia | 8 | 0 |
| Psiquiátrico | ||
| Depressão | 2 | 3 |
| Excitação | 0 | 1 |
| Nervoso | 1 | 0 |
| Efeito de comportamento adverso | 5 | 0 |
| Sentidos especiais | ||
| Perturbação visual | 4 | 0 |
| Prove a mudança | 1 | 0 |
| Sensibilidade dos olhos à luz | 1 | 0 |
| Diminua a acomodação | 4 | 1 |
| Pontos diante dos olhos | 0 | 1 |
| Urogenital | ||
| Impotência | 3 | 0 |
A seguinte tabulação de eventos adversos foi derivada de 36 crianças (2 anos) a 12) em um julgamento aberto de 24 semanas do ORAP em Tourette's Disorder.
| Sistema Corporal / Reação Adversa | Número de pacientes que experimentam cada evento (%) | |
| Todos os eventos (N = 36) |
Eventos relacionados a drogas (N = 36) |
|
| Corpo como um todo | ||
| Astenia | 9 (25,0) | 5 (13,8) |
| Dor de cabeça | 8 (22,2) | 1 (2,7) |
| Gastrointestinal | ||
| Disfagia | 1 (2,7) | 1 (2,7) |
| Aumento da salivação | 5 (13,8) | 2 (5,5) |
| Musculoesquelético | ||
| Mialgia | 1 (2,7) | 1 (2,7) |
| Sistema nervoso central | ||
| Sonhando anormal | 1 (2,7) | 1 (2,7) |
| Hipercinesia | 2 (5,5) | 1 (2,7) |
| Sonolência | 10 (27,7) | 9 (25,0) |
| Torticollis | 1 (2,7) | 1 (2,7) |
| Tremor, membros | 1 (2,7) | 1 (2,7) |
| Psiquiátrico | ||
| Efeito de comportamento adverso | 10 (27,7) | 8 (22,2) |
| Nervoso | 3 (8,3) | 2 (5,5) |
| Pele | ||
| Erupção cutânea | 3 (8,3) | 1 (2,7) |
| Sentidos especiais | ||
| Perturbação visual | 2 (5,5) | 1 (2,7) |
| Cardiovascular | ||
| ECG anormal | 1 (2,7) | 1 (2,7) |
Porque experiência clínica de investigação com ORAP no Transtorno de Tourette é limitado, reações adversas incomuns podem não ter sido detectadas. O médico deve considerar que outras reações adversas associadas aos antipsicóticos pode ocorrer.
Outras reações adversas
Além das reações adversas listadas acima, as listadas abaixo têm foi relatado em ensaios clínicos dos EUA de ORAP em outras condições que não a de Tourette Desordem.
Corpo como um todo : Astenia, dor no peito, edema periorbital
Cardiovascular / respiratório : Hipotensão postural, hipotensão, hipertensão taquicardia, palpitações
Gastrointestinal: Maior salivação, náusea, vômito, anorexia GI angústia
Endócrino: Perda de libido
Metabólico / Nutricional : Ganho de peso, perda de peso
Sistema nervoso central : Tontura, tremor, parkinsonismo, desmaio, discinesia
Psiquiátrico: Excitação
Pele: Erupção cutânea, sudorese, irritação na pele
Sentidos especiais : Visão turva, catarata
Urogenital : Noctúria, frequência urinária
Relatórios de pós-comercialização
As seguintes experiências foram descritas em relatórios espontâneos de pós-comercialização. Esses relatórios não fornecem informações suficientes para estabelecer um causal claro relação com o uso do ORAP .
Gastrointestinal: Hiperplasia gengival em um paciente
Hematológico: Anemia hemolítica
Metabólico / Nutricional : Hiponatremia
De outros: Apreensão
INTERAÇÕES DE DROGAS
Porque ORAP prolonga o intervalo QT do eletrocardiograma, um aditivo efeito no intervalo QT seria antecipado se administrado com outros medicamentos como fenotiazinas, antidepressivos tricíclicos ou agentes antiarrítmicos, que prolongam o intervalo QT. Consequentemente, a pimozida não deve ser administrada dofetilida, sotalol, quinidina, outros antiarrítmicos de classe Ia e III, mesoridazina, tioridazina, clorpromazina, droperidol, esparfloxacina, gatifloxacina, moxifloxacina, halofantrina, mefloquina, pentamidina, trióxido de arsênico, acetato de levometadilo mesilato de dolasetron, probucol, tacrolimus, ziprasidona ou outros medicamentos que demonstraram prolongamento do intervalo QT como um dos seus efeitos farmacodinâmicos. Além disso, o uso de antibióticos macrólidos em pacientes com intervalos prolongados de QT tem raramente foi associado a arritmias ventriculares. Administração concomitante não deve ser realizado (ver CONTRA-INDICAÇÕES).
Uma vez que o ORAP é parcialmente metabolizado através do CYP 3A4, não deve ser administrado concomitantemente com inibidores deste sistema metabólico, como antifúngico azole agentes e inibidores de protease (ver CONTRA-INDICAÇÕES).
Pimozida e Celexa: Em um estudo controlado, uma dose única de pimozida 2 mg co-administrado com citalopram racêmico 40 mg administrado uma vez ao dia por 11 dias associado a um aumento médio nos valores de QTc de aproximadamente 10 ms em comparação pimozida dada sozinha. O citalopram racêmico não alterou a AUC ou a Cmax média de pimozida. O mecanismo dessa interação farmacodinâmica não é conhecido. O uso concomitante de pimozida e Celexa ou Lexapro é contra-indicado (ver CONTRA-INDICAÇÕES).
Inibidores do CYP 2D6: Em indivíduos saudáveis, a administração concomitante de pimozida 2 mg (dose única) e paroxetina 60 mg resultaram em um aumento de 151% na AUC da pimozida e um aumento de 62% na Cmax da pimozida em comparação com a pimozida administrada isoladamente. O aumento da AUC e da Cmax da pimozida está relacionado às propriedades inibitórias do CYP 2D6 de paroxetina. Uso concomitante de pimozida e paroxetina ou outro CYP forte Os inibidores de 2D6 são contra-indicados (ver CONTRA-INDICAÇÕES). Como CYP 1A2 também pode contribuir para o metabolismo do ORAP, os prescritores devem estar cientes o potencial teórico para interações medicamentosas com inibidores dessa enzimática sistema.
O ORAP pode ser capaz de potencializar depressores do SNC, incluindo analgésicos sedativos, ansiolíticos e álcool.
Relatos de casos raros sugeriram possíveis efeitos aditivos da pimozida e fluoxetina levando à bradicardia.
A administração concomitante de pimozida e sertralina deve ser contra-indicada (Vejo CONTRA-INDICAÇÕES).
Farmacogenômica
Indivíduos com variações genéticas resultando em metabolismo fraco do CYP 2D6 (aproximadamente 5 a 10% da população) exibem concentrações mais altas de pimozida do que extensas Metabolizadores do CYP 2D6. As concentrações observadas em metabolizadores fracos do CYP 2D6 são semelhantes aos observados com inibidores fortes do CYP 2D6, como a paroxetina. Espera-se que o tempo para atingir concentrações de pimozida no estado estacionário seja mais longo (aproximadamente 2 semanas) em metabolizadores fracos do CYP 2D6 devido ao prolongado meia-vida. Estratégias de dosagem alternativas são recomendadas em pacientes que são metabolizadores do CYP 2D6 geneticamente pobres (ver DOSAGEM E ADMINISTRAÇÃO).
Interação com alimentos
Os pacientes devem evitar o suco de toranja, pois pode inibir o metabolismo de pimozida pelo CYP 3A4.
Categoria C. Estudos de reprodução realizados em ratos e coelhos por via oral doses até 8 vezes a dose máxima humana não revelaram evidência de teratogenicidade. No rato, no entanto, esse múltiplo da dose humana resultou em diminuição da gravidez e no desenvolvimento retardado de fetos. Pensa-se que esses efeitos sejam devido a uma inibição ou atraso no implante, que também é observado em roedores administrou outros medicamentos antipsicóticos. No coelho, toxicidade materna, mortalidade diminuição do ganho de peso e embriotoxicidade, incluindo aumento de reabsorções relacionado à dose. Porque os estudos de reprodução animal nem sempre são preditivos da resposta humana, a pimozida deve ser dada a uma mulher grávida apenas se a os benefícios potenciais do tratamento superam claramente os riscos potenciais.
Efeitos não teratogênicos
Neonatos expostos a medicamentos antipsicóticos, durante o terceiro trimestre de gravidez estão em risco de sintomas extrapiramidais e / ou de abstinência após o parto. Houve relatos de agitação, hipertonia, hipotonia, tremor, sonolência dificuldade respiratória e distúrbio alimentar nesses neonatos. Essas complicações variaram em gravidade; enquanto em alguns casos os sintomas foram autolimitados em outros casos, os neonatos exigiram apoio da unidade de terapia intensiva e prolongaram-se hospitalização.
ORAP deve ser usado durante a gravidez apenas se o benefício potencial justificar o risco potencial para o feto.
General
Extrapyramidal Reactions
Neuromuscular (extrapyramidal) reactions during the administration of ORAP® (pimozide) have been reported frequently, often during the first few days of treatment. In most patients, these reactions involved Parkinson-like symptoms which, when first observed, were usually mild to moderately severe and usually reversible.
Other types of neuromuscular reactions (motor restlessness, dystonia, akathisia, hyperreflexia, opisthotonos, oculogyric crises) have been reported far less frequently. Severe extrapyramidal reactions have been reported to occur at relatively low doses. Generally the occurrence and severity of most extrapyramidal symptoms are dose-related since they occur at relatively high doses and have been shown to disappear or become less severe when the dose is reduced. Administration of antiparkinson drugs such as benztropine mesylate or trihexyphenidyl hydrochloride may be required for control of such reactions. It should be noted that persistent extrapyramidal reactions have been reported and that the drug may have to be discontinued in such cases.
Withdrawal Emergent Neurological Signs
Generally, patients receiving short term therapy experience no problems with abrupt discontinuation of antipsychotic drugs.
However, some patients on maintenance treatment experience transient dyskinetic signs after abrupt withdrawal. In certain of these cases the dyskinetic movements are indistinguishable from the syndrome described below under “Tardive Dyskinesia” except for duration. It is not known whether gradual withdrawal of antipsychotic drugs will reduce the rate of occurrence of withdrawal emergent neurological signs, but until further evidence becomes available, it seems reasonable to gradually withdraw use of ORAP.
Tardive Dyskinesia
ORAP may be associated with persistent dyskinesias. Tardive dyskinesia, a syndrome consisting of potentially irreversible, involuntary, dyskinetic movements, may appear in some patients on long-term therapy or may occur after drug therapy has been discontinued. The risk appears to be greater in elderly patients on high-dose therapy, especially females. The symptoms are persistent and in some patients appear irreversible. The syndrome is characterized by rhythmical involuntary movements of tongue, face, mouth or jaw (e.g., protrusion of tongue, puffing of cheeks, puckering of mouth, chewing movements). Sometimes these may be accompanied by involuntary movements of extremities and the trunk.
There is no known effective treatment for tardive dyskinesia; antiparkinson agents usually do not alleviate the symptoms of this syndrome. It is suggested that all antipsychotic agents be discontinued if these symptoms appear. Should it be necessary to reinstitute treatment, or increase the dosage of the agent, or switch to a different antipsychotic agent, this syndrome may be masked.
It has been reported that fine vermicular movement of the tongue may be an early sign of tardive dyskinesia and if the medication is stopped at that time the syndrome may not develop.
Electrocardiographic Changes
Electrocardiographic changes have been observed in clinical trials of ORAP in Tourette's Disorder and schizophrenia. These have included prolongation of the QT interval, flattening, notching and inversion of the T wave and the appearance of U waves. Sudden, unexpected deaths and grand mal seizure have occurred at doses above 20 mg/day.
Neuroleptic Malignant Syndrome
Neuroleptic malignant syndrome (NMS) has been reported with ORAP. (See WARNINGS for further information concerning NMS.)
Hyperpyrexia
Hyperpyrexia has been reported with other antipsychotic drugs.
Clinical Trials
The following adverse reaction tabulation was derived from 20 patients in a 6-week long placebo-controlled clinical trial of ORAP in Tourette's Disorder.
| Body System/ Adverse Reaction | Pimozide (N = 20) |
Placebo (N = 20) |
| Body as a Whole | ||
| Headache | 1 | 2 |
| Gastrointestinal | ||
| Dry Mouth | 5 | 1 |
| Diarrhea | 1 | 0 |
| Nausea | 0 | 2 |
| Vomiting | 0 | 1 |
| Constipation | 4 | 2 |
| Eructations | 0 | 1 |
| Thirsty | 1 | 0 |
| Appetite increase | 1 | 0 |
| Endocrine | ||
| Menstrual disorder | 0 | 1 |
| Breast secretions | 0 | 1 |
| Musculoskeletal | ||
| Muscle cramps | 0 | 1 |
| Muscle tightness | 3 | 0 |
| Stooped posture | 2 | 0 |
| CNS | ||
| Drowsiness | 7 | 3 |
| Sedation | 14 | 5 |
| Insomnia | 2 | 2 |
| Dizziness | 0 | 1 |
| Akathisia | 8 | 0 |
| Rigidity | 2 | 0 |
| Speech disorder | 2 | 0 |
| Handwriting change | 1 | 0 |
| Akinesia | 8 | 0 |
| Psychiatric | ||
| Depression | 2 | 3 |
| Excitement | 0 | 1 |
| Nervous | 1 | 0 |
| Adverse behavior effect | 5 | 0 |
| Special Senses | ||
| Visual disturbance | 4 | 0 |
| Taste change | 1 | 0 |
| Sensitivity of eyes to light | 1 | 0 |
| Decrease accommodation | 4 | 1 |
| Spots before eyes | 0 | 1 |
| Urogenital | ||
| Impotence | 3 | 0 |
The following adverse event tabulation was derived from 36 children (age 2 to 12) in a 24-week open trial of ORAP in Tourette's Disorder.
| Body System/ Adverse Reaction | Number of Patients Experiencing Each Event (%) | |
| All Events (N=36) |
Drug-Related Events (N=36) |
|
| Body as a Whole | ||
| Asthenia | 9 (25.0) | 5 (13.8) |
| Headache | 8 (22.2) | 1 (2.7) |
| Gastrointestinal | ||
| Dysphagia | 1 (2.7) | 1 (2.7) |
| Increased Salivation | 5 (13.8) | 2 (5.5) |
| Musculoskeletal | ||
| Myalgia | 1 (2.7) | 1 (2.7) |
| Central Nervous System | ||
| Dreaming Abnormal | 1 (2.7) | 1 (2.7) |
| Hyperkinesia | 2 (5.5) | 1 (2.7) |
| Somnolence | 10 (27.7) | 9 (25.0) |
| Torticollis | 1 (2.7) | 1 (2.7) |
| Tremor, Limbs | 1 (2.7) | 1 (2.7) |
| Psychiatric | ||
| Adverse Behavior Effect | 10 (27.7) | 8 (22.2) |
| Nervous | 3 (8.3) | 2 (5.5) |
| Skin | ||
| Rash | 3 (8.3) | 1 (2.7) |
| Special Senses | ||
| Visual Disturbance | 2 (5.5) | 1 (2.7) |
| Cardiovascular | ||
| ECG Abnormal | 1 (2.7) | 1 (2.7) |
Because clinical investigational experience with ORAP in Tourette's Disorder is limited, uncommon adverse reactions may not have been detected. The physician should consider that other adverse reactions associated with antipsychotics may occur.
Other Adverse Reactions
In addition to the adverse reactions listed above, those listed below have been reported in U.S. clinical trials of ORAP in conditions other than Tourette's Disorder.
Body as a Whole: Asthenia, chest pain, periorbital edema
Cardiovascular/Respiratory: Postural hypotension, hypotension, hypertension, tachycardia, palpitations
Gastrointestinal: Increased salivation, nausea, vomiting, anorexia, GI distress
Endocrine: Loss of libido
Metabolic/Nutritional: Weight gain, weight loss
Central Nervous System: Dizziness, tremor, parkinsonism, fainting, dyskinesia
Psychiatric: Excitement
Skin: Rash, sweating, skin irritation
Special Senses: Blurred vision, cataracts
Urogenital: Nocturia, urinary frequency
Postmarketing Reports
The following experiences were described in spontaneous postmarketing reports. These reports do not provide sufficient information to establish a clear causal relationship with the use of ORAP.
Gastrointestinal: Gingival hyperplasia in one patient
Hematologic: Hemolytic anemia
Metabolic/Nutritional: Hyponatremia
Other: Seizure
Em geral, os sinais e sintomas de superdosagem com ORAP (pimozida) seriam ser um exagero de efeitos farmacológicos conhecidos e reações adversas, o o mais proeminente seria: 1) anormalidades eletrocardiográficas, 2) reações extrapiramidais graves, 3) hipotensão, 4) um estado de coma com respiratório depressão.
Em caso de sobredosagem, lavagem gástrica, estabelecimento de uma via aérea patente e, se necessário, recomenda-se a respiração assistida mecanicamente. Eletrocardiográfico o monitoramento deve começar imediatamente e continuar até os parâmetros do ECG estão dentro da faixa normal. Hipotensão e colapso circulatório podem ser neutralizados pelo uso de fluidos intravenosos, plasma ou albumina concentrada e vasopressor agentes como metaraminol, fenilefrina e noradrenalina.
Epinefrina não deve ser usada. Em caso de reações extrapiramidais graves, medicação antiparkinson deve ser administrada. Por causa da meia-vida longa de pimozida, os pacientes que tomam uma overdose devem ser observados por pelo menos 4 dias. Como em todos os medicamentos, o médico deve considerar entrar em contato com um controle de veneno centro para informações adicionais sobre o tratamento de sobredosagem.


