









コンポーネント:
治療オプション:
Fedorchenko Olga Valeryevna 、薬局による医学的評価、 最終更新日:27.03.2022

アテンション! そのこのページの情報は医療専門家のみを対象としています! その情報が収集したオープン源を含めることが可能である重大な誤差! 注意して、このページ上のすべての情報を再確認してください!


医薬品の形態と強み。
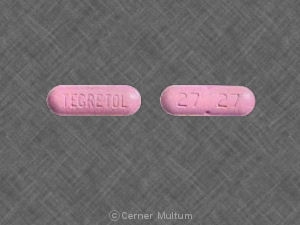
経口投与用の徐放性を持つEQUETRO(カルバマゼピン)カプセルは、3つの用量強度で提供されます。
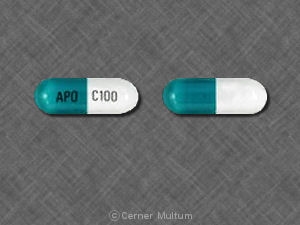
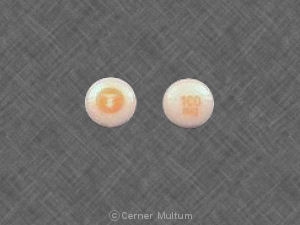
- 100 mg。 -2部構成のハードゼラチンカプセルイエロー不透明キャップ。片側にSPD417、反対側にSPD417と100 mgを白インクで印刷した青緑の不透明ボディ。
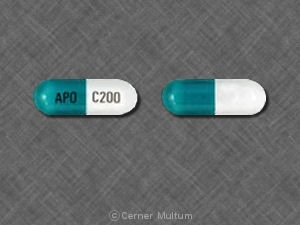
- 200 mg。 -2部構成のハードゼラチンカプセルイエロー不透明キャップ。片側にSPD417、反対側にSPD417と200 mgが白インクで印刷された青の不透明なボディ。.
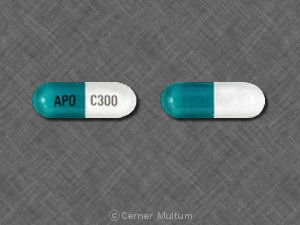
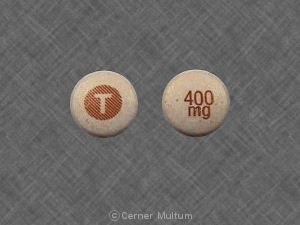
- 300 mg。 -2部構成のハードゼラチンカプセルイエロー不透明キャップ。片側にSPD417、反対側にSPD417と300 mgを白インクで印刷した青いボディ。.
保管と取り扱い。
EQUETRO(カルバマゼピン)徐放カプセルは、3つの投与強度で供給されます。
25°C(77°F)で買い物をします。 15〜30°C(59〜86°F)までの遠足。.
光と湿気から保護してください。
データセンター向けに作成されたValidusは、Pharmaceuticals LLC、119 Cherry Hill Road、Suite 310、Parsippany、NJ 07054を買収しました。. 改訂:2016年9月。

双極性I障害に関連する急性 ⁇ 病または混合エピソード。
EQUETROは、双極性I障害に関連する急性 ⁇ 病または混合エピソードの患者の治療に適応されます。.
痛み三 ⁇ 神経痛。
EQUETROは、三 ⁇ 神経痛に関連する痛みの治療に使用されます。. 好結果は、舌 ⁇ 頭神経痛でも報告されています。. この薬は単純な鎮痛剤ではなく、 ⁇ 細な痛みや痛みを和らげるために使用しないでください。.
てんかん。
EQUETROは、複雑な症状を伴う部分発作の治療に使用されます(例:. 精神運動、側頭葉)、全身性強直間代発作(大 ⁇ )および混合発作パターン。ここにリストされている発作のタイプまたは他の部分的または全身性発作が含まれます。..
使用制限。
EQUETROは、不在のない発作の治療には適応されません(プチマル)。. カルバマゼピンは、これらの患者の全身性けいれんの頻度の増加と関連しています。.

治療前スクリーニング。
EQUETROによる治療を開始する前に、HLA-B * 1502対立遺伝子の存在について、遺伝的に絶滅危 ⁇ 種の祖先を持つ患者をテストします。. 高解像度遺伝子型テストは、1つまたは2つのHLA-B * 1502対立遺伝子が存在する場合に陽性です。. 利点が明らかにリスクを上回らない限り、対立遺伝子が陽性であった患者ではEQUETROを使用しないでください。.
血小板、場合によっては網状赤血球および血清鉄を含む血球の完全な前処理をベースラインとして取得する必要があります。. 治療中に患者が白血球または血小板数が少ないか減少している場合は、患者を注意深く監視する必要があります。. 骨髄抑制の兆候がある場合は、EQUETROの中止を検討する必要があります。.
EQUETROによる治療中、特に肝疾患の病歴のある患者では、肝機能の基本的および定期的な検査を実施する必要があります。これは、肝障害が発生する可能性があるためです。. 重度の肝機能障害または活動性肝疾患がある場合は、EQUETROを停止してください。.
多くのフェノチアジンと関連薬が目の変化を引き起こすことが示されているので、スリットランプ、眼底のコピー、調度測定を含む基本的および定期的な目の検査が推奨されます。.
観察された腎障害のためにこの製品で治療された患者には、ベースラインと定期的な完全尿分析とBUN測定が推奨されます。.
双極性I障害に関連する急性 ⁇ 病または混合エピソードの投与量。
EQUETROの推奨開始用量は、1日2回200 mgです。. 最適な臨床反応を達成するために、用量を1日あたり200 mg増やすことができます。. 双極性障害に関連する ⁇ 病では、1日あたり1600 mgを超える用量は研究されていません。.
痛みのための投与量三 ⁇ 神経痛。
初期:初日に1日1回200 mgカプセルから始めます。. この用量は、効果的で耐容性のある用量を達成するために、12時間ごとに100 mgのステップで最大200 mg /日までしか増加できません。. 1日の総投与量1200 mgを超えないようにしてください。.
メンテナンス:痛みの制御は、毎日400 mg〜800 mgのほとんどの患者で維持できます。. ただし、一部の患者は毎日200 mgしか服用できませんが、他の患者は毎日最大1200 mgを服用できます。. 治療期間中少なくとも3か月ごとに、用量を最小有効レベルに減らすか、薬物を停止させる試みを行う必要があります。.
てんかんの投与量。
12歳以上の大人と子供。
推奨される開始用量は、1日2回200 mgです。. 最適な反応が達成されるまで、1日2回の均等に分散された1日2回投与として投与される、1日あたり200 mgの週単位の増加。. 12歳から15歳の子供では、通常、1日2回500 mgを超えてはなりません。. 15〜18歳の子供には1日2回600 mg。成人では1日2回800 mg。.
12歳未満の子供。
最適な臨床反応は通常、35 mg / kg未満の1日量で達成されます。. 35 mg / kg / 24時間を超える用量でのEQUETROの安全性に関する推奨はありません。.
他のAEDとの同時投与。
EQUETROは、単独で、または他のAEDで使用できます。. 既存のAEDに追加する場合は、他のAEDの投与量を維持または徐々に減らしながら、徐々にEQUETROを追加します。. カルバマゼピンを他のAEDと併用する場合は、潜在的な薬物相互作用を考慮する必要があります。.
すぐに放出されるカルバマゼピンからEQUETROに変更します。
EQUETROは、1日2回の投与用に拡張リリースの配合です。. カルバマゼピンの即時放出のある患者を長期放出のEQUETROカプセルに変換する場合、カルバマゼピンの同じ1日総量をmgで投与する必要があります。. EQUETROに切り替えた後、患者は発作の制御について注意深く監視する必要があります。. 変換後の治療反応に応じて、推奨される投与量の指示内で1日の総投与量を調整する必要がある場合があります。.
EQUETROを設定します。
適応症ごとにEQUETROの服用を中止した場合は、徐々に用量を減らし、突然の中止を避けて発作のリスクを減らしてください。.
血清中のカルバマゼピン濃度を監視します。
血清中のカルバマゼピン濃度のモニタリングは、特にEQUETRO代謝の変化が発生する可能性のある臨床条件(例:. 薬物相互作用)。. てんかんのためにEQUETROで治療された小児患者で満足のいく臨床反応が得られなかった場合は、血漿レベルを測定して、治療範囲内かどうかを判断します。.
投与方法。
EQUETROカプセルを丸ごとまたは開けて、小さじ1杯のアップルソースのように真 ⁇ を食品に振りかけます。. EQUETROカプセルやカプセル内の真 ⁇ を粉砕したり噛んだりしないでください。. EQUETROは食事の有無にかかわらず服用できます。.

- 骨髄抑制。.
- アナフィラキシーや重度の過敏反応など、カルバマゼピンに対する既知の過敏症。.
- 三環化合物の1つに対する既知の過敏症(例:.、アミトリプチリン、デジプラミン、イミプラミン、プロトリプチリン、ノルトリプチリン。. 過敏症反応には、アナフィラキシーと重度の発疹が含まれます。.
- CYP3A4の基質であるデラビルジンまたは他の非ヌクレオシド系逆転写酵素阻害剤の同時使用。. EQUETROは、CYP3A4を誘導することにより、これらの薬物の濃度を大幅に低減できます。. これはウイルス学的反応の喪失とこれらの薬物に対する可能な抵抗につながる可能性があります。.
- モノアミンオキシダーゼ阻害剤(MAOI)の同時使用。. EQUETROによる治療を開始する前に、MAOIを少なくとも14日間中止する必要があります。. 同時使用するとセロトニン症候群を引き起こす可能性があります。.
- ネファゾドンの同時使用。. これは、治療効果を達成するために、ネファゾドンとその活性代謝物の血漿濃度が不十分になる可能性があります。.

警告。
の一部として含まれています。 「注意」。 セクション。
注意。
重度の皮膚反応。
カルバマゼピン治療では、中毒性表皮壊死症(TEN)やスティーブンスジョンソン症候群(SJS)などの重 ⁇ で、時には致命的な皮膚反応が報告されています。. これらの症候群は、粘膜 ⁇ 瘍、発熱、痛みを伴う発疹を伴う可能性があります。. SJS / TENを投与されたカルバマゼピン治療患者の90%以上が、治療の最初の数か月以内にこれらの反応を発症しました。. これらの反応のリスクは、主に白人の人口を持つ国の新規ユーザー10,000人あたり約1〜6人と推定されています。. ただし、一部のアジア諸国では、リスクは約10倍と推定されています。. DER患者に深刻な皮膚反応があると思われる場合は、EQUETROを停止してください。. 兆候または症状がSJS / TENを示している場合は、EQUETROによる治療を再開しないでください。
SJS、TEN、HLA-B * 1502対立遺伝子。
遡及的症例対照研究は、中国系の患者では、EQUETRO治療によるSJS / TENの発症リスクとHLA-B * 1502対立遺伝子(HLA-B-遺伝性の変異体)の存在との間に強い関連があることを示しています遺伝子)が存在します)。. EQUETRO療法を開始する前に、患者でこのHLA-B * 1502の対立遺伝子検査を実施する可能性が高くなります。. 高解像度遺伝子型テストは、1つまたは2つのHLA-B * 1502対立遺伝子が存在する場合に陽性です。. HLA-B * 1502対立遺伝子に陽性である患者では、深刻な皮膚反応のリスクを明らかに上回らない限り、EQUETROを使用しないでください。. 陰性対立遺伝子を有する検査を受けた患者は、カルバマゼピン治療に関連するSJS / TENのリスクが低いと考えられています。.
HLA-B * 1502対立遺伝子の有病率は、アジアの人口で高くなる可能性があります。香港、タイ、マレーシア、フィリピンの一部(15%以上)。台湾(10%)、中国北部(4%);インド人を含む南アジア人(2〜4%)。日本と韓国(1%未満)。. HLA-B * 1502は、アジア出身ではない人々(例:. 白人、アフリカ系アメリカ人、ヒスパニックおよびインディアン)。. これらの集団におけるHLAB * 1502対立遺伝子の推定率の精度は、民族グループ内の率の大きな変動、民族的起源の決定の困難さ、および混合降下の可能性によって制限される場合があります。.
HLA-B * 1502対立遺伝子は、黄斑丘疹の発疹(MPE)などのカルバマゼピンによるそれほど深刻ではない副皮膚反応のリスクを予測したり、好酸球増加症や全身症状(DRESS)を伴う薬物反応を予測したりすることはわかっていません。.
限られた証拠は、HLA-B * 1502が、フェニトインを含むSJS / TENに関連する他の抗てんかん薬を服用している中国生まれの患者におけるSJS / TENの発症の危険因子である可能性があることを示唆しています。. HLA-B * 1502人の陽性患者でSJS / TENに関連する他の医薬品を使用しないでください。.
過敏反応とHLA-A * 3101対立遺伝子。
ヨーロッパ、韓国、日本系の患者を対象とした遡及的症例対照研究は、過敏反応を発症するリスクと、カルバマゼピンの患者におけるHLA-A遺伝性対立遺伝子であるHLA-A * 3101の存在との間に中程度の関係があります。見つかりました。. これらの過敏反応には、SJS / TEN、黄斑丘疹の発疹、好酸球増加症および全身症状を伴う薬物反応が含まれます。.
予想通りです。, HLA-A * 3101は次の頻度で存在します:日本の患者では15%以上。, インド人。, 南インド。 (例えば。, タミルナードゥ州。) そしてアラブ系。; 患者の最大約10%は中国人です。, 韓国人。, ヨーロッパ人。, ラテンアメリカおよびその他のインド系。; アフリカ系アメリカ人とタイ人患者では最大約5%。, 台湾人と中国人の家系。 (香港。).
HLA-A * 3101に陽性であることが知られている患者では、EQUETROを考慮する前に、EQUETRO療法のリスクと利点を検討する必要があります。.
HLAジェノタイピングの過敏症と制限。
スクリーニングツールとしてのHLAジェノタイピングの使用には重要な制限があり、適切な臨床的警戒と患者管理に取って代わってはなりません。. 多くのHLA-B * 1502陽性およびHLA-A * 3101-EQUETROで治療された陽性患者はSJS / TENまたは他の過敏反応を発症せず、これらの反応はHLA-B * 1502陰性およびHLA-Aで見ることができます* 3101民族の否定的な患者はまだほとんど発生しません。. SJS / TENの発生と ⁇ 患率、およびAED用量、コンプライアンス、付随する薬物、併存症、皮膚モニタリングの程度などの他の過敏反応における他の考えられる要因の役割は研究されていません。.
再生不良性貧血と無 ⁇ 粒球症。
再生不良性貧血とアグラヌロサイトーシスは、カルバマゼピンで治療された患者で発生しました。. 人口ベースの症例対照研究のデータは、これらの反応を発症するリスクが一般人口の5〜8倍であることを示唆しています。. しかし、未治療の一般集団におけるこれらの反応の全体的なリスクは低く、無 ⁇ 粒球症では年間人口100万人あたり約6人の患者、再生不良性貧血では年間2人の患者100万人あたり2人の患者です。.
カルバマゼピンの使用に関連する一時的または持続的な血小板レベルの低下または白血球の報告は珍しいことではありませんが、発生率または結果を正確に推定するためのデータはありません。. しかし、白血球減少症の症例の大部分は、再生不良性貧血または無 ⁇ 粒球症のより深刻な状態に進んでいません。.
無 ⁇ 粒球症と再生不良性貧血の発生率が非常に低いため、EQUETROに基づく患者の監視で観察された軽微な血液学的変化の大部分は、いずれかの異常の発生を示す可能性は低いです。. それにもかかわらず、血液検査の完全な前処理は基礎として取得されるべきです。. 治療中に患者が白血球または血小板数が少ないか減少している場合は、患者を注意深く監視する必要があります。. 骨髄抑制の兆候がある場合は、EQUETROの停止を検討してください。. 臨床的特徴には、発熱、運動中の呼吸困難、疲労、軽度のあざ、点状出血、鼻血、歯茎の出血、重度の月経などがあります。.
好酸球増加症と全身症状/多臓器過敏症を伴う薬物反応。
カルバマゼピンで、多臓器過敏症としても知られている好酸球増加症および全身症状(DRESS)を伴う薬物反応が発生しました。. これらの出来事のいくつかは致命的または生命を脅かすものでした。. ストレスは通常、発熱、発疹、リンパ節腫 ⁇ 、および/または顔面の腫れと併せて、肝炎、腎炎、血液異常、心筋炎または筋炎などの他の臓器系の関与と併せて発生します。. 好酸球増加症がよく見られます。. この障害はあなたの表現に変化し、ここで言及されていない他の臓器系が関与している可能性があります。. 過敏症の初期の症状(例:.、発熱、リンパ節腫 ⁇ )、発疹は明らかではありません。. そのような兆候や症状がある場合は、患者を直ちに検査する必要があります。. 兆候や症状の代替病因を特定できない場合は、EQUETROを中止する必要があります。.
過敏症。
カルバマゼピンに対する過敏反応は、フェニトイン、プリミドン、フェノバルビタールなどの抗けいれん薬に対して以前にこの反応を示した患者で報告されています。. そのような履歴が存在する場合は、使用とリスクを慎重に検討する必要があります。EQUETROが開始される場合は、過敏症の兆候と症状を注意深く監視する必要があります。.
カルバマゼピンに対して過敏反応を示した患者は、オックスカルバゼピンに対して約25〜30%の過敏反応を経験する可能性があります。.
自殺行動とイデオロギー。
EQUETROを含む抗てんかん薬(AED)は、各適応症についてこれらの薬を服用している患者の思考や行動のリスクを高めます。. 適応症のためにAEDで治療された患者は、うつ病の発生または悪化、自殺または行動の考え、および/または異常な気分または行動の変化について監視する必要があります。.
199のプラセボ対照臨床試験のプールされた分析。 (モノ-そして追加の治療。) 11の異なるAEDが示されました。, AEDの1つを持つ無作為化患者は、リスクの約2倍でした。 (調整された相対リスク1.8。, 95%CI:1.2。, 2.7。) 患者と比較した自殺念慮や行動の。, プラセボで治療するために無作為化されました。. これらの研究では、平均治療期間は12週間です。, AEDで治療された27,863人の患者における自殺行動または思想の推定発生率は、プラセボ治療を受けた16,029人の患者の0.24%と比較して0.43%でした。, これは、治療を受けた530人の患者ごとに自殺念慮または行動の約1例の増加に相当します。. 研究では薬物治療を受けた患者に4人の自殺があり、プラセボ治療を受けた患者には自殺がありませんでしたが、その数は小さすぎて自殺に対する薬物効果について結論を出すことができません。.
AEDによる自殺念慮または行動のリスクの増加は、AEDによる薬物治療の開始から1週間後に観察され、治療期間中は評価されたままでした。. 分析に含まれるほとんどの研究は24週間を超えなかったため、自殺念慮や行動のリスクは24週間を超えて評価できませんでした。.
自殺の考えや行動のリスクは、一般的に薬物の分析データで一貫していた。. アクションのメカニズムが異なり、多くの適応症にわたってAEDのリスクが増加していることが判明すると、リスクは各適応症に使用されるすべてのAEDに適用されることがわかります。. 分析された臨床試験では、リスクは年齢(5〜100歳)によって有意に変化しませんでした。 . 表1は、評価されたすべてのAEDの指標による絶対リスクと相対リスクを示しています。.
表1プールされた分析での適応後の抗てんかん薬における思考または行動(反応)のリスク。
自殺念慮や行動の相対リスクは、てんかんの臨床試験では、精神疾患やその他の疾患の臨床試験よりも高かったが、てんかんと精神医学的適応症の絶対的な違いは類似していた。.
EQUETROまたは別のAEDの処方を検討している人は、自殺念慮や行動のリスクと未治療の疾患のリスクを両立させる必要があります。. てんかんおよびAEDが処方されている他の多くの疾患は、それ自体が ⁇ 患率と死亡率、および思考と自殺行動のリスクの増加に関連しています。. 治療中に自殺の考えや行動が発生した場合、処方医師は、これらの症状が治療対象の疾患を持つ特定の患者で発生する可能性があるかどうかを確認する必要があります。.
患者。, あなたの介護者と家族に通知する必要があります。, AEDは自殺の考えや行動のリスクを高めること。, そして、必要性を認識させてください。, うつ病の徴候および症状の発生または悪化について。, 異常な気分や行動の変化、または自殺の考えの発生。, -行動や思考に自傷行為を認識させるため。. 行動については、すぐに医療提供者に報告する必要があります。.
胚胎児毒性。
EQUETROはカテゴリーDの薬です。 .
EQUETROは、妊娠中の女性に投与すると胎児の損傷を引き起こす可能性があります。. このリスクの可能性がある女性を称賛します。. 治療の潜在的な使用がリスクを上回る場合にのみ、妊娠中に使用してください。
疫学データは、妊娠中のカルバマゼピンの使用と二分脊椎を含む先天性奇形との間にリンクがあるかもしれないことを示唆しています。. この薬が妊娠中に使用された場合、または患者がこの薬を服用している間に妊娠した場合、患者は胎児への潜在的なリスクについて通知されるべきです。.
遡及的症例評価は、単剤療法と比較して、併用療法での抗けいれん薬の使用に関連して催奇形性効果のより高い有病率が発生する可能性があることを示唆しています。.
ヒトでは、カルバマゼピンの経胎盤通過が速く(30〜60分)、薬物は胎児組織で見られ、脳や肺よりも肝臓と腎臓のレベルが高くなります。.
カルバマゼピンは、1200 mg / kgベースのヒト1日用量の10〜25倍、または1200 mg〜mg / mのヒト1日用量の1.5〜4倍の用量で経口投与した場合、ラットの生殖試験に悪影響を与えることが示されています。2ベース。. ラットの奇形研究では、250 mg / kgの135の子孫関節 ⁇ 骨のうち2つと119の子孫のうち4つが650 mg / kgで他の異常を示しました(ガム ⁇ 間、1;タリペス、1;無眼球増加、2)。.
現在認識されている手順による欠陥検出テストは、EQUETROを受ける出産の可能性のある女性の定期的な出産前ケアの一部と見なされるべきです。
子宮内でのEQUETROへの曝露の影響に関する追加情報を提供するため。, 医師は、北米の抗てんかん薬の妊娠登録への登録を推奨することをお勧めします。 (NAAED。) EQUETROを服用している妊娠中の患者へ。これはフリーダイヤル1-888-233-2334で行うことができ、患者自身が実行する必要があります。. 登録情報は、ウェブサイトhttp://www.aedpregnancyregistry.org/にもあります。
突然の離乳と発作のリスク。
発作やその他の離脱症状/症状のリスクがあるため、突然EQUETROを止めないでください。. 発作障害のある患者は、発作およびてんかん重積症を発症するリスクが高く、低酸素症と生命への危険が伴います。. ただし、アレルギー反応または過敏反応が発生した場合は、代替療法のより迅速な代替が必要になることがあります。.
低ナトリウム血症。
低ナトリウム血症は、EQUETROによる治療の結果として発生する可能性があります。多くの場合、低ナトリウム血症は不適切な抗利尿ホルモン分 ⁇ 症候群(SIADH)によって引き起こされているようです)。. EQUETRO治療でSIADHを発症するリスクは、用量依存的であるようです。. 高齢患者と利尿薬で治療された患者は、低ナトリウム血症を発症するリスクが高くなります。. 低ナトリウム血症の兆候と症状には、頭痛、発作の頻度が新たに増加または増加、集中困難、記憶障害、混乱、衰弱、転倒につながる可能性のある落ち着きのなさなどがあります。. 症候性低ナトリウム血症患者のEQUETROの停止を検討してください。.
認知障害および運動障害の可能性。
EQUETROは、判断力、認知、運動機能を損なう可能性があります。. EQUETROがあなたに悪影響を及ぼさないことが合理的に確実になるまで、車を含む危険な機械を操作している患者に注意してください。. 双極性障害の臨床試験に含まれる副作用(EQUETRO、N = 251およびプラセボ、N = 248):傾眠(32%vs. 13%)、運動失調(15%)。. 0.4%)、めまい(44%)。. 12%)、めまい(2%)。. 1%)、異常だと思う(2%対. 0.4%)、振戦3%対. 1%)ぼやけています(6%vs. 2%)。.
EQUETROを同時に使用する場合、CYP3A4の基質である非ヌクレオシド系逆転写酵素阻害剤に対するウイルス学的反応が失われる可能性があります。
EQUETROとデラビルジンを含む非ヌクレオシド系逆転写酵素阻害剤との同時投与は、ウイルス学的反応の喪失と耐性の可能性につながる可能性があるため、禁 ⁇ です。. CYP3A4を誘導することにより、EQUETROはこれらの薬物の濃度を大幅に低減できます。. デラビルジン、NNRTI、およびCYP3A4とEQUETROの基質を併用投与すると、デラビルジン濃度を90%低下させることができます。.
肝障害。
肝酵素の軽度の増加からまれな肝不全までの肝への影響が報告されています。. 場合によっては、薬物を止めたにもかかわらず、肝効果が進行することがあります。. 胆管症候群の消失のまれなケースも報告されています。. この症候群は、劇症から怠惰までの範囲の可変臨床経過を伴う胆 ⁇ うっ滞プロセスで構成され、肝内胆道の破壊と消失を伴います。. すべてではありませんが、一部の症例は、深刻な皮膚反応や好酸球増加症を伴う薬物反応や全身症状/多臓器過敏症など、他の免疫性症候群と重複する特徴に関連しています。.
肝機能障害が発生する可能性があるため、特に肝疾患の病歴のある患者では、この薬による治療中に肝機能の基本的かつ定期的な評価を行う必要があります。. 重度の肝機能障害または活動性肝疾患が発生した場合は、直ちに中止する必要があります。.
AVハートブロック。
カルバマゼピン治療後、2度目と3度のブロックを含むAV心臓ブロックが報告されています。. これは一般的に発生しましたが、それだけでなく、根本的なECG異常またはライン障害の危険因子がある患者でも発生しました。.
肝性ポルフィリン症。
EQUETROの使用は、肝ポルフィリン症の病歴がある患者では避けてください(例:. 急性間欠性ポルフィリン症、カラフルなポルフィリン症、ポルフィリン症クルタネアタルダ)。. 急性発作は、カルバマゼピン療法を受けている患者で報告されています。. EQUETROの投与により、げっ歯類のポルフィリン前駆体が増加することも示されています。これは、急性ポルフィリン発作の誘発の疑いがあるメカニズムです。.
眼圧の上昇。
カルバマゼピンは軽度の抗コリン作用があります。. 眼圧の上昇の病歴がある患者では、治療を開始する前に、治療中に定期的に眼圧を評価する必要があります。.
患者アドバイス情報。
FDA承認の患者ラベル(。薬ガイド。 ).
薬物ガイドが利用可能であることを患者と介護者に伝えます。. あなたに指示してください。 薬ガイド。 EQUETROを服用する前に読むこと。
- 重度の皮膚反応。
致命的で深刻な皮膚反応のリスクと、深刻な皮膚反応を示す可能性のある兆候や症状について、患者と看護師に通知します。. EQUETROによる治療中に皮膚反応が発生した場合は、直ちに医師に相談するよう患者に指示してください。 - 無 ⁇ 粒球症と再生不良性貧血。
致命的な可能性のある無 ⁇ 粒球症と再生不良性貧血のリスク、およびこれらの反応を示す可能性のある兆候と症状について、患者と介護者に伝えます。. 症状が現れたらすぐに医師に伝えてください。. - 好酸球増加症と全身症状を伴う薬物反応。
血液学的、皮膚学的、過敏症または肝反応の可能性のある初期の毒性徴候および症状について患者に伝えます。. これらの兆候や症状は深刻な反応を示す可能性があることを患者に伝え、兆候があればすぐに医師に報告してください。. - 自殺と行動の考え。
患者に助言する。, 介護者。, そしてそのAEDの家族。, EQUETROを含みます。, 自殺念慮や行動のリスクを高める可能性があります。, うつ病の症状に対応または悪化する必要性をお知らせします。, 異常な気分や行動の変化。, または自殺の考えに気づくようになる。, 自傷行為についての行動や考え。. 患者、介護者、家族に、心配な行動をすぐに医療提供者に報告するように指示します。. - 胚胎児毒性。
EQUETROが胎児の損傷を引き起こす可能性があることを出産の可能性のある女性に助言します。. 治療の潜在的な使用がリスクを上回る場合にのみ、妊娠中に使用してください。. - 突然の停止と発作のリスク。
EQUETROを突然停止すると、発作や発作の頻度が増加する可能性があることを患者に通知します。. 離乳時に薬を服用する必要があることを患者に助言します。. - 低ナトリウム血症。
特にナトリウムを下げる可能性のある他の薬を服用している場合は、EQUETROが血清中のナトリウムレベルを下げる可能性があることを患者に伝えます。. 吐き気、疲労、エネルギー不足、混乱、発作、またはより頻繁またはより重度の発作などの低ナトリウム症状を報告するよう患者に助言します。. - 認知障害および運動障害の可能性。
十分な経験があるまで、機械を運転または操作しないように患者にアドバイスします。 EQUETROは、それが機械の運転または操作能力に影響を与えるかどうかを測定します。. アルコールをEQUETRO療法と組み合わせて服用する場合は、患者に注意するようアドバイスしてください。 可能な相加的な鎮静効果。. - 他のカルバマゼピン製品との同時使用。
EQUETROにはカルバマゼピンが含まれており、カルバマゼピンを含む他の薬と組み合わせて使用 しないでください。. - 経口避妊薬の有効性の低下。
EQUETROは経口避妊の効果を大幅に低下させる可能性があることを患者に伝えます。. これは避妊の失敗または画期的な出血につながる可能性があります。.
妊娠したら、北米の抗てんかん規制登録(NAAED)に登録するよう患者に奨励します。. このレジスターは、妊娠中の抗てんかん薬の安全性に関する情報を収集します。.
非臨床毒物学。
発がん、変異誘発および生殖能力障害。
発がん性物質。
25、75、250 mg / kg /日の用量で2年間にわたって食品にカルバマゼピンをSprague-Dawleyラットに投与(低用量1200 mg〜mg / mのヒト1日用量の約0.2倍)。2 -基礎)は、女性の肝細胞腫瘍の発生率と男性の精巣の良性間質性セラデノーマの用量関連の増加につながりました。.
変異原性。
カルバマゼピンを用いた細菌および哺乳類の変異原性試験により、陰性の結果が得られました。.
不妊の障害。
カルバマゼピンが男性と女性の生殖能力に及ぼす影響は研究されていません。.
ホデナトロフィーは、50〜400 mg / kg /日の用量で4〜52週間のカルバマゼピンを経口投与したラットで発生しました。. さらに、25、75、250 mg / kg /日の用量で2年間食品にカルバマゼピンを投与されたラットは、用量に関連した精巣 ⁇ 縮および精子形成の発生率を示しました。.
特定の集団で使用します。
妊娠。
妊娠カテゴリーD
リスクの概要。
EQUETROは、妊娠中の女性に投与すると胎児の損傷を引き起こす可能性があります。. 疫学データは、妊娠中のカルバマゼピンの使用と二分脊椎を含む先天性奇形との間にリンクがあるかもしれないことを示唆しています。. カルバマゼピンを用いた動物生殖試験で有害な発達効果が観察されています。. この薬が妊娠中に使用された場合、または患者が薬を服用している間に妊娠した場合、患者は胎児への潜在的なリスクについて通知されるべきです。.
妊娠登録。
患者は、妊娠したときに北米の抗てんかん規制登録(NAAED)に登録するように奨励されるべきです。. このレジスターは、妊娠中の抗てんかん薬の安全性に関する情報を収集します。. 登録するには、患者はフリーダイヤル1888-233-2334に電話できます。. 北米医薬品妊娠登録に関する情報は、http://www.aedpregnancyregistry.org/にあります。.
臨床上の考慮事項。
妊娠中の女性をEQUETROで治療するときは、治療の潜在的なリスクと利点の両方を注意深く検討し、適切にアドバイスしてください。. 現在認識されている手順に従って深刻な先天性奇形を検出するテストは、カルバマゼピンを投与されている妊婦の定期的な出生前ケアの一部と見なされるべきです。.
人間のデータ。
疫学データは、妊娠中のカルバマゼピンの使用と二分脊椎を含む先天性奇形との間にリンクがあるかもしれないことを示唆しています。. 遡及的症例評価は、単剤療法と比較して、併用療法での抗けいれん薬の使用に関連して催奇形性効果のより高い有病率が発生する可能性があることを示唆しています。.
カルバマゼピンの経胎盤通過は速く(30〜60分)、薬物は胎児組織に蓄積され、脳や肺よりも肝臓と腎臓のレベルが高くなります。.
母体カルバマゼピンおよびその他の抗けいれん薬の使用に関連する新生児発作および/または呼吸抑制のいくつかのケースがありました。. 母親でのカルバマゼピンの使用により、新生児の ⁇ 吐、下 ⁇ 、および/または摂食の減少のいくつかのケースも報告されています。. これらの症状は新生児離脱症候群である可能性があります。.
動物データ。
カルバマゼピンは、1200 mg / kgベースのヒト1日用量の10〜25倍、または1200 mg〜mg / mのヒト1日用量の1.5〜4倍の用量で経口投与した場合、ラットの生殖試験に悪影響を与えることが示されています。2ベース。. ラットの奇形研究では、250 mg / kgの135の子孫関節 ⁇ 骨のうち2つと119の子孫のうち4つが650 mg / kgで他の異常を示しました(ガム ⁇ 間、1;タリペス、1;無眼球増加、2)。.
仕事と配達。
人間の仕事と出産に対するカルバマゼピンの影響は不明です。. カルバマゼピンとそのエポキシ代謝産物は、授乳中に母乳に変換されます。. カルバマゼピンに曝露された授乳中の乳児に深刻な副作用が発生することがあります。. 母乳育児の母親は、母親にとっての薬物の重要性を考慮して、ケアを中止するか、EQUETRO治療を中止するかを決定する際に、治療の潜在的な利点とリスクを考慮する必要があります。.
母乳育児の母親。
カルバマゼピンとそのエポキシ代謝物は母乳中に排 ⁇ されます。. EQUETROに曝露された乳児に深刻な副作用が生じる可能性があるため、母親にとっての薬物の重要性を考慮して、ケアを停止するか、EQUETROによる治療を中止するかを決定する必要があります。.
小児用。
小児および青年期の患者におけるEQUETROの安全性と有効性は確立されていません。.
老人病アプリケーション。
EQUETROによる臨床試験には、65歳以上の被験者が含まれておらず、若い被験者とは異なる反応を示すかどうかを判断できませんでした。. 他の報告された臨床経験は、高齢者と若い患者の間の反応に違いを発見していません。. 一般に、高齢患者の用量選択は注意する必要があり、通常は用量範囲の下限から始まり、肝機能、腎臓、または心機能の低下の頻度の増加、および付随する疾患やその他の薬物療法を反映します。.
| プラセボ。 | 抗てんかん薬。 | |||
| 注。 | 1000人の患者あたりの反応。 | 1000人の患者あたりの反応。 | 相対リスク:AEDグループでの反応の発生率/プラセボグループでの反応の発生率。 | リスクの違い:患者1000人あたりのイベントがある追加の薬物患者。 |
| てんかん。 | 1.0。 | 3.4。 | 3.5。 | 2.4。 |
| 精神科。 | 5.7。 | 8.5。 | 1.5。 | 2.9。 |
| その他。 | 1.0。 | 1.8。 | 1.9。 | 0.9。 |
| 合計。 | 2.4。 | 4.3。 | 1.8。 | 1.9。 |

すぐに放出されるカルバマゼピンからEQUETROに変更します。
EQUETROは、1日2回の投与用に拡張リリースの配合です。. カルバマゼピンの即時放出のある患者を長期放出のEQUETROカプセルに変換する場合、カルバマゼピンの同じ1日総量をmgで投与する必要があります。. EQUETROに切り替えた後、患者は発作の制御について注意深く監視する必要があります。. 変換後の治療反応に応じて、推奨される投与量の指示内で1日の総投与量を調整する必要がある場合があります。.
EQUETROを設定します。
適応症ごとにEQUETROの服用を中止した場合は、徐々に用量を減らし、突然の中止を避けて発作のリスクを減らしてください。.
血清中のカルバマゼピン濃度を監視します。
血清中のカルバマゼピン濃度のモニタリングは、特にEQUETRO代謝の変化が発生する可能性のある臨床条件(例:. 薬物相互作用)。. てんかんのためにEQUETROで治療された小児患者で満足のいく臨床反応が得られなかった場合は、血漿レベルを測定して、治療範囲内かどうかを判断します。.
投与方法。
EQUETROカプセルを丸ごとまたは開けて、小さじ1杯のアップルソースのように真 ⁇ を食品に振りかけます。. EQUETROカプセルやカプセル内の真 ⁇ を粉砕したり噛んだりしないでください。. EQUETROは食事の有無にかかわらず服用できます。.
提供方法。
医薬品の形態と強み。
経口投与用の徐放性を持つEQUETRO(カルバマゼピン)カプセルは、3つの用量強度で提供されます。
- 100 mg。 -2部構成のハードゼラチンカプセルイエロー不透明キャップ。片側にSPD417、反対側にSPD417と100 mgを白インクで印刷した青緑の不透明ボディ。
- 200 mg。 -2部構成のハードゼラチンカプセルイエロー不透明キャップ。片側にSPD417、反対側にSPD417と200 mgが白インクで印刷された青の不透明なボディ。.
- 300 mg。 -2部構成のハードゼラチンカプセルイエロー不透明キャップ。片側にSPD417、反対側にSPD417と300 mgを白インクで印刷した青いボディ。.
保管と取り扱い。
EQUETRO(カルバマゼピン)徐放カプセルは、3つの投与強度で供給されます。
25°C(77°F)で買い物をします。 15〜30°C(59〜86°F)までの遠足。.
光と湿気から保護してください。
データセンター向けに作成されたValidusは、Pharmaceuticals LLC、119 Cherry Hill Road、Suite 310、Parsippany、NJ 07054を買収しました。. 改訂:2016年9月。
副作用と薬物相互作用。副作用。
マックス。
臨床試験は非常に異なる条件下で行われるため、ある薬物の臨床試験で観察された副作用率は、別の薬物の臨床試験の率と直接比較することはできず、臨床診療で観察された率を反映しない場合があります。.
双極性I障害(研究1および2)に関連する急性 ⁇ 病の患者を対象としたプールされた3週間のプラセボ対照試験で最も一般的に報告された副作用(EQUETROグループで5%以上、プラセボで少なくとも2倍)は、めまい、傾眠でした、吐き気、 ⁇ 吐、運動失調、便秘、かゆみ、口渇。. 使用されたEQUETROの用量は、1日あたり400〜1600 mgでした。.
表2。. 双極性障害に関する研究1および2で報告された一般的な副作用(発生率> 2%、プラセボより多い)。
ポストマーケティングの経験。
承認後にEQUETROを使用すると、次の副作用が確認されています。. これらの反応は不確実なサイズの集団から自発的に報告されるため、頻度を確実に推定したり、薬物曝露との因果関係を確立したりすることは常に可能ではありません。.
神経系:。 混乱、複視、眼球運動障害、眼振、言語障害、異常な不随意運動、耳鳴り。.
消化器系 :。 胃の不快感、腹痛、下 ⁇ 、食欲不振。.
臨床検査:。 甲状腺機能検査(T3、T4)-値の低下。
その他:。 エリテマトーデス様症候群。
カルバマゼピンを他の薬と組み合わせて服用している患者で、ミオクローヌスと末 ⁇ 好酸球増加症を伴う無菌性髄膜炎の症例が報告されています。. 患者は首を ⁇ られ、髄膜炎が再びカルバマゼピンで治療されたときに再び現れました。.
カルバマゼピンに関連する追加の副作用。
以下は、他の形態のカルバマゼピンに関する臨床試験または市販後報告で特定され、上記のEQUETROで報告されていない追加の副作用のリストです。. これらの反応は不確実なサイズの集団から自発的に報告されたため、頻度を確実に推定したり、薬物曝露との因果関係を確立したりすることは常に可能ではありません。.
神経系:。 悪性神経遮断薬の分離された症例は、他の向精神薬の同時使用の有無にかかわらず、カルバマゼピンの使用で報告されています。.
皮膚:。 オニコマデス、急性一般化発疹性 ⁇ (AGEP)。.
移動したバイワーキングを報告するには、Validus Pharmaceuticals LLC(1-8669VALIDUS(1-866-982-5438))またはFDA(1-800-FDA-1088またはwww.fda.gov/medwatch)に連絡してください。
医薬品との相互作用。
EQUETROに対する他の薬の薬物動態効果。
シトクロムP450 3A4(CYP3A4)を阻害する薬。
EQUETROは主にCYP3A4によって活性カルバマゼピン-10,11エポキシドに代謝され、エポキシヒドロラーゼによってトランスジオールにさらに代謝されます。. CYP 3A4および/またはエポキシヒドロラーゼの阻害剤は、EQUETROおよびその活性代謝物の血漿レベルを増加させ、EQUETROの血漿濃度を増加させ、副作用のリスクを高める可能性があります。. CYP3A4および/またはエポキシヒドロラーゼ阻害剤と併用する場合、EQUETROの用量を減らす必要があるかもしれません。. 以下の薬はCYP3A4阻害剤です。
アセタゾラミド、アプレピタント、アゾール系抗真菌薬(例:. ケトコナゾール、イトラコナゾール、フルコナゾール、ボリコナゾール、、。 シメチジン、シプロフロキサシン、クラリスロマイシン、ダルフォプリスチン、ダナゾール、ダントロレン、デラビルジン、ジルチアゼム、エリスロマイシン、 フルオキセチン、フルボキサミン、グレープフルーツジュース、イブプロフェン、イソニアジド、ロラタジン、ネファゾドン、ナイアシンアミド、ニコチンアミド、 オランザピン、オメプラゾール、オキシブチニン、キニーネ、チヌプリスチン、チクロピジン、トロレアンドマイシン、バルプロ酸、ベラパミル、 ジリュートン。.
医薬品、エポキシヒドロラーゼおよびCYP3A4阻害剤。
クラリスロマイシン、エリスロマイシン、ロキサピン、クエチアピン、バルプロ酸もエポキシヒドロラーゼを阻害し、活性代謝物カルバマゼピン-10,11エポキシドの反射を増加させます。.
CYP3A4を誘発する薬。
CYP3A4インデューサーは、EQUETRO血清濃度を下げ、その有効性を低下させることができます。. CYP3A4インデューサーと一緒に使用する場合、EQUETROの用量を増やす必要がある場合があります。. そのような薬は次のとおりです。
アミノフィリン、シスプラチン、ドキソルビシン、フェルバメート、ホスヘニトイン、メトキシミド、フェノバルビタール、フェニトイン、プリミドン、リファンピン、テオフィリン。.
EQUETROが他の薬に及ぼす薬物動態効果。
EQUETROは、肝臓3A4の強力な誘導剤であり、CYP1A2、2B6、2C9 / 19の誘導剤としても知られているため、主にCYP 1A2、2B6、2C9 / 19によって代謝される併用療法の血漿濃度を低下させることができます。代謝の誘導による3A4。. EQUETROと同時に使用する場合は、これらの薬剤の濃度の監視または用量の調整が必要になる場合があります。.
EQUETRO代謝を誘発することにより、以下の薬物の濃度を減らします。
経口避妊薬(CYP3A4基質)。
EQUETROはCYP3A4の強力な誘導剤です。. EQUETROは、特定の経口避妊薬(CYP3A4誘導による)の代謝を増加させる可能性があり、これにより濃度が大幅に低下します。. これは避妊の失敗または画期的な出血につながる可能性があります。. CYP3A4の誘導によって著しく影響を受ける経口避妊薬の代替案を検討するか、EQUETROの代替案を検討してください。
デラビルジンおよび他の非ヌクレオシド系逆転写酵素阻害剤(CYP3A4基質)。
CYP3A4を誘導することにより、EQUETROはデラビルジンと特定の非ヌクレオシド系逆転写酵素阻害剤の代謝を高め、これらの薬物の血漿濃度を大幅に低減します。. これは、不十分な抗ウイルス活性、ウイルス学的反応の喪失、およびデラビルジンまたは他の非ヌクレオシド系逆転写酵素阻害剤に対する耐性の可能性につながる可能性があります。. したがって、EQUETROの使用は、これらの非ヌクレオシド系逆転写酵素阻害剤では禁 ⁇ です。
ネファゾドン(CYP3A4基質)。
ネファゾドンの治療効果を達成するためにネファゾドンとその活性代謝物の血漿濃度が不十分になる可能性があるため、ネファゾドンを使用する場合、EQUETROの使用は禁 ⁇ です。.
ワルファリン(CYP1A2およびCYP3A4基質)。
CYP1A2とCYP3A4を誘導することにより、EQUETROはワルファリンの濃度を低下させ、抗凝固効果を低下させます。.
アリピプラゾール。
カルバマゼピンをアリピプラゾールに追加する場合は、アリピプラゾールの用量を2倍にする必要があります。. 追加の線量増加は、臨床評価に基づくべきです。. カルバマゼピンが後で中止される場合は、アリピプラゾールの用量を減らす必要があります。.
タクロリムス。
カルバマゼピンをタクロリムスと一緒に使用する場合は、タクロリムスの血中濃度のモニタリングと適切な用量調整が推奨されます。.
テムシロリムス。
カルバマゼピンなどの強力なCYP3A4誘導剤の使用は、テムシロリムスでは避ける必要があります。. 患者がテムシロリムスと一緒にカルバマゼピンを投与する必要がある場合は、テミロリムス投与量の調整を検討する必要があります。.
ラパチニブ。
ラパチニブによるカルバマゼピンの使用は、一般的に避けられるべきです。. すでにラパチニブを服用している患者でカルバマゼピンが開始された場合、ラパチニブの用量は徐々に滴定されるべきです。. カルバマゼピンが中止された場合、ラパチニブの用量を減らす必要があります。.
HIVプロテアーゼ阻害剤。
カルバマゼピンによるCYP3A4の強力な誘導のため、HIVプロテアーゼ阻害剤によるEQUETROの使用は推奨されません。.
その他のcyp1a2およびCYP3A4基質。
EQUETROはCYP1A2とCYP3A4を誘導し、CYP3A4またはCYP1A2によって代謝される医薬品の濃度を低下させます。. EQUETROと同時に使用する場合は、そのような薬の用量を増やす必要がある場合があります。. CYP3A4またはCYP1A2によって代謝される医薬品には、以下が含まれます。
アセトアミノフェン、アルベンダゾール、アルプラゾラム、アプレピタント、ブプレノルフォン、ブプロピオン、バスピロン、シタロプラム、クロバザム、クロナゼパム、クロザピン、シクロスポリン、デラビルジン、デシプラミン、ジアゼパム、ジクマロール、ジヒドロピリジンカルシウムチャネルブロッカー(。.、フェロジピン)、ドキシサイクリン、エトスクシミド、エベロリムス、フェルバメート、グルココルチコイド、ハロペリドール、イマチニブ、イトラコナゾール、ラモトリギン、レボチロキシン、ロラゼパム、メタドン、メトスカミド、ミアンセリン、ミダゾラム、ミルタザピン。. イミプラミン、アミトリプチリン、ノルトリプチリン)、トラゾドン、バルプロ酸、ワルファリン、ジプラシドン、ゾニサミド。.
EQUETRO代謝を阻害することにより、以下の薬物の血漿中濃度を上昇させます。
クロミプラミン、フェニトイン、プリミドン。
EQUETROは、クロミプラミン、フェニトイン、プリミドンの濃度を上昇させることができます。. 患者がこのカテゴリーのこれらの薬剤の1つで安定した用量に滴定され、その後EQUETROによる治療が開始された場合、これらの薬の用量を減らす必要があるかもしれません。.
フェニトイン。
フェニトインレベルは、カルバマゼピンの存在下で増加または減少すると報告されています。. EQUETROで使用すると、フェニトインレベルを変更するための薬物動態メカニズムがいくつかあります。 EQUETROを同時に使用する場合は、フェニトイン血清レベルを注意深く監視してください。.
シクロホスファミド。
シクロホスファミドは不活性なプロドラッグであり、CYP3Aによって部分的にその活性代謝物に変換されます。シクロホスファミドの代謝率と白血球形成活性は、CYP3A4インデューサーの慢性同時投与によって増加すると報告されています。. カルバマゼピンと同時投与すると、シクロホスファミド毒性が増加する可能性があります。.
薬物との薬力学的相互作用。
モノアミンオキシダーゼ阻害剤。
EQUETROとの併用治療は、MAOIの使用中、またはMAOIの停止後14日以内に禁 ⁇ です。併用するとセロトニン症候群を引き起こす可能性があります。.
リチウム。
EQUETROとリチウムの同時投与は、神経毒性の副作用のリスクを高める可能性があります。. これらの薬を同時に服用している場合は、リチウムまたはEQUETROの用量を減らすことを検討してください。.
イソニアジド。
カルバマゼピンとイソニアジドの併用は、イソニアジド誘発肝毒性を増加させると報告されています。.
CNS抑制剤。
EQUETROと他のCNS抑制剤の同時投与は、呼吸抑制、深い鎮静、低血圧および失神のリスクを高める可能性があります。. CNS抑制剤には、アルコール、オピオイド鎮痛薬、ベンゾジアゼピン、三環系抗うつ薬、鎮静剤/催眠薬、抗けいれん薬、抗精神病薬、抗ヒスタミン薬、抗コリン薬、アルファおよびベータ遮断薬、全身麻酔薬、筋 ⁇ 緩薬、違法なCNS抑制剤が含まれます。. 同時にこれらの薬を服用している場合は、CNS抑制剤またはEQUETROの用量を減らすことを検討してください。.
クロロキンとメフロキン。
マラリアメディッククロロキンとメフロキンは、EQUETROの活性に ⁇ 抗できます。
神経筋遮断薬。
非脱分極性神経筋遮断薬パンクロニウム、ベクロニウム、ロクロニウム、シサトラクリウムの神経筋遮断効果に対する耐性は、慢性カルバマゼピンを投与された患者で発生しました。. カルバマゼピンが他の非脱分極剤に同じ効果をもたらすかどうかは不明です。. 患者は神経筋遮断から予想よりも早く回復するように注意深く監視する必要があり、注入率の要件が高くなる可能性があります。.
| 副作用。 | エケトロ。® (N = 251)。 |
プラセボ。 (N = 248)。 |
| めまい。 | 44%。 | 12%。 |
| 眠気。 | 32%。 | 13%。 |
| 吐き気。 | 29%。 | 10%。 |
| ⁇ 吐。 | 18%。 | 3% |
| 不規則。 | 15%。 | 0.4%。 |
| 便秘。 | 10%。 | 5% |
| かゆみ。 | 8% | 2% |
| 口渇。 | 8% | 3% |
| 弱点。 | 8% | 4% |
| 発疹。 | 7% | 4% |
| ぼやけています。 | 6% | 2% |
| 言語障害。 | 6% | 0.4%。 |
| 高血圧。 | 3% | 0.4%。 |
| 感覚異常。 | 2% | 1% |
| 異常だと思います。 | 2% | 0.4%。 |
| 振戦。 | 3% | 1% |
| けいれんする。 | 2% | 1% |
| めまい。 | 2% | 1% |

妊娠カテゴリーD
リスクの概要。
EQUETROは、妊娠中の女性に投与すると胎児の損傷を引き起こす可能性があります。. 疫学データは、妊娠中のカルバマゼピンの使用と二分脊椎を含む先天性奇形との間にリンクがあるかもしれないことを示唆しています。. カルバマゼピンを用いた動物生殖試験で有害な発達効果が観察されています。. この薬が妊娠中に使用された場合、または患者が薬を服用している間に妊娠した場合、患者は胎児への潜在的なリスクについて通知されるべきです。.
妊娠登録。
患者は、妊娠したときに北米の抗てんかん規制登録(NAAED)に登録するように奨励されるべきです。. このレジスターは、妊娠中の抗てんかん薬の安全性に関する情報を収集します。. 登録するには、患者はフリーダイヤル1888-233-2334に電話できます。. 北米医薬品妊娠登録に関する情報は、http://www.aedpregnancyregistry.org/にあります。.
臨床上の考慮事項。
妊娠中の女性をEQUETROで治療するときは、治療の潜在的なリスクと利点の両方を注意深く検討し、適切にアドバイスしてください。. 現在認識されている手順に従って深刻な先天性奇形を検出するテストは、カルバマゼピンを投与されている妊婦の定期的な出生前ケアの一部と見なされるべきです。.
人間のデータ。
疫学データは、妊娠中のカルバマゼピンの使用と二分脊椎を含む先天性奇形との間にリンクがあるかもしれないことを示唆しています。. 遡及的症例評価は、単剤療法と比較して、併用療法での抗けいれん薬の使用に関連して催奇形性効果のより高い有病率が発生する可能性があることを示唆しています。.
カルバマゼピンの経胎盤通過は速く(30〜60分)、薬物は胎児組織に蓄積され、脳や肺よりも肝臓と腎臓のレベルが高くなります。.
母体カルバマゼピンおよびその他の抗けいれん薬の使用に関連する新生児発作および/または呼吸抑制のいくつかのケースがありました。. 母親でのカルバマゼピンの使用により、新生児の ⁇ 吐、下 ⁇ 、および/または摂食の減少のいくつかのケースも報告されています。. これらの症状は新生児離脱症候群である可能性があります。.
動物データ。
カルバマゼピンは、1200 mg / kgベースのヒト1日用量の10〜25倍、または1200 mg〜mg / mのヒト1日用量の1.5〜4倍の用量で経口投与した場合、ラットの生殖試験に悪影響を与えることが示されています。2ベース。. ラットの奇形研究では、250 mg / kgの135の子孫関節 ⁇ 骨のうち2つと119の子孫のうち4つが650 mg / kgで他の異常を示しました(ガム ⁇ 間、1;タリペス、1;無眼球増加、2)。.

マックス。
臨床試験は非常に異なる条件下で行われるため、ある薬物の臨床試験で観察された副作用率は、別の薬物の臨床試験の率と直接比較することはできず、臨床診療で観察された率を反映しない場合があります。.
双極性I障害(研究1および2)に関連する急性 ⁇ 病の患者を対象としたプールされた3週間のプラセボ対照試験で最も一般的に報告された副作用(EQUETROグループで5%以上、プラセボで少なくとも2倍)は、めまい、傾眠でした、吐き気、 ⁇ 吐、運動失調、便秘、かゆみ、口渇。. 使用されたEQUETROの用量は、1日あたり400〜1600 mgでした。.
表2。. 双極性障害に関する研究1および2で報告された一般的な副作用(発生率> 2%、プラセボより多い)。
ポストマーケティングの経験。
承認後にEQUETROを使用すると、次の副作用が確認されています。. これらの反応は不確実なサイズの集団から自発的に報告されるため、頻度を確実に推定したり、薬物曝露との因果関係を確立したりすることは常に可能ではありません。.
神経系:。 混乱、複視、眼球運動障害、眼振、言語障害、異常な不随意運動、耳鳴り。.
消化器系 :。 胃の不快感、腹痛、下 ⁇ 、食欲不振。.
臨床検査:。 甲状腺機能検査(T3、T4)-値の低下。
その他:。 エリテマトーデス様症候群。
カルバマゼピンを他の薬と組み合わせて服用している患者で、ミオクローヌスと末 ⁇ 好酸球増加症を伴う無菌性髄膜炎の症例が報告されています。. 患者は首を ⁇ られ、髄膜炎が再びカルバマゼピンで治療されたときに再び現れました。.
カルバマゼピンに関連する追加の副作用。
以下は、他の形態のカルバマゼピンに関する臨床試験または市販後報告で特定され、上記のEQUETROで報告されていない追加の副作用のリストです。. これらの反応は不確実なサイズの集団から自発的に報告されたため、頻度を確実に推定したり、薬物曝露との因果関係を確立したりすることは常に可能ではありません。.
神経系:。 悪性神経遮断薬の分離された症例は、他の向精神薬の同時使用の有無にかかわらず、カルバマゼピンの使用で報告されています。.
皮膚:。 オニコマデス、急性一般化発疹性 ⁇ (AGEP)。.
移動したバイワーキングを報告するには、Validus Pharmaceuticals LLC(1-8669VALIDUS(1-866-982-5438))またはFDA(1-800-FDA-1088またはwww.fda.gov/medwatch)に連絡してください。
| 副作用。 | エケトロ。® (N = 251)。 |
プラセボ。 (N = 248)。 |
| めまい。 | 44%。 | 12%。 |
| 眠気。 | 32%。 | 13%。 |
| 吐き気。 | 29%。 | 10%。 |
| ⁇ 吐。 | 18%。 | 3% |
| 不規則。 | 15%。 | 0.4%。 |
| 便秘。 | 10%。 | 5% |
| かゆみ。 | 8% | 2% |
| 口渇。 | 8% | 3% |
| 弱点。 | 8% | 4% |
| 発疹。 | 7% | 4% |
| ぼやけています。 | 6% | 2% |
| 言語障害。 | 6% | 0.4%。 |
| 高血圧。 | 3% | 0.4%。 |
| 感覚異常。 | 2% | 1% |
| 異常だと思います。 | 2% | 0.4%。 |
| 振戦。 | 3% | 1% |
| けいれんする。 | 2% | 1% |
| めまい。 | 2% | 1% |

人間の経験。
カルバマゼピンの既知の最低致死量:成人、60グラム以上(39歳の男性)。. 最も高い既知の線量は生き残った:大人、30グラム(31歳の女性);子供、10グラム(6歳の男の子);小さな子供、5グラム(3歳の女の子)。.
兆候と症状。
カルバマゼピンの過剰摂取の最初の兆候と症状は、1〜3時間後に現れます。. 神経筋障害が最も顕著です。. 心血管疾患は一般に穏やかで、重度の心臓合併症は非常に高用量(60グラム以上)が服用された場合にのみ発生します。.
呼吸。
不規則な呼吸、呼吸抑制。.
心血管系。
頻脈、低血圧または高血圧、ショック、伝導障害。.
神経系と筋肉。
深い ⁇ 睡までの意識の難しさ。. けいれん、特に幼児。. 運動不安、筋肉のけいれん、振戦、アテトイド運動、オピストノス、運動失調、眠気、めまい、散 ⁇ 、眼振、筋ドキネジア、バリズム、精神運動障害、対称性。. 最初の高反射症とそれに続く低反射症。.
消化管。
吐き気、 ⁇ 吐。.
腎臓と ⁇ 。
尿症または乏尿、尿閉。.
実験室の結果。
過剰摂取の孤立した症例には、白血球増加症、白血球数の減少、糖尿およびアセトン尿症が含まれます。. EKGは不整脈を示すことができます。.
複合中毒。
アルコール、三環系抗うつ薬、バルビツール酸塩またはヒダントインを同時に服用すると、急性カルバマゼピン中毒の兆候と症状が悪化または変化する可能性があります。.
過剰摂取の管理。
EQUETROの過剰摂取の管理に関する最新情報については、お住まいの地域の認定毒物センター(1-800-222-1222)(またはwww.poison.org)にお問い合わせください。. 過剰摂取の場合、綿密な医療モニタリングとモニタリングを含む支援的ケア。. 治療は、薬物による過剰摂取の治療に使用される一般的な対策で構成する必要があります。. 複数の薬を過剰摂取する可能性を検討してください。. 適切な気道、酸素供給、換気を確保します。. 心臓のリズムと重要な機能を監視します。. 支持的で症状のある対策を使用してください。.

カルバマゼピン(CBZ)。
吸収。
カルバマゼピンの長期放出を伴う200 mgの単回経口投与後、血漿濃度は1.9±0.3 mcg / mLであり、ピークに達するまでの時間は19±7時間でした。. 投与量を繰り返し投与した後(12時間ごとに800 mg)、ピーク値は11.0±2.5 mcg / mLで、ピークに達するまでの時間は5.9±1.8時間でした。. 徐放性によるカルバマゼピンの薬物動態は、200〜800 mgの単回投与範囲にわたって直線的です。.
カルバマゼピンの76%は血漿タンパク質に結合しています。. カルバマゼピンは主に肝臓で代謝されます。. チトクロームP450 3A4は、カルバマゼピン-10,11エポキシドの形成に関与する主要なアイソフォームとして識別されています。. カルバマゼピンは独自の代謝を誘発するため、半減期もさまざまです。. 平均半減期は、長期放出を伴うカルバマゼピンの単回投与後35〜40時間、反復投与後12〜17時間の範囲でした。. 見かけの経口クリアランスは、単回投与後25±5 mL /分、複数回投与で80±30 mL /分でした。.
カルバマゼピン-10,11-エポキシド(CBZ-E)。
カルバマゼピン-10,11-エポキシドはカルバマゼピンの活性代謝物と見なされます。. 摂取のためのカルバマゼピンの200 mgの長期放出用量の1回後、カルバマゼピン-10,11-エポキシド0.11±0.012 mcg / mLの最大血漿濃度は36±6時間でした。. カルバマゼピン(12時間ごとに800 mg)の長期放出を伴う用量の慢性投与後、カルバマゼピン-10,11-エポキシドのピーク値は2.2±0.9 mcg / mLであり、ピークに達するまでの時間は14±8でした。時間。. カルバマゼピンの投与後のカルバマゼピン-10,11エポキシドの血漿半減期は34±です。 9時間。. 長期放出(200-800 mg)を伴うカルバマゼピンの単回経口投与後、カルバマゼピン-10.11エポキシドのAUCおよびCmaxは、カルバマゼピンの10%未満でした。. 徐放性でカルバマゼピンを複数回投与した後。 (14日間毎日800〜1600 mg。) カルバマゼピン-10,11エポキシドのAUCとCmaxは用量依存的でした。, 15.7 mcg.hr / mLおよび1.5 mcg / mLの範囲で、800 mg /日で最大32.6 mcg.hr / mLおよび3.2 mcg / mLで1600 mg /日で30%未満のカルバマゼピン。. カルバマゼピン-10,11-エポキシドは血漿タンパク質に50%結合しています。.
食物効果。
高脂肪食は、400 mg単回投与の吸収率を高めました(平均Tmaxは空腹時の24時間から14時間に減少し、Cmaxは3.2から4.3 mcg / mLに増加しました)が、その範囲(AUC)は増加しませんでした吸収の。. 排 ⁇ 半減期は、摂食状態と高速状態の間で変化しませんでした。. 摂食状態で実施された複数回投与試験では、定常状態のCMAX値が治療濃度範囲内にあることが示されました。. 長期放出を伴うカルバマゼピンの薬物動態プロファイルは、地味な状態で投与された無傷のカプセルと比較して、リンゴソースに真 ⁇ を振りかけることによって投与された場合と同様でした。.
除去。
の経口投与後。 14C-カルバマゼピンは、尿中に投与された放射能の72%、 ⁇ 便中に28%を発見しました。. 尿中のこの放射能は、主にヒドロキシル化および抱合代謝物で構成され、カルバマゼピンは3%しか変化していません。
代謝。
in vitro。 データは、カルバマゼピンが主にチトクロームP450(CYP)3A4によって代謝されて、活性カルバマゼピン-10,11-エポキシドになり、エポキシヒドロラーゼによってトランスジオールにさらに代謝されることを示しています。. ヒトミクロソームエポキシヒドロラーゼは、カルバマゼピン-10.11エポキシドからの10.11トランスジオール誘導体の形成に関与する酵素として識別されています。.
腎障害。
カルバマゼピンの薬物動態に対する腎障害の影響は不明です。.
肝障害。
カルバマゼピンの薬物動態に対する肝機能障害の影響は不明です。. 肝障害のある患者の投与量を減らすことを検討してください。.
年齢の影響。
カルバマゼピンは、大人よりも小さな子供で速くカルバマゼピン-10,11-エポキシドに代謝されます。. 15歳未満の子供は、CBZ-E / CBZ比と年齢の増加との間に逆の関係があります。. EQUETROの安全性と有効性。® 小児および青年期の患者では証拠は見つかりませんでした。.
ジェンダー効果。
男性と女性の間のカルバマゼピンとカルバマゼピン-10,11エポキシドの平均AUCとCmaxに違いは見られませんでした。.

However, we will provide data for each active ingredient


