









Componentes:
Método de ação:
Opção de tratamento:
Medicamente revisado por Fedorchenko Olga Valeryevna, Farmácia Última atualização em 27.03.2022

Atenção! As informações na página são apenas para profissionais de saúde! As informações são coletadas em fontes abertas e podem conter erros significativos! Tenha cuidado e verifique novamente todas as informações desta página!


Formas e forças farmacêuticas
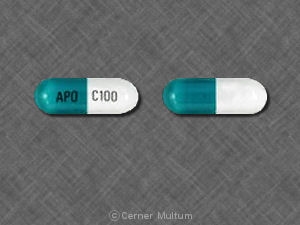
As cápsulas de EQUETRO (carbamazepina) com liberação prolongada para administração oral são fornecidas em três doses:
- 100 mg - Tampa opaca amarela da cápsula de gelatina dura em duas partes com corpo opaco verde azulado impresso com SPD417 em uma extremidade e SPD417 e 100 mg no outro lado em tinta branca
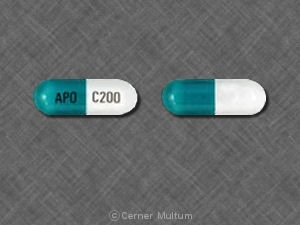
- 200 mg - Tampa opaca amarela da cápsula de gelatina dura em duas partes com corpo opaco azul impresso com SPD417 em uma extremidade e SPD417 e 200 mg no outro lado em tinta branca.
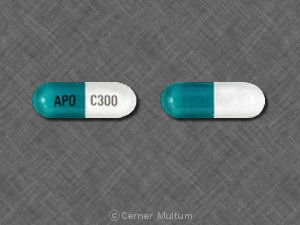
- 300 mg - Tampa opaca amarela da cápsula de gelatina dura em duas partes com corpo azul impresso com SPD417 em uma extremidade e SPD417 e 300 mg no outro lado em tinta branca.
Armazenamento e manuseio
As cápsulas de liberação prolongada de EQUETRO (carbamazepina) são fornecidas em três doses
Compre a 25 ° C (77 ° F); Excursões de até 15 a 30 ° C (59 a 86 ° F).
Proteger da luz e umidade
Feito para data centers, a Validus adquiriu a Pharmaceuticals LLC, 119 Cherry Hill Road, Suite 310, Parsippany, NJ 07054. Revisado: setembro de 2016

Episódios maníacos ou mistos agudos relacionados a um distúrbio bipolar I
EQUETRO está indicado no tratamento de pacientes com episódios maníacos ou mistos agudos em conexão com um distúrbio bipolar I.
Dor A neuralgia trigêmea
EQUETRO está indicado no tratamento da dor associada à neuralgia do trigêmeo. Resultados positivos também foram relatados na neuralgia glossofaríngea. Este medicamento não é um analgésico simples e não deve ser usado para aliviar dores ou dores triviais.
Epilepsia
EQUETRO é indicado para o tratamento de convulsões parciais com sintomas complexos (por exemplo,. psicomotor, lobo temporal), convulsões tônico-clônicas generalizadas (grand mal) e padrões de convulsões mistas, que incluem os tipos de convulsões listadas aqui ou outras convulsões parciais ou generalizadas..
Restrições de uso
EQUETRO não está indicado no tratamento de convulsões sem ausência (petit mal). A carbamazepina tem sido associada a um aumento da frequência de cãibras generalizadas nesses pacientes.

Triagem pré-tratamento
Antes de iniciar o tratamento com EQUETRO, teste pacientes com ancestrais em populações geneticamente ameaçadas de extinção quanto à presença do alelo HLA-B * 1502. O teste de genótipo de alta resolução é positivo se um ou dois alelos HLA-B * 1502 estiverem presentes. Evite usar EQUETRO em pacientes que apresentaram resultado positivo para alelo, a menos que o benefício supere claramente o risco.
O pré-tratamento completo das contagens sanguíneas, incluindo plaquetas e possivelmente reticulócitos e ferro sérico, deve ser obtido como linha de base. Se um paciente tiver contagem baixa ou diminuída de glóbulos brancos ou plaquetas durante o tratamento, ele deve ser monitorado de perto. A descontinuação de EQUETRO deve ser considerada se houver sinais de depressão significativa da medula óssea.
Durante o tratamento com EQUETRO, devem ser realizados exames básicos e regulares da função hepática, especialmente em pacientes com histórico de doenças hepáticas, uma vez que podem ocorrer danos no fígado. Pare EQUETRO se tiver disfunção hepática grave ou doença hepática ativa.
Exames oculares básicos e regulares, incluindo lâmpada de fenda, cópia de fundo e tonometria, são recomendados, pois foi demonstrado que muitas fenotiazinas e medicamentos relacionados causam alterações oculares.
A análise completa da linha de base e periódica da urina e as determinações do BUN são recomendadas para pacientes tratados com este produto devido a uma insuficiência renal observada.
Dosagem para episódios maníacos ou mistos agudos relacionados a um distúrbio bipolar I
A dose inicial recomendada de EQUETRO é de 200 mg duas vezes ao dia. A dose pode ser aumentada em 200 mg por dia para obter uma resposta clínica ideal. Doses de mais de 1600 mg por dia não foram estudadas na mania relacionada ao transtorno bipolar.
Dosagem Para dor A neuralgia trigêmea
Inicial: comece com uma cápsula de 200 mg uma vez ao dia no primeiro dia. Esta dose só pode ser aumentada em até 200 mg / dia em etapas de 100 mg a cada 12 horas, a fim de obter uma dose eficaz e tolerável. Não exceda uma dose diária total de 1200 mg.
Manutenção: O controle da dor pode ser mantido na maioria dos pacientes com 400 mg a 800 mg por dia. No entanto, alguns pacientes podem tomar apenas 200 mg por dia, enquanto outros precisam de até 1200 mg por dia. Pelo menos a cada 3 meses durante o período de tratamento, deve-se tentar reduzir a dose para o nível efetivo mínimo ou até mesmo parar o medicamento.
Dosagem Para epilepsia
Adultos e crianças com mais de 12 anos
A dose inicial recomendada é de 200 mg duas vezes ao dia. Aumento em incrementos semanais de 200 mg por dia, administrados como uma dose uniformemente distribuída, duas vezes ao dia, até que a resposta ideal seja alcançada. A dosagem geralmente não deve exceder 500 mg duas vezes ao dia em crianças de 12 a 15 anos. 600 mg duas vezes ao dia em crianças de 15 a 18 anos; e 800 mg duas vezes ao dia em adultos.
Crianças menores de 12 anos
A resposta clínica ideal é geralmente alcançada em doses diárias abaixo de 35 mg / kg. Nenhuma recomendação sobre a segurança do EQUETRO em doses acima de 35 mg / kg / 24 horas pode ser dada.
Co-administração com outros DEAs
O EQUETRO pode ser usado sozinho ou com outros DEAs. Quando adicionado aos DEAs existentes, adicione gradualmente EQUETRO, mantendo ou reduzindo gradualmente a (s) dose (s) de outros DEAs. Interações medicamentosas em potencial devem ser consideradas ao usar carbamazepina com outros DEAs.
Mude da carbamazepina com liberação imediata para EQUETRO
EQUETRO é uma formulação com liberação prolongada para administração duas vezes ao dia. Ao converter pacientes com liberação imediata de carbamazepina em cápsulas de EQUETRO com liberação prolongada, a mesma dose diária total de carbamazepina deve ser administrada em mg. Após mudar para EQUETRO, os pacientes devem ser monitorados de perto quanto ao controle de crises. Dependendo da resposta terapêutica após a conversão, a dose diária total pode precisar ser ajustada dentro das instruções de dosagem recomendadas.
Configurando EQUETRO
Se parar de tomar EQUETRO para cada indicação, reduza gradualmente a dose e evite a descontinuação abrupta para reduzir o risco de convulsões.
Monitorando a concentração de carbamazepina no soro
O monitoramento das concentrações de carbamazepina no soro pode ser útil para a seleção da dose, minimizando a toxicidade e verificando a conformidade com o medicamento, especialmente em condições clínicas em que podem ocorrer alterações no metabolismo do EQUETRO (por exemplo,. interações medicamentosas). Se não for alcançada uma resposta clínica satisfatória em pacientes pediátricos tratados com EQUETRO para epilepsia, meça os níveis plasmáticos para determinar se você está ou não na faixa terapêutica.
Instruções para administração
Engula as cápsulas EQUETRO inteiras ou abertas e polvilhe as pérolas sobre os alimentos como uma colher de chá de molho de maçã. Não esmague ou mastigue cápsulas EQUETRO ou pérolas na cápsula. EQUETRO pode ser tomado com ou sem refeições.

- depressão da medula óssea.
- Hipersensibilidade conhecida à carbamazepina, como anafilaxia ou reação de hipersensibilidade grave.
- Hipersensibilidade conhecida a um dos compostos tricíclicos (por exemplo,., Amitriptilina, Desipramina, Imipramina, protriptilina e nortriptilina. As reações de hipersensibilidade incluem anafilaxia e erupção cutânea grave.
- Uso simultâneo de delavirdina ou outros inibidores da transcriptase reversa não nucleósidos que são substratos para o CYP3A4. O EQUETRO pode reduzir significativamente as concentrações desses medicamentos induzindo o CYP3A4. Isso pode levar à perda de resposta virológica e possível resistência a esses medicamentos.
- Uso simultâneo de inibidores da monoamina oxidase (MAOIs). Antes de iniciar o tratamento com EQUETRO, as MAOIs devem ser descontinuadas por pelo menos 14 dias. O uso simultâneo pode causar síndrome da serotonina.
- Uso simultâneo de nefazodona. Isso pode levar a concentrações plasmáticas insuficientes de nefazodona e seu metabólito ativo, a fim de obter um efeito terapêutico.

AVISO
Contido como parte do "PRECAUÇÕES" Seção
PRECAUÇÕES
Reações dermatológicas graves
Reações dermatológicas graves e às vezes fatais, incluindo necrólise epidérmica tóxica (RTE) e síndrome de Stevens-Johnson (SJS), foram relatadas com o tratamento com carbamazepina. Essas síndromes podem ser acompanhadas por úlceras mucosas, febre ou erupção cutânea dolorosa. Mais de 90% dos pacientes tratados com carbamazepina que tiveram SJS / RTE desenvolveram essas reações nos primeiros meses de tratamento. Estima-se que o risco dessas reações seja de cerca de 1 a 6 por 10.000 novos usuários em países com uma população principalmente caucasiana. Em alguns países asiáticos, no entanto, estima-se que o risco seja cerca de dez vezes. Pare o EQUETRO se suspeitar que o paciente com DER tem uma resposta dermatológica séria. Se sinais ou sintomas indicarem SJS / RTE, não retome o tratamento com EQUETRO
SJS, RTE e HLA-B * 1502 alelo
Estudos retrospectivos de controle de caso mostraram que em pacientes de descendência chinesa existe uma forte conexão entre o risco de desenvolver SJS / RTE com tratamento com EQUETRO e a presença do alelo HLA-B * 1502 (uma variante herdada do HLA-B- Gene) existe). Antes de iniciar a terapia com EQUETRO, é mais provável que realize esse teste de alelo para HLA-B * 1502 em pacientes. O teste de genótipo de alta resolução é positivo se um ou dois alelos HLA-B * 1502 estiverem presentes. Evite usar EQUETRO em pacientes positivos para o alelo HLA-B * 1502, a menos que supere claramente o risco de reações dermatológicas graves. Acredita-se que pacientes testados com alelo negativo tenham um baixo risco de SJS / RTE associado ao tratamento com carbamazepina.
A prevalência do alelo HLA-B * 1502 pode ser maior nas populações asiáticas: Hong Kong, Tailândia, Malásia e partes das Filipinas (mais de 15%); Taiwan (10%), norte da China (4%); Asiáticos do Sul, incluindo índios (2 a 4%); e Japão e Coréia (menos de 1%). O HLA-B * 1502 está em grande parte ausente de pessoas que não são de origem asiática (por exemplo,. Caucasianos, afro-americanos, hispânicos e indianos). A precisão das taxas estimadas do alelo HLAB * 1502 nessas populações pode ser limitada por uma grande variabilidade nas taxas dentro dos grupos étnicos, a dificuldade em determinar a origem étnica e a probabilidade de descida mista.
Não foi encontrado o alelo HLA-B * 1502 para prever o risco de reações adversas cutâneas menos graves da carbamazepina, como erupção maculopapular (EMP) ou para prever uma reação medicamentosa com eosinofilia e sintomas sistêmicos (DRESS).
Evidências limitadas sugerem que o HLA-B * 1502 pode ser um fator de risco para o desenvolvimento de SJS / RTE em pacientes nascidos na China que tomam outros antiepiléticos associados ao SJS / RTE, incluindo fenitoína. Evite usar outros medicamentos associados ao SJS / RTE em pacientes positivos com HLA-B * 1502 se terapias alternativas forem igualmente aceitáveis.
reações de hipersensibilidade e alelo HLA-A * 3101
Estudos retrospectivos de controle de caso em pacientes de descendência européia, coreana e japonesa têm uma relação moderada entre o risco de desenvolver reações de hipersensibilidade e a presença de HLA-A * 3101, uma variante all herdada do gene HLA-a, em pacientes com carbamazepina encontrado. Essas reações de hipersensibilidade incluem SJS / RTE, erupções maculopapulares e reações medicamentosas com eosinofilia e sintomas sistêmicos.
É esperado, que o HLA-A * 3101 está presente nas seguintes frequências: mais de 15% em pacientes japoneses, Indiano, Sul da Índia (Por exemplo, Tamil Nadu) e alguma descida árabe; até cerca de 10% em pacientes mais chineses, Coreano, Europeu, Descendência latino-americana e outras descendentes de indianos; e até cerca de 5% em pacientes afro-americanos e tailandeses, Descendência de Taiwan e chinesa (Hong Kong).
Os riscos e benefícios da terapia com EQUETRO devem ser ponderados antes de levar em consideração o EQUETRO em pacientes que são conhecidos por serem positivos para o HLA-A * 3101.
Hipersensibilidade e limitações da genotipagem do HLA
O uso da genotipagem do HLA como ferramenta de triagem tem limitações importantes e nunca deve substituir a vigilância clínica e o gerenciamento adequado do paciente. Muitos pacientes positivos para HLA-B * 1502 e HLA-A * 3101 - pacientes positivos tratados com EQUETRO não desenvolvem SJS / RTE ou outras reações de hipersensibilidade, e essas reações podem ser observadas em HLA-B * 1502 negativo e HLA-A * 3101 pacientes negativos de qualquer etnia ainda raramente ocorrem. O papel de outros fatores possíveis no desenvolvimento e morbidade de SJS / RTE e outras reações de hipersensibilidade, como dose de DEA, conformidade, medicamentos acompanhantes, comorbidade e grau de monitoramento dermatológico, não foi estudado.
Anemia aplástica e agranulocitose
Anemia aplástica e agranulocitose ocorreram em pacientes tratados com carbamazepina. Dados de um estudo de caso-controle de base populacional sugerem que o risco de desenvolver essas reações é 5-8 vezes maior do que na população em geral. No entanto, o risco geral dessas reações na população geral não tratada é baixo, cerca de seis pacientes por milhão de habitantes por ano para agranulocitose e dois pacientes por milhão de habitantes por ano para anemia aplástica.
Embora relatos de níveis plaquetários reduzidos temporários ou persistentes ou glóbulos brancos associados ao uso de carbamazepina não sejam incomuns, não há dados disponíveis para estimar com precisão sua incidência ou resultado. No entanto, a grande maioria dos casos de leucopenia não é avançada para condições mais graves de anemia aplástica ou agranulocitose.
Devido à incidência muito baixa de agranulocitose e anemia aplástica, é improvável que a grande maioria das pequenas alterações hematológicas observadas na vigilância de pacientes sob EQUETRO sinalize a ocorrência de anomalias. No entanto, o pré-tratamento completo dos testes hematológicos deve ser obtido como base. Se um paciente tiver hemácias ou plaquetas baixas ou diminuídas durante o tratamento, ele deve ser monitorado de perto. Considere parar o EQUETRO se houver sinais de depressão significativa da medula óssea. As características clínicas podem incluir febre, dispnéia durante o esforço, fadiga, hematomas leves, petéquias, epistaxe, gengivas hemorrágicas e menstruação grave.
Reação medicamentosa Com eosinofilia E sintomas sistêmicos / hipersensibilidade a múltiplos órgãos
Ocorreram reações medicamentosas com eosinofilia e sintomas sistêmicos (DRESS), também conhecidos como hipersensibilidade multiorgan, com a carbamazepina. Alguns desses eventos foram fatais ou com risco de vida. O VESTIDO geralmente ocorre, se não exclusivamente, em conjunto com febre, erupção cutânea, linfadenopatia e / ou inchaço facial em conjunto com o envolvimento de outros órgãos, como hepatite, nefrite, anormalidades hematológicas, miocardite ou miosite, que às vezes se assemelham a uma infecção viral aguda. A eosinofilia está frequentemente presente. Esse distúrbio é variável em sua expressão e outros sistemas orgânicos que não são mencionados aqui podem estar envolvidos. É importante observar que manifestações precoces de hipersensibilidade (por exemplo,.Febre, linfadenopatia), embora a erupção cutânea não seja óbvia. Se houver tais sinais ou sintomas, o paciente deve ser examinado imediatamente. O EQUETRO deve ser descontinuado se nenhuma etiologia alternativa para os sinais ou sintomas puder ser identificada.
Hipersensibilidade
Foram relatadas reações de hipersensibilidade à carbamazepina em pacientes que anteriormente tiveram essa reação a anticonvulsivantes, incluindo fenitoína, primidona e fenobarbital. Se esse histórico existir, o uso e o risco devem ser cuidadosamente considerados e, quando o EQUETRO for iniciado, os sinais e sintomas de hipersensibilidade devem ser cuidadosamente monitorados.
Pacientes que demonstraram reações de hipersensibilidade à carbamazepina podem experimentar aproximadamente 25 a 30% de reações de hipersensibilidade à oxcarbazepina.
Comportamento suicida e ideologia
Antiepiléticos (DEA), incluindo EQUETRO, aumentam o risco de pensamentos ou comportamentos em pacientes que tomam esses medicamentos para cada indicação. Os pacientes tratados com um DEA para indicações devem ser monitorados quanto à ocorrência ou agravamento da depressão, pensamentos de suicídio ou comportamento e / ou alterações incomuns de humor ou comportamento.
Análises combinadas de 199 estudos clínicos controlados por placebo (mono - e terapia adicional) com 11 DEAs diferentes mostrados, que pacientes randomizados com um dos DEAs estavam aproximadamente com o dobro do risco (risco relativo ajustado 1.8, IC 95%: 1,2, 2.7) de pensamento ou comportamento suicida em comparação com os pacientes, que foram randomizados para serem tratados com placebo. Nestes estudos com uma duração média de tratamento de 12 semanas, a taxa de incidência estimada de comportamento ou ideação suicida em 27.863 pacientes tratados com DEA foi de 0,43%, em comparação com 0,24% entre 16.029 pacientes tratados com placebo, o que corresponde a um aumento de aproximadamente um caso de pensamentos ou comportamentos suicidas para cada 530 pacientes tratados. Houve quatro suicídios em pacientes tratados com drogas nos estudos e nenhum em pacientes tratados com placebo, mas o número é muito pequeno para tirar conclusões sobre o efeito da droga no suicídio.
O risco aumentado de pensamentos ou comportamentos suicidas com DEAs foi observado uma semana após o início do tratamento medicamentoso com DEAs e permaneceu avaliado durante o tratamento. Como a maioria dos estudos incluídos na análise não ultrapassou as 24 semanas, o risco de pensamentos ou comportamentos suicidas não pôde ser avaliado além de 24 semanas.
O risco de pensamentos ou comportamento de suicídio era geralmente consistente nos dados analisados para drogas. Encontrar um risco aumentado em DEAs com diferentes mecanismos de ação e em várias indicações sugere que o risco se aplica a todos os DEAs usados para cada indicação. Nos estudos clínicos analisados, o risco não variou significativamente por idade (5 a 100 anos) . A Tabela 1 mostra o risco absoluto e relativo por indicação para todos os DEAs avaliados.
Tabela 1 Risco de pensamentos ou comportamentos (reações) em antiepiléticos após indicação na análise combinada
O risco relativo de pensamentos ou comportamentos suicidas foi maior em estudos clínicos com epilepsia do que em estudos clínicos com doenças psiquiátricas ou outras, mas as diferenças absolutas foram semelhantes em epilepsia e indicações psiquiátricas.
Qualquer pessoa que considere prescrever EQUETRO ou outro DEA deve reconciliar o risco de pensamentos ou comportamentos suicidas com o risco de uma doença não tratada. A epilepsia e muitas outras doenças para as quais os DEAs são prescritos estão associadas à morbimortalidade e a um risco aumentado de pensamentos e comportamento de suicídio. Se pensamentos e comportamento de suicídio ocorrerem durante o tratamento, o médico prescritor deve verificar se esses sintomas podem ocorrer em um paciente em particular com a doença a ser tratada.
Pacientes, Seus cuidadores e famílias devem ser informados, que os DEAs aumentam o risco de pensamentos e comportamentos de suicídio, e esteja ciente da necessidade, na ocorrência ou agravamento dos sinais e sintomas de depressão, mudanças incomuns de humor ou comportamento ou a ocorrência de pensamentos de suicídio, - Tornar comportamento ou pensamentos conscientes de auto-mutilação. Com relação aos comportamentos, devem ser relatados imediatamente aos profissionais de saúde.
toxicidade embrião-fetal
EQUETRO é um medicamento da categoria D .
EQUETRO pode causar danos fetais quando administrado a uma mulher grávida. Avalie as mulheres no potencial desse risco. Use durante a gravidez apenas se o uso potencial do tratamento exceder os riscos
Dados epidemiológicos sugerem que pode haver uma ligação entre o uso de carbamazepina durante a gravidez e malformações congênitas, incluindo espinha bífida. Se este medicamento for usado durante a gravidez ou se a paciente engravidar enquanto estiver tomando este medicamento, ela deve ser informada do risco potencial para o feto.
Avaliações retrospectivas de casos sugerem que, comparada à monoterapia, uma prevalência mais alta de efeitos teratogênicos pode ocorrer em conexão com o uso de anticonvulsivantes em terapia combinada.
Nos seres humanos, a passagem transplacentária da carbamazepina é rápida (30-60 minutos) e a droga é encontrada nos tecidos fetais, com níveis mais altos no fígado e nos rins do que no cérebro e nos pulmões.
Foi demonstrado que a carbamazepina tem efeitos adversos em estudos reprodutivos em ratos quando administrada por via oral em doses 10 a 25 vezes uma dose diária humana de 1200 mg / kg com base ou 1,5 a 4 vezes a dose diária humana de 1200 mg a mg / m2-base. Em estudos teratológicos em ratos, 2 das 135 costelas articuladas da prole a 250 mg / kg e 4 das 119 filhotes apresentaram outras anormalidades a 650 mg / kg (fenda da gengiva, 1; talipes, 1; anoftalmo, 2).
Os testes de detecção de defeitos de acordo com os procedimentos atualmente reconhecidos devem ser considerados parte do pré-natal de rotina para mulheres com potencial para engravidar que recebem EQUETRO
Fornecer informações adicionais sobre os efeitos da exposição no útero ao EQUETRO, os médicos são aconselhados a recomendar o registro no registro de gravidez do antiepilético norte-americano (NAAED) a doentes grávidas a tomar EQUETRO. Isso pode ser feito sob o número gratuito 1-888-233-2334 e deve ser realizado pelos próprios pacientes. Informações de registro também podem ser encontradas no site http://www.aedgravidezregistry.org/
Desmame abrupto e risco de convulsões
Não pare o EQUETRO abruptamente, pois há risco de convulsões e outros sintomas / sintomas de abstinência. Pacientes com distúrbios convulsivos têm um risco aumentado de desenvolver convulsões e status epilepticus com hipóxia concomitante e perigo para a vida. No caso de uma reação alérgica ou de hipersensibilidade, no entanto, pode ser necessária uma substituição mais rápida da terapia alternativa.
Hiponatremia
A hiponatremia pode ocorrer como resultado do tratamento com EQUETRO. Em muitos casos, a hiponatremia parece ser causada pela síndrome da secreção inadequada de hormônio antidiurético (SIADH)). O risco de desenvolver SIADH com tratamento com EQUETRO parece depender da dose. Pacientes idosos e pacientes tratados com diuréticos correm maior risco de desenvolver hiponatremia. Sinais e sintomas de hiponatremia incluem dor de cabeça, frequência de crises nova ou aumentada, dificuldade de concentração, problemas de memória, confusão, fraqueza e inquietação que podem levar a quedas. Considere parar o EQUETRO em pacientes com hiponatremia sintomática.
Potencial de comprometimento cognitivo e motor
O EQUETRO pode prejudicar o julgamento, a cognição e a função motora. Cuidado com os pacientes que operam máquinas perigosas, incluindo carros, até ter certeza razoável de que o EQUETRO não o afetará adversamente. Efeitos colaterais incluídos em estudos clínicos em transtorno bipolar (EQUETRO, N = 251 e placebo, N = 248): sonolência (32% vs. 13%), ataxia (15%). 0,4%), tontura (44%). 12%), tontura (2%). 1%), pense anormal (2% vs. 0,4%), tremor 3% vs. 1%) e veja desfocado (6% vs. 2%).
Potencial de perda de resposta virológica a inibidores da transcriptase reversa não nucleósidos que são substratos para o CYP3A4 Quando o EQUETRO é usado ao mesmo tempo
A administração concomitante de EQUETRO com inibidores da transcriptase reversa não nucleósidos, incluindo a delavirdina, é contra-indicada, pois isso pode levar à perda de resposta virológica e possível resistência. Ao induzir o CYP3A4, o EQUETRO pode reduzir significativamente as concentrações desses medicamentos. A administração concomitante de delavirdina, um NNRTI e um substrato do CYP3A4 e EQUETRO pode reduzir a concentração de delavirdina em 90%.
Danos no fígado
Foram relatados efeitos hepáticos, variando de aumentos leves nas enzimas hepáticas a casos raros de insuficiência hepática. Em alguns casos, os efeitos do fígado podem progredir apesar da interrupção do medicamento. Casos raros de síndrome do ducto biliar em fuga também foram relatados. Essa síndrome consiste em um processo colestático com um curso clínico variável que varia de fulminante a indolente e envolve a destruição e o desaparecimento do trato biliar intra-hepático. Alguns, mas não todos, casos estão associados a características que se sobrepõem a outras síndromes imunomergênicas, como reações dermatológicas graves e reações a medicamentos com eosinofilia e sintomas sistêmicos / hipersensibilidade a múltiplos órgãos.
Avaliações básicas e regulares da função hepática, especialmente em pacientes com histórico de doença hepática, devem ser realizadas durante o tratamento com este medicamento, pois podem ocorrer danos no fígado. O medicamento deve ser interrompido imediatamente em caso de disfunção hepática grave ou doença hepática ativa.
Bloco cardíaco AV
Bloco cardíaco AV, incluindo blocos de segundo e terceiro graus, foi relatado após o tratamento com carbamazepina. Isso geralmente ocorreu, mas não apenas, em pacientes com anormalidades subjacentes ao ECG ou fatores de risco para distúrbios de linha.
Porfiria hepática
O uso de EQUETRO deve ser evitado em pacientes com histórico de porfiria hepática (por exemplo,. porfiria intermitente aguda, porfiria colorida, porfiria cutanea tarda). Foram relatadas convulsões agudas em pacientes recebendo terapia com carbamazepina. Também foi demonstrado que a administração de EQUETRO aumenta os precursores de porfirina em roedores, um mecanismo suspeito para a indução de ataques agudos de porfiria.
Pressão intra-ocular aumentada
A carbamazepina possui atividade anticolinérgica leve. Em pacientes com histórico de aumento da pressão intra-ocular, você deve avaliar a pressão intra-ocular antes de iniciar o tratamento e periodicamente durante o tratamento.
Informações de aconselhamento do paciente
Consulte o rótulo do paciente aprovado pela FDA (Guia de medicamentos ).
Diga aos pacientes e cuidadores que um guia sobre medicamentos está disponível. Instrua você a Guia de medicamentos para ler antes de tomar EQUETRO .
- Reações dermatológicas graves
Informe pacientes e enfermeiros sobre o risco de reações cutâneas potencialmente fatais e graves e os sinais e sintomas que podem indicar uma reação grave da pele. Instrua os pacientes a consultar seu médico imediatamente se ocorrer uma reação cutânea durante o tratamento com EQUETRO - Agranulocitose e anemia aplástica
Informe pacientes e cuidadores sobre o risco de agranulocitose potencialmente fatal e anemia aplástica, bem como os sinais e sintomas que podem sinalizar essas reações. Informe imediatamente o seu médico se os sintomas aparecerem. - Reação medicamentosa com eosinofilia e sintomas sistêmicos
Informe os pacientes sobre os primeiros sinais e sintomas tóxicos de uma possível reação hematológica, dermatológica, hipersensibilidade ou hepática. Diga aos pacientes que esses sinais e sintomas podem sinalizar uma reação séria e relatar qualquer sinal ao seu médico imediatamente. - Pensamentos de suicídio e comportamento
Aconselhe os pacientes, cuidadores, e famílias que DEAs, incluindo EQUETRO, pode aumentar o risco de pensamentos e comportamentos suicidas, e informá-lo da necessidade de responder ou piorar os sintomas da depressão, mudanças incomuns de humor ou comportamento, ou que ocorram cientes dos pensamentos de suicídio, comportamento ou pensamentos sobre auto-mutilação. Instrua pacientes, cuidadores e famílias a relatar comportamentos preocupantes aos profissionais de saúde imediatamente. - toxicidade embrião-fetal
Aconselhe as mulheres com potencial para engravidar que o EQUETRO pode causar danos fetais. Use durante a gravidez apenas se o uso potencial do tratamento exceder os riscos. - Descontinuação abrupta e risco de convulsões
Informe os pacientes que a interrupção abrupta do EQUETRO pode causar convulsões ou um aumento na frequência das convulsões. Informe os pacientes que o medicamento deve ser tomado ao desmamar. - Hiponatremia
Diga aos pacientes que o EQUETRO pode diminuir os níveis de sódio no soro, especialmente se você estiver tomando outros medicamentos que podem diminuir o sódio. Aconselhe os pacientes a relatar sintomas de baixo teor de sódio, como náusea, fadiga, falta de energia, confusão, convulsões ou convulsões mais frequentes ou mais graves. - Potencial de comprometimento cognitivo e motor
Aconselhe os pacientes a não dirigir ou operar máquinas até que tenham experiência suficiente EQUETRO para medir se isso afeta sua capacidade de dirigir ou operar máquinas. Aconselhe os pacientes a tomar cuidado ao tomar álcool em combinação com a terapia com EQUETRO, porque possível efeito calmante aditivo. - Uso simultâneo com outros produtos de carbamazepina
Informe os pacientes que EQUETRO contém carbamazepina e não deve ser usado em combinação com outros medicamentos que contêm carbamazepina. - Diminuição da eficácia dos contraceptivos orais
Diga aos pacientes que o EQUETRO pode reduzir significativamente a eficácia da contracepção oral. Isso pode levar a falha contraceptiva ou sangramento inovador.
Incentive os pacientes a se matricularem no Registro Regulatório Antiepilético da América do Norte (NAAED) quando engravidarem. Este registro coleta informações sobre a segurança dos antiepiléticos durante a gravidez.
Toxicologia não clínica
Carcinogênese, mutagênese e comprometimento da fertilidade
Carcinogênio
Administração de carbamazepina em ratos Sprague-Dawley durante um período de 2 anos em alimentos nas doses de 25, 75 e 250 mg / kg / dia (dose baixa cerca de 0,2 vezes a dose diária humana de 1200 mg a mg / m2 - base) levou a um aumento relacionado à dose na incidência de tumores hepatocelulares em mulheres e celadenomas intersticiais benignos nos testículos dos homens.
Mutagenicidade
Estudos de mutagenicidade bacteriana e em mamíferos com carbamazepina levaram a resultados negativos.
Compromisso da fertilidade
Os efeitos da carbamazepina na fertilidade masculina e feminina não foram estudados.
Hodenatrofia ocorreu em ratos recebendo carbamazepina por via oral de 4 a 52 semanas em doses de 50 a 400 mg / kg / dia. Além disso, os ratos que receberam carbamazepina em alimentos nas doses de 25, 75 e 250 mg / kg / dia durante 2 anos tiveram uma incidência relacionada à dose de atrofia testicular e aspermatogênese.
Use em certas populações
Gravidez
Categoria de gravidez D
Visão geral do risco
EQUETRO pode causar danos fetais quando administrado a uma mulher grávida. Dados epidemiológicos sugerem que pode haver uma ligação entre o uso de carbamazepina durante a gravidez e malformações congênitas, incluindo espinha bífida. Efeitos adversos no desenvolvimento foram observados em estudos de reprodução animal com carbamazepina. Se este medicamento for utilizado durante a gravidez ou se a paciente engravidar enquanto estiver tomando o medicamento, a paciente deve ser informada do risco potencial para o feto.
Registro de gravidez
Os pacientes devem ser incentivados a se inscrever no Registro Regulatório Antiepilético da América do Norte (NAAED) quando engravidarem. Este registro coleta informações sobre a segurança dos antiepiléticos durante a gravidez. Para se registrar, os pacientes podem ligar gratuitamente para 1888-233-2334. Informações sobre o Registro de Gravidez de Medicamentos da América do Norte podem ser encontradas em http://www.aedgravidezregistry.org/.
Considerações clínicas
Ao tratar uma mulher grávida com EQUETRO, considere cuidadosamente os riscos potenciais e os benefícios do tratamento e informe-o adequadamente. Testes para detectar malformações congênitas graves de acordo com os procedimentos atualmente reconhecidos devem ser considerados parte do pré-natal de rotina em mulheres grávidas que recebem carbamazepina.
Dados humanos
Dados epidemiológicos sugerem que pode haver uma ligação entre o uso de carbamazepina durante a gravidez e malformações congênitas, incluindo espinha bífida. Avaliações retrospectivas de casos sugerem que, comparada à monoterapia, uma prevalência mais alta de efeitos teratogênicos pode ocorrer em conexão com o uso de anticonvulsivantes em terapia combinada.
A passagem transplacentária da carbamazepina é rápida (30-60 minutos) e a droga é acumulada nos tecidos fetais, com níveis mais altos no fígado e nos rins do que no cérebro e nos pulmões.
Houve alguns casos de convulsões de recém-nascidos e / ou depressão respiratória associada à carbamazepina materna e outro uso simultâneo de drogas anticonvulsivantes. Alguns casos de vômito, diarréia e / ou diminuição da alimentação de recém-nascidos também foram relatados com o uso de carbamazepina em mães. Esses sintomas podem ser síndrome de abstinência neonatal.
Dados em animais
Foi demonstrado que a carbamazepina tem efeitos adversos em estudos reprodutivos em ratos quando administrada por via oral em doses 10 a 25 vezes uma dose diária humana de 1200 mg / kg com base ou 1,5 a 4 vezes a dose diária humana de 1200 mg a mg / m2-base. Em estudos teratológicos em ratos, 2 das 135 costelas articuladas da prole a 250 mg / kg e 4 das 119 filhotes apresentaram outras anormalidades a 650 mg / kg (fenda da gengiva, 1; talipes, 1; anoftalmo, 2).
Trabalho e entrega
O efeito da carbamazepina no trabalho humano e no parto é desconhecido. A carbamazepina e seu metabólito epóxi são convertidos em leite materno durante a amamentação. Podem ocorrer efeitos colaterais graves em lactentes expostos à carbamazepina. As mães que amamentam devem considerar os benefícios e riscos potenciais do tratamento ao decidir interromper o tratamento ou interromper o tratamento com EQUETRO, levando em consideração a importância do medicamento para a mãe.
Mães que amamentam
A carbamazepina e seu metabólito epóxi são excretados no leite materno. Devido ao potencial de efeitos colaterais graves em crianças que estão expostas ao EQUETRO, deve-se decidir se o tratamento deve ser interrompido ou se o tratamento com EQUETRO deve ser interrompido, levando em consideração a importância do medicamento para a mãe.
Uso pediátrico
A segurança e eficácia do EQUETRO em pacientes pediátricos e adolescentes não foram estabelecidas.
Aplicação geriátrica
Os estudos clínicos da EQUETRO não incluíram um número suficiente de indivíduos com 65 anos ou mais para determinar se você responde de maneira diferente dos indivíduos mais jovens. Outras experiências clínicas relatadas não encontraram diferenças nas reações entre pacientes idosos e jovens. Em geral, a seleção da dose para um paciente idoso deve ser cuidadosa, geralmente começando na extremidade inferior do intervalo de doses, refletindo o aumento da frequência de diminuição da função hepática, renal ou cardíaca e uma doença associada ou outra terapia medicamentosa.
| Placebo | Antiepiléticos | |||
| Nota | Reações Por 1000 pacientes | Reações Por 1000 pacientes | Risco relativo: incidência de reações no grupo AED / incidência de reações no grupo placebo | Diferença de risco: Pacientes medicamentosos adicionais com eventos por 1000 pacientes |
| Epilepsia | 1.0 | 3.4 | 3.5 | 2.4 |
| Psiquiátrico | 5.7 | 8.5 | 1.5 | 2.9 |
| De outros | 1.0 | 1.8 | 1.9 | 0,9 |
| Total | 2.4 | 4.3 | 1.8 | 1.9 |

Mude da carbamazepina com liberação imediata para EQUETRO
EQUETRO é uma formulação com liberação prolongada para administração duas vezes ao dia. Ao converter pacientes com liberação imediata de carbamazepina em cápsulas de EQUETRO com liberação prolongada, a mesma dose diária total de carbamazepina deve ser administrada em mg. Após mudar para EQUETRO, os pacientes devem ser monitorados de perto quanto ao controle de crises. Dependendo da resposta terapêutica após a conversão, a dose diária total pode precisar ser ajustada dentro das instruções de dosagem recomendadas.
Configurando EQUETRO
Se parar de tomar EQUETRO para cada indicação, reduza gradualmente a dose e evite a descontinuação abrupta para reduzir o risco de convulsões.
Monitorando a concentração de carbamazepina no soro
O monitoramento das concentrações de carbamazepina no soro pode ser útil para a seleção da dose, minimizando a toxicidade e verificando a conformidade com o medicamento, especialmente em condições clínicas em que podem ocorrer alterações no metabolismo do EQUETRO (por exemplo,. interações medicamentosas). Se não for alcançada uma resposta clínica satisfatória em pacientes pediátricos tratados com EQUETRO para epilepsia, meça os níveis plasmáticos para determinar se você está ou não na faixa terapêutica.
Instruções para administração
Engula as cápsulas EQUETRO inteiras ou abertas e polvilhe as pérolas sobre os alimentos como uma colher de chá de molho de maçã. Não esmague ou mastigue cápsulas EQUETRO ou pérolas na cápsula. EQUETRO pode ser tomado com ou sem refeições.
COMO ENTREGADO
Formas e forças farmacêuticas
As cápsulas de EQUETRO (carbamazepina) com liberação prolongada para administração oral são fornecidas em três doses:
- 100 mg - Tampa opaca amarela da cápsula de gelatina dura em duas partes com corpo opaco verde azulado impresso com SPD417 em uma extremidade e SPD417 e 100 mg no outro lado em tinta branca
- 200 mg - Tampa opaca amarela da cápsula de gelatina dura em duas partes com corpo opaco azul impresso com SPD417 em uma extremidade e SPD417 e 200 mg no outro lado em tinta branca.
- 300 mg - Tampa opaca amarela da cápsula de gelatina dura em duas partes com corpo azul impresso com SPD417 em uma extremidade e SPD417 e 300 mg no outro lado em tinta branca.
Armazenamento e manuseio
As cápsulas de liberação prolongada de EQUETRO (carbamazepina) são fornecidas em três doses
Compre a 25 ° C (77 ° F); Excursões de até 15 a 30 ° C (59 a 86 ° F).
Proteger da luz e umidade
Feito para data centers, a Validus adquiriu a Pharmaceuticals LLC, 119 Cherry Hill Road, Suite 310, Parsippany, NJ 07054. Revisado: setembro de 2016
Efeitos colaterais e interações medicamentosasEfeitos colaterais
Máx
Como os ensaios clínicos são conduzidos em condições muito diferentes, as taxas de efeitos colaterais observadas nos ensaios clínicos de um medicamento não podem ser comparadas diretamente com as taxas nos ensaios clínicos de outro medicamento e podem não refletir as taxas observadas na prática clínica.
Os efeitos colaterais mais comumente relatados (> 5% no grupo EQUETRO e pelo menos duas vezes placebo) nos estudos combinados controlados por placebo de 3 semanas em pacientes com mania aguda associada ao transtorno bipolar I (estudos 1 e 2) foram tonturas, sonolência, náusea, vômito, ataxia, constipação, coceira, boca seca. As doses de EQUETRO utilizadas foram de 400 a 1600 mg por dia.
Quadro 2. Efeitos colaterais comuns relatados nos estudos 1 e 2 sobre distúrbios bipolares (incidência> 2% e mais que o placebo)
Pós-experiência de marketing
Os seguintes efeitos colaterais foram identificados ao usar o EQUETRO após a aprovação. Como essas reações são relatadas voluntariamente a partir de uma população de tamanho incerto, nem sempre é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição a medicamentos.
Sistema nervoso: Confusão, diplopia, distúrbios oculomotores, nistagmo, distúrbios da fala, movimentos involuntários anormais, zumbido.
Sistema digestivo: Desconforto no estômago, dor abdominal, diarréia, anorexia.
Testes laboratoriais : testes de função da tireóide (T3, T4) - valores reduzidos
De outros: síndrome do tipo lúpus eritematoso
Foi relatado um caso de meningite asséptica, acompanhada de mioclonia e eosinofilia periférica, em um paciente em uso de carbamazepina em combinação com outros medicamentos. O paciente foi decapitado com sucesso e a meningite reapareceu quando foi tratado com carbamazepina novamente.
Efeitos colaterais adicionais associados à carbamazepina
Abaixo está uma lista de efeitos colaterais adicionais que foram identificados em ensaios clínicos ou relatórios de pós-comercialização sobre outras formas de carbamazepina e não foram relatados para EQUETRO acima. Como essas reações foram relatadas voluntariamente a partir de uma população de tamanho incerto, nem sempre é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição a medicamentos.
Sistema nervoso: Casos isolados de síndromes neurolépticas malignas foram relatados com o uso de carbamazepina com e sem o uso simultâneo de outras drogas psicotrópicas.
Pele: onicomadesia, pustulose exanthemática generalizada aguda (AGEP).
para relatar BY-WIRKINGS MOVID, entre em contato com a Validus Pharmaceuticals LLC pelo telefone 1-8669VALIDUS (1-866-982-5438) ou FDA pelo telefone 1-800-FDA-1088 ou www.fda.gov/medwatch
Interações com MEDICAMENTOS
Efeitos farmacocinéticos de outros medicamentos no EQUETRO
Medicamentos que inibem o citocromo P450 3A4 (CYP3A4)
O EQUETRO é metabolizado principalmente pelo CYP3A4 no epóxido ativo de carbamazepina-10,11, que é posteriormente metabolizado em transdiol pela epóxi-hidrolase. Inibidores do CYP 3A4 e / ou epoxi-hidrolase podem aumentar os níveis plasmáticos de EQUETRO e seus metabólitos ativos, aumentar as concentrações plasmáticas de EQUETRO e aumentar o risco de efeitos colaterais. Quando usado concomitantemente com inibidores da CYP3A4 e / ou epóxi-hidrolase, pode ser necessário reduzir a dose de EQUETRO. Os seguintes medicamentos são inibidores do CYP3A4:
Acetazolamida, aprepitant, antifúngicos azólicos (por exemplo,. cetoconazol, itraconazol, fluconazol, voriconazol,, Cimetidina, ciprofloxacina, claritromicina, dalfopristina, danazol, dantroleno, delavirdina, diltiazem, eritromicina, Fluoxetina, fluvoxamina, suco de toranja, ibuprofeno, isoniazida, loratadina, nefazodona, niacinamida, nicotinamida, Olanzapina, omeprazol, oxibutinina, quinina, chinupristina, ticlopidina, troleandomicina, valproato, verapamil, zileuton.
Medicamentos, epóxi-hidrolase e inibidores do CYP3A4
Claritromicina, eritromicina, loxapina, quetiapin e valproato também inibem a epóxi-hidrolase, o que leva ao aumento da reflexão do metabólito ativo carbamazepina-10,11 epóxido.
Medicamentos que induzem o CYP3A4
Os indutores do CYP3A4 podem reduzir as concentrações séricas de EQUETRO e reduzir sua eficácia. Quando usado com um indutor do CYP3A4, pode ser necessário aumentar a dose de EQUETRO. Tais drogas incluem:
Aminofilina, cisplatina, doxorrubicina, felbamato, fosfenitoína, metoximida, fenobarbital, fenitoína, primidona, rifampicina e teofilina.
Efeitos farmacocinéticos de EQUETRO em outros medicamentos
EQUETRO é um potente indutor de 3A4 hepático e também é conhecido como indutor de CYP1A2, 2B6, 2C9 / 19 e, portanto, pode reduzir as concentrações plasmáticas de co-medicação, que são principalmente metabolizadas pelos CYP 1A2, 2B6, 2C9 / 19 e 3A4, por indução do seu metabolismo. Quando usado concomitantemente com EQUETRO, pode ser necessário monitorar as concentrações ou ajustar a dose desses agentes.
EQUETRO Reduz as concentrações dos seguintes medicamentos, induzindo seu metabolismo:
Contraceptivos orais (substratos do CYP3A4)
EQUETRO é um forte indutor do CYP3A4. O EQUETRO pode aumentar o metabolismo de certos contraceptivos orais (por indução do CYP3A4), o que leva a concentrações significativamente mais baixas. Isso pode levar a falha contraceptiva ou sangramento inovador. Considere a alternativa aos contraceptivos orais que são significativamente afetados pela indução do CYP3A4 ou considere a alternativa ao EQUETRO
Delavirdina e outros inibidores da transcriptase reversa não nucleósidos (substratos do CYP3A4)
Ao induzir o CYP3A4, o EQUETRO aumenta o metabolismo da delavirdina e de certos inibidores da transcriptase reversa não nucleósidos e reduz significativamente as concentrações plasmáticas desses medicamentos. Isso pode levar a atividade antiviral insuficiente, perda de resposta virológica e possível resistência a delavirdina ou outros inibidores da transcriptase reversa não nucleósidos. Portanto, o uso de EQUETRO é contra-indicado com esses inibidores da transcriptase reversa não nucleósidos
Nefazodona (substrato do CYP3A4)
O uso de EQUETRO é contra-indicado ao usar nefazodona, uma vez que o uso concomitante pode levar a concentrações plasmáticas insuficientes de nefazodona e seu metabólito ativo, a fim de obter um efeito terapêutico da nefazodona.
Varfarina (substrato do CYP1A2 e CYP3A4)
Ao induzir o CYP1A2 e o CYP3A4, o EQUETRO reduz a concentração de varfarina e reduz sua eficácia anticoagulante.
Aripiprazol
Se a carbamazepina for adicionada ao aripiprazol, a dose de aripiprazol deve ser duplicada. Aumentos adicionais da dose devem ser baseados na avaliação clínica. Se a carbamazepina for descontinuada posteriormente, a dose de aripiprazol deve ser reduzida.
Tacrolimus
Quando a carbamazepina é usada com tacrolimus, recomenda-se o monitoramento das concentrações sanguíneas de tacrolimus e os ajustes adequados da dose.
Temsirolimus
O uso de indutores fortes do CYP3A4, como a carbamazepina, deve ser evitado com o temsirolimus. Se os pacientes precisarem administrar carbamazepina com temsirolimus, deve-se considerar um ajuste na dose de temirolimus.
Lapatinib
O uso de carbamazepina com lapatinib deve geralmente ser evitado. Quando a carbamazepina é iniciada em um paciente que já está tomando lapatinib, a dose de lapatinib deve ser gradualmente titulada. Se a carbamazepina for descontinuada, a dose de lapatinib deve ser reduzida.
Inibidores da protease do HIV
Devido à forte indução do CYP3A4 pela carbamazepina, o uso de EQUETRO com inibidores da protease do HIV não é recomendado.
Outros substratos cyp1a2 e CYP3A4
O EQUETRO induz o CYP1A2 e o CYP3A4, o que leva a concentrações reduzidas de medicamentos metabolizados pelo CYP3A4 ou CYP1A2. Quando usado concomitantemente com EQUETRO, pode ser necessário aumentar as doses desses medicamentos. Os medicamentos metabolizados pelo CYP3A4 ou CYP1A2 incluem o seguinte:
Acetaminofeno, albendazol, alprazolam, aprepitant, buprenorfona, bupropiona, buspiron, citalopram, clobazam, clonazepam, clozapina, ciclosporina, delavirdina, desipramina, diazepam, dicumarol, bloqueador dos canais de cálcio dihidropiridina (.felodipina), doxiciclina, etosuximida, everolimus, felbamato, glicocorticóide, haloperidol, imatinibe, itraconazol, lamotrigina, levotiroxina, lorazepam, metadona, metsuxamida, mianserina, midazolam, mirtazapina. Imipramina, amitriptilina, nortriptilina), trazodona, valproato, varfarina, ziprasidona e zonisamida.
EQUETRO Aumenta os níveis plasmáticos dos seguintes medicamentos, inibindo seu metabolismo :
Clomipramina, fenitoína e primidona
EQUETRO pode aumentar as concentrações de clomipramina, fenitoína e primidona. Se um paciente foi titulado para uma dose estável com um desses agentes nesta categoria e o tratamento com EQUETRO começar, pode ser necessário reduzir a dose desses medicamentos.
Fenitoína
Foi relatado que os níveis de fenitoína aumentam ou diminuem na presença de carbamazepina. Existem vários mecanismos farmacocinéticos para alterar os níveis de fenitoína quando usados com EQUETRO. Monitore cuidadosamente os níveis séricos de fenitoína ao usar EQUETRO ao mesmo tempo.
Ciclofosfamida
A ciclofosfamida é um pró-fármaco inativo e é parcialmente convertida em seus metabólitos ativos pelo CYP3A. A taxa metabólica e a atividade leucopênica da ciclofosfamida são relatadas como aumentadas pela administração simultânea crônica de indutores do CYP3A4. Existe potencial para aumentar a toxicidade da ciclofosfamida quando co-administrado com carbamazepina.
Interações farmacodinâmicas com medicamentos
Inibidor da monoamina oxidase
O tratamento concomitante com EQUETRO é contra-indicado durante o uso de um MAOI ou dentro de 14 dias após a interrupção de um MAOI. O uso concomitante pode causar síndrome da serotonina.
Lítio
A administração concomitante de EQUETRO e lítio pode aumentar o risco de efeitos colaterais neurotóxicos. Considere reduzir a dose de lítio ou EQUETRO se estiver tomando esses medicamentos ao mesmo tempo.
Isoniazid
Foi relatado que o uso concomitante de carbamazepina e isoniazida aumenta a hepatotoxicidade induzida por isoniazida.
Depressores do CNS
A administração concomitante de EQUETRO e outros depressores do SNC pode aumentar o risco de depressão respiratória, sedação profunda, hipotensão e síncope. Os depressores do SNC incluem: álcool, analgésicos opióides, benzodiazepínicos, antidepressivos tricíclicos, sedativos / hipnóticos, anticonvulsivantes, antipsicóticos, anti-histamínicos, anticolinérgicos, bloqueadores alfa e beta, anestésicos gerais, relaxantes musculares e depressores ilegais do SNC. Considere reduzir a dose de depressores do SNC ou EQUETRO se estiver tomando esses medicamentos ao mesmo tempo.
Cloroquina e mefloquina
A cloroquina malariamédica e a mefloquina podem antagonizar a atividade do EQUETRO
Bloqueadores neuromusculares
Ocorreu resistência ao efeito de bloqueio neuromuscular dos agentes bloqueadores neuromusculares não despolarizantes pancuronium, vecurônio, rocurônio e cisatracúrio em pacientes que receberam carbamazepina crônica. Não se sabe se a carbamazepina tem o mesmo efeito em outros agentes não despolarizantes ou não. Os pacientes devem ser monitorados de perto para se recuperar do bloqueio neuromuscular mais rápido do que o esperado, e os requisitos de taxa de infusão podem ser maiores.
| Efeitos colaterais | EQUETRO® (N = 251) |
Placebo (N = 248) |
| Tontura | 44% | 12% |
| Sonolência | 32% | 13% |
| Náusea | 29% | 10% |
| Vômito | 18% | 3% |
| Irregularidade | 15% | 0,4% |
| Constipação | 10% | 5% |
| Comichão | 8% | 2% |
| Boca seca | 8% | 3% |
| Fraqueza | 8% | 4% |
| Erupção cutânea | 7% | 4% |
| Veja desfocado | 6% | 2% |
| Distúrbio de linguagem | 6% | 0,4% |
| Hipertensão | 3% | 0,4% |
| Parestesia | 2% | 1% |
| Pense anormal | 2% | 0,4% |
| Tremor | 3% | 1% |
| Para se contorcer | 2% | 1% |
| Tontura | 2% | 1% |

Categoria de gravidez D
Visão geral do risco
EQUETRO pode causar danos fetais quando administrado a uma mulher grávida. Dados epidemiológicos sugerem que pode haver uma ligação entre o uso de carbamazepina durante a gravidez e malformações congênitas, incluindo espinha bífida. Efeitos adversos no desenvolvimento foram observados em estudos de reprodução animal com carbamazepina. Se este medicamento for utilizado durante a gravidez ou se a paciente engravidar enquanto estiver tomando o medicamento, a paciente deve ser informada do risco potencial para o feto.
Registro de gravidez
Os pacientes devem ser incentivados a se inscrever no Registro Regulatório Antiepilético da América do Norte (NAAED) quando engravidarem. Este registro coleta informações sobre a segurança dos antiepiléticos durante a gravidez. Para se registrar, os pacientes podem ligar gratuitamente para 1888-233-2334. Informações sobre o Registro de Gravidez de Medicamentos da América do Norte podem ser encontradas em http://www.aedgravidezregistry.org/.
Considerações clínicas
Ao tratar uma mulher grávida com EQUETRO, considere cuidadosamente os riscos potenciais e os benefícios do tratamento e informe-o adequadamente. Testes para detectar malformações congênitas graves de acordo com os procedimentos atualmente reconhecidos devem ser considerados parte do pré-natal de rotina em mulheres grávidas que recebem carbamazepina.
Dados humanos
Dados epidemiológicos sugerem que pode haver uma ligação entre o uso de carbamazepina durante a gravidez e malformações congênitas, incluindo espinha bífida. Avaliações retrospectivas de casos sugerem que, comparada à monoterapia, uma prevalência mais alta de efeitos teratogênicos pode ocorrer em conexão com o uso de anticonvulsivantes em terapia combinada.
A passagem transplacentária da carbamazepina é rápida (30-60 minutos) e a droga é acumulada nos tecidos fetais, com níveis mais altos no fígado e nos rins do que no cérebro e nos pulmões.
Houve alguns casos de convulsões de recém-nascidos e / ou depressão respiratória associada à carbamazepina materna e outro uso simultâneo de drogas anticonvulsivantes. Alguns casos de vômito, diarréia e / ou diminuição da alimentação de recém-nascidos também foram relatados com o uso de carbamazepina em mães. Esses sintomas podem ser síndrome de abstinência neonatal.
Dados em animais
Foi demonstrado que a carbamazepina tem efeitos adversos em estudos reprodutivos em ratos quando administrada por via oral em doses 10 a 25 vezes uma dose diária humana de 1200 mg / kg com base ou 1,5 a 4 vezes a dose diária humana de 1200 mg a mg / m2-base. Em estudos teratológicos em ratos, 2 das 135 costelas articuladas da prole a 250 mg / kg e 4 das 119 filhotes apresentaram outras anormalidades a 650 mg / kg (fenda da gengiva, 1; talipes, 1; anoftalmo, 2).

Máx
Como os ensaios clínicos são conduzidos em condições muito diferentes, as taxas de efeitos colaterais observadas nos ensaios clínicos de um medicamento não podem ser comparadas diretamente com as taxas nos ensaios clínicos de outro medicamento e podem não refletir as taxas observadas na prática clínica.
Os efeitos colaterais mais comumente relatados (> 5% no grupo EQUETRO e pelo menos duas vezes placebo) nos estudos combinados controlados por placebo de 3 semanas em pacientes com mania aguda associada ao transtorno bipolar I (estudos 1 e 2) foram tonturas, sonolência, náusea, vômito, ataxia, constipação, coceira, boca seca. As doses de EQUETRO utilizadas foram de 400 a 1600 mg por dia.
Quadro 2. Efeitos colaterais comuns relatados nos estudos 1 e 2 sobre distúrbios bipolares (incidência> 2% e mais que o placebo)
Pós-experiência de marketing
Os seguintes efeitos colaterais foram identificados ao usar o EQUETRO após a aprovação. Como essas reações são relatadas voluntariamente a partir de uma população de tamanho incerto, nem sempre é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição a medicamentos.
Sistema nervoso: Confusão, diplopia, distúrbios oculomotores, nistagmo, distúrbios da fala, movimentos involuntários anormais, zumbido.
Sistema digestivo: Desconforto no estômago, dor abdominal, diarréia, anorexia.
Testes laboratoriais : testes de função da tireóide (T3, T4) - valores reduzidos
De outros: síndrome do tipo lúpus eritematoso
Foi relatado um caso de meningite asséptica, acompanhada de mioclonia e eosinofilia periférica, em um paciente em uso de carbamazepina em combinação com outros medicamentos. O paciente foi decapitado com sucesso e a meningite reapareceu quando foi tratado com carbamazepina novamente.
Efeitos colaterais adicionais associados à carbamazepina
Abaixo está uma lista de efeitos colaterais adicionais que foram identificados em ensaios clínicos ou relatórios de pós-comercialização sobre outras formas de carbamazepina e não foram relatados para EQUETRO acima. Como essas reações foram relatadas voluntariamente a partir de uma população de tamanho incerto, nem sempre é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição a medicamentos.
Sistema nervoso: Casos isolados de síndromes neurolépticas malignas foram relatados com o uso de carbamazepina com e sem o uso simultâneo de outras drogas psicotrópicas.
Pele: onicomadesia, pustulose exanthemática generalizada aguda (AGEP).
para relatar BY-WIRKINGS MOVID, entre em contato com a Validus Pharmaceuticals LLC pelo telefone 1-8669VALIDUS (1-866-982-5438) ou FDA pelo telefone 1-800-FDA-1088 ou www.fda.gov/medwatch
| Efeitos colaterais | EQUETRO® (N = 251) |
Placebo (N = 248) |
| Tontura | 44% | 12% |
| Sonolência | 32% | 13% |
| Náusea | 29% | 10% |
| Vômito | 18% | 3% |
| Irregularidade | 15% | 0,4% |
| Constipação | 10% | 5% |
| Comichão | 8% | 2% |
| Boca seca | 8% | 3% |
| Fraqueza | 8% | 4% |
| Erupção cutânea | 7% | 4% |
| Veja desfocado | 6% | 2% |
| Distúrbio de linguagem | 6% | 0,4% |
| Hipertensão | 3% | 0,4% |
| Parestesia | 2% | 1% |
| Pense anormal | 2% | 0,4% |
| Tremor | 3% | 1% |
| Para se contorcer | 2% | 1% |
| Tontura | 2% | 1% |

Experiência humana
Dose letal mais baixa conhecida de carbamazepina: adultos, mais de 60 gramas (homem de 39 anos). As doses mais altas conhecidas sobreviveram: adultos, 30 gramas (mulher de 31 anos); Crianças, 10 gramas (menino de 6 anos); crianças pequenas, 5 gramas (menina de 3 anos).
Sinais e sintomas
Os primeiros sinais e sintomas da sobredosagem com carbamazepina aparecem após 1 a 3 horas. Os distúrbios neuromusculares são os mais proeminentes. As doenças cardiovasculares são geralmente mais leves e complicações cardíacas graves ocorrem apenas quando doses muito altas (mais de 60 gramas) foram tomadas.
Respiração
Respiração irregular, depressão respiratória.
Sistema cardiovascular
Taquicardia, hipotensão ou hipertensão, choque, distúrbios de condução.
Sistema nervoso e músculos
Dificuldade na consciência até o coma profundo. Cãibras, especialmente em crianças pequenas. Agitação motora, espasmos musculares, tremores, movimentos atetóides, opistotonos, ataxia, sonolência, tontura, midríase, nistagmo, adiadochokinesia, balismo, distúrbios psicomotor, dismetria. Hiperreflexia inicial seguida de hiporeflexia.
Trato gastrointestinal
Náusea, vômito.
Rins e bexiga
Anúria ou oligúria, retenção urinária.
Resultados laboratoriais
Casos isolados de sobredosagem incluem leucocitose, contagem reduzida de leucócitos, glicosúria e acetonúria. O eletrocardiograma pode mostrar disritmias.
Envenenamento combinado
Se forem tomados álcool, antidepressivos tricíclicos, barbitúricos ou hidantoínas ao mesmo tempo, os sinais e sintomas de envenenamento agudo por carbamazepina podem ser agravados ou alterados.
Gerenciamento de overdose
Para obter as informações mais recentes sobre o gerenciamento da overdose de EQUETRO, entre em contato com o centro de veneno certificado para sua região pelo telefone 1-800-222-1222 (ou em www.poison.org). em caso de sobredosagem, cuidados de suporte, incluindo monitoramento e monitoramento médicos próximos. O tratamento deve consistir nas medidas gerais usadas para tratar uma overdose com um medicamento. Considere a possibilidade de overdose de vários medicamentos. Garanta vias aéreas adequadas, suprimento de oxigênio e ventilação. Monitore o ritmo cardíaco e as funções vitais. Use medidas de suporte e sintomáticas.

Carbamazepina (CBZ)
Absorção
Após uma dose oral única de 200 mg com liberação prolongada de carbamazepina, a concentração plasmática foi de 1,9 ± 0,3 mcg / mL e o tempo para atingir o pico foi de 19 ± 7 horas. Após administração repetida da dose (800 mg a cada 12 horas), os valores de pico foram de 11,0 ± 2,5 mcg / mL e o tempo até o pico ser atingido foi de 5,9 ± 1,8 horas. A farmacocinética da carbamazepina com liberação prolongada é linear no intervalo de doses únicas de 200-800 mg.
76% da carbamazepina está ligada às proteínas plasmáticas. A carbamazepina é principalmente metabolizada no fígado. O citocromo P450 3A4 foi identificado como a principal isoforma responsável pela formação do epóxido de carbamazepina-10,11. Como a carbamazepina induz seu próprio metabolismo, a meia-vida também é variável. A meia-vida média variou de 35 a 40 horas após uma dose única de carbamazepina com liberação prolongada e de 12 a 17 horas após doses repetidas. A depuração oral aparente foi de 25 ± 5 mL / min após uma dose única e 80 ± 30 mL / min com doses múltiplas.
Carbamazepina-10,11-epóxido (CBZ-E)
A carbamazepina-10,11-epóxido é considerada um metabolito ativo da carbamazepina. Após uma dose única de liberação prolongada de 200 mg de carbamazepina para ingestão, a concentração plasmática máxima de carbamazepina-10,11-epóxido 0,11 ± 0,012 mcg / mL e o tempo para atingir o pico foi de 36 ± 6 horas. Após administração crônica de uma dose com liberação prolongada de carbamazepina (800 mg a cada 12 horas), os valores máximos de carbamazepina-10,11-epóxido foram de 2,2 ± 0,9 mcg / mL e o tempo para atingir o pico foi de 14 ± 8 horas. A meia-vida plasmática do carbamazepina-10,11 epóxido após a administração de carbamazepina é de 34 & maismn; 9 horas. Após uma dose oral única de carbamazepina com liberação prolongada (200-800 mg), a AUC e a Cmax do epóxido de carbamazepina-10.11 foram inferiores a 10% de carbamazepina. Após doses múltiplas de carbamazepina com liberação prolongada (800-1600 mg por dia durante 14 dias) a AUC e a Cmax do carbamazepina-10,11 epóxido dependiam da dose, na faixa de 15,7 mcg.hr/mL e 1,5 mcg / mL a 800 mg / dia até 32,6 mcg.hr/mL e 3,2 mcg / mL a 1600 mg / dia e menos de 30% de carbamazepina. A carbamazepina-10,11-epóxido está 50% ligada às proteínas plasmáticas.
Efeito alimentar
Uma refeição rica em gordura aumentou a taxa de absorção de uma dose única de 400 mg (a Tmax média foi reduzida de 24 horas em jejum para 14 horas e a Cmax aumentou de 3,2 para 4,3 mcg / mL), mas não a extensão (AUC) de absorção. A meia-vida de eliminação permaneceu inalterada entre o estado alimentado e o rápido. O estudo de doses múltiplas realizado no estado alimentado mostrou que os valores de CMAX no estado estacionário estão dentro da faixa de concentração terapêutica. O perfil farmacocinético da carbamazepina com liberação prolongada foi semelhante quando administrado por aspersão das pérolas sobre o molho de maçã em comparação com a cápsula intacta administrada no estado sóbrio.
Eliminação
Após administração oral de 14A C-carbamazepina encontrou 72% da radioatividade administrada na urina e 28% nas fezes. Essa radioatividade na urina consistia em grande parte de metabólitos hidroxilados e conjugados, com apenas 3% de carbamazepina inalterada
Metabolismo
in vitro os dados mostram que a carbamazepina é metabolizada principalmente pelo citocromo P450 (CYP) 3A4 em carbamazepina-10,11-epóxido ativo, que é ainda metabolizado em trans-diol pela epoxi-hidrolase. A epoxi-hidrolase microssomal humana foi identificada como a enzima responsável pela formação do derivado transdiol 10.11 do epóxido de carbamazepina-10.11.
Compromisso renal
O efeito da insuficiência renal na farmacocinética da carbamazepina é desconhecido.
Compromisso hepático
O efeito da disfunção hepática na farmacocinética da carbamazepina é desconhecido. Considere reduzir a dose em pacientes com insuficiência hepática.
Efeito da idade
A carbamazepina é metabolizada em carbamazepina-10,11-epóxido mais rapidamente em crianças pequenas do que em adultos. Crianças menores de 15 anos têm uma relação reversa entre a proporção CBZ-E / CBZ e o aumento da idade. A segurança e eficácia do EQUETRO® Nenhuma evidência foi encontrada em pacientes pediátricos e adolescentes.
Efeito de gênero
Nenhuma diferença foi encontrada na AUC e na Cmax médias da carbamazepina e do epóxido de carbamazepina-10,11 entre homens e mulheres.

However, we will provide data for each active ingredient


