
Componentes:
Método de ação:
Medicamente revisado por Oliinyk Elizabeth Ivanovna, Farmácia Última atualização em 26.06.2023

Atenção! As informações na página são apenas para profissionais de saúde! As informações são coletadas em fontes abertas e podem conter erros significativos! Tenha cuidado e verifique novamente todas as informações desta página!
20 principais medicamentos com os mesmos componentes:

Comtan

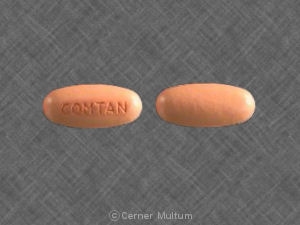
Comtan (entacapona) é fornecido na forma de comprimidos revestidos por película de 200 mg para administração oral. Os comprimidos de forma oval são cor-de-laranja acastanhado, sem coloração e gravados em "Comtan" numa das faces. Os comprimidos são fornecidos em recipientes de polietileno de alta densidade da seguinte forma::
Frascos de 100 NDC 0078-0327-05
Conservar a 25 ° C (77°F), excursões permitidas até 15°C a 30°C (59°F a 86°F).
Fabricado por: Orion Corporation, Orion Pharma (Espoo, Finlândia). Revisão: Fev 2016

Comtan está indicado como adjuvante da levodopa e da carbidopa no tratamento do "desgaste" do fim da dose em doentes com doença de Parkinson (ver secção 4. 4). FARMACOLOGIA CLÍNICA, clinico).
A eficácia do Comtan não foi sistematicamente avaliada em doentes com doença de Parkinson que não experimentam "desgaste"em fim de dose.

A dose recomendada de Comtan (entacapona) é de um comprimido de 200 mg administrado concomitantemente com cada dose de levodopa e carbidopa até um máximo de 8 vezes por dia (200 mg x 8 = 1.600 mg por dia). A experiência clínica com doses diárias superiores a 1.600 mg é limitada.
Comtan deve ser sempre administrado em associação com levodopa e carbidopa. O Entacapone não tem efeito antiparkinsónico próprio.
Em estudos clínicos, a maioria dos doentes necessitou de uma diminuição da dose diária de levodopa se a sua dose diária de levodopa tivesse sido superior ou igual a 800 mg ou se os doentes tivessem disquinesia moderada ou grave antes do início do tratamento.
Para optimizar a resposta de um doente individual, podem ser necessárias reduções na dose diária de levodopa ou um prolongamento do intervalo entre as doses. Em estudos clínicos, a redução média da dose diária de levodopa foi de cerca de 25% nos doentes que necessitavam de uma redução da dose de levodopa. (Mais de 58% dos doentes com doses de levodopa superiores a 800 mg por dia necessitaram desta redução.)
O Comtan pode ser combinado com as formulações de libertação imediata e prolongada de levodopa e carbidopa.
Comtan pode ser tomado com ou sem alimentos (ver FARMACOLOGIA CLÍNICA).
Doentes Com Compromisso Da Função Hepática
Os doentes com compromisso hepático devem ser tratados com precaução. A AUC e a Cmax do entacapone duplicaram aproximadamente em doentes com doença hepática documentada, comparativamente aos controlos. No entanto, estes estudos foram realizados com dose única de entacapona sem levodopa e dopa descarboxilase inibidor de administração concomitante, e, portanto, os efeitos da doença hepática na cinética do administrado cronicamente entacapona não foram avaliadas (ver FARMACOLOGIA CLÍNICA, Farmacocinética Da Entacapona).
Retirar Os Doentes Do Comtan
A interrupção rápida ou a redução abrupta da dose de Comtan podem levar ao aparecimento de sinais e sintomas da doença de Parkinson (ver secção 4. 4). FARMACOLOGIA CLÍNICA, clinico), e pode levar a hiperpirexia e confusão, um complexo de sintomas semelhante ao SMN (ver PRECAUCAO, Outros Factos Notificados Com Terapeutica Dopaminérgica). Esta síndrome deve ser considerada no diagnóstico diferencial para qualquer paciente que desenvolva febre alta ou rigidez grave. Se for tomada a decisão de interromper o tratamento com Comtan, os doentes devem ser cuidadosamente vigiados e outros tratamentos dopaminérgicos devem ser ajustados conforme necessário. Embora o Comtan não tenha sido sistematicamente avaliado, parece prudente retirar os doentes lentamente se for tomada a decisão de interromper o tratamento.

Comtan está contra-indicado em doentes que tenham demonstrado hipersensibilidade ao medicamento ou aos seus ingredientes.

AVISO
Monoamino oxidase (MAO) e COMT são as duas principais enzimas sistemas envolvidos no metabolismo das catecolaminas. É teoricamente assim, é possível que a combinação de Comtan (entacapona) e inibidores não selectivos da MAO (por exemplo, fenelzina e tranilcipromina) resultariam na inibição da maioria das vias responsáveis pelo normal metabolismo da catecolamina. Por esta razão, os tratado concomitantemente com Comtan e um inibidor não selectivo da MAO.
O Entacapone pode ser tomado concomitantemente com uma Inibidor da MAO-B (por exemplo, selegilina).
Medicamentos metabolizados pela catecol-o-metiltransferase (COMT))
Quando foi administrada uma dose única de 400 mg de entacapona com isoprenalina intravenosa (isoproterenol) e epinefrina sem administração concomitante levodopa e inibidor da dopa descarboxilase, as a frequência cardíaca durante a perfusão foi cerca de 50% e 80% superior à do placebo, quando isoprenalina e epinefrina, respectivamente.
Portanto, drogas conhecidas por serem metabolizadas pela COMT, tais como isoproterenol, epinefrina, norepinefrina, dopamina, dobutamina, Alfa-metildopa, apomorfina, isoetherina e bitolterol devem ser administrado com precaução em doentes a receber entacapone independentemente da via de administração (incluindo inalação), uma vez que a sua interacção pode resultar aumento da frequência cardíaca, possíveis arritmias e alterações excessivas na pressão arterial.
Observou-se taquicardia Ventricular numa criança de 32 anos. voluntários saudáveis do sexo masculino num estudo de interacção após perfusão de epinefrina e administração oral de entacapone. Foi necessário o tratamento com propranolol. A a relação causal com a administração de entacapone parece provável, mas não pode ser atribuído com certeza.
Adormecer Durante As Actividades Da Vida Diária E Sonolência
Doentes com doença de Parkinson tratados com Comtan, o que aumenta os níveis plasmáticos de levodopa, ou com levodopa, relataram subitamente adormecer sem aviso prévio de sonolência durante actividades da vida diária (incluindo o funcionamento dos veículos a motor). Alguns destes episódios resultaram em acidentes. Embora muitos destes doentes tenham notificado sonolência durante o tratamento com Comtan, alguns não detectaram sinais de aviso, tais como sonolência excessiva, e acreditava que estavam alerta imediatamente antes de evento. Alguns destes eventos foram relatados até um ano depois início do tratamento.
O risco de sonolência aumentou (Comtan 2% e placebo 0%) em estudos controlados. Foi relatado que adormecer enquanto envolvido em atividades de vida diária sempre ocorre em um ambiente pré-existente sonolência, embora os doentes possam não apresentar tais antecedentes. Por esta razão, os médicos devem reavaliar os doentes quanto a sonolência ou sonolência, especialmente uma vez que alguns dos acontecimentos ocorrem bem após o início do tratamento. Prescritor deve também estar ciente de que os doentes podem não reconhecer sonolência ou sonolência até ser directamente questionado sobre sonolência ou sonolência durante actividade. Os doentes devem ser aconselhados a ter precaução durante a condução., utilizar máquinas ou trabalhar em alturas durante o tratamento com Comtan. Doentes que já experimentaram sonolência e/ou episódios súbitos de sonolência o início do sono não deve participar nestas actividades durante o tratamento com Comtan
Antes de iniciar o tratamento com Comtan, aconselhe os doentes do potencial para desenvolver sonolência e perguntar especificamente sobre os factores que pode aumentar este risco, tais como o uso concomitante de medicamentos sedativos e presença de distúrbios do sono. Se um doente desenvolver sonolência diurna ou episódios de adormecimento durante actividades que exigem participação activa (por exemplo, conversas, comer, etc.), Comtan deve ser normalmente interrompido (ver DATA E ADMINISTRAÇÃO para orientação sobre a interrupção do Comtan). Se a decisão é de continuar com Comtan, os doentes devem ser aconselhados a não conduzir e evitar outras actividades potencialmente perigosas. Há informação insuficiente para determinar se a redução da dose irá eliminar episódios de adormecimento durante atividades da vida diária.
PRECAUCAO
Hipotensão, Hipotensão Ortostática E Síncope
A terapêutica dopaminérgica em doentes com doença de Parkinson tem foi associada a hipotensão ortostática. A entacapona aumenta a levodopa a biodisponibilidade e, portanto, é de esperar que aumente a ocorrência de hipotensão ortostática. Em estudos controlados, aproximadamente 1, 2% e 0, 8% dos 200 mg de entacapona e placebo, respectivamente, notificaram pelo menos um episódio de síncope. As notificações de síncope foram geralmente mais frequentes em doentes em ambos os grupos de tratamento que tiveram um episódio de hipotensão documentada.
Alucinações E Comportamento Psicótico
Terapêutica dopaminérgica em doentes com doença de Parkinson tem sido associada a alucinações. Em estudos clínicos, alucinações levou à interrupção do fármaco e à interrupção prematura em 0, 8% e 0% dos doentes tratados com 200 mg de Comtan e placebo, respectivamente. As alucinações levaram a hospitalização em 1, 0% e 0, 3% dos doentes nos 200 mg de Comtan e placebo grupos, respectivamente. Ocorreu agitação em 1% dos doentes tratados com COMTAN e 0% tratados com placebo.
Os relatórios pós-comercialização indicam que os experiência de novo ou agravamento do estado mental e alterações comportamentais, que podem ser grave, incluindo comportamento tipo psicótico durante o tratamento com Comtan ou após iniciar ou aumentar a dose de Comtan. Outros medicamentos prescritos para melhorar os sintomas da doença de Parkinson podem ter efeitos semelhantes no pensamento e comportamento. Pensamento e comportamento anormais podem causar ideação paranóica, delírios, alucinações, confusão, desorientação, comportamento agressivo, agitação e delírio. Comportamentos do tipo psicótico foram também observados durante a desenvolvimento clínico do Comtan.
Doentes com perturbações psicóticas major devem normalmente não ser tratado com Comtan devido ao risco de exacerbação psicose. Além disso, certos medicamentos utilizados no tratamento da psicose podem exacerbar os sintomas da doença de Parkinson e pode diminuir a eficácia do Comtan.
Controlo De Impulsos E Comportamentos Compulsivos
As notificações pós-comercialização sugerem que os doentes tratados com medicamentos anti-Parkinson podem experimentar impulsos intensos para jogar, aumento impulsos sexuais, impulsos intensos para gastar dinheiro incontrolável, e outros intensos Instar. Os doentes podem ser incapazes de controlar estes impulsos enquanto tomam um ou mais dos medicamentos utilizados para o tratamento da doença de Parkinson e que aumentam o tom dopaminérgico central, incluindo o Comtan tomado com levodopa e carbidopa. Em alguns casos, embora nem todos, estes impulsos foram reportados para interromperam quando a dose de medicamentos anti-Parkinson foi reduzida ou descontinuado. Porque os doentes podem não reconhecer estes comportamentos como anormais. é importante que os médicos prescritores perguntem especificamente aos doentes ou aos seus prestadores de cuidados sobre o desenvolvimento de novos ou maiores impulsos de jogo, desejos sexuais, despesa descontrolada ou outros impulsos durante o tratamento com entacapona. Os médicos devem considerar a redução da dose ou a interrupção do Comtan se um doente desenvolve estes impulsos enquanto toma Comtan
Diarreia E Colite
Em estudos clínicos, a diarreia desenvolveu-se em 60 de 603 (10%) e 16 de 400 (4%) dos doentes tratados com 200 mg de Comtan e placebo, respectivamente. Em doentes tratados com Comtan, a diarreia foi geralmente ligeira a gravidade moderada (8.6%) , mas foi considerado grave em 1.3%. Diarreia resultou na retirada de 10 de 603 (1.7%).2%) com diarreia moderada e 3 (0.5%) com diarreia grave. Diarreia geral resolvido após interrupção do Comtan. Dois doentes com diarreia foram internar. Normalmente, a diarréia apresenta dentro de 4 semanas a 12 semanas após entacapone é iniciado, mas pode aparecer tão cedo quanto a primeira semana e tão tarde tantos meses após o início do tratamento. Diarreia pode estar associada com perda de peso, desidratação e hipocaliemia
A experiência pós-comercialização demonstrou que a diarréia pode ser um sinal de colite microscópica induzida por fármacos, principalmente colite linfocítica. Em estes casos diarreia tem sido geralmente moderada a grave, aguado, e não sangrento, por vezes associado a desidratação, dor abdominal, perda de peso, e hipocaliemia. Na maioria dos casos, diarreia e outras colites relacionadas os sintomas resolveram-se ou melhoraram significativamente quando o tratamento com Comtan foi interrompido. Em alguns doentes com colite confirmada por biopsia, a diarreia tinha resolvido ou melhorou significativamente após a descontinuação de Comtan, mas voltou após retratamento com Comtan.
Se a diarreia prolongada é suspeita de estar relacionada com Comtan, o medicamento deve ser interrompido e deve ser feita uma terapêutica médica apropriada. considerado. Se a causa da diarreia prolongada permanece obscura ou continua depois de parar o entacapone, em seguida, outras investigações de diagnóstico, incluindo a colonoscopia e as biopsias devem ser consideradas.
Discinesia
Comtan pode potenciar os efeitos secundários dopaminérgicos do levodopa e pode causar ou exacerbar disquinesia pré-existente. Embora diminuir a dose de levodopa pode melhorar este efeito secundário, muitos doentes em estudos controlados, a redução da dose de levodopa. A incidência de discinésia foi de 25% para tratamento com Comtan e 15% para placebo. Incidência da abstinência do estudo para a discinésia foi de 1, 5% para 200 mg de Comtan e de 0, 8% para o placebo.
Outros Acontecimentos Notificados Com Terapêutica Dopaminérgica
Os eventos listados abaixo são eventos associados com o uso de medicamentos que aumentam a actividade dopaminérgica.
Rabdomiólise
Foram notificados casos de rabdomiólise grave. após a aprovação do Comtan. Embora as reacções tipicamente tenham ocorrido enquanto os doentes foram tratados com Comtan, a natureza complicada destes casos torna difícil determinar qual o papel, se é que algum, que o Comtan desempenhou nos seus patogenese. A actividade motora prolongada grave, incluindo discinesia, pode ter para rabdomiólise. Os sinais e sintomas incluem febre, alteração da consciência, mialgia, valores aumentados de creatina fosfoquinase (CPK) e mioglobina (ver PRECAUCAO, Outros Concorrentes Notificados Com Dopaminérgico Terapia).
Hiperpirexia e confusão
Casos de um complexo de sintomas semelhante a neurolépticos síndrome maligna (SMN) caracterizada por temperatura elevada, muscular foram notificados casos de rigidez, alteração da consciência e elevação da CPK em doentes com insuficiência renal crónica. associação com a rápida redução da dose ou suspensão de outros dopaminérgicos droga. Na maioria destes casos, os sintomas começaram após uma interrupção abrupta dos tratamento com entacapona ou redução da sua dose, ou após o início da tratamento com entacapona. A natureza complicada destes casos torna-o difícil determinar que papel, se algum, Comtan pode ter desempenhado em patogenese. Não foram notificados casos após a retirada abrupta ou redução da dose do tratamento com entacapona durante estudos clínicos
Os médicos prescritores devem ter precaução quando interrompem o tratamento. tratamento com entacapone. Quando necessário, deve proceder-se à retirada. lentamente. Se for tomada a decisão de interromper o tratamento com Comtan, as recomendações incluem a monitorização cuidadosa do doente e o ajuste da dose. tratamentos dopaminérgicos, conforme necessário. Esta síndrome deve ser considerada na diagnóstico diferencial para qualquer doente que desenvolva febre elevada ou febre grave rigidez. O Comtan não foi sistematicamente avaliado.
Complicações Fibróticas
Casos de fibrose retroperitoneal, infiltrações pulmonares, foram notificados derrame pleural e espessamento pleural em alguns doentes. tratados com agentes dopaminérgicos derivados da cravagem de centeio. Estas complicações podem resolver quando a droga é descontinuada, mas a resolução completa nem sempre ocorre. Embora se considere que estes efeitos adversos estão relacionados com a ergolina estrutura destes compostos, quer outros, derivados de nonergot (e.g., entacapona) que aumentam a actividade dopaminérgica pode provocá-las é desconhecida. Ele note-se que a incidência esperada de complicações fibróticas é tão baixa que mesmo se entacapone causou estas complicações em taxas semelhantes às atribuível a outras terapêuticas dopaminérgicas, é improvável que tenha foi detectada numa coorte do tamanho exposto ao entacapone. Quatro caixas de foram notificados casos de fibrose pulmonar durante o desenvolvimento clínico da entacapona., três destes doentes foram também tratados com pergolida e um com bromocriptina. A duração do tratamento com entacapona variou entre 7 meses a 17 meses
Melanoma
Estudos epidemiológicos mostraram que doentes com A doença de Parkinson tem um risco mais elevado (2 a aproximadamente 6 vezes superior) de desenvolver melanoma do que a população em geral. Se o risco aumentado foi observado devido à doença de Parkinson ou a outros factores, tais como tratar a doença de Parkinson, não é claro.
Pelas razões acima expostas, os doentes e os prestadores de cuidados de saúde são aconselhado a monitorizar os melanomas com frequência e de forma regular ao utilizar Comtan para qualquer indicação. Idealmente, os exames periódicos da pele devem ser realizado por indivíduos devidamente qualificados (por exemplo, dermatologistas).
Toxicidade Renal
Num estudo de toxicidade com a duração de 1 ano, a entacapona (exposição plasmática 20 vezes superior à dose diária máxima recomendada no ser humano de 1. 600 mg) causou um aumento da incidência de nefrotoxicidade em ratos machos que foi caracterizado por túbulos regenerativos, espessamento de membranas basais, infiltração de células mononucleares e moldes tubulares de proteínas. Efeito não foram associados a alterações nos parâmetros de química clínica, e há nenhum método estabelecido para a monitorização da possível ocorrência destes lesões em humanos. Embora esta toxicidade possa representar uma espécie específica efeito, ainda não há provas de que assim seja.
hepatica
Os doentes com compromisso hepático devem ser tratados com cuidado. A AUC e a Cmax do entacapone duplicaram aproximadamente em doentes com doença hepática documentada em comparação com os controlos (ver FARMACOLOGIA CLÍNICA, Farmacocinética da Entacapona e DATA E ADMINISTRAÇÃO).
exame
Comtan é um quelante do ferro. O impacto da entacapona sobre as reservas de ferro do organismo são desconhecidas, no entanto, uma tendência para a diminuição do foram observadas concentrações de ferro em estudos clínicos. Num estudo níveis séricos de ferritina (como marcador de deficiência em ferro e subclínica anemia) não foram alterados com entacapona em comparação com o placebo após um ano de tratamento e não houve diferença nas taxas de anemia ou diminuição níveis de hemoglobina.
Populações Especiais
Os doentes com compromisso hepático devem ser tratados com atenção (ver INDICACAO, DATA E ADMINISTRAÇÃO).
Carcinogénese
Os estudos de carcinogenicidade de entacapona, com a duração de dois anos, foram realizado em ratinhos e ratos. Os ratos foram tratados uma vez por dia por sonda esofágica oral com doses de entacapona de 20, 90 ou 400 mg / kg. Um aumento da incidência de verificou-se a presença de adenomas e carcinomas tubulares em ratos do sexo masculino tratados com a dose mais elevada. dose de entacapona. As exposições plasmáticas (AUC) associadas a esta dose foram aproximadamente 20 vezes mais elevada do que a exposição plasmática estimada do ser humano receber a dose diária máxima recomendada (MRDD) de entacapone (1. 600 mg). Os ratinhos foram tratados uma vez por dia por sonda esofágica oral com doses de 20, 100 ou 600 mg / kg. de entacapona (0.05, 0.3, e 2 vezes o MRDD para o ser humano numa base de mg / m2). Devido a uma elevada incidência de mortalidade prematura em ratinhos que receberam a dose mais elevada de entacapona, o estudo com ratinhos não é uma avaliação adequada da carcinogenicidade. Embora não tenham sido observados tumores relacionados com o tratamento em animais ao receber as doses mais baixas, o potencial carcinogénico da entacapona não tem sido foi totalmente avaliada. O potencial carcinogénico da entacapona administrada em não foi avaliada a associação com levodopa e carbidopa.
Mutagénese
A entacapona foi mutagénica e clastogénica na in vitro rato linfoma tk clastogénico em linfócitos humanos cultivados na presença de metabolismo activacao. Entacapona, em monoterapia ou em combinação com levodopa e a carbidopa, não foi clastogénica na in vivo ensaio de micronúcleos em ratos ou mutagénico no ensaio de mutação reversa bacteriana (teste de Ames).
Diminuição Da Fertilidade
O Entacapone não afectou a fertilidade nem a desempenho reprodutivo em ratos tratados com até 700 mg / kg / dia (AUC do plasma) 28 vezes as do ser humano a receber o MRDD de 1.600 mg). Acasalamento tardio, mas não foi evidente diminuição da fertilidade em ratos fêmea tratados com 700 mg / kg / dia de entacapone.
Gravidez
Gravidez Categoria C
Em estudos de desenvolvimento embriofetal, a entacapona foi administrados a animais prenhes durante toda a organogénese em doses até 1. 000 mg / kg / dia em ratos e 300 mg / kg / dia em coelhos. Aumento da incidência de as variações fetais foram evidentes nas ninhadas de ratos tratados com as doses mais elevadas. dose, na ausência de sinais evidentes de toxicidade materna. O plasma materno a exposição ao fármaco (AUC) associada a esta dose foi aproximadamente 34 vezes superior à exposição ao fármaco. exposição plasmática estimada em seres humanos a receber a dose diária máxima recomendada dose (MRDD) de 1. 600 mg. Aumento da frequência de abortos, tardio e total foram observadas reabsorções e pesos fetais reduzidos nas ninhadas de coelhos tratados com doses maternalmente tóxicas de 100 mg/kg/dia (AUC plasmática 0.4 vezes aqueles em seres humanos que recebem o MRDD) ou maior. Não havia provas de teratogenicidade nestes estudos
No entanto, quando o entacapone foi administrado a ratos fêmeas antes do acasalamento e durante a gestação precoce, um aumento da incidência do olho fetal foram observadas anomalias (macrophthalmia, microftalmia, anoftalmia) no sistema nervoso central. ninhadas de mães tratadas com doses de 160 mg / kg / dia (AUCs plasmáticas 7 vezes superiores às em seres humanos a receber o MRDD) ou superiores, na ausência de toxicidade materna. Administração até 700 mg/kg/dia (AUC plasmática 28 vezes a do ser humano) receber o MRDD) a ratos fêmeas durante a última parte da gestação e durante todo o aleitamento não houve evidência de diminuição do desenvolvimento no descendência.
Entacapona é sempre administrado concomitantemente com levodopa e carbidopa, que é conhecida por causar malformações viscerais e esqueléticas em coelho. Potencial teratogénico do entacapone em combinação com levodopa e a carbidopa não foi avaliada em animais.
Não existe experiência de estudos clínicos relativamente a a utilização de Comtan em mulheres grávidas. Assim, Comtan deve ser utilizado durante gravidez apenas se os potenciais benefícios justificarem os potenciais riscos para o feto.
Mulheres A Amamentar
Em estudos em animais, o entacapone foi excretado na mãe. leite de rato.
Desconhece-se se a entacapona é excretada no ser humano. leite. Uma vez que muitos medicamentos são excretados no leite humano, devem ser tomadas precauções quando o entacapone é administrado a uma mulher a amamentar.
Uso Pediátrico
A segurança e eficácia em doentes pediátricos não foi estabelecida.

Ver INTERACCAO.

Gravidez Categoria C
Em estudos de desenvolvimento embriofetal, a entacapona foi administrados a animais prenhes durante toda a organogénese em doses até 1. 000 mg / kg / dia em ratos e 300 mg / kg / dia em coelhos. Aumento da incidência de as variações fetais foram evidentes nas ninhadas de ratos tratados com as doses mais elevadas. dose, na ausência de sinais evidentes de toxicidade materna. O plasma materno a exposição ao fármaco (AUC) associada a esta dose foi aproximadamente 34 vezes superior à exposição ao fármaco. exposição plasmática estimada em seres humanos a receber a dose diária máxima recomendada dose (MRDD) de 1. 600 mg. Aumento da frequência de abortos, tardio e total foram observadas reabsorções e pesos fetais reduzidos nas ninhadas de coelhos tratados com doses maternalmente tóxicas de 100 mg/kg/dia (AUC plasmática 0.4 vezes aqueles em seres humanos que recebem o MRDD) ou maior. Não havia provas de teratogenicidade nestes estudos
No entanto, quando o entacapone foi administrado a ratos fêmeas antes do acasalamento e durante a gestação precoce, um aumento da incidência do olho fetal foram observadas anomalias (macrophthalmia, microftalmia, anoftalmia) no sistema nervoso central. ninhadas de mães tratadas com doses de 160 mg / kg / dia (AUCs plasmáticas 7 vezes superiores às em seres humanos a receber o MRDD) ou superiores, na ausência de toxicidade materna. Administração até 700 mg/kg/dia (AUC plasmática 28 vezes a do ser humano) receber o MRDD) a ratos fêmeas durante a última parte da gestação e durante todo o aleitamento não houve evidência de diminuição do desenvolvimento no descendência.
Entacapona é sempre administrado concomitantemente com levodopa e carbidopa, que é conhecida por causar malformações viscerais e esqueléticas em coelho. Potencial teratogénico do entacapone em combinação com levodopa e a carbidopa não foi avaliada em animais.
Não existe experiência de estudos clínicos relativamente a a utilização de Comtan em mulheres grávidas. Assim, Comtan deve ser utilizado durante gravidez apenas se os potenciais benefícios justificarem os potenciais riscos para o feto.

Porque os estudos clínicos são conduzidos sob muito diferentes condições, a incidência de reações adversas (número de pacientes tendo uma reação adversa associada com o tratamento por número total de doentes tratados) observaram, em estudos clínicos de uma droga não pode ser diretamente comparada com a incidência de reações adversas em estudos clínicos, de outra droga, e podem não refletir a incidência de reações adversas observadas na prática.
Um total de 1.450 doentes com doença de Parkinson foram tratados com Comtan em estudos clínicos pré-comercialização. Foram incluídos doentes com sintomas flutuantes, bem como doentes com respostas estáveis à terapêutica com levodopa. No entanto, todos os doentes receberam tratamento concomitante com preparações de levodopa e foram semelhantes noutros aspectos clínicos.
As reacções adversas mais frequentemente observadas (incidência pelo menos 3% superior à do placebo) em estudos em dupla ocultação, controlados com placebo (N=1. 003) associados ao uso de Comtan foram: discinésia, descoloração da urina, diarreia, náuseas, hiperquinésia, dor abdominal, vómitos e boca seca. Aproximadamente 14% dos 603 doentes aos quais foi administrado entacapone nos estudos em dupla ocultação, controlados com placebo interromperam o tratamento devido a reacções adversas, em comparação com 9% dos 400 doentes que receberam placebo. As causas de interrupção mais frequentes, Por ordem decrescente, foram: perturbações do foro psiquiátrico (2% vs. 1%), diarreia (2% vs. 0%), discinésia e hiperquinésia (2% vs. 1%), náuseas (2% vs. 1%), e dor abdominal (1% vs. 0%)
Incidência De Acontecimentos Adversos Em Estudos Clínicos Controlados
A tabela 4 lista os acontecimentos adversos emergentes com o tratamento que ocorreram em pelo menos 1% dos doentes tratados com entacapone que participaram nos estudos em dupla ocultação, controlados com placebo e que foram numericamente mais frequentes no grupo Comtan, comparativamente ao placebo. Nestes estudos, foi adicionado Comtan ou placebo à levodopa e carbidopa (ou levodopa e benserazida).
Tabela 4: Resumo dos doentes com contactos concorrentes após o início do sistema de administração do sistema pelo menos 1% no grupo Comtan e superior ao Placebo
| CLASSES DE SISTEMAS DE ÓRGÃOS Termo preferido | Comtan | Placebo |
| (n = 603) | (N = 400)) | |
| % de doentes | % de doentes | |
| OPERAÇÕES DOS TECIDOS | ||
| Aumento da sudação | 2 | 1 |
| DOENÇAS DO SISTEMA MUSCULOSQUELÉTICO | ||
| Dor | 2 | 1 |
| DOENÇAS DO SISTEMA NERVOSO CENTRAL E PERIFÉRICO | ||
| Discinesia | 25 | 15 |
| Hipercinesia | 10 | 5 |
| Hipocinésia | 9 | 8 |
| Tontura | 8 | 6 |
| SENTIDOS ESPECIAIS, OUTRAS DOENÇAS | ||
| Alteração do paladar | 1 | 0 |
| PERTURBAÇÕES DO FORO PSIQUIÁTRICO | ||
| Ansiedade | 2 | 1 |
| Sonolência | 2 | 0 |
| Agitacao | 1 | 0 |
| DOENÇAS GASTROINTESTINAIS | ||
| Nausea | 14 | 8 |
| Diarréia | 10 | 4 |
| Dor | 8 | 4 |
| Prisão de ventre | 6 | 4 |
| Vomito | 4 | 1 |
| Secura de boca | 3 | 0 |
| Dispepsia | 2 | 1 |
| Flatulência | 2 | 0 |
| Gastrite | 1 | 0 |
| Doenças gastrointestinais | 1 | 0 |
| DOENÇAS RESPIRATORIAS | ||
| Dispneia | 3 | 1 |
| DOENÇAS DAS PLAQUETAS, DA HEMORRAGIA E DA COAGULAÇÃO | ||
| Purpura | 2 | 1 |
| DOENÇAS DO SISTEMA URINÁRIO | ||
| Descrição da urina | 10 | 0 |
| PERTURBAÇÕES GERAIS E ALTERAÇÕES NO LOCAL DE ADMINISTRAÇÃO | ||
| Dor | 4 | 2 |
| Fadiga | 6 | 4 |
| Astenia | 2 | 1 |
| PERTURBAÇÕES DO MECANISMO DE RESISTÊNCIA | ||
| Infecção bacteriana | 1 | 0 |
Efeitos Do Sexo E Da Idade Nas Reacções Adversas
Não se observaram diferenças na taxa de acontecimentos adversos atribuíveis ao entacapone por idade ou sexo.
Pós-Comercialização
As notificações espontâneas seguintes de acontecimentos adversos temporariamente associados com Comtan foram identificadas desde a introdução no mercado e não estão listadas no quadro 4. Uma vez que estas reacções são notificadas voluntariamente a partir de uma população de dimensão desconhecida, nem sempre é possível estimar de forma fiável a sua frequência ou estabelecer uma relação causal com a exposição ao Comtan.
Foi notificada hepatite com características principalmente colestáticas.

Os dados pós-comercialização incluem vários casos de sobredosagem. A dose mais elevada notificada de entacapona foi de pelo menos 40.000 mg. O agudo de sintomas e sinais comumente observados nestes casos incluídos sonolência e diminuição da atividade, os estados relacionados com deprimido nível de consciência (por exemplo, coma, confusão e desorientação) e descolorações da pele, língua, e urina, bem como inquietude, agitação e agressividade.
A inibição da COMT pelo tratamento com entacapone é dependente da dose. Uma sobredosagem maciça de Comtan (entacapone) pode, teoricamente, produzir uma inibição de 100% da enzima COMT no ser humano, impedindo assim o metabolismo dos catecóis endógenos e exógenos.
A dose diária mais elevada administrada ao ser humano foi de 2, 400 mg, administrada num estudo na forma de 400 mg seis vezes por dia com levodopa e carbidopa durante 14 dias em 15 doentes com doença de Parkinson, e noutro estudo na forma de 800 mg três vezes por dia durante 7 dias em 8 voluntários saudáveis. Nesta dose diária, as concentrações plasmáticas máximas de entacapona foram, em média, de 2.0 mcg por mL (45 minutos, em comparação com 1.0 mcg por mL e 1.2 mcg por mL com 200 mg de entacapona em 45 minutos). As dores abdominais e as fezes moles foram os acontecimentos adversos mais frequentemente observados durante este estudo.. Doses diárias 2.000 mg Comtan ter sido administrado como 200 mg 10 vezes ao dia, com levodopa e carbidopa ou levodopa e benserazide por pelo menos 1 ano em 10 pacientes, por pelo menos 2 anos em 8 pacientes e pelo menos 3 anos em 7 pacientes. Globalmente, contudo, a experiência clínica com doses diárias superiores a 1. 600 mg é limitada.
O intervalo de concentrações plasmáticas letais de entacapona, com base em dados em animais, foi de 80 mcg por mL a 130 mcg por mL em ratinhos. Foram observadas dificuldades respiratórias, ataxia, hipoactividade e convulsões em ratinhos após doses orais elevadas (gavage).
Tratamento Da Sobredosagem
Tratamento da sobredosagem com Comtan é sintomático, não existe antídoto conhecido para Comtan. Recomenda-se hospitalização e está indicada a prestação de cuidados gerais de suporte.. Não há experiência com hemodiálise ou hemoperfusão, mas é improvável que estes procedimentos sejam benéficos, porque Comtan está altamente ligado às proteínas plasmáticas.. Uma lavagem gástrica imediata e doses repetidas de carvão vegetal ao longo do tempo podem acelerar a eliminação do Comtan diminuindo a sua absorção e reabsorção a partir do tracto gastrointestinal (GI).. A adequação dos sistemas respiratório e circulatório deve ser cuidadosamente monitorizada e devem ser utilizadas medidas de suporte adequadas. Deve ter-se em conta a possibilidade de Interacções medicamentosas, especialmente com medicamentos estruturados em catecol.

Fev 2016
However, we will provide data for each active ingredient
Disponível em países
 Argentina
Argentina Australia
Australia Austria
Austria Bangladesh
Bangladesh Belgium
Belgium Brazil
Brazil Bulgaria
Bulgaria Canada
Canada China
China Croatia (Hrvatska)
Croatia (Hrvatska) Cyprus
Cyprus Czech Republic
Czech Republic Denmark
Denmark Ecuador
Ecuador Egypt
Egypt Estonia
Estonia Finland
Finland France
France Germany
Germany Greece
Greece Hong Kong
Hong Kong Hungary
Hungary Iceland
Iceland Indonesia
Indonesia Ireland
Ireland Israel
Israel Italy
Italy Japan
Japan Latvia
Latvia Liechtenstein
Liechtenstein Lithuania
Lithuania Luxembourg
Luxembourg Malaysia
Malaysia Malta
Malta Netherlands
Netherlands New Zealand
New Zealand Norway
Norway Peru
Peru Philippines
Philippines Poland
Poland Portugal
Portugal Romania
Romania Serbia
Serbia Slovakia
Slovakia Slovenia
Slovenia South Africa
South Africa Spain
Spain Sweden
Sweden Switzerland
Switzerland Taiwan
Taiwan Thailand
Thailand Tunisia
Tunisia Turkey
Turkey United Kingdom
United Kingdom USA
USA Venezuela
Venezuela
