Composición:
Usado en tratamiento:
Revisión médica por Militian Inessa Mesropovna Última actualización de farmacia el 15.03.2022

¡Atención! ¡La información en la página es solo para profesionales médicos! ¡La información se recopila en Fuentes abiertas y puede contener errores significativos! ¡Tenga cuidado y vuelva a verificar toda la información de esta página!
Los 20 mejores medicamentos con los mismos ingredientes:


Formas de dosificación y fortalezas
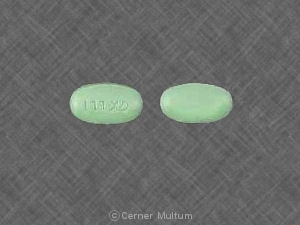
TRIZIVIR las tabletas contienen 300 mg de abacavir como abacavir sulfato, 150 mg de lamivudina y 300 mg de zidovudina. Las tabletas son azul verdoso, en forma de cápsula, recubierto con película e impreso con "GX LL1" en uno lado sin marcas en el reverso.
Almacenamiento y manejo
TRIZIVIR está disponible en tabletas. Cada tableta contiene 300 mg de abacavir como sulfato de abacavir, 150 mg de lamivudina y 300 mg de zidovudina. Las tabletas tienen forma de cápsula azul-verde, recubiertas con película y impreso con GX LL1 en un lado sin marcas en el reverso. Ellos se empaquetan de la siguiente manera:
Botellas de 60 tabletas (NDC 49702-217-18).
Almacenar a 25 ° C (77 ° F); excursiones permitidas a 15 ° a 30 ° C (59 ° a 86 ° F) (ver Temperatura ambiente controlada por USP).
Fabricado para: ViiV Healthcare, Research Triangle Park, NC 27709 por: GlaxoSmithKline Research Triangle Park, NC 27709. Revisado: septiembre de 2015

TRIZIVIR se indica en combinación con otros antirretrovirales o solos para el tratamiento del tipo de virus de inmunodeficiencia humana 1 infección (VIH-1).
Limitaciones de uso
- Existen datos limitados sobre el uso de TRIZIVIR solo en pacientes con niveles de carga viral basal más altos (más de 100,000 copias por ml).

Detección de HLA-B * 5701 Alelo antes del inicio TRIZIVIR
Pantalla para el alelo HLA-B * 5701 antes de iniciar terapia con TRIZIVIR .
Dosis recomendada para adultos y pacientes pediátricos Pesaje al menos 40 kg
La dosis recomendada de TRIZIVIR es una tableta tomada oralmente dos veces al día con o sin comida.
No recomendado debido a la falta de ajuste de dosis
Porque TRIZIVIR es una tableta de dosis fija y no puede serlo ajustado a la dosis, TRIZIVIR no se recomienda en :
- pacientes pediátricos que pesan menos de 40 kg
- pacientes con aclaramiento de creatinina inferior a 50 ml por minuto
- pacientes con insuficiencia hepática leve. TRIZIVIR es contraindicado en pacientes con insuficiencia hepática moderada o grave.

TRIZIVIR está contraindicado en pacientes:
- que tienen el alelo HLA-B * 5701.
- con reacción de hipersensibilidad previa a abacavir, lamivudina o zidovudina.
- con insuficiencia hepática moderada o grave.

ADVERTENCIAS
Incluido como parte de la PRECAUCIONES sección.
PRECAUCIONES
Reacciones de hipersensibilidad
Reacciones de hipersensibilidad graves y a veces fatales han ocurrido con abacavir, un componente de TRIZIVIR. Estas hipersensibilidad Las reacciones han incluido insuficiencia multiorgánica y anafilaxia y típicamente ocurrió dentro de las primeras 6 semanas de tratamiento con abacavir (tiempo medio para el inicio fue de 9 días); aunque se han producido reacciones de hipersensibilidad a abacavir en cualquier momento durante el tratamiento. Pacientes que portan el alelo HLA-B * 5701 tiene un mayor riesgo de hipersensibilidad al abacavir reacciones; aunque, los pacientes que no llevan el alelo HLA-B * 5701 sí lo tienen desarrolló reacciones de hipersensibilidad. Se informó hipersensibilidad al abacavir en aproximadamente 206 (8%) de 2,670 pacientes en 9 ensayos clínicos con productos que contienen abacavir donde no se realizó la detección de HLA-B * 5701. Los La incidencia de sospechas de reacciones de hipersensibilidad a abacavir en ensayos clínicos fue 1% cuando los sujetos que portan el alelo HLA-B * 5701 fueron excluidos. En cualquier paciente tratado con abacavir, el diagnóstico clínico de la reacción de hipersensibilidad debe ser seguir siendo la base de la toma de decisiones clínicas.
Debido al potencial de severidad, grave y posiblemente reacciones de hipersensibilidad fatal con abacavir :
- Todos los pacientes deben ser examinados para detectar el alelo HLA-B * 5701 antes de iniciar la terapia con TRIZIVIR o reiniciar la terapia con TRIZIVIR, a menos que los pacientes tengan un alelo HLA-B * 5701 previamente documentado evaluación.
- TRIZIVIR está contraindicado en pacientes con experiencia previa reacción de hipersensibilidad a abacavir y en pacientes con HLA-B * 5701 positivo.
- Antes de comenzar TRIZIVIR, revise el historial médico de exposición previa a cualquier producto que contenga abacavir. NUNCA reinicie TRIZIVIR o ninguno otro producto que contiene abacavir después de una reacción de hipersensibilidad abacavir, independientemente del estado HLA-B * 5701.
- Para reducir el riesgo de una hipersensibilidad potencialmente mortal reacción, independientemente del estado HLA-B * 5701, suspenda TRIZIVIR inmediatamente si Se sospecha una reacción de hipersensibilidad, incluso cuando hay otros diagnósticos posible (p. ej., enfermedades respiratorias de inicio agudo como neumonía, bronquitis, faringitis o influenza; gastroenteritis; o reacciones a otros medicamentos).
- Si no se puede descartar una reacción de hipersensibilidad, hágalo no reinicie TRIZIVIR o cualquier otro producto que contenga abacavir porque más síntomas graves, que pueden incluir hipotensión potencialmente mortal y muerte, can ocurrir en cuestión de horas.
- Si se descarta una reacción de hipersensibilidad, los pacientes pueden hacerlo reiniciar TRIZIVIR. En raras ocasiones, los pacientes que han detenido abacavir por otras razones que los síntomas de hipersensibilidad también han sufrido amenazas para la vida reacciones a las pocas horas de reiniciar la terapia con abacavir. Por lo tanto, reintroducción de TRIZIVIR o cualquier otro producto que contenga abacavir se recomienda solo si Se puede acceder fácilmente a la atención médica.
- Una guía de medicamentos y una tarjeta de advertencia que proporcionan debe haber información sobre el reconocimiento de las reacciones de hipersensibilidad a abacavir dispensado con cada nueva receta y recarga.
Toxicidad hematológica / Supresión de médula ósea
La zidovudina, un componente de TRIZIVIR, se ha asociado con toxicidad hematológica que incluye neutropenia y anemia, particularmente en pacientes con enfermedad avanzada por VIH-1. TRIZIVIR debe usarse con precaución en pacientes que tienen compromiso de médula ósea evidenciado por el recuento de granulocitos menos de 1,000 células por mm³ o hemoglobina menos de 9.5 gramos por dL
Los recuentos sanguíneos frecuentes son muy recomendables en pacientes con enfermedad avanzada por VIH-1 que son tratados con TRIZIVIR. Periódico Se recomiendan recuentos sanguíneos para otros pacientes infectados con VIH-1. Si anemia o se desarrolla neutropenia, puede ser necesaria la interrupción de la dosis.
Miopatía
Miopatía y miositis, con cambios patológicos similares a la producida por la enfermedad del VIH-1, se han asociado con el uso prolongado de zidovudina y, por lo tanto, puede ocurrir con terapia con TRIZIVIR
Acidosis láctica y hepatomegalia severa con esteatosis
Acidosis láctica y hepatomegalia severa con esteatosis incluidos casos fatales, se han informado con el uso de análogos de nucleósidos y otros antirretrovirales. Consulte la información de prescripción completa para ZIAGEN® (abacavir), EPIVIR® (lamivudina) y RETROVIR® (zidovudina). Tratamiento con TRIZIVIR debe suspenderse en cualquier paciente que desarrolle clínica o hallazgos de laboratorio que sugieren acidosis láctica o hepatotoxicidad pronunciada (que puede incluir hepatomegalia y esteatosis incluso en ausencia de marcado elevaciones de transaminasas).
Pacientes con coinfección por el virus de la hepatitis B
Exacerbaciones posteriores al tratamiento de la hepatitis
Evidencia clínica y de laboratorio de exacerbaciones de La hepatitis ha ocurrido después de la interrupción de lamivudina. Ver lleno prescripción de información para EPIVIR (lamivudina). Los pacientes deben estar cerca monitoreado con seguimiento clínico y de laboratorio durante al menos varios meses después de suspender el tratamiento.
Aparición del VHB resistente a la lamivudina
La seguridad y la eficacia de lamivudina no lo han sido establecido para el tratamiento de la hepatitis B crónica en sujetos con infección doble con VIH-1 y VHB. Aparición de variantes del virus de la hepatitis B asociadas con Se ha informado resistencia a la lamivudina en sujetos infectados con VIH – 1 que sí lo han hecho recibió regímenes antirretrovirales que contienen lamivudina en presencia de infección concurrente con el virus de la hepatitis B. Ver prescripción completa información para EPIVIR (lamivudina).
Úselo con regímenes basados en interferón y ribavirina
Pacientes que reciben interferón alfa con o sin ellos la ribavirina y TRIZIVIR deben controlarse de cerca para determinar si están asociados con el tratamiento toxicidades, especialmente descompensación hepática, neutropenia y anemia. Ver lleno prescripción de información para EPIVIR (lamivudina) y RETROVIR (zidovudina). La interrupción de TRIZIVIR debe considerarse médicamente apropiada. Dosis reducción o interrupción de interferón alfa, ribavirina, o ambos también deberían hacerlo ser considerado si se observan empeoramiento de las toxicidades clínicas, incluido el hepático descompensación (p. ej., Child-Pugh mayor que 6) (ver prescripción completa información para interferón y ribavirina).
Se ha informado exacerbación de la anemia en el VIH-1 / VHC pacientes coinfectados que reciben ribavirina y zidovudina. Administración conjunta de ribavirina y TRIZIVIR no se recomienda.
Síndrome de Reconstitución Inmune
Se ha informado el síndrome de reconstitución inmune en pacientes tratados con terapia antirretroviral combinada, incluido TRIZIVIR Durante la fase inicial del tratamiento antirretroviral combinado, los pacientes cuyo sistema inmunitario responde puede desarrollar una respuesta inflamatoria a indolente o infecciones oportunistas residuales (como la infección por Mycobacterium avium) citomegalovirus, neumonía por Pneumocystis jirovecii [PCP] o tuberculosis) que puede requerir una mayor evaluación y tratamiento.
Trastornos autoinmunes (como la enfermedad de Graves) También se ha informado que la polimiositis y el síndrome de Guillain-Barré) ocurren en el establecimiento de la reconstitución inmune; sin embargo, el tiempo de inicio es mayor variable, y puede ocurrir muchos meses después del inicio del tratamiento.
Redistribución gorda
Redistribución / acumulación de grasa corporal, incluida la central obesidad, agrandamiento de la grasa dorsocervical (joroba de búfalo), desgaste periférico han sido desperdicios faciales, aumento de senos y "apariencia cushingoide" observado en pacientes que reciben terapia antirretroviral. El mecanismo y Las consecuencias a largo plazo de estos eventos son actualmente desconocidas. Una causalidad La relación no se ha establecido.
Infarto de miocardio
En una perspectiva publicada, observacional, ensayo epidemiológico diseñado para investigar la tasa de infarto de miocardio (MI) en pacientes en terapia antirretroviral combinada, el uso de abacavir en los 6 meses anteriores se correlacionó con un mayor riesgo de IM. En un análisis agrupados de ensayos clínicos realizados por el patrocinador, no hubo un riesgo excesivo de IM observado en sujetos tratados con abacavir en comparación con sujetos de control. En totalidad, los datos disponibles de la cohorte observacional y de la clínica los ensayos no son concluyentes.
Como precaución, el riesgo subyacente del corazón coronario la enfermedad debe considerarse al recetar terapias antirretrovirales incluyendo abacavir y medidas tomadas para minimizar todos los factores de riesgo modificables (p. ej., hipertensión, hiperlipidemia, diabetes mellitus, tabaquismo).
Pacientes con experiencia en terapia
En ensayos clínicos, sujetos con previo prolongado exposición al inhibidor de la transcriptasa inversa nucleósido (NRTI) o que tenía VIH-1 aislamientos que contenían múltiples mutaciones que confieren resistencia a los INTI respuesta limitada al abacavir. El potencial de resistencia cruzada entre abacavir y otros INTI deben considerarse al elegir nuevos terapéuticos regímenes en pacientes con experiencia en terapia.
Productos relacionados que no están recomendados
TRIZIVIR es una combinación de dosis fija de 3 nucleósidos inhibidores análogos de la transcriptasa inversa (abacavir, lamivudina y zidovudina). Administración concomitante de TRIZIVIR con otros productos no se recomienda contener abacavir, lamivudina o zidovudina. Además, no administre TRIZIVIR en combinación con productos que contengan emtricitabina.
Información de asesoramiento del paciente
Aconseje al paciente que lea al paciente aprobado por la FDA etiquetado (Guía de medicación).
Reacción de hipersensibilidad
Informar a los pacientes
- que una guía de medicación y una tarjeta de advertencia que resume el síntomas de la reacción de hipersensibilidad a abacavir y otros productos el farmacéutico dispensará información con cada nueva receta y recargue TRIZIVIR e indique al paciente que lea la Guía de medicamentos y Tarjeta de advertencia cada vez para obtener cualquier información nueva que pueda estar presente TRIZIVIR. El texto completo de la Guía de medicamentos se reproduce al final de este documento.
- para llevar la tarjeta de advertencia con ellos.
- cómo identificar una reacción de hipersensibilidad.
- que si desarrollan síntomas consistentes con a reacción de hipersensibilidad deberían llamar a su proveedor de atención médica de inmediato para determinar si deben dejar de tomar TRIZIVIR .
- que una reacción de hipersensibilidad puede empeorar y conducir a hospitalización o muerte si TRIZIVIR no se suspende de inmediato.
- para no reiniciar TRIZIVIR o cualquier otro que contenga abacavir producto después de una reacción de hipersensibilidad porque pueden aparecer síntomas más graves ocurrir en cuestión de horas y puede incluir hipotensión potencialmente mortal y muerte.
- que una reacción de hipersensibilidad suele ser reversible si se detecta rápidamente y TRIZIVIR se detiene de inmediato.
- que si han interrumpido TRIZIVIR por otras razones que síntomas de hipersensibilidad (por ejemplo, aquellos que tienen una interrupción en el suministro de medicamentos), puede ocurrir una reacción de hipersensibilidad grave o fatal reintroducción de abacavir.
- para no reiniciar TRIZIVIR o cualquier otro que contenga abacavir producto sin consulta médica y solo si la atención médica puede ser fácil accedido por el paciente u otros.
Productos relacionados que no están recomendados
Informe a los pacientes que no deben tomar TRIZIVIR ATRIPLA®, COMBIVIR, COMPLERA®, DUTREBIS™, EMTRIVA®, EPIVIR, EPIVIR-HBV®, EPZICOM® , RETROVIR, STRIBILD®, TRIUMEQ®, TRUVADA®, o ZIAGEN .
Neutropenia y Anemia
Informe a los pacientes que las toxicidades importantes asociadas con zidovudina son neutropenia y / o anemia. Infórmeles de la extrema importancia de que sus recuentos sanguíneos se sigan de cerca durante la terapia, especialmente para pacientes con enfermedad avanzada por VIH-1.
Miopatía
Informe a los pacientes con miopatía y miositis Los cambios patológicos, similares a los producidos por la enfermedad del VIH-1, han sido asociado con el uso prolongado de zidovudina.
Acidosis láctica / Hepatomegalia
Informe a los pacientes que algunos medicamentos contra el VIH, incluidos TRIZIVIR, puede causar una condición rara pero grave llamada acidosis láctica agrandamiento del hígado (hepatomegalia).
Pacientes con coinfección por hepatitis B o C
Informe a los pacientes coinfectados con VIH-1 y VHB que El empeoramiento de la enfermedad hepática ha ocurrido en algunos casos cuando se trata con él lamivudina fue descontinuada. Aconseje a los pacientes que discutan cualquier cambio en el régimen con su médico.
Informe a los pacientes con coinfección por VIH-1 / VHC que sea hepática se ha producido descompensación (algunas fatales) en pacientes coinfectados con VIH-1 / VHC recibir terapia antirretroviral combinada para VIH-1 e interferón alfa con o sin ribavirina.
Síndrome de Reconstitución Inmune
En algunos pacientes con infección avanzada por VIH, signos y Los síntomas de inflamación de infecciones previas pueden ocurrir poco después del anti-VIH Se inicia el tratamiento. Se cree que estos síntomas se deben a un mejora en la respuesta inmune del cuerpo, permitiendo que el cuerpo luche infecciones que pueden haber estado presentes sin síntomas obvios. Asesorar a los pacientes informar a su proveedor de atención médica de inmediato sobre cualquier síntoma de infección.
Redistribución / Acumulación de grasa corporal
Informar a los pacientes que redistribución o acumulación de la grasa corporal puede ocurrir en pacientes que reciben terapia antirretroviral y que el La causa y los efectos a largo plazo en la salud de estas afecciones no se conocen en esto hora.
Información sobre la infección por VIH-1
TRIZIVIR no es una cura para la infección por VIH-1 y los pacientes puede continuar experimentando enfermedades asociadas con la infección por VIH-1, incluyendo infecciones oportunistas. Los pacientes deben permanecer en terapia continua contra el VIH controlar la infección por VIH-1 y disminuir la enfermedad relacionada con el VIH. Informar a los pacientes que Las disminuciones sostenidas en el ARN del VIH en plasma se han asociado con un riesgo reducido de progresión al SIDA y la muerte.
Aconseje a los pacientes que permanezcan bajo el cuidado de un médico cuando use TRIZIVIR. Aconseje a los pacientes que tomen todos los medicamentos contra el VIH exactamente como prescrito. Aconseje a los pacientes que eviten hacer cosas que puedan propagarse por el VIH-1 infección a otros.
Aconseje a los pacientes que no vuelvan a usar o compartan agujas u otras equipo de inyección.
Aconseje a los pacientes que no compartan artículos personales que puedan tener sangre o fluidos corporales sobre ellos, como cepillos de dientes y cuchillas de afeitar.
Aconseje a los pacientes que siempre practiquen sexo seguro usando a condón de látex o poliuretano para reducir la posibilidad de contacto sexual con el semen secreciones vaginales o sangre.
Se debe aconsejar a las pacientes que no amamanten. Las madres con VIH-1 no deben amamantar porque el VIH-1 puede transmitirse a la bebé en la leche materna.
Indique a los pacientes que si omiten una dosis, deberían hacerlo tómalo tan pronto como lo recuerden. Si no recuerdan hasta que sea hora de hacerlo la siguiente dosis, se les debe indicar que omitan la dosis omitida y vuelvan a ella El horario regular. Los pacientes no deben duplicar su próxima dosis o tomar más que la dosis prescrita.
Indique a los pacientes que lean el Guía de medicación antes comenzar TRIZIVIR y volver a leerlo cada vez que se renueve la receta. Indique a los pacientes que informen a su médico o farmacéutico si desarrollan alguno síntoma inusual, o si algún síntoma conocido persiste o empeora.
Toxicología no clínica
Carcinogénesis, mutagénesis, deterioro de la fertilidad
Carcinogenicidad
Abacavir: Abacavir se administró por vía oral a las 3 niveles de dosificación para separar grupos de ratones y ratas en carcinogenicidad de 2 años estudios. Los resultados mostraron un aumento en la incidencia de malignos y tumores no malignos. Los tumores malignos ocurrieron en la glándula prepucial de los machos y la glándula del clítoris de las hembras de ambas especies, y en el hígado de la hembra ratas. Además, también se produjeron tumores no malignos en el hígado y la tiroides glándula de ratas hembras. Estas observaciones se hicieron a exposiciones sistémicas en el rango de 6 a 32 veces la exposición humana a la dosis recomendada de 600 mg.
Lamivudina: Estudios de carcinogenicidad a largo plazo con lamivudina en ratones y ratas no mostró evidencia de potencial carcinogénico en exposiciones hasta 10 veces (ratones) y 58 veces (ratas) las exposiciones humanas en el dosis recomendada de 300 mg.
Zidovudina: La zidovudina se administró por vía oral a 3 niveles de dosificación para separar grupos de ratones y ratas (60 hembras y 60 machos adentro cada grupo). Las dosis diarias únicas iniciales fueron 30, 60 y 120 mg por kg por día en ratones y 80, 220 y 600 mg por kg por día en ratas. Las dosis en ratones fueron reducido a 20, 30 y 40 mg por kg por día después del día 90 debido a anemia relacionada con el tratamiento, mientras que en ratas solo la dosis alta se redujo a 450 mg por kg por día en el día 91 y luego a 300 mg por kg por día en el día 279.
En ratones, 7 vaginales de aparición tardía (después de 19 meses) neoplasias (5 carcinomas de células escamosas no metástasis, 1 célula escamosa papiloma y 1 pólipo escamoso) ocurrieron en animales que recibieron la dosis más alta. Un papiloma de células escamosas de aparición tardía ocurrió en la vagina de a animal de dosis media. No se encontraron tumores vaginales en la dosis más baja.
En ratas, 2 de aparición tardía (después de 20 meses) los carcinomas de células escamosas vaginales no metástasis ocurrieron en animales dados el dosis más alta. No se produjeron tumores vaginales a la dosis baja o media en ratas. No Se observaron otros tumores relacionados con drogas en cualquier sexo de cualquiera de las especies.
A dosis que produjeron tumores en ratones y ratas, el la exposición estimada al fármaco (medida por AUC) fue aproximadamente 3 veces (ratón) y 24 veces (rata) la exposición humana estimada en el terapéutico recomendado dosis de 100 mg cada 4 horas.
No se sabe cuán predictivos son los resultados del roedor Los estudios de carcinogenicidad pueden ser para humanos.
Se realizaron dos estudios de carcinogenicidad transplacentaria en ratones. Un estudio administró zidovudina a dosis de 20 mg por kg por día o 40 mg por kg por día desde el día de gestación 10 hasta el parto y la lactancia con la dosificación continua en la descendencia durante 24 meses después del parto. A estas dosis, las exposiciones fueron aproximadamente 3 veces la exposición humana estimada en el dosis recomendadas. Después de 24 meses a la dosis de 40 mg por kg por día, an Se observó un aumento en la incidencia de tumores vaginales sin aumento en los tumores el hígado o el pulmón o cualquier otro órgano en cualquier género. Estos hallazgos son consistente con los resultados del estudio estándar de carcinogenicidad oral en ratones, as descrito anteriormente. Un segundo estudio administró zidovudina al máximo tolerado dosis de 12.5 mg por día o 25 mg por día (aproximadamente 1,000 mg por kg peso corporal no embarazado o aproximadamente 450 mg por kg de peso corporal a término) a ratones preñados de los días 12 a 18 de gestación. Hubo un aumento en La cantidad de tumores en el pulmón, el hígado y las vías reproductivas femeninas en el descendencia de ratones que reciben el nivel de dosis más alto de zidovudina.
Mutagenicidad
Abacavir: Abacavir indujo aberraciones cromosómicas tanto en presencia como en ausencia de activación metabólica en an in vitro citogenético estudio en linfocitos humanos. El abacavir fue mutagénico en ausencia de metabólico activación, aunque no fue mutagénico en presencia de metabólico activación en un ensayo de linfoma de ratón L5178Y. El abacavir fue clastogénico en los hombres y no clastogénico en mujeres en an in vivo micronúcleos de médula ósea de ratón ensayo. Abacavir no fue mutagénico en los ensayos de mutagenicidad bacteriana en el presencia y ausencia de activación metabólica.
Lamivudina: La lamivudina fue mutagénica en un L5178Y ensayo de linfoma de ratón y clastogénico en un ensayo citogenético utilizando cultivado linfocitos humanos. La lamivudina no fue mutagénica en una mutagenicidad microbiana ensayo, en un in vitro ensayo de transformación celular, en una prueba de micronúcleos de rata, en un ensayo citogenético de médula ósea de rata y en un ensayo para ADN no programado síntesis en hígado de rata.
Zidovudina: La zidovudina fue mutagénica en un L5178Y ensayo de linfoma de ratón, positivo en an in vitro ensayo de transformación celular, clastogénico en un ensayo citogenético con linfocitos humanos cultivados, y positivo en pruebas de micronúcleos de ratón y rata después de dosis repetidas. Era negativo en un estudio citogenético en ratas que recibieron una dosis única.
Deterioro de la fertilidad
Abacavir o Lamivudina: Abacavir o lamivudina lo hicieron no afecta la fertilidad masculina o femenina en ratas a una dosis asociada con exposiciones aproximadamente 8 o 130 veces, respectivamente, más que las exposiciones en humanos a las dosis de 600 mg y 300 mg (respectivamente).
Zidovudina: Zidovudina, administrada a hombres y ratas hembras a dosis de hasta 7 veces la dosis habitual para adultos según la superficie corporal consideraciones de área, no tuvo efecto sobre la fertilidad juzgada por las tasas de concepción.
Uso en poblaciones específicas
Embarazo
Embarazo Categoría C
No hay estudios adecuados y bien controlados de TRIZIVIR en mujeres embarazadas. Estudios de reproducción con abacavir, lamivudina y La zidovudina se ha realizado en animales (ver Abacavir, lamivudina y Secciones de zidovudina a continuación). TRIZIVIR debe usarse solo durante el embarazo si los beneficios potenciales superan los riesgos.
Registro de exposición al embarazo
Hay un registro de exposición al embarazo que monitorea resultados del embarazo en mujeres expuestas a TRIZIVIR durante el embarazo. Médicos se alienta a registrar pacientes llamando al embarazo antirretroviral Registro al 1-800-258-4263.
Abacavir
Los estudios en ratas preñadas mostraron que abacavir es transferido al feto a través de la placenta. Malformaciones fetales (aumentado incidentes de anasarca fetal y malformaciones esqueléticas) y de desarrollo toxicidad (peso corporal fetal deprimido y longitud reducida de la grupa de la corona) fueron observado en ratas a una dosis que produjo 35 veces la exposición humana, según AUC Toxicidades embrionarias y fetales (aumento de las resorciones, disminución del fetal pesos corporales) y toxicidades para la descendencia (mayor incidencia de muerte fetal y pesos en la parte inferior del cuerpo) ocurrieron a la mitad de la dosis mencionada anteriormente en estudios separados de fertilidad realizados en ratas. En el conejo, no toxicidad del desarrollo y no se produjeron aumentos en las malformaciones fetales dosis que produjeron 8,5 veces la exposición humana a la dosis recomendada en AUC .
Lamivudina
Los estudios en ratas preñadas mostraron que la lamivudina es transferido al feto a través de la placenta. Estudios de reproducción con oralmente La lamivudina administrada se ha realizado en ratas y conejos a dosis produciendo niveles plasmáticos hasta aproximadamente 35 veces mayores que los recomendados dosis de VIH en adultos. No se observó evidencia de teratogenicidad debido a lamivudina. Se observó evidencia de embrioletalidad temprana en el conejo a niveles de exposición similar a los observados en humanos, pero no hubo indicios de este efecto en la rata a niveles de exposición hasta 35 veces mayores que en humanos.
Zidovudina
Estudios de reproducción con zidovudina administrada por vía oral en la rata y en el conejo a dosis de hasta 500 mg por kg por día revelaron no evidencia de teratogenicidad con zidovudina. El tratamiento con zidovudina resultó en toxicidad embrionaria / fetal como lo demuestra un aumento en la incidencia de fetal reabsorciones en ratas que recibieron 150 o 450 mg por kg por día y conejos que recibieron 500 mg por kg por día. Las dosis utilizadas en los estudios de teratología dieron como resultado un pico concentraciones plasmáticas de zidovudina (después de la mitad de la dosis diaria) en ratas 66 a 226 veces, y en conejos de 12 a 87 veces, significa pico humano en estado estacionario concentraciones plasmáticas (después de una sexta parte de la dosis diaria) logradas con el dosis diaria recomendada (100 mg cada 4 horas). En un estudio de teratología adicional en ratas, una dosis de 3.000 mg por kg por día (muy cerca de la mediana oral letal dosis en ratas de aproximadamente 3,700 mg por kg) causó una marcada toxicidad materna y un aumento en la incidencia de malformaciones fetales. Esta dosis resultó en concentraciones plasmáticas máximas de zidovudina 350 veces el plasma humano máximo concentraciones. No se vio evidencia de teratogenicidad en este experimento en dosis de 600 mg por kg por día o menos. Dos estudios de carcinogenicidad en roedores fueron conducido.
Lactancia
Los Centros para el Control y la Prevención de Enfermedades lo recomiendan que las madres infectadas con VIH-1 en los Estados Unidos no amamantan a sus bebés para evitar el riesgo de transmisión postnatal de la infección por VIH-1. Por el Se debe indicar a las madres potenciales de transmisión del VIH-1 que no lo hagan amamantar.
Uso pediátrico
TRIZIVIR no se recomienda en niños que pesan menos de 40 kg porque es una tableta de dosis fija que no se puede ajustar para estos poblaciones de pacientes.
Ensayo pediátrico con experiencia en terapia
Un ensayo aleatorizado, doble ciego, CNA3006, comparado ZIAGEN más lamivudina y zidovudina versus lamivudina y zidovudina en sujetos pediátricos, la mayoría de los cuales fueron pretratados ampliamente con nucleósido agentes antirretrovirales analógicos. Los sujetos en este juicio tuvieron una respuesta limitada a abacavir.
Uso geriátrico
Ensayos clínicos de abacavir, lamivudina y zidovudina no incluyó un número suficiente de sujetos de 65 años o más para determinar si responden de manera diferente a los sujetos más jóvenes. En general, precaución debe ejercerse en la administración de TRIZIVIR en pacientes de edad avanzada reflejando la mayor frecuencia de disminución hepática, renal o cardíaca función y de enfermedad concomitante u otra terapia farmacológica.
Pacientes con función renal deteriorada
TRIZIVIR no se recomienda para pacientes con creatinina espacio libre inferior a 50 ml por minuto porque TRIZIVIR es una combinación de dosis fija y la dosis de los componentes individuales no se puede ajustar. Si una dosis Se requiere la reducción de los componentes de lamivudina o zidovudina de TRIZIVIR para pacientes con insuficiencia renal, los componentes individuales deben ser usado.
Pacientes con insuficiencia hepática
TRIZIVIR es una combinación de dosis fija y la dosis de Los componentes individuales no se pueden ajustar. Si una reducción de la dosis de abacavir, Se requiere un componente de TRIZIVIR para pacientes con insuficiencia hepática leve (Child-Pugh Clase A), entonces se deben usar los componentes individuales.
La seguridad, la eficacia y las propiedades farmacocinéticas de abacavir no se ha establecido en pacientes con clase moderada (Child-Pugh B) o insuficiencia hepática grave (Child-Pugh Clase C); por lo tanto, TRIZIVIR es contraindicado en estos pacientes.
La zidovudina se elimina principalmente por el metabolismo hepático y las concentraciones de zidovudina aumentan en pacientes con insuficiencia hepática función, que puede aumentar el riesgo de toxicidad hematológica. Frecuente Se recomienda controlar las toxicidades hematológicas.

Se realizaron los ensayos de interacción farmacológica descritos abacavir, lamivudina o zidovudina como entidades individuales; sin interacción farmacológica Se han realizado ensayos con TRIZIVIR. No hay fármaco clínicamente significativo Se esperan interacciones entre abacavir, lamivudina y zidovudina.
Enzimas del citocromo P450: Abacavir, lamivudina y la zidovudina no se metaboliza significativamente por las enzimas del citocromo P450; por lo tanto, es poco probable que las interacciones farmacológicas clínicamente significativas lo hagan ocurrir con fármacos metabolizados a través de estas vías.
Glucuronil Transferase: Debido a lo común vías metabólicas de abacavir y zidovudina a través de glucuronil transferasa, 15 Los sujetos infectados con VIH-1 se inscribieron en un ensayo cruzado que evaluó individualmente dosis de abacavir (600 mg), lamivudina (150 mg) y zidovudina (300 mg) sola o en combinación. El análisis no mostró cambios clínicamente relevantes en el farmacocinética de abacavir con la adición de lamivudina o zidovudina o La combinación de lamivudina y zidovudina. Exposición a lamivudina (AUC disminuyó 15%) y la exposición a zidovudina (el AUC aumentó 10%) no se mostró cambios clínicamente relevantes con abacavir concurrente.
Otras interacciones
Etanol: Abacavir no tiene efecto sobre el propiedades farmacocinéticas de etanol. El etanol disminuye la eliminación de abacavir provoca un aumento en la exposición general.
Interferón Alfa: No hubo significativo interacción farmacocinética entre lamivudina e interferón alfa en un ensayo de 19 sujetos varones sanos.
Metadona: En un ensayo de 11 infectados con VIH-1 sujetos que reciben terapia de mantenimiento con metadona (40 mg y 90 mg diarios), con 600 mg de abacavir dos veces al día (el doble de la dosis recomendada actualmente), oral El aclaramiento de metadona aumentó un 22% (IC 90%: 6% a 42%). La adición de metadona no tiene un efecto clínicamente significativo sobre el propiedades farmacocinéticas de abacavir.
Ribavirina: In vitro los datos indican ribavirina reduce la fosforilación de lamivudina, estavudina y zidovudina. Sin embargo no farmacocinético (p. ej., concentraciones plasmáticas o trifosforilado intracelular concentraciones activas de metabolitos) o farmacodinámicas (p. ej., pérdida de VIH-1 / VHC supresión virológica) se observó interacción cuando ribavirina y lamivudina (n = 18), estavudina (n = 10) o zidovudina (n = 6) se administraron conjuntamente como parte de un régimen antidrogas para sujetos coinfectados con VIH-1 / VHC.
Los efectos de otros medicamentos administrados conjuntamente sobre el abacavir lamivudina o zidovudina se proporcionan en la Tabla 4.
Tabla 4: Efecto de los medicamentos administrados conjuntamente en el abacavir
Lamivudina y Zidovudina AUCa
| Drogas y dosis administradas conjuntamente | Drogas y Dosis | n | Concentraciones de abacavir, lamivudina o zidovudina | Concentración de fármaco coadministrado | |
| AUC | Variabilidad | ||||
| Etanol 0.7 g / kg | Abacavir solo 600 mg | 24 | ↑ 41% | IC del 90%: 35% a 48% | ↔b |
| Nelfinavir 750 mg cada 8 h x 7 a 10 días | Lamivudina Single 150 mg | 11 | ↑ 10% | IC del 95%: 1% a 20% | ↔ |
| Trimetoprima 160 mg / sulfametoxazol 800 mg diarios x 5 días | Lamivudina simple 300 mg | 14 | ↑ 43% | IC del 90%: 32% a 55% | ↔ |
| Atovacuona 750 mg cada 12 h con alimentos | Zidovudina 200 mg cada 8 h | 14 | ↑ 31% | Rango: 23% a 78%c | ↔ |
| Claritromicina 500 mg dos veces al día | Zidovudina 100 mg cada 4 h x 7 días | 4 | ↓ 12% | Rango: ↓34% a ↑ 14% | No reportado |
| Fluconazol 400 mg diarios | Zidovudina 200 mg cada 8 h | 12 | ↑ 74% | IC del 95%: 54% a 98% | No reportado |
| Metadona 30 a 90 mg diarios | Zidovudina 200 mg cada 4 h | 9 | ↑ 43% | Rango: 16% a 64% c | ↔ |
| Nelfinavir 750 mg cada 8 h x 7 a 10 días | Zidovudina sola 200 mg | 11 | ↓ 35% | Rango: 28% a 41% | ↔ |
| Probenecid 500 mg cada 6 h x 2 días | Zidovudina 2 mg / kg cada 8 h x 3 días | 3 | ↑ 106% | Rango: 100% a 170%c | No evaluado |
| Rifampina 600 mg diarios x 14 días | Zidovudina 200 mg cada 8 h x 14 días | 8 | ↓ 47% | IC del 90%: 41% a 53% | No evaluado |
| Ritonavir 300 mg cada 6 h x 4 días | Zidovudina 200 mg cada 8 h x 4 días | 9 | ↓ 25% | IC del 95%: 15% a 34% | ↔ |
| Ácido valproico 250 mg o 500 mg cada 8 h x 4 días | Zidovudina 100 mg cada 8 h x 4 días | 6 | ↑ 80% | Rango: 64% a 130%c | No evaluado |
| ↑ = Aumentar; ↓ = Disminución; ↔ = no
cambio significativo; AUC = área bajo la curva de concentración versus tiempo; IC =
intervalo de confianza. aVer INTERACCIONES DE DROGAS para información adicional sobre drogas interacciones. bLa interacción fármaco-fármaco solo se evaluó en hombres. cRango estimado de diferencia porcentual. |

Embarazo Categoría C
No hay estudios adecuados y bien controlados de TRIZIVIR en mujeres embarazadas. Estudios de reproducción con abacavir, lamivudina y La zidovudina se ha realizado en animales (ver Abacavir, lamivudina y Secciones de zidovudina a continuación). TRIZIVIR debe usarse solo durante el embarazo si los beneficios potenciales superan los riesgos.
Registro de exposición al embarazo
Hay un registro de exposición al embarazo que monitorea resultados del embarazo en mujeres expuestas a TRIZIVIR durante el embarazo. Médicos se alienta a registrar pacientes llamando al embarazo antirretroviral Registro al 1-800-258-4263.
Abacavir
Los estudios en ratas preñadas mostraron que abacavir es transferido al feto a través de la placenta. Malformaciones fetales (aumentado incidentes de anasarca fetal y malformaciones esqueléticas) y de desarrollo toxicidad (peso corporal fetal deprimido y longitud reducida de la grupa de la corona) fueron observado en ratas a una dosis que produjo 35 veces la exposición humana, según AUC Toxicidades embrionarias y fetales (aumento de las resorciones, disminución del fetal pesos corporales) y toxicidades para la descendencia (mayor incidencia de muerte fetal y pesos en la parte inferior del cuerpo) ocurrieron a la mitad de la dosis mencionada anteriormente en estudios separados de fertilidad realizados en ratas. En el conejo, no toxicidad del desarrollo y no se produjeron aumentos en las malformaciones fetales dosis que produjeron 8,5 veces la exposición humana a la dosis recomendada en AUC .
Lamivudina
Los estudios en ratas preñadas mostraron que la lamivudina es transferido al feto a través de la placenta. Estudios de reproducción con oralmente La lamivudina administrada se ha realizado en ratas y conejos a dosis produciendo niveles plasmáticos hasta aproximadamente 35 veces mayores que los recomendados dosis de VIH en adultos. No se observó evidencia de teratogenicidad debido a lamivudina. Se observó evidencia de embrioletalidad temprana en el conejo a niveles de exposición similar a los observados en humanos, pero no hubo indicios de este efecto en la rata a niveles de exposición hasta 35 veces mayores que en humanos.
Zidovudina
Estudios de reproducción con zidovudina administrada por vía oral en la rata y en el conejo a dosis de hasta 500 mg por kg por día revelaron no evidencia de teratogenicidad con zidovudina. El tratamiento con zidovudina resultó en toxicidad embrionaria / fetal como lo demuestra un aumento en la incidencia de fetal reabsorciones en ratas que recibieron 150 o 450 mg por kg por día y conejos que recibieron 500 mg por kg por día. Las dosis utilizadas en los estudios de teratología dieron como resultado un pico concentraciones plasmáticas de zidovudina (después de la mitad de la dosis diaria) en ratas 66 a 226 veces, y en conejos de 12 a 87 veces, significa pico humano en estado estacionario concentraciones plasmáticas (después de una sexta parte de la dosis diaria) logradas con el dosis diaria recomendada (100 mg cada 4 horas). En un estudio de teratología adicional en ratas, una dosis de 3.000 mg por kg por día (muy cerca de la mediana oral letal dosis en ratas de aproximadamente 3,700 mg por kg) causó una marcada toxicidad materna y un aumento en la incidencia de malformaciones fetales. Esta dosis resultó en concentraciones plasmáticas máximas de zidovudina 350 veces el plasma humano máximo concentraciones. No se vio evidencia de teratogenicidad en este experimento en dosis de 600 mg por kg por día o menos. Dos estudios de carcinogenicidad en roedores fueron conducido.

Las siguientes reacciones adversas se analizan en otros secciones del etiquetado :
- Reacciones de hipersensibilidad graves y a veces fatales.
- Toxicidad hematológica, incluida la neutropenia y la anemia.
- Miopatía sintomática.
- Acidosis láctica y hepatomegalia severa con esteatosis.
- Exacerbaciones de la hepatitis B
- Descompensación hepática en pacientes coinfectados con VIH-1 y hepatitis C .
- Exacerbación de la anemia en pacientes coinfectados con VIH-1 / VHC recibiendo ribavirina y zidovudina.
- Síndrome de reconstitución inmune.
- Redistribución gorda.
- Infarto de miocardio.
Experiencia en ensayos clínicos
Porque los ensayos clínicos se realizan ampliamente condiciones variables, tasas de reacción adversas observadas en los ensayos clínicos de a el fármaco no se puede comparar directamente con las tasas en los ensayos clínicos de otro fármaco y puede no reflejar las tasas observadas en la práctica clínica.
Hipersensibilidad grave y mortal asociada a abacavir Reacciones
En ensayos clínicos, graves y a veces fatales Se han producido reacciones de hipersensibilidad con abacavir, un componente de TRIZIVIR Estas reacciones se han caracterizado por 2 o más.de los siguientes signos o síntomas: (1) fiebre; (2) erupción cutánea; (3) gastrointestinal síntomas (incluyendo náuseas, vómitos, diarrea o dolor abdominal); (4) síntomas constitucionales (incluyendo malestar generalizado, fatiga o dolor); (5) síntomas respiratorios (incluyendo disnea, tos o faringitis). Casi todo Las reacciones de hipersensibilidad a abacavir incluyen fiebre y / o erupción cutánea como parte de la síndrome.
Otros signos y síntomas han incluido letargo, dolor de cabeza mialgia, edema, artralgia y parestesia. Anafilaxia, insuficiencia hepática, renal insuficiencia, hipotensión, síndrome de dificultad respiratoria del adulto, insuficiencia respiratoria, La miólisis y la muerte han ocurrido en asociación con estas hipersensibilidad reacciones. Los hallazgos físicos han incluido linfadenopatía, membrana mucosa lesiones (conjuntivitis y ulceraciones bucales) y maculopapulares o urticariales erupción cutánea (aunque algunos pacientes tenían otros tipos de erupciones cutáneas y otros no una erupción). Hubo informes de eritema multiforme. Anomalías de laboratorio incluyó químicos hepáticos elevados, creatina fosfoquinasa elevada, elevada creatinina y linfopenia, y hallazgos anormales de rayos X en el pecho (predominantemente infiltrados, que fueron localizados).
Reacciones adversas adicionales con el uso de TRIZIVIR
Reacciones adversas clínicas emergentes del tratamiento (calificadas por el investigador como moderado o severo) con una frecuencia mayor o igual al 5% durante la terapia con abacavir 300 mg dos veces al día, lamivudina 150 mg dos veces diariamente, y zidovudina 300 mg dos veces al día en comparación con indinavir 800 mg 3 veces diariamente, lamivudina 150 mg dos veces al día y zidovudina 300 mg dos veces al día CNA3005 se enumeran en la Tabla 1.
Tabla 1: Adversal de tratamiento-emergente (toda causalidad)
Reacciones de intensidad moderada menor (grados 2-4, mayor o igual a
5% de frecuencia) en adultos de terapia ingenua (CNA3005) a través de 48 semanas de tratamiento
| Reacción adversa | ZIAGEN más Lamivudina / Zidovudina (n = 262) |
Indinavir más lamivudina / zidovudina (n = 264) |
| Náuseas | 19% | 17% |
| Dolor de cabeza | 13% | 9% |
| Malestar y fatiga | 12% | 12% |
| Náuseas y vómitos | 10% | 10% |
| Reacción de hipersensibilidad | 8% | 2% |
| Diarrea | 7% | 5% |
| Fiebre y / o escalofríos | 6% | 3% |
| Trastornos depresivos | 6% | 4% |
| Dolor musculoesquelético | 5% | 7% |
| Erupciones cutáneas | 5% | 4% |
| Infecciones de oído / nariz / garganta | 5% | 4% |
| Infecciones respiratorias virales | 5% | 5% |
| Ansiedad | 5% | 3% |
| Signos renales / síntomas | <1% | 5% |
| Dolor (no específico del sitio) | <1% | 5% |
Cinco sujetos recibiendo abacavir en CNA3005 experimentó un empeoramiento de la depresión preexistente en comparación a ninguno en el brazo de indinavir. Las tasas de fondo de la depresión preexistente fueron similares en los 2 brazos de tratamiento.
Anomalías de laboratorio
Anomalías de laboratorio en CNA3005 se enumeran en la Tabla 2.
Tabla 2: Tratamiento-emergente
Anomalías de laboratorio (Grados 3/4) en CNA3005
| Parámetro de laboratorio | ZIAGEN más Lamivudina / Zidovudina (n = 262) |
Indinavir más lamivudina / zidovudina (n = 264) |
| CPK elevado (> 4 x ULN) | 18 (7%) | 18 (7%) |
| ALT (> 5.0 x ULN) | 16 (6%) | 16 (6%) |
| Neutropenia (<750 / mm³) | 13 (5%) | 13 (5%) |
| Hipertrigliceridemia (> 750 mg / dL) | 5 (2%) | 3 (1%) |
| Hiperamiasemia (> 2.0 x ULN) | 5 (2%) | 1 (<1%) |
| Hiperglucemia (> 13.9 mmol / L) | 2 (<1%) | 2 (<1%) |
| Anemia (Hgb ≤ 6.9 g / dL) | 0 (0%) | 3 (1%) |
| ULN = límite superior de la normalidad. n = Número de sujetos evaluados. |
Otros eventos adversos
Además de adverso reacciones en las Tablas 1 y 2, otros eventos adversos observados en el expandido El programa de acceso para abacavir fue pancreatitis y aumento de GGT
Experiencia de postmarketing
Las siguientes reacciones adversas han sido identificados durante el uso posterior a la comercialización. Porque estas reacciones son reportado voluntariamente de una población de tamaño desconocido, no siempre es así posible estimar de manera confiable su frecuencia o establecer una relación causal a la exposición a drogas.
Abacavir
Cardiovascular: Infarto de miocardio.
Piel: Sospechoso síndrome de Stevens-Johnson (SJS) y Se ha informado necrólisis epidérmica tóxica (TEN) en pacientes que reciben abacavir principalmente en combinación con medicamentos que se sabe que están asociados SJS y TEN, respectivamente. Debido a la superposición de signos clínicos y síntomas entre hipersensibilidad a abacavir y SJS y TEN, y el posibilidad de múltiples sensibilidades a los medicamentos en algunos pacientes, debe ser abacavir descontinuado y no reiniciado en tales casos. También ha habido informes de eritema multiforme con uso de abacavir.
Abacavir, lamivudina y / o zidovudina
Cuerpo en su conjunto: Redistribución / acumulación de grasa corporal.
Cardiovascular: Cardiomiopatía.
Digestivo: Estomatitis.
Endocrino y Metabólico: Ginecomastia.
Gastrointestinal: Anorexia y / o disminución apetito, dolor abdominal, dispepsia, pigmentación de la mucosa oral.
General: Vasculitis, debilidad.
Hemica y Linfática : Anemia aplásica, anemia (incluida la aplasia pura de glóbulos rojos y las anemias severas que progresan en la terapia) linfadenopatía, esplenomegalia, trombocitopenia.
Hepático: Acidosis láctica y esteatosis hepática, elevada bilirrubina, transaminasas elevadas, exacerbaciones posteriores al tratamiento de la hepatitis B
Hipersensibilidad : Reacciones de sensibilización (incluida la anafilaxia), urticaria.
Musculoesquelético : Artralgia, mialgia, músculo debilidad, rabdomiólisis. Nervioso: mareos, parestesia, periférico neuropatía, convulsiones.
Psiquiátrico: Insomnio y otros trastornos del sueño. Respiratorio: Sonidos de respiración anormales / sibilancias. Piel: alopecia, eritema multiforme Síndrome de Stevens-Johnson.

No se conoce un tratamiento específico para la sobredosis con TRIZIVIR. Si se produce una sobredosis, el paciente debe ser monitoreado y estándar tratamiento de apoyo aplicado según sea necesario.
Abacavir
No se sabe si se puede eliminar el abacavir diálisis peritoneal o hemodiálisis.
Lamivudina
Porque se eliminó una cantidad insignificante de lamivudina (4 horas) hemodiálisis, diálisis peritoneal ambulatoria continua y automatizada diálisis peritoneal, no se sabe si proporcionaría hemodiálisis continua beneficio clínico en un evento de sobredosis de lamivudina.
Zidovudina
Se han informado sobredosis agudas de zidovudina en pacientes pediátricos y adultos. Estas implicaron exposiciones de hasta 50 gramos. No Se han identificado síntomas o signos específicos después de una sobredosis aguda con zidovudina aparte de los enumerados como eventos adversos como fatiga, dolor de cabeza, etc vómitos e informes ocasionales de trastornos hematológicos. Pacientes recuperado sin secuelas permanentes. Hemodiálisis y diálisis peritoneal parece tener un efecto insignificante en la eliminación de zidovudina, mientras que eliminación de su metabolito primario, 3'azido-3'-desoxi-5'-O-β-D-glucopiranuronosiltimidina (GZDV), está mejorado.

Farmacocinética en adultos
En un ensayo de biodisponibilidad cruzada de 3 vías de dosis única de 1 tableta TRIZIVIR versus 1 tableta ZIAGEN (300 mg), 1 tableta EPIVIR (150 mg) más 1 tableta RETROVIR (300 mg) administrada simultáneamente en sujetos sanos (n = 24), no hubo diferencia en el grado de absorción, según lo medido el área bajo la curva de concentración plasmática-tiempo (AUC) y el pico máximo concentración (Cmax), de los 3 componentes. Una tableta TRIZIVIR fue bioequivalente a 1 tableta ZIAGEN (300 mg), 1 tableta EPIVIR (150 mg), más 1 Comprimido RETROVIR (300 mg) después de la administración de dosis única al ayuno sujetos sanos (n = 24).
Abacavir: Después de la administración oral, abacavir se absorbe rápidamente y se distribuye ampliamente. Después de la administración oral de 300 mg de abacavir dos veces al día en 20 sujetos, la Cmáx fue de 3.0 ± 0.89 mcg por ml (media ± DE) y AUC (0-12 h) fue de 6.02 ± 1.73 mcg • hora por ml. Unión de abacavir a proteínas plasmáticas humanas es aproximadamente del 50% y era independiente de concentración. Concentraciones totales de radiactividad relacionada con el fármaco en sangre y plasma son idénticos, lo que demuestra que el abacavir se distribuye fácilmente en eritrocitos. Las principales rutas de eliminación de abacavir son el metabolismo por alcohol deshidrogenasa para formar el ácido 5'-carboxílico y el glucuronilo transferase para formar el 5'-glucurónido.
Lamivudina: Después de la administración oral, la lamivudina se absorbe rápidamente y se distribuye ampliamente. Unión al plasma La proteína es baja. Aproximadamente el 70% de una dosis intravenosa de lamivudina es recuperado como fármaco inalterado en la orina. El metabolismo de la lamivudina es menor de edad ruta de eliminación. En humanos, el único metabolito conocido es el metabolito transsulfóxido (aproximadamente el 5% de una dosis oral después de 12 horas).
Zidovudina: Después de la administración oral, La zidovudina se absorbe rápidamente y se distribuye ampliamente. Unión al plasma La proteína es baja. La zidovudina se elimina principalmente por metabolismo hepático. Los El metabolito principal de la zidovudina es el GZDV. El AUC de GZDV es aproximadamente 3 veces mayor que el AUC de zidovudina. La recuperación urinaria de zidovudina y GZDV representa el 14% y 74% de la dosis después de la administración oral, respectivamente. Un segundo se ha identificado metabolito, 3'-amino-3'desoxitimidina (AMT) plasma. El AMT AUC fue una quinta parte del AUC de zidovudina
En humanos, abacavir, lamivudina y zidovudina no lo son metabolizado significativamente por las enzimas del citocromo P450.
Las propiedades farmacocinéticas de abacavir, lamivudina y la zidovudina en sujetos en ayunas se resumen en la Tabla 3.
Tabla 3: Parámetros farmacocinéticosa para
Abacavir, lamivudina y zidovudina en adultos
| Parámetro | Abacavir | Lamivudina | Zidovudina | |||
| Biodisponibilidad oral (%) | 86 ± 25 | n = 6 | 86 ± 16 | n = 12 | 64 ± 10 | n = 5 |
| Volumen aparente de distribución (L / kg) | 0.86 ± 0.15 | n = 6 | 1.3 ± 0.4 | n = 20 | 1.6 ± 0.6 | n = 8 |
| Espacio libre sistémico (L / h / kg) | 0.80 ± 0.24 | n = 6 | 0.33 ± 0.06 | n = 20 | 1.6 ± 0.6 | n = 6 |
| Espacio libre renal (L / h / kg) | 0.007 ± 0.008 | n = 6 | 0.22 ± 0.06 | n = 20 | 0.34 ± 0.05 | n = 9 |
| Vida media de eliminación (h) | 1.45 ± 0.32 | n = 20 | 5 a 7b | 0.5 a 3b | ||
| aDatos presentados como media ± desviación estándar
excepto donde se indique. bRango aproximado. |
Efecto de los alimentos sobre la absorción de TRIZIVIR
Administración con alimentos en una dosis única de biodisponibilidad el ensayo resultó en una Cmax más baja, similar a los resultados observados anteriormente para el formulaciones de referencia. La disminución promedio [IC 90%] en abacavir, lamivudina, y la Cmáx de zidovudina fue del 32% [24% al 38%], del 18% [10% al 25%] y del 28% [13% al 40%] respectivamente, cuando se administra con una comida rica en grasas, en comparación con administración en condiciones de ayuno. Administración de TRIZIVIR con alimentos no alteró el alcance de la absorción de abacavir, lamivudina y zidovudina (AUC), en comparación con la administración en condiciones de ayuno (n = 24).

Fuentes:
Disponible en países
 Australia
Australia Austria
Austria Belgium
Belgium Bulgaria
Bulgaria Canada
Canada China
China Croatia (Hrvatska)
Croatia (Hrvatska) Cyprus
Cyprus Czech Republic
Czech Republic Denmark
Denmark Ecuador
Ecuador Estonia
Estonia Finland
Finland France
France Georgia
Georgia Germany
Germany Greece
Greece Hong Kong
Hong Kong Hungary
Hungary Iceland
Iceland Ireland
Ireland Israel
Israel Italy
Italy Latvia
Latvia Liechtenstein
Liechtenstein Lithuania
Lithuania Luxembourg
Luxembourg Malta
Malta Netherlands
Netherlands Norway
Norway Oman
Oman Peru
Peru Poland
Poland Portugal
Portugal Romania
Romania Russia
Russia Serbia
Serbia Slovakia
Slovakia Slovenia
Slovenia Spain
Spain Sweden
Sweden Switzerland
Switzerland Taiwan
Taiwan United Kingdom
United Kingdom USA
USA
