

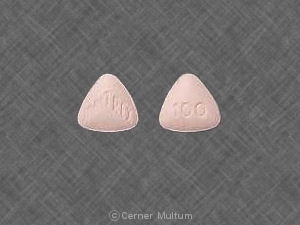

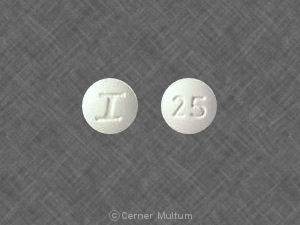
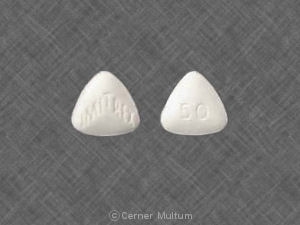














Komposition:
Anwendung:
Wird bei der Behandlung verwendet:
Medizinisch geprüft von Militian Inessa Mesropovna, Apotheke Zuletzt aktualisiert am 24.03.2022

Achtung! Die Informationen auf der Seite sind nur für medizinisches Fachpersonal! Die Informationen werden in öffentlichen Quellen gesammelt und können aussagekräftige Fehler enthalten! Seien Sie vorsichtig und überprüfen Sie alle Informationen auf dieser Seite!
Top 20 Medikamente mit den gleichen Inhaltsstoffen:



Alkohol Migräneattacken (mit oder ohne Aura).
Alkoholtester Migräne-Angriffe (mit und ohne Aura).
Alkohol Migräne greift mit oder ohne Aura an.

Im Inneren intranasal. Es wird empfohlen, Imitrex (subkutan) so früh wie möglich nach Beginn des Migräneangriffs zu verwenden. Dies ist jedoch in jeder Phase des Angriffs gleichermaßen wirksam.
Innerhalb (Die Tablette wird vollständig durch Trinkwasser geschluckt) für Erwachsene: Die empfohlene Dosis beträgt 1 Tablette 50 mg (einige Patienten benötigen möglicherweise eine höhere Dosis - 100 mg).
Intranasal Erwachsene (18 Jahre und älter) - 20 mg (1 Dosis) Imitrex (subkutan) und als Spray in einer Nasenhälfte. Es sei daran erinnert, dass die Absorption von Sumatriptan- und Migräneattacken in Stärke und klinischer Manifestation nicht nur bei verschiedenen Patienten, sondern auch bei demselben Patienten unterschiedlich sein kann, sodass eine Dosis von 10 mg wirksam sein kann.
Wenn die Symptome von Migräne nicht verschwinden und nach Einnahme der ersten Dosis von Imitrex (subkutan) a (unabhängig von der Verwendungsmethode) nicht abnehmen, sollte die Einnahme einer zweiten Dosis zum Kauf des gleichen Angriffs nicht zugewiesen werden. Imitrex (subkutan) kann jedoch verwendet werden, um nachfolgende Migräneattacken zu kaufen. Wenn der Patient nach der ersten Dosis eine Besserung verspürte und die Symptome wieder aufgenommen wurden, kann innerhalb der nächsten 24 Stunden eine zweite Dosis eingenommen werden. Die maximale Dosis von Imitrex (subkutan) a darf 300 mg für einen Zeitraum von 24 Stunden (bei Einnahme) oder zwei Dosen von Imitrex (subkutan) von 20 mg (bei intranasaler Anwendung) nicht überschreiten.
Innerhalb. Die Tablette wird vollständig durch Trinkwasser geschluckt. Erwachsene haben eine Einzeldosis von 0,05 g (in einigen Fällen - 0,1 g), die maximale Tagesdosis beträgt 0,3 g. Wenn die Symptome von Migräne nach Einnahme der ersten Dosis nicht verschwinden und nicht abnehmen, sollte die zweite Dosis, um denselben Angriff zu kaufen, nicht zugewiesen werden. Wenn die Symptome abgenommen oder bestanden und dann wieder aufgenommen wurden, kann innerhalb der nächsten 24 Stunden eine zweite Dosis eingenommen werden. Das Intervall zwischen den Dosen beträgt mindestens 2 Stunden.
Innerhalb, Schlucken Sie beim Essen oder auf leeren Magen ganz und trinken Sie Wasser.
Die empfohlene Dosis beträgt 50 mg. Einige Patienten benötigen möglicherweise eine höhere Dosis von 100 mg. Wenn die Symptome von Migräne nach der ersten Dosis nicht verschwinden und nicht abnehmen, sollte das Medikament nicht erneut eingenommen werden, um denselben Angriff zu kaufen. Das Medikament kann jedoch verwendet werden, um nachfolgende Migräneattacken zu kaufen.
Wenn der Patient nach der ersten Dosis eine Besserung verspürte und die Symptome wieder aufgenommen wurden, kann innerhalb der nächsten 24 Stunden eine zweite Dosis eingenommen werden, sofern der Abstand zwischen dem Empfang mindestens 2 Stunden beträgt. Die maximale Tagesdosis von Sumatriptan sollte 300 mg nicht überschreiten.
Spezielle Patientengruppen
Pädiatrisches Versagen. Die empfohlene Dosis beträgt 50 mg.
Kinder und Jugendliche (unter 18 Jahren). Sumatriptan wird wegen fehlender Daten zur Sicherheit und Effizienz nicht zur Anwendung bei Kindern und Jugendlichen empfohlen.
Älteres Alter (über 65). Die Erfahrung mit der Anwendung von Sumatriptan bei Patienten über 65 Jahren ist begrenzt. Die Pharmakokinetik des Arzneimittels unterscheidet sich nicht signifikant von der bei jüngeren Patienten. Bevor jedoch zusätzliche klinische Daten erhalten, wird die Anwendung von Sumatriptan bei Patienten über 65 Jahren nicht empfohlen.
Rektal 1 Soupp. (im Falle eines Migräneangriffs).
Wenn die Symptome von Migräne nach Anwendung der ersten Dosis nicht verschwinden und nicht abnehmen, sollte das Medikament nicht wiederverwendet werden, um denselben Angriff zu kaufen. Das Medikament kann jedoch verwendet werden, um nachfolgende Migräneattacken zu kaufen.
Wenn der Patient nach der ersten Dosis eine Verbesserung verspürte und die Symptome wieder aufgenommen wurden, kann innerhalb der nächsten 24 Stunden eine zweite Dosis angewendet werden. Die maximale Sumatriptan-Dosis sollte über einen Zeitraum von 24 Stunden 300 mg nicht überschreiten.

Überempfindlichkeit; hemiplegische, basale und ophthalmoplegische Formen von Migräne; Myokardinfarkt (einschließlich h. in der Geschichte); IBS oder Verdacht auf seine Anwesenheit; Princemetal Angina pectoris; Krankheiten der peripheren Gefäße; vorübergehender zerebrovaskulärer Unfall (einschließlich.h. in der Geschichte); Schlaganfall (einschließlich.h. in der Geschichte) unkontrollierte arterielle Hypertonie; eine ausgeprägte Verletzung der Funktion der Leber und / oder der Nieren; gleichzeitiger Empfang von Imitrex (Subkutan) mit Ergotamin oder seinen Derivaten (einschließlich Mesergid) sowie die gleichzeitige Einnahme von MAO-Inhibitoren und einen Zeitraum von bis zu 2 Wochen nach ihrer Aufhebung.
Mit Vorsicht: Epilepsie (einschließlich h. jede Erkrankung mit einer Abnahme der Schwelle der Krampfbereitschaft), arterielle Hypertonie (kontrolliert), Schwangerschaft, Stillzeit, Alter bis zu 18 Jahren (Sicherheit und Effizienz sind nicht festgelegt), Alter über 65 Jahre.
Individuelle Unverträglichkeit des Arzneimittels IBS, einschließlich.h. Angina pectoris, hemiplegische, basale oder ophthalmoplegische Formen von Migräne, Okklusionskrankheiten peripherer Arterien, unkontrollierte arterielle Hypertonie, Schlaganfall oder vorübergehende zerebrale Zirkulation bei Anamnese, Leberversagen, Schwangerschaft, Stillzeit, Kindheit, Alter (Vergangenheit 6 Jahre).
Mit Vorsicht - Epilepsie (einschließlich.h. jede Erkrankung mit einer verringerten epileptischen Schwelle), arterieller Hypertonie (kontrolliert), gleichzeitige Einnahme von MAO-Inhibitoren und einer Frist von bis zu 14 Tagen nach ihrer Aufhebung.
Überempfindlichkeit gegen eine Komponente des Arzneimittels;
Laktasemangel, Laktoseintoleranz, Glukose-Galaktose-Malabsorption;
hemiplegische, basiläre und ophthalmoplegische Formen von Migräne;
koronare Herzkrankheit (einschließlich.h. Myokardinfarkt, Herzlerose nach dem Infarkt, Princemetal Angina pectoris) sowie das Vorhandensein von Symptomen, die darauf hinweisen;
Okklusionskrankheiten von Peripheriegefäßen;
Schlaganfall oder vorübergehender ischämischer Angriff (einschließlich h. in der Geschichte);
arterielle Hypertonie II - III des Schweregrads;
unkontrollierte arterielle Hypertonie;
gleichzeitiger Empfang mit Ergotamin oder seinen Derivaten (einschließlich Metzergid);
gleichzeitiger Empfang mit anderen Tryptanen / Agonisten 5-HT1Rezeptoren;
Verwendung vor dem Hintergrund des Empfangs von MAO-Inhibitoren oder früher als 2 Wochen nach ihrer Aufhebung;
ausgeprägte beeinträchtigte Leberfunktion und / oder Nieren;
Schwangerschaft;
Stillzeit;
Alter bis 18 Jahre und älter 65 Jahre (Sicherheit und Effizienz nicht festgelegt).

Die Anwendung von Sumatriptan ist in der Schwangerschaft kontraindiziert. Das Stillen sollte während der Behandlung abgebrochen werden. Bei Einnahme des Arzneimittels ist das Stillen frühestens 24 Stunden möglich.

Allgemeine Symptome : Schmerzen, Kribbeln, Gefühl von Hitze, Gefühl von Druck oder Schweregrad (Diese Symptome sind normalerweise vorübergehend, kann aber intensiv sein und in jedem Teil des Körpers auftreten, einschließlich Brust und Rachen) Gezeiten, Schwindel, ein Gefühl von Schwäche und / oder Müdigkeit, Schläfrigkeit (normalerweise schwach oder mäßig ausgedrückt und vorübergehend).
Aus dem Herz-Kreislauf-System : arterielle Hypotonie, Bradykardie, Tachykardie (einschließlich h. ventrikulär), Herzschlag, vorübergehender AD-Boost (kurz nach Einnahme von Sumatriptan beobachtet); Es gibt seltene Berichte über Herzrhythmusstörungen (bis zum Flimmern), die Veränderungen des ischämischen EKG-Typs, des Myokardinfarkts und des Krampf der Koronararterien erfahren. manchmal entwickelt sich das Reino-Syndrom.
Aus dem Magen-Darm-Trakt : Bei einigen Patienten wurden Übelkeit und Erbrechen festgestellt (der Zusammenhang dieser Nebenwirkungen mit der Einnahme von Sumatriptan wurde nicht festgestellt); ein leichter Anstieg der Aktivität von Leberenzymen, Dysphagie, ein Gefühl von Unbehagen im Bauch; selten - ischämische Kolitis.
Vom ZNS und vom Sehkörper : Es gibt einige seltene Berichte über Anfälle nach Einnahme von Sumatriptan. In einigen Fällen wurden sie bei Patienten mit Krämpfen in der Vorgeschichte oder unter Bedingungen beobachtet, die für das Auftreten von Anfällen prädisponieren. Bei einigen Patienten wurden prädisponierende Faktoren nicht nachgewiesen. Manchmal wurden nach der Einnahme von Imitrex (subkutan) a Diplash in den Augen, Nystagmus, Vieh und eine Abnahme der Sehschärfe festgestellt. Ein teilweiser vorübergehender Verlust des Sehvermögens hat sich selten entwickelt. Es sollte jedoch berücksichtigt werden, dass eine Sehbehinderung mit dem Angriff von Migräne verbunden sein kann.
Empfindlichkeitsreaktionen : Hautmanifestationen (Drash, Urtikaria, Juckreiz, Erythem); in seltenen Fällen - Anaphylaxie.
Lokale Symptome (beim Auftragen des Sprays): leichte vorübergehende Reizung oder ein brennendes Gefühl in der Nasenhöhle oder im Hals, Nasenbluten.
Das Gefühl des Kribbelns, Hitze, Schwerkraft, Druck in verschiedenen Körperteilen, Hyperämie der Haut und der Schleimhäute; Schwindel, Müdigkeit, Schwäche, Schläfrigkeit; ein Angriff von Angina pectoris, Hypotonie, Tachykardie, Herzschlag, Transitoranstieg des Blutdrucks, vorübergehende Veränderungen im echemischen EKG, Bradykardie, in Einzelfällen — Reino-Syndrom; ein Gefühl von Unbehagen im Magen, Dysphagie, Übelkeit, Erbrechen, ischämische Kolitis; Sehbehinderung (Diplopie, Vieh, verminderte Sehschärfe) allergische Reaktionen (Ausschlag, Urtikaria, Juckreiz, Erythem, Anaphylaxie) Veränderung der funktionellen Leberproben; Myalgie.
Abhängig von der Häufigkeit des Auftretens werden die folgenden Gruppen von Nebenwirkungen unterschieden: sehr oft - ≥ 1/10; oft - ≥ 1/100, <1/10; selten - ≥1/1000, <1/100; selten - ≥1/10000, <1/1000; sehr selten - <1/100;.
Von der Seite des Nervensystems : oft - Schwindel, Schläfrigkeit, beeinträchtigte Empfindlichkeit, einschließlich Pastezia und Hypestessie; Häufigkeit unbekannt - Krampfanfälle (in einigen Fällen wurden sie bei Patienten mit Krämpfen in der Vorgeschichte oder unter Bedingungen beobachtet, die für Anfälle prädisponiert waren; bei einigen Patienten gab es keine prädisponierenden Faktoren), Zittern, Dystonie, Angstzustände.
Von der Seite des Sichtkörpers : Häufigkeit unbekannt - Diplashing, Flackern vor den Augen, verminderte Sehschärfe, teilweiser vorübergehender oder anhaltender Verlust des Sehvermögens, Nystagmus, Vieh. Es sollte jedoch berücksichtigt werden, dass eine Sehbehinderung mit dem Angriff von Migräne verbunden sein kann.
Von der Seite des MSS : oft - ein vorübergehender Blutdruckanstieg (kurz nach Einnahme von Sumatriptan beobachtet), Gezeiten; Häufigkeit unbekannt - Bradykardie, Tachykardie, Blutdruckabfall, Herzrhythmusstörungen, vorübergehende Veränderungen des EKG nach ischämischem Typ, Myokardinfarkt, Krampfanfall der Herzkranzgefäße, Angina-Stenokardie, Reyno-Syndrom, ein Gefühl von Herzschlag.
Von der Seite des LCD : oft - Übelkeit, Erbrechen; sehr selten - Dysphagie, ein Gefühl von Unbehagen im Bauch; Häufigkeit unbekannt - ischämische Kolitis, Durchfall.
Von der Seite des Bewegungsapparates : oft - Myalgie; selten - Gelenkschmerzen; Häufigkeit unbekannt - Steifheit der okzipitalen Muskeln.
Aus den Atemwegen und den Brustorganen : oft - Kurzatmigkeit, leichte vorübergehende Reizung der Schleimhaut oder ein brennendes Gefühl in der Nasenhöhle oder im Hals, Nasenbluten.
Laborindikatoren : sehr selten - geringfügige Veränderungen in der Aktivität von Lebertransaminasen.
Allergische Reaktionen : sehr selten - Überempfindlichkeitsreaktionen reichen von Hautmanifestationen (Drash, Urtikaria, Juckreiz, Erythem) bis hin zu Anaphylaxiefällen.
Von der Haut und dem Unterhautgewebe : Häufigkeit unbekannt - Hyperhydrose.
Andere: oft - ein Gefühl von Hitze oder Kälte, Schmerzen, ein Gefühl von Kompression oder Schwere (sind vorübergehend und können in jedem Körperteil auftreten, einschließlich Brust und Rachen), ein Gefühl von Schwäche, ein Gefühl von Müdigkeit, das normalerweise ausgedrückt wird schwach oder mäßig und vorübergehend. Es kann vorkommen, dass starke Schmerzen und Verlegenheit in der Brust überwunden werden und sich bis zum Hals ausbreiten.

Empfang von Imitrex (Subkutan) und nach innen in einer Dosis von mehr als 400 mg, oder eine einmalige p / c-Verabreichung in einer Dosis von 16 mg, oder die Einführung von Imitrex (Subkutan) und einmal in einer Dosis von 40 g verursachte intranal keine anderen als die oben aufgeführten Nebenwirkungen.
Behandlung: Überwachung des Zustands der Patienten mindestens 10 Stunden, falls erforderlich, Standardtherapie. Es gibt keine Hinweise auf die Wirkung von Hämodialyse oder Peritonealdialyse auf die Konzentration von Sumatriptan im Plasma.
Im Falle einer Überdosierung sollte der Patient 10 Stunden lang beobachtet werden, wobei gegebenenfalls eine symptomatische Therapie durchgeführt wird.
Symptome : Die Einnahme von Sumatriptan nach innen in einer Dosis von mehr als 400 mg verursachte keine anderen als die oben aufgeführten Nebenwirkungen.
Behandlung: Die Patienten sollten mindestens 10 Stunden überwacht und erforderlichenfalls eine symptomatische Therapie durchgeführt werden. Es gibt keine Hinweise auf die Wirkung von Hämodialyse oder Peritonealdialyse auf die Konzentration von Sumatriptan im Plasma.

Bei Tieren verengt Sumatriptan selektiv Gefäße im Halsschlagadersystem, verändert jedoch nicht den Gehirnblutfluss. Es wird angenommen, dass die Ausdehnung dieser Gefäße und / oder die Schwellung ihrer Wände der Hauptmechanismus für das Auftreten von Migräne beim Menschen ist. Zusätzlich wird experimentell festgestellt, dass Sumatriptan die Aktivität des Triune-Nervs hemmt. Beide Effekte können der antimigrenösen Wirkung des Sumatriptans zugrunde liegen.
Verengt selektiv die Gefäße im System der Halsschlagader, hemmt die Aktivität des Triune-Nervus. Reduziert die Schwere des Schmerzsyndroms während der Migräne. Der klinische Effekt wird nach 30 Minuten beobachtet.
Sumatriptan ist ein spezifischer selektiver Agonist von Gefäß-5-hydroxytriptamin-1-Rezeptoren (5-HT1D) betrifft keine anderen Subtypen von 5-NT-Rezeptoren (5-NT2–5-NT7). 5-HT-Rezeptoren1D Sie befinden sich hauptsächlich in den Blutgefäßen des Gehirns und ihre Stimulation führt zu einer Verengung dieser Gefäße. Reduziert die Empfindlichkeit des gediehten Nervs. Beide Effekte können der antimigrenösen Wirkung des Sumatriptans zugrunde liegen. Die klinische Wirkung wird normalerweise nach 30 Minuten nach Einnahme des Arzneimittels im Inneren beobachtet.

Sumatriptan absorbierte schnell nach Einnahme und nach intranasaler Verabreichung. Bei Aufnahme nach innen 70% von Cmax im Plasma wird nach 45 Minuten erreicht, wenn es in einer Dosis von 100 mg C eingenommen wirdmax im Plasma beträgt durchschnittlich 54 ng / ml. Nach intranasaler Verabreichung Cmax im Plasma wird nach 1–1,5 Stunden erreicht und beträgt 12,9 ng / ml.
Der durchschnittliche Wert der absoluten Bioverfügbarkeit bei oraler Einnahme beträgt 14% aufgrund des präsystemischen Metabolismus und der unvollständigen Absorption. Aufgrund des präsystemischen Metabolismus beträgt der durchschnittliche Wert der absoluten Bioverfügbarkeit während der intranasalen Anwendung 15,8% bei p / c-Einführung. Bei Patienten mit eingeschränkter Leberfunktion ist aufgrund einer Abnahme der Presystem-Clearance ein Anstieg des Sumatriptanspiegels im Plasma zu erwarten.
Der Bindungsgrad mit Plasmaproteinen ist gering (14–21%), die Gesamtverteilung beträgt durchschnittlich 170 l, T1/2 - ca. 2 Stunden. Die Gesamtplasma-Cl beträgt durchschnittlich 1160 ml / min, die Nieren-Cl - 260 ml / min, die nach der Montage-Clearance - etwa 80% der Gesamtclearance.
Bei Jugendlichen (12–17 Jahre) der Durchschnittswert von Cmax im Plasma beträgt 13,9 ng / ml, durchschnittliches T1/2 - ca. 2 Stunden. Bei Jugendlichen mit Übergewicht nimmt die Clearance und Verteilung des Arzneimittels zu, sodass sie bei einem geringeren Körpergewicht eine höhere Exposition gegenüber Sumatriptan aufweisen.
Der Hauptmechanismus zur Entfernung von Sumatriptan ist der oxidative Metabolismus, der unter dem Einfluss des MAO-Typ-A-Enzyms durchgeführt wird. Der Hauptmetabolit - das submatriptane endoraceous Analogon - wird hauptsächlich mit Urin abgeleitet, wo er in Form von freier Säure und Glucuronidkonjugat vorliegt. Dieser Metabolit hat keine Aktivität in Bezug auf 5-HT1- oder 5-HT2Rezeptoren. Sekundärmetaboliten werden nicht identifiziert. Die Anfälle von Migräne scheinen keinen signifikanten Einfluss auf die Pharmakokinetik von Sumatriptan zu haben, das nach innen oder intranasal eingenommen wird.
Im Inneren wird das Sumatriptan schnell absorbiert. 70% von Cmax im Serum wird nach 45 Minuten erreicht. Der Durchschnittswert der absoluten Bioverfügbarkeit beträgt aufgrund des Presystemstoffwechsels und der unvollständigen Absorption 14%. Der Bindungsgrad mit Plasmaproteinen ist gering (14–21%), T1/2 - 2 Stunden. Der Hauptmetabolit (Induxusanalogon des Sumatriptans) wird hauptsächlich mit Urin in Form von freier Säure und seinem Glucuronidkonjugat abgeleitet.
Nach der Einnahme absorbierte das Sumatriptan schnell 70% von Cmax im Plasma wird nach 45 Minuten erreicht. Nach Einnahme von 100 mg Cmax im Blutplasma sind durchschnittlich 54 ng / ml. Die Bioverfügbarkeit beträgt 14% aufgrund des intensiven Vorsystemstoffwechsels und der unvollständigen Absorption. Die Bindung von Plasmaproteinen ist gering (14–21%). Sumatriptan wird unter dem Einfluss von MAO-A metabolisiert. Der Hauptmetabolit - das submatriptane endoraceous Analogon - wird hauptsächlich mit Urin in Form von freier Säure ausgeschieden und mit Glucuronsäure konjugiert. Dieser Metabolit hat keine Aktivität in Bezug auf 5-NT1- und 5-NT2-Serotoninrezeptoren. Die Anfälle von Migräne scheinen keinen signifikanten Einfluss auf die Pharmakokinetik des nach innen gerichteten Sumatriptans zu haben.


- Anti-Migren-Medikament [Serotonerge Mittel]

Die Wechselwirkung von Sumatriptan mit Propranolol, Flunarizin, Pysotifen und Ethylalkohol wurde nicht festgestellt. Gleichzeitig wurde mit Ergotamin ein langfristiger Gefäßkrampf beobachtet (Sumatriptan kann frühestens 24 Stunden nach Einnahme von Ergotamin enthaltenden Arzneimitteln verschrieben werden, und Ergotamin enthaltende Arzneimittel können frühestens 6 Stunden nach Einnahme des Sumatriptans verschrieben werden). Möglicherweise ist die Wechselwirkung zwischen dem Sumatriptan und den MAO-Inhibitoren bei ihrer gleichzeitigen Anwendung kontraindiziert.
Es gibt separate Berichte über die Entwicklung von Schwäche, Hyperreflexie und beeinträchtigter Koordination bei Patienten nach gleichzeitiger Einnahme von Sumatriptan und Medikamenten aus der Gruppe der selektiven Serotonin-Wiederaufnahmehemmer (SIOS). Bei gleichzeitiger Ernennung von Sumatriptan und SSRIs sollte der Zustand des Patienten sorgfältig überwacht werden.
Wir werden die gleichzeitige Verwendung von Mitteln, die schwammige Alkaloide, Lithiumpräparate, neuronalen Entzug von Serotonin und MAO-Inhibitoren enthalten, nicht zulassen.
Die Wechselwirkung von Sumatriptan mit Propranolol, Flunarizin, Pysotifen und Ethylalkohol wurde nicht festgestellt.
Gleichzeitig mit Ergotamin oder anderen Tryptanen / Agonisten der 5-NT-Rezeptor1 Ein längerer Krampf der Gefäße wurde festgestellt. Sumatriptan kann frühestens 24 Stunden nach Einnahme von Arzneimitteln verschrieben werden, die Ergotamin oder andere Tryptane / Agonisten des 5-NT-Rezeptors enthalten1 Im Gegenteil, ergotaminhaltige Arzneimittel können frühestens 6 Stunden nach Einnahme des Sumatriptans und Tryptane / Agonisten des 5-NT-Rezeptors verschrieben werden.1 - nicht früher als 24 Stunden nach Einnahme des Sumatriptans.
Vielleicht ist die Wechselwirkung zwischen dem Sumatriptan und den MAO-Inhibitoren, deren gleichzeitige Anwendung kontraindiziert ist.
Es gibt sehr seltene Berichte aus der Überwachung nach dem Inverkehrbringen über die Entwicklung des Serotonin-Syndroms (einschließlich psychischer Störungen, vegetativer Labilität und neuromuskulärer Störungen) infolge der gleichzeitigen Anwendung von SSRIs und Sumatriptan. Die Entwicklung des Serotonin-Syndroms vor dem Hintergrund der gleichzeitigen Ernennung von Tryptanen mit SSRIs wurde ebenfalls berichtet.
However, we will provide data for each active ingredient


