









Kompozisyon:
Tedavide kullanılır:
Oliinyk Elizabeth Ivanovna tarafından tıbbi olarak gözden geçirilmiştir, Eczane Son güncelleme: 25.03.2022

Dikkat! Sayfadaki bilgiler sadece sağlık profesyonelleri içindir! Bilgi kamu kaynaklarında toplanır ve anlamlı hatalar içerebilir! Dikkatli olun ve bu sayfadaki tüm bilgileri tekrar kontrol edin!

Çekirdek CR

Dozaj Formları Ve Güçlü Yönleri
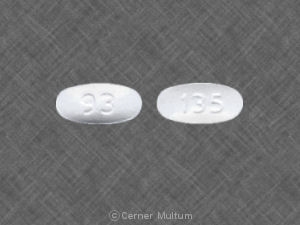
Sert jelatin kapsüller beyaz ile doldurulur kirli beyaz mikropartiküller ve aşağıdaki güçlerde mevcuttur:
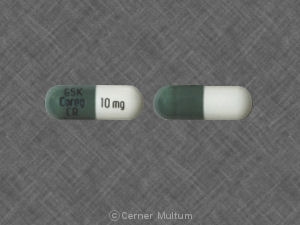
- 10 mg - " GSK " ile basılmış beyaz ve yeşil kapsül kabuğu Çekirdek CR " ve " 10 mg”
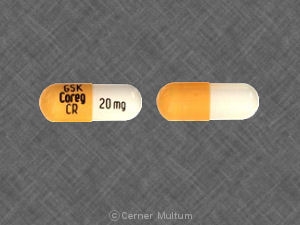
- 20 mg - " GSK " ile basılmış beyaz ve sarı kapsül kabuğu Çekirdek CR " ve " 20 mg”
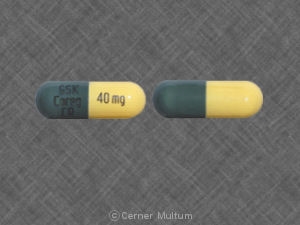
- 40 mg - " GSK " ile basılmış sarı ve yeşil kapsül kabuğu Çekirdek CR " ve " 40 mg”
- 80 mg - "GSK COREG CR" ile basılmış beyaz kapsül kabuğu” ve " 80 mg”
Depolama Ve Taşıma
Sert jelatin kapsüller aşağıdaki gibi mevcuttur güçler:
- 10 mg - " GSK " ile basılmış beyaz ve yeşil kapsül kabuğu Çekirdek CR " ve " 10 mg”
- 20 mg - " GSK " ile basılmış beyaz ve sarı kapsül kabuğu Çekirdek CR " ve " 20 mg”
- 40 mg - " GSK " ile basılmış sarı ve yeşil kapsül kabuğu Çekirdek CR " ve " 40 mg”
- 80 mg - "GSK COREG CR" ile basılmış beyaz kapsül kabuğu” ve " 80 mg”
10 mg 30 şişe: NDC 0007-3370-13
20 mg 30 şişe: NDC 0007-3371-13
40 mg 30 şişe: NDC 0007-3372-13
80 mg 30 şişe: NDC 0007-3373-13
25°C (77°F) sıcaklıkta saklayın, 15° ila 30°C (59 ° ila 86°F). Sıkı, ışığa dayanıklı bir kapta dağıtın.
GlaxoSmithKline, Araştırma Üçgen Parkı, NC 27709. Revize: Ekim 2015

Kalp Yetmezliği
COREG CR® için endikedir hafif ila şiddetli kronik kalp yetmezliğinin iskemik veya kardiyomiyopatik kökenli, genellikle diüretikler, ACE inhibitörleri ve digitalis, sağkalımı artırmak ve ayrıca riskini azaltmak için hastane.
Aşağıdaki Sol Ventrikül Disfonksiyonu Miyokard Enfarktüsü
COREG CR azaltmak için endikedir hayatta kalan klinik olarak stabil hastalarda kardiyovasküler mortalite miyokard enfarktüsünün akut fazı ve sol ventrikül ejeksiyonu %40'a eşit veya daha az fraksiyon (semptomatik kalpli veya kalpsiz yetmezlik).
Hipertansiyon
COREG CR için endikedir esansiyel hipertansiyon tedavisi. Bu olabilir tek başına veya diğer antihipertansif ajanlarla kombinasyon halinde kullanılır, özellikle tiyazid tipi diüretikler.

COREG CR, genişletilmiş bir sürümdür kapsül günde bir kez uygulama için tasarlanmıştır. İle kontrol edilen hastalar karvedilol tabletlerinin tek başına veya diğer ilaçlarla kombinasyon halinde derhal salınması ilaçlar, Aşağıdakilere bağlı olarak COREG CR genişletilmiş salımlı kapsüllere geçirilebilir Tablo 1'de gösterilen toplam günlük dozlar.
Tablo 1: Doz Dönüşüm
| Hemen salınan karvedilol tabletlerinin günlük dozu | COREG CR kapsüllerinin günlük dozubir |
| 6.25 mg (günde iki kez 3.125 mg) | Günde bir kez 10 mg |
| 12.5 mg (günde iki kez 6.25 mg) | Günde bir kez 20 mg |
| 25 mg (günde iki kez 12.5 mg) | Günde bir kez 40 mg |
| 50 mg (günde iki kez 25 mg) | Günde bir kez 80 mg |
| bir Karvedilol 12.5 mg veya 25 mg arasında geçen yaparken günde iki kez mg, başlangıç dozu COREG CR 20 mg veya günde bir kez 40 mg, buna göre, yaşlı hastalar veya yüksek risk altındakiler için garanti edilebilir hipotansiyon, baş dönmesi veya bayılma. Daha yüksek dozlara müteakip titrasyon uygun şekilde, en az 2 haftalık bir aralıktan sonra yapılmalıdır. |
COREG CR, sabahları günde bir kez alınmalıdır. yem. COREG CR bir bütün kapsül olarak yutulmalıdır. COREG CR ve / veya ıts içerikler ezilmemeli, çiğnenmemeli veya bölünmüş dozlarda alınmamalıdır.
Alternatif Yönetim
Kapsüller dikkatlice açılabilir ve boncuklar bir kaşık elma püresi üzerine serpilir. Elma püresi sıcak olmamalıdır çünkü bu formülasyonun değiştirilmiş salım özelliklerini etkileyebilir. İlaç ve elma püresi karışımı hemen tüketilmelidir. bütünlük. İlaç ve elma püresi karışımı gelecekteki kullanım için saklanmamalıdır. Diğer gıdalara serpilen boncukların emilimi test edilmemiştir.
Kalp Yetmezliği
DOZAJ BİREYSELLEŞTİRİLMELİ VE BİR DOKTOR TARAFINDAN YAKINDAN İZLENMELİDİR. TİTRASYON SIRASINDA DOKTOR. COREG CR'NİN başlatılmasından önce, sıvı tutulumunun en aza indirilmesi önerilir. Önerilen başlangıç dozu COREG CR, 2 hafta boyunca günde bir kez 10 mg'dır. 10 mg'lık bir dozu tolere eden hastalar günde bir kez, dozları art arda 20, 40 ve 80 mg'a yükseltilebilir en az 2 haftalık aralıklarla. Hastalar aşağıdaki durumlarda daha düşük dozlarda tutulmalıdır daha yüksek dozlar tolere edilmez.
Hastalara tedaviye başlanması tavsiye edilmelidir ve (daha az ölçüde) dozaj artışları geçici ile ilişkili olabilir ilk baş dönmesi veya baş dönmesi belirtileri (ve nadiren bayılma) dozdan bir saat sonra. Bu nedenle, bu dönemlerde, durumlardan kaçınmalıdırlar semptomların yaralanmaya neden olabileceği sürüş veya tehlikeli görevler gibi. Vazodilatatör semptomlar genellikle tedavi gerektirmez, ancak aşağıdakiler için yararlı olabilir ACE inhibitörünün dozlama süresini ACE inhibitörünün dozlama süresinden ayırın veya ACE inhibitörünün dozunu geçici olarak azaltın. Çekirdek CR dozu olmalıdır kötüleşen kalp yetmezliği veya vazodilatasyon belirtileri ortaya çıkana kadar artmamalıdır stabilize edildi
Sıvı tutma (geçici bozulma ile veya olmadan kalp yetmezliği belirtileri) dozunda bir artış ile tedavi edilmelidir söktürücüler.
Hastalar aşağıdaki durumlarda COREG CR dozu azaltılmalıdır bradikardi yaşayın (kalp atış hızı dakikada 55 atımdan az).
Baş dönmesi veya sıvı tutma atakları sırasında COREG CR'NİN başlatılması genellikle kesilmeden yönetilebilir tedavi ve sonraki başarılı titrasyon engellemez, veya bir COREG CR'YE olumlu tepki.
Miyokard Sonrası Sol Ventrikül Disfonksiyonu Enfarktüs
DOZAJ BİREYSELLEŞTİRİLMELİ VE TEDAVİ SIRASINDA İZLENMELİDİR. YUKARI TİTRASYON. COREG CR ile tedavi yatarak veya yatarak başlatılabilir. ayakta tedavi ve hasta hemodinamik olarak stabil hale geldikten sonra başlatılmalıdır ve sıvı tutma en aza indirildi. COREG CR olması tavsiye edilir günde bir kez 20 mg ile başladı ve 3 ila 10 gün sonra arttı tolere edilebilirlik, günde bir kez 40 mg'a, daha sonra bir kez 80 mg'lık hedef doza günlük. Daha düşük bir başlangıç dozu (günde bir kez 10 mg) ve / veya klinik olarak endikasyonlara göre titrasyon yavaşlayabilir (e.bin dolar. nedeniyle düşük kan basınç veya kalp atış hızı veya sıvı tutma). Hastalar üzerinde muhafaza edilmelidir daha yüksek dozlar tolere edilmezse daha düşük dozlar. Önerilen doz rejimi serum ile tedavi değişmiş olması gerekmez ya da sözlü miyokard enfarktüsünün akut fazında β-bloker
Hipertansiyon
DOZAJ BİREYSELLEŞTİRİLMELİDİR. Önerilen başlangıç COREG CR dozu günde bir kez 20 mg'dır. Bu doz tolere edilirse, Ayakta durma sistolik basınç, doz kılavuz olarak dozlandıktan yaklaşık 1 saat sonra ölçülür 7 ila 14 gün boyunca muhafaza edilmeli ve daha sonra günde bir kez 40 mg'a yükseltilmelidir gerekirse, yalak kan basıncına dayanarak, yine ayakta sistolik kullanarak tolerans için bir kılavuz olarak dozlamadan 1 saat sonra basınç. Bu doz da olmalıdır 7 ila 14 gün boyunca muhafaza edilir ve daha sonra günde bir kez 80 mg'a kadar ayarlanabilir tolere edilirse ve gerekirse. Özellikle çalışılmamış olsa da, beklenir COREG CR'NİN tam antihipertansif etkisi 7 ila 14 gün içinde görülecektir karvedilolün hemen salınmasıyla gösterildiği gibi. Toplam günlük doz gereken 80 mg aşmayacak
Bir diüretik ile birlikte uygulama beklenebilir katkı etkileri üretmek ve ortostatik bileşeni abartmak karvedilolün etkisi.
Karaciğer Yetmezliği
COREG Cr şiddetli olan hastalara verilmemelidir karaciğer bozukluğu.
Geriatrik Kullanım
Yaşlı hastaları değiştirirken (65 yaş ve üstü) acil salımlı karvedilol tabletlerinin (25 mg) daha yüksek dozlarını kim alıyor günde iki kez) COREG CR'YE, daha düşük bir başlangıç dozu (40 mg) COREG CR baş dönmesi, bayılma veya hipotansiyon olasılığını en aza indirmek için önerilir. Geçiş yapan ve tolere eden hastalar COREG CR, uygun şekilde, bir aralıktan sonra dozlarını arttırmalıdır en az 2 hafta.

COREG CR aşağıdaki durumlarda kontrendikedir:
- Bronş astım veya ilgili bronkospastik durumları. Tek dozların ardından durum astmaticus'tan ölüler bildirildi hemen serbest bırakma karvedilol.
- İkinci veya üçüncü derece AV bloğu.
- Hasta sinüs sendrom.
- Şiddetli bradikardi (kalici bir kalp pili olmadığı süre yer).
- Kardiyojenik şok olan veya dekompanse olan hastalar intravenöz inotropik tedavinin kullanımını gerektiren kalp yetmezliği. Bu tür hastalar COREG CR'Yİ başlatmadan önce önce intravenöz tedaviden vazgeçilmelidir.
- Şiddetli karaciger yetmezliği olan hastalar.
- Ciddi bir aşık duyarlık öyküsü olan hastalar Stevens-Johnson sendrom, anafilaktik reaksiyon, anjiyoödem) carvedilol veya COREG CR bileşenlerinden herhangi biri.

UYARMALAR
Bir parçası olarak dahil TEDBİRLER bölme.
TEDBİRLER
İle deneklerde COREG CR klinik çalışmalarda hipertansiyon (338 denek) ve sol ventrikül disfonksiyonu olan deneklerde miyokard enfarktüsü veya kalp yetmezliğinden sonra (187 denek), profil karvedilol fosfat ile gözlenen advers olayların genel olarak benzerdi bu, karvedilolün derhal salınmasıyla gözlenir. Bu nedenle, bu bölümde yer alan bilgiler aşağıdaki verilere dayanmaktadır: COREG CR ile kontrollü klinik çalışmaların yanı sıra anında serbest bırakma carvedilol.
Tedavinin Kesilmesi
Koroner arter hastalığı olan hastalar COREG CR ile tedavi, ani kesilmesine karşı düşünülmelidir tedavi. Anjinanın şiddetli alevlenmesi ve miyokard oluşumu anjina hastalarında enfarktüs ve ventrikler aritmiler bildirilmiştir β-blokerler ile tedavinin aniden kesilmesinden sonra. Son 2 kompleks, hastanın alevlenmesinden önce veya önce ortaya çıkabilir. anjina pektoris. Diğer β-blokerlerde olduğu gibi, COREG CR planlanıyor, hastalar dikkatlı bir şekilde izlenmeli ve önerilmelidir fiziksel aktiviti en aza indir. COREG CR 1'den fazla durdurulmalıdır Mümkün olduğunda 2 hafta. Anjina kötüleşirse veya akut koroner yeterli gelişim, COREG CR'NİN derhal yapımı önerilir en azından geçen olarak yeniden yerleştirildi. Çünkü koroner arter hastalığı yaygındır ve tanıyamaz, tedaviyi bırakmamak gerekir COREG CR, sadece hipertansion veya kalp için tedavi edilen hastalarda safra aniden başarzlısızklık
Bradikardi
Hemen salınan karvedilol ile klinik çalışmalarda, hipertansif hastaların yaklaşık %2'sinde, kalbin %9'unda bradikardi bildirilmiştir başarısız denekler ve sol miyokard enfarktüsü olan deneklerin %6.5'i ventriküler disfonksiyon. Bradikardi alan deneklerin %0.5'inde bildirilmiştir Kalp yetmezliği ve miyokard enfarktüsü deneklerinin çalışmasında COREG CR sol ventrikül disfonksiyonu olan denekler. Hiçbir rapor yoktu hipertansiyonda COREG CR'NİN klinik çalışmasında bradikardi. Ancak, nabız hızı dakikada 55 atımın altına düşer, COREG CR dozu aşağıdaki gibi olmalıdır düşük.
Hipotansiyon
Öncelikle hafif ila orta dereceli kalbin klinik çalışmalarında hemen salınan karvedilol, hipotansiyon ve postural hipotansiyon ile başarısızlık 9 yılında meydana geldi.% 7 ve 3 senkop.Karvedilol alan deneklerin %4'ü karşılaştırıldığında 3 ile.6 % ve 2.Plasebo deneklerinin %5'i sırasıyla. Bu olaylar için risk dozlamanın ilk 30 günü boyunca en yüksek seviyedeydi. titrasyon periyodu ve 0'da tedavinin kesilmesine neden oldu.%7 karvedilol denekleri, 0 ile karşılaştırıldığında.Plasebo deneklerin %4'ü. Uzun vadede, şiddetli kalp yetmezliği (COPERNİCUS), hipotansiyon ve postural hipotansiyon 15 yaşında ortaya çıktı.1 % ve senkop 2.Deneklerin %9'u 8 ile karşılaştırıldığında karvedilol alan kalp yetmezliği.7 % ve 2.Plaseboların %3'ü konular, sırasıyla. Bu olayların kesilmesi için bir neden vardı 1'de terapi.Karvedilol deneklerinin %1'i, 0 ile karşılaştırıldığında.Plasebo deneklerin %8'i
Kalp yetmezliği olan denekleri karşılaştıran bir çalışmada CR çekirdeğini oluşturmak veya karvedilolün hemen salınmasını sağlamak için 2 kat vardı hipotansiyon, bayılma veya baş dönmesi kombine insidansında artış yaşlı denekler (65 yaşından büyük) en yüksek dozdan geçti karvedilol (günde iki kez 25 mg) günde bir kez 80 mg çekirdeğe.
Hipertansif hastalarda COREG CR'NİN klinik çalışmasında denekler, COREG CR alan deneklerin %0.3'ünde senkop rapor edildi. deneklerin %0'ı plasebo ile tedavi edilir. Postüral hiçbir rapor yoktu bu denemede hipotansiyon. Postural hipotansiyon %1.8 ve senkopta meydana geldi Hemen salınan karvedilol alan hipertansif hastaların %0.1'i, öncelikle başlangıç dozunu takiben veya doz artışı sırasında ve bunun için bir neden oldu deneklerin %1'inde tedavinin kesilmesi.
Oğlak burcunda akut bir hastalıktan kurtulanların yargılanması sol ventriküler disfonksiyon, hipotansiyon ile miyokard infarktüsü ya postural hipotansiyon, karvedilol alan deneklerin %20.2'sinde meydana geldi plasebo deneklerin %12.6'sı ile karşılaştırıldığında. Senkop %3.9 ve %1.9 olarak rapor edildi% denekler, sırasıyla. Bu olayların kesilmesi için bir neden vardı karvedilol alan deneklerin %2.5'inde tedavi, plaseboların %0.2'sine kıyasla Konulular.
Düşük dozdan başlayarak, gıda ile uygulama ve kademeli titrasyon, bayılma veya aşırı bayılma olasılığını azaltmalıdır hipotansiyon.
Tedavinin başlatılması sırasında hasta aşağıdaki gibi olmalıdır: yaralanmaların meydana geldiği sürüş veya tehlikeli görevler gibi durumlardan kaçınmaya dikkat edin ortaya senkop gerekir neden olabilir.
Kalp Yetmezliği / Sıvı Tutma
Kötüleşen kalp yetmezliği veya sıvı retansiyonu oluşabilir karvedilolün titrasyonu sırasında. Eğer bu belirtiler görülürse, diüretik olmalıdır artmış ve COREG CR dozu klinik stabiliteye kadar ilerlememelidir ettiriyor. Bazen bunu yapmak için gereklidir COREG CR dozunu azaltın veya geçici olarak durdurun. Bu tür bölümler yok çekirdeğin sonraki başarılı titrasyonunu veya olumlu tepkisini ortadan kaldırın CR. Ciddi kalp yetmezliği olan deneklerin plasebo kontrollü bir çalışmasında, ilk 3 ay boyunca kötüleşen kalp yetmezliği benzer bir şekilde rapor edildi hemen salınan karvedilol ve plasebo ile derece. Tedavi ne zaman yapıldı 3 aydan fazla süren kalp yetmezliğinin alevlenmesi daha az rapor edildi karvedilol ile tedavi edilen deneklerde plasebodan daha sık görülür. Kötüleşmiş uzun süreli tedavi sırasında gözlenen kalp yetmezliğinin AŞAĞIDAKİLERLE ilişkili olması daha olasıdır hastaların altta yatan hastalığı karvedilol ile tedavi edilmekten daha fazladır
Alerjik olmayan bronkospazm
Bronkospastik hastalığı olan hastalar (örneğin, kronik bronşit ve amfizem) genel olarak β-blokerleri almamalıdır. ATENOLOL CR dikkatli kullanılması, ancak hasta olabilir cevap , veya diğer antihipertansif ajanlara tahammül edemez. COREG CR ise ihtiyatlı en küçük etkili dozu kullanmak için kullanılır, böylece endojen inhibisyonu veya eksojen β-agonistleri en aza indirilir.
Kalp yetmezliği olan deneklerin klinik çalışmalarında, bronkospastik hastalığı olan denekler, oral tedaviye ihtiyaç duymazlarsa kayıt altına alındı veya bronkospastik hastalıklarını tedavi etmek için inhale ilaç. Bu tür hastalarda, COREG CR'NİN dikkatli kullanılması önerilir. Dozajlama öneriler yakından takip edilmeli ve aşağıdaki durumlarda doz azaltılmalıdır titrasyon sırasında herhangi bir bronkospazm belirtisi gözlenir.
Tip 2 Diabetes Mellitusta Glisemik Kontrol
Genel olarak, β-blokerler bazı maskeleyebilir hipoglisemi belirtileri, özellikle taşikardi. Seçici olmayan β-blokerler insüline bağlı hipoglisemiyi güçlendirebilir ve iyileşmeyi geciktirebilir serum glikoz seviyeleri. Spontan hipoglisemiye maruz kalan hastalar veya insülin veya oral hipoglisemik ajanlar alan diabetes mellituslu hastalar bu olasılıklar konusunda uyardı.
Diabetes mellituslu kalp yetmezliği hastalarında karvedilol terapi, yoğunlaşmaya cevap veren kötüleşen hiperglisemiye yol açabilir hipoglisemik tedavi. Aşağıdaki durumlarda kan şekeri seviyelerinin izlenmesi önerilir COREG CR ile dozlama başlatılır, ayarlanır veya durdurulur. Tasarlanan denemeler karvedilolün glisemik kontrol üzerindeki etkilerini incelemek diyabet ve kalp yetmezliği yapılmamıştır.
Etkilerini incelemek için tasarlanmış bir çalışmada hafif ila orta şiddette bir popülasyonda glisemik kontrolde karvedilolün derhal salınması hipertansiyon ve iyi kontrol edilen tip 2 diabetes mellitus, karvedilol yoktu HbA1c ölçümlerine dayanan glisemik kontrol üzerinde olumsuz etki.
Periferik Vasküler Hastalık
β-blokerler hastalığın semptomlarını tetikleyebilir veya şiddetlendirebilir. periferik vasküler hastalığı olan hastalarda arteriyel yetmezlik. Dikkat bu tür bireylerde egzersiz yapılmalıdır.
Böbrek Fonksiyonunun Bozulması
Nadiren, kalp yetmezliği olan hastalarda karvedilol kullanımı böbrek fonksiyonlarının bozulmasına neden oldu. Risk altındaki hastalar düşük tansiyonu olanlar (sistolik kan basıncı 100 mm Hg'den az), iskemik kalp hastalığı ve diffüz vasküler hastalık ve/veya altta yatan böbrek hastalığı yetmezlik. Karvedilol olduğunda böbrek fonksiyonu başlangıç seviyesine geri döndü Durmuş. Bu risk faktörlerine sahip hastalarda böbrek yetmezliği önerilir. COREG CR'NİN titrasyonu ve ilacın durdurulması sırasında fonksiyon izlenmelidir veya böbrek fonksiyonunun kötüleşmesi durumunda dozaj azaltılır.
Büyük Cerrahi
Kronik olarak uygulanan beta blokerlerle tedavi edilmemelidir bununla birlikte, büyük bir ameliyattan önce rutin olarak geri çekilmek, refleks adrenerjik uyaranlara cevap vermek için kalp, genel anestezi ve cerrahi işlemler.
Tirotoksikoz
β-adrenerjik blokaj klinik bulguları maskeleyebilir taşikardi gibi hipertiroidizm. Β-blokajın ani geri çekilmesi olabilir hipertiroidizm semptomlarının alevlenmesi veya tiroid fırtınasını çökeltin.
Feokromositoma
Feokromositomalı hastalarda α-blokaj ajan, herhangi bir β-bloke edici ajan kullanılmadan önce başlatılmalıdır. Engelleme farmakolojik Allegra hem a rağmen - ve beta- bununla birlikte, bu durumda kullanımı ile ilgili herhangi bir deneyim olmamıştır. Bu nedenle, karvedilol alırken dikkatli olunmalıdır. feokromositoma olduğundan şüphelenilen hastalar.
Prinzmetal'in varyant Anjinası
Seçici olmayan β-bloke edici aktiviteye sahip ajanlar Prinzmetal'in varyant anjinası olan hastalarda göğüs ağrısına neden olur. Orada olmuştur bu hastalarda karvedilol ile klinik deneyim olmamasına rağmen α-bloke edici aktivite bu tür semptomları önleyebilir. Ancak, dikkatli olunmalıdır COREG CR'NİN uygulanmasından şüphelenilen hastalara alınması Prinzmetal'in varyant anjinası.
Anafilaktik Reaksiyon Riski
Β-blokerleri alırken, öyküsü olan hastalar alerjenler çeşitli ciddi anafilaktik reaksiyon daha reaktif olabilir tekrarlanan meydan okuma, kazara, teşhis veya tedavi edici. Böyle hastalar tedavi etmek için kullanılan normal epinefrin dozlarına yanıt vermeyebilir alerjik reaksiyon.
İntraoperatif Disket İris Sendromu
İntraoperatif disket İris sendromu (IFIS) alfa-1 blokerleri ile tedavi edilen bazı hastalarda katarakt ameliyatı sırasında gözlenir (COREG CR bir alfa / beta engelleyicidir). Küçük pupil sendromunun bu varyantı buna yanıt olarak dalgalanan sarkık bir irisin kombinasyonu ile karakterize edilir intraoperatif sulama akımları, ilerleyici intraoperatif miyozis standart midriatik ilaçlarla preoperatif dilatasyon ve potansiyel prolapsus fakoemülsifikasyon insizyonlarına doğru iris. Hasta oftalmolog cerrahide Olası değişiklikler için hazırlanmalıdır iris kancaları, iris dilatör halkaları veya iris dilatör halkaları gibi teknikler. viskoelastik maddeler. Durmanın bir yararı yok gibi görünüyor katarakt ameliyatı öncesi alfa-1 bloker tedavisi
Hasta Danışmanlığı Bilgileri
Hastaya FDA onaylı hastası okumasını tavsiye edin etiketleme (hasta bilgileri).
COREG CR alan hastalar tavsiye edilmelidir izleyen:
- Hastalar COREG'İ kesmemeli veya kesmemelidir Doktor tavsiyesi olmadan CR.
- Kalp yetmezliği olan hastalar danışmalısınız doktor, kötüleşen kalp yetmezliği tanımları veya semptomları yaşarsa kilo alımı veya artan nefes darlığı gibi.
- Hastalar kan baskında bir düşüş yaşayabilir ayakta durmak, baş dönmesi ve nadir bayılma ile sonuçlanır. Hastalar oturmalı veya bu düşük tansion tanımları ortaya çıktığı uzanın.
- Baş dönmesi veya yorgunluk yaşar, hastalar sürüş veya teknik görevlerden kaçının.
- Hastalar yaşarsa bir doktora danışmalıdır dozajın ayarlanması durumunda baş dönmesi veya bayılma.
- Hastalar COREG CR kapsüllerini ezmemeli veya çiğnememelidir.
- Hastalar COREG CR'Yİ yiyerek birlikte almaktır.
- Diabetes mellituslu hastalar kandaki herhangi bir değişimi bildirmelidir doktorlara şeker sevisi.
- Kontakt lens kullananlar azalmış olabilir lakrimasyon.
Klinik Olmayan Toksikoloji
Karsinogenez, Mutajenez, Doğurganlık Bozukluğu
Sıçanlarda yapılan 2 yıllık çalışmalarda karvedilol at verildi. günde kg başına 75 mg'a kadar dozlar (m2 başına mg ile karşılaştırıldığında MRHD'NİN 12 katı baz) veya farelerde günde kg başına 200 mg'a kadar verilir (mg başına MRHD'NİN 16 katı m2 bazında), karvedilolün kanserojen etkisi yoktu.
Karvedilol, bir bataryada test edildiğinde negatifti Ames ve Cho/HGPRT testleri de dahil olmak üzere genotoksisite testleri mutajenite ve in vitro hamster mikronükleus ve in vivo insan lenfosit klastojenite için hücre testleri.
Günde kg başına 200 mg'dan büyük veya eşit dozlarda (m2 başına mg olarak MRHD'NİN 32 katından büyük veya eşit) karvedilol toksikti yetişkin sıçanlara (sedasyon, kilo alımında azalma) ve kilo alımında azalma ile ilişkiliydi. başarılı çiftleşme sayısı, uzun süreli çiftleşme süresi, önemli ölçüde daha az corpora lutea ve baraj başına implantlar ve %18'in tam rezorpsiyonu çöpler. Açık toksisite ve ilacın bozulması için gözlemlenmemiş etki doz seviyesi doğurganlık günde kg başına 60 mg idi (m2 başına mg olarak MRHD'NİN 10 katı).
Belirli Popülasyonlarda Kullanım
Gebelik
Gebelik Kategorisi C
Hamile sıçanlarda ve tavşanlarda yapılan çalışmalar karvedilol, sıçanlarda 300 mg dozlarında implantasyon sonrası kayıpların arttığını gösterdi günde kg başına (m2 başına mg olarak önerilen maksimum insan dozunun [MRHD] 50 katı) ve tavşanlarda günde kg başına 75 mg dozlarda (m2 başına mg olarak MRHD'NİN 25 katı). Sıçanlarda, maternal olarak fetal vücut ağırlığında da bir azalma vardı toksik doz günde kg başına 300 mg'dır (m2 başına mg olarak MRHD'NİN 50 katı). gecikmiş iskelet ile fetüslerin sıklığında bir artış eşlik eder geliştirme (eksik veya bodur 13. kaburga). Sıçanlarda gözlemlenmemiş etki seviyesi gelişimsel toksisite için günde kg başına 60 mg (mg olarak MRHD'NİN 10 katı m2 başına), tavşanlarda günde kg başına 15 mg idi (m2 başına mg olarak MRHD'NİN 5 katı). Gebe kadınlarda yeterli ve iyi kontrol edilen çalışmalar yoktur. ÇEKİRDEK CR hamilelik sırasında sadece potansiyel fayda haklı çıkarsa kullanılmalıdır. fetus için potansiyel risk
Emziren Anneler
Bu ilacın insan vücudundan atılıp atılmadığı bilinmemektedir süt. Sıçanlarda yapılan çalışmalar, karvedilol ve/veya metabolitlerinin (as diğer β-blokerler gibi) plasental bariyeri geçer ve vücuttan atılır. anne sütü. Yenidoğanlarda doğum sonrası 1. haftada mortalite arttı günde kg başına 60 mg ile tedavi edilen sıçanlardan (m2 başına mg olarak MRHD'NİN 10 katı) ve son trimesterde laktasyonun 22. gününe kadar. Çünkü birçok ilaçlar insan sütüne atılır ve ciddi enfeksiyon potansiyeli nedeniyle. emziren bebeklerde β-blokerlerden kaynaklanan ADVERS REAKSİYONLAR, özellikle bradikardi, emzirmeyi bırakmaya veya bırakmaya karar verilmelidir ilacın anne için önemini dikkate alarak ilaç. Bu diğer α - ve β-bloke edici ajanların etkileri perinatal ve neonatal sıkıntı
Pediatrik Kullanım
18 yaşından küçük hastalarda karvedilolün etkinliği yıllar kurulmamıştır.
Çift kör bir çalışmada, 161 çocuk (ortalama yaş: 6 yıl, Aralık: 2 ay ila 17 yıl, 2 yıldan %45 daha genç) kronik kalp ile başarısızlık [NYHA Sınıf II-IV, sol ventrikül ejeksiyon fraksiyonu %40'dan az sistemik sol ventrikül (LV) ve orta-şiddetli ventriküler sistemik ventrikülü olanlar için niteliksel olarak echo disfonksiyonu standart arka plan tedavisi alan bir LV değil] randomize edildi plasebo veya 2 doz karvedilol seviyesine kadar. Üretilen bu doz seviyeleri dakikada 4 ila 6 kalp atışının plasebo düzeltilmiş kalp atış hızı azalması, β-blokaj aktivitesinin göstergesi. Maruz kalma daha düşük olduğu ortaya çıktı yetişkinlerden daha pediatrik konular. 8 aylık takipten sonra tedavinin klinik sonuçlar üzerindeki önemli etkisi. Bu durumda ADVERS REAKSİYONLAR tedavi edilen deneklerin %10'undan fazlasında meydana gelen bir çalışma karvedilolün derhal salınması ve plasebo ile tedavi edilen deneklerin iki katı oranında göğüs ağrısı (%17'ye karşı %6), baş dönmesi (%13'e karşı %2) ve nefes darlığı dahil (%11'e karşı 0%)
Geriatrik Kullanım
Deneklerde COREG CR'NİN ilk klinik denemeleri hipertansiyon, kalp yetmezliği ve sol ventrikül disfonksiyonu miyokard enfarktüsü 65 yaşında yeterli sayıda denek içermiyordu daha gençlerden farklı tepki verip vermediklerini belirlemek için yıllar veya daha büyük hastalar.
Hafif hastalıklı denekleri karşılaştıran randomize bir çalışma (n = 405) ciddi kalp yetmezliğine COREG CR'YE geçti veya hemen serbest bırakıldığında devam etti karvedilol, 65 yaş ve üstü 220 deneği içeriyordu. Bunda yaşlı alt grup, baş dönmesi, hipotansiyon veya senkop kombine insidansı deneklerin %24'ü (18/75) en yüksek derhal serbest bırakma dozundan geçti karvedilol (günde iki kez 25 mg) en yüksek COREG CR dozuna (bir kez 80 mg günlük), hemen serbest bırakıldığında sürdürülen deneklerde %11 (4/36) ile karşılaştırıldığında karvedilol (günde iki kez 25 mg). Daha yüksek dozlardan anında serbest bırakıldığında carvedilol COREG CR'YE, yaşlılar için daha düşük bir başlangıç dozu önerilir hastalar
Aşağıdaki bilgiler ile denemeler için kullanılabilir hemen serbest bırakma karvedilol. Kalp yetmezliği olan 765 denekten randomize ABD klinik çalışmalarında karvedilol için, %31'i (235) 65 yaş ve üstü idi ve 7.%3'ü (56) 75 yaş ve üstü idi. 1.156 denekten randomize ciddi kalp yetmezliğinde uzun süreli, plasebo kontrollü bir çalışmada karvedilol, Bunların %47'si (547) 65 yaş ve üstü, %15'i (174) 75 yaş ve üstü idi. büyük. Kalp yetmezliği denemelerinde karvedilol alan 3,025 denek dünya çapında, %42'si 65 yaş ve üstü. Miyokardiyal 975 denekten Oğlak denemesinde karvedilol ile randomize enfarktüs, %48 (468) yaşlandı 65 yaş ve üstü ve %11'i (111) 75 yaş ve üstü idi. Arasında 2,065 ABD klinik çalışmalarında etkinlik veya güvenlik konusunda hipertansif denekler karvedilol ile tedavi edilen hastaların %21'i (436) 65 yaş ve üstü idi. 3,722 arasında hipertansiyon klinik çalışmalarında hemen salınan karvedilol alan denekler dünya çapında yapılanların %24'ü 65 yaş ve üstü
Hipertansif hastalarda baş dönmesi hariç (yaşlılarda insidans %8.8, genç deneklerde %6), genel olarak yok güvenlik veya etkinlikteki farklılıklar gözlendi (bkz. Şekil 2 ve 4) bu popülasyonların her birinde yaşlı denekler ve genç denekler arasında. Benzer şekilde, bildirilen diğer klinik deneyimler, yaşlı ve genç denekler arasındaki tepkiler, ancak daha fazla duyarlılık bazı yaşlı bireyler göz ardı edilemez.

YAN ETKİLER
Klinik Denemeler Deneyimi
Karvedilol ile deneklerde güvenlik açısından değerlendirilmiştir sol ventrikülü olan hastalarda kalp yetmezliği (hafif, orta ve şiddetli) miyokard enfarktüsü sonrası disfonksiyon ve hipertansif hastalarda. Bu gözlenen advers olay profili ilacın farmakolojisi ile tutarlıydı ve klinik çalışmalarda deneklerin sağlık durumu. Yan etkiler bu popülasyonların her biri için COREG CR veya COREG Cr kullanımını yansıtan rapor edilmiştir. karvedilolün hemen salınması aşağıda verilmiştir. Hariç tutulan advers olaylar bilgilendirici olmak için çok genel olarak kabul edilir ve makul bir şekilde ilişkili olmayanlar bu durum ile ilişkili olduğu için ilacın kullanımı ile tedavi edilen veya tedavi edilen popülasyonda çok yaygındır. Advers olayların oranları genel olarak demografik alt kümeler arasında benzerdi (erkekler ve kadınlar, yaşlılar ve yaşlılar). yaşlı olmayan, siyahlar ve siyahlar). COREG CR güvenlik açısından değerlendirildi 4 Hafta (2 hafta hemen serbest bırakma karvedilol ve 2 hafta çekirdek CR) stabil hafif hastalığı olan 157 deneği içeren klinik çalışma (n = 187) , orta veya şiddetli kronik kalp yetmezliği ve sol ventrikül ile 30 denekler akut miyokard enfarktüsü sonrası disfonksiyon. Olumsuz profil bu küçük, kısa süreli çalışmada COREG CR ile gözlenen olaylar genellikle hemen salınan karvedilol ile gözlemlenene benzer. Farklılıklar çekirdek için plazma seviyelerindeki benzerliğe bağlı olarak güvenlik beklenmez CR ve hemen serbest bırakma karvedilol
Kalp Yetmezliği
Aşağıdaki bilgiler Güvenlik deneyimini açıklar hemen salınan karvedilol ile kalp yetmezliğinde.
Karvedilol kalp yetmezliğinde güvenlik açısından değerlendirildi dünya çapında 4.500'den fazla konuda 2.100'den fazla kişi katıldı plasebo kontrollü klinik çalışmalar. Tedavi edilen toplamın yaklaşık %60'ı plasebo kontrollü klinik çalışmalarda popülasyon at için karvedilol aldı en az 6 ay ve %30'u en az 12 ay boyunca karvedilol aldı. KUYRUKLUYILDIZIN içinde hafif ila orta derecede kalp yetmezliği olan 1511 denek ile tedavi edildi 5'e kadar karvedilol.9 yıl (ortalama: 4.8 yıl). Her ikisi de ABD'de klinik çalışmalarda günlük dozlarda karvedilol ile karşılaştırıldığında hafif ila orta derecede kalp yetmezliği Plasebo (n = 437) ile 100 mg (n = 765) ve çok uluslu bir klinik çalışmada şiddetli kalp yetmezliğinde (COPERNİCUS), günlük dozlarda karvedilolü karşılaştırdı plasebo (n = 1,133) ile 50 mg'a (n = 1,156) kadar, olumsuz deneyimler karvedilol ve plasebo deneklerinde benzerdi. İçinde plasebo kontrollü klinik çalışmalar, ilacın kesilmesinin tek nedeni daha büyüktür. %1'den fazla ve karvedilol üzerinde daha sık meydana gelen baş dönmesi (1.% 3 açık carvedilol, 0.COPERNİCUS denemesinde plaseboda %6)
Tablo 2, deneklerde bildirilen advers olayları göstermektedir ABD plasebo kontrollü klinikte kayıtlı hafif ila orta derecede kalp yetmezliği çalışmalar ve COPERNİCUS denemesinde kayıtlı ciddi kalp yetmezliği ile. Gösterilen ilaçla tedavi edilen deneklerde daha sık meydana gelen advers olaylar deneklerde insidansı %3'ten fazla olan plasebo ile tedavi edilen denekler nedensellikten bağımsız olarak karvedilol ile tedavi edilir. Medyan deneme ilaç maruz kalma 6 idi.Denemelerde hem karvedilol hem de plasebo denekleri için 3 ay hafif ila orta derecede kalp yetmezliği ve 10.Deneklerin yargılanmasında 4 ay şiddetli kalp yetmezliği ile. Karvedilolün advers olay profili KUYRUKLUYILDIZIN uzun vadeli çalışması genellikle ABD'de gözlemlenene benziyordu Kalp Yetmezliği Denemeleri.11
Tablo 2: Daha Sık Meydan Gelen Advers Olaylar (%)
Karvedilolün plasebodan hemen salınması ile denekler
(HF) hafif-Orta Kalp yeterliği BİZİ Kalp Yetmezliği Denemeler veya Kayıtlı
COPERNİCUS çalışmasında ciddi kalp yetmezliği olan denekler (insidans > %3
Nedensellikten bağımsız olarak karvedilol ile tedavi edilen denekler)
| Vücut Sistemi / Olumsuz Olay | Hafif ila orta derecede HF | Şiddetli HF | ||
| Karvedilol (n = 765) |
Plasebo (n = 437) |
Karvedilol (n = 1,156) |
Plasebo (n = 1,133) |
|
| Bir bütün olarak vücut | ||||
| Asteni | 7 | 7 | 11 | 9 |
| Yorgunluk | 24 | 22 | — | — |
| Digoksin seviyesi arttı | 5 | 4 | 2 | 1 |
| Ödeme genelleştirildi | 5 | 3 | 6 | 5 |
| Ödemeli | 4 | 2 | — | — |
| Kardiyovasküler sistem | ||||
| Bradikardi | 9 | 1 | 10 | 3 |
| Hipotansiyon | 9 | 3 | 14 | 8 |
| Senkop | 3 | 3 | 8 | 5 |
| Anjina pektoris | 2 | 3 | 6 | 4 |
| Merkezi Sinir Sistemi | ||||
| Baş dönmesi | 32 | 19 | 24 | 17 |
| Ağrı | 8 | 7 | 5 | 3 |
| Gastrointestinal sistem | ||||
| Ishal | 12 | 6 | 5 | 3 |
| Bulantı | 9 | 5 | 4 | 3 |
| Kusan | 6 | 4 | 1 | 2 |
| Metabolizma | ||||
| Hiperglisemi | 12 | 8 | 5 | 3 |
| Ağırlık artışı | 10 | 7 | 12 | 11 |
| Topuz arttı | 6 | 5 | — | — |
| NPN arttı | 6 | 5 | — | — |
| Hiperkolesterolemi | 4 | 3 | 1 | 1 |
| Periferik ödeme | 2 | 1 | 7 | 6 |
| Iskelet | ||||
| Artralji | 6 | 5 | 1 | 1 |
| Solunum | ||||
| Öksürük arttı | 8 | 9 | 5 | 4 |
| Hırıltı | 4 | 4 | 4 | 2 |
| Görüş | ||||
| Görme anormal | 5 | 2 | — | — |
Bu hastalarda kalp yetmezliği ve nefes darlığı da bildirilmiştir ancak plasebo alan deneklerde oranlar eşit veya daha yüksekti.
Aşağıdaki advers olaylar bir frekans %1'den fazla, ancak %3'ten az veya eşit ve daha sık deneklerde ABD plasebo kontrollü çalışmalarda karvedilol ile hafif ila orta derecede kalp yetmezliği veya şiddetli kalp yetmezliği olan deneklerde COPERNİCUS davası.
İnsidans %1'den Fazla Veya 3'e Eşit%
Bir bütün olarak vücut: Alerji, halsizlik, hipovolemi, ateş, bacak ödemi.
Kardiyovasküler sistem: Sıvı aşırı yük, postural hipotansiyon, ağırlaştırılmış anjina pektoris, av blokajı, çarpıntı, hipertansiyon.
Merkezi ve çevre sinir sistemi: Hipestezi, vertigo, parestezi.
Gastrointestinal sistem: Melena, periodontitis.
Karaciger ve safra sistemi: SGPT arttı, SGOT artmak.
Metabolik ve beslenme: Hiperürisemi, hipoglisemi, hiponatremi, artmış alkalin fosfataz, glikozüri, hipervolemi, diabetes mellitus, GGT artışı, kilo kaybı, hiperkalemi, kreatinin arttı.
Iskelet: Kas krampları.
Trombosit, kanama ve sıkıştırma: Protrombin azalmış, purpura, trombositopeni.
Psikiyatri: Uyku hali.
Üreme, erkek: İktidarsızlık.
Özel Duyular: Bulanık görme.
Ürün Sistemi: Böbrek yetmezliği, albüminüri, hematüri.
Miyokard sonrası sol ventrikül disfonksiyonu Enfarktüs
Aşağıdaki bilgiler Güvenlik deneyimini açıklar akut miyokard enfarktüsü sonrası sol ventrikül disfonksiyonu ile hemen serbest bırakma karvedilol.
Karvedilol, hayatta kalanlarda güvenlik açısından değerlendirildi sol ventrikül disfonksiyonu ile akut miyokard enfarktüsü Karvedilol alan 969 denek ve 980 denek içeren Oğlak davası plasebo aldı. Deneklerin yaklaşık %75'i at için karvedilol aldı en az 6 ay ve %53'ü en az 12 ay boyunca karvedilol aldı. Konulular ortalama 12.9 ay ve 12.8 ay boyunca karvedilol ve sırasıyla plasebo.
Karvedilol ile bildirilen en yaygın advers olaylar Oğlak denemesinde ABD'de ilacın profili ile tutarlıydı kalp yetmezliği denemeleri ve COPERNİCUS denemesi. Tek ek olumsuz Oğlak burcunda bildirilen olaylar, deneklerin %3'ünden fazlası ve daha fazlası genellikle karvedilol üzerinde dispne, anemi ve akciğer ödemi vardı. Aşağıdaki olumsuz olaylara daha az %1 den daha büyük bir frekans ile bildirildi ama veya karvedilol ile %3'e eşit ve daha sık: grip sendromu, serebrovasküler kaza, periferik vasküler bozukluk, hipotoni, depresyon, gastrointestinal ağrı, artrit ve gut. Genel oranlar advers olaylara bağlı süreksizlikler her iki grupta da benzerdi. Bu veritabanında, ilacın kesilmesinin tek nedeni %1'den fazladır ve karvedilolde daha sık görülen hipotansiyon (1.Karvedilol üzerinde %5, 0.2 % açık plasebo)
Hipertansiyon
COREG CR, 8 haftada güvenlik açısından değerlendirildi esansiyel hipertansiyonu olan 337 denekte çift kör deneme. Profil COREG CR ile gözlenen advers olaylar genellikle gözlemlenene benzerdi hemen serbest bırakılan karvedilol ile. Nedeniyle süreksizliklerin genel oranları coreg CR ve plasebo arasında advers olaylar benzerdi.
Tablo 3: Daha Sık Meydan Gelen Advers Olaylar (%)
arteriyel hipertansiyon olan deneklerde plaseboya göre COREG CR ile (ınsidans ≥ 1%
Nedensellikten bağımsız olarak karvedilol ile tedavi edilen deneklerde)
| Olumsuz Olay | ÇEKİRDEK CR (n = 253) |
Plasebo (n = 84) |
| Nazofarenjit | 4 | 0 |
| Baş dönmesi | 2 | 1 |
| Bulantı | 2 | 0 |
| Periferik ödeme | 2 | 1 |
| Burun tıkanı | 1 | 0 |
| Parestezi | 1 | 0 |
| Sinüs tıkanığı | 1 | 0 |
| Ishal | 1 | 0 |
| Uykusuzluk | 1 | 0 |
Aşağıdaki bilgiler Güvenlik deneyimini açıklar hemen salınan karvedilol ile hipertansiyonda.
Karvedilol hipertansiyonda güvenlik açısından değerlendirildi ABD klinik çalışmalarında 2.193 denek ve 2.976 denek uluslararası klinik çalışmalar. Tedavi edilen toplamın yaklaşık %36'sı nüfus en az 6 ay boyunca karvedilol aldı. Genel olarak, karvedilol günde 50 mg'a kadar olan dozlarda iyi tolere edildi. Bildirilen yan etkilerin çoğu karvedilol tedavisi sırasında hafif ila orta şiddette idi. ABD'de kontrollü 50 mg'a kadar olan dozlarda karvedilol monoterapisini doğrudan karşılaştıran klinik çalışmalar plasebo ile (n = 1.142) (n = 462), 4.Karvedilol deneklerinin %9'u durduruldu 5'e karşı advers olaylar için.Plasebo deneklerin %2'si. Hiçbir olmasına rağmen süreksizlik oranlarındaki genel fark, süreksizlikler daha yaygındı postural hipotansiyon için karvedilol grubunda (%1'e karşı 0). Genel ABD plasebo kontrollü çalışmalarda advers olayların insidansı bulundu artan karvedilol dozu ile artış. Bireysel advers olaylar için bu sadece 2'den sıklık olarak artan baş dönmesi için ayırt edilebilir% toplam günlük doz 6'dan arttıkça %5'e kadar.Tek veya bölünmüş olarak 25 mg ila 50 mg dozlar
Tablo 4, plasebo kontrollü ABD'deki advers olayları göstermektedir daha büyük bir insidans ile ortaya çıkan hipertansiyon için klinik çalışmalar nedensellik ne olursa olsun %1'e eşit veya daha fazla ve bu daha sıktı plasebo ilaç-tedavi konular-konular ele.
Tablo 4: ABD plasebo kontrol advers olaylar (% oluşumu)
Hemen salınan karvedilol ile hipertansion denemeleri (insidans ≥ 1%
Nedensellikten bağımsız olarak karvedilol ile tedavi edilen deneklerde)*
| Olumsuz Olay | Karvedilol (n = 1.142) |
Plasebo (n = 462) |
| Kardiyovasküler sistem | ||
| Bradikardi | 2 | — |
| Postural hipotansiyon | 2 | — |
| Periferik ödeme | 1 | — |
| Merkezi Sinir Sistemi | ||
| Baş dönmesi | 6 | 5 |
| Uykusuzluk | 2 | 1 |
| Gastrointestinal sistem | ||
| Ishal | 2 | 1 |
| Hematolojik | ||
| Trombositopeni | 1 | — |
| Metabolizma | ||
| Hipertrigliseridemi | 1 | — |
| * Gösterilen oran > %1 ile olaylar en yakın yuvarlanır tamsayi'yi. | ||
Bu çalışmalarda nefes darlığı ve yorgunluk da bildirilmiştir, ancak plasebo alan deneklerde oranlar eşit veya daha yüksekti.
Yukarıda açıklanmayan aşağıdaki yan etkiler şunlardı dünya çapında açık veya açık olarak karvedilol ile ilgili olarak rapor edilmiştir. hipertansiyon ya da kalp ile konularda Allegra ile kontrollü deneyler başarısızlık.
İnsidans %0.1'den Büyük Veya 1'e Eşit%
Kardiyovasküler sistem: Periferik iskemi, taşikardi.
Merkezi ve çevre sinir sistemi: Hipokinezi.
Gastrointestinal sistem: Bilirubinemi, artmış karaciğer enzimler (hipertansiyon hastalarının %0.2'si ve kalp yetmezliği hastalarının %0.4'ü) hepatik enzimlerdeki artışlar nedeniyle tedaviden çıkarıldı).
Psikiyatri: Sinirlilik, uyku bozukluğu, ağırlaştırılmış depresyon, konsantrasyon bozukluğu, anormal düşünme, paroniria, duygusal kararsızlık.
Solunum Sistemi: Astma.
Üreme, erkek: Libido azaldı.
Cilt ve ekler: Kaşıntı, eritematöz döküntü, döküntü makülopapüler, döküntü sedef formu, ışığa duyarlılık reaksiyonu.
Özel Duyular: Kulak çınlaması.
Ürün Sistemi: İşeme sıklığı arttı.
Otonom Sinir Sistemi: Ağız kuruluğu, terleme artmak.
Metabolik ve beslenme: Hipokalemi, hipertrigliseridemi.
Hematolojik: Anemi, aşırı üretimi.
Aşağıdaki olaylar eşit veya daha az rapor edildi deneklerin %0.1'ine kadar ve potansiyel olarak önemlidir: tam AV bloğu, paket dal blokajı, miyokardiyal iskemi, serebrovasküler bozukluk, konvülsiyonlar, migren, nevralji, parezi, anafilaktoid reaksiyon, alopesi, eksfolyatif dermatit, amnezi, gastrointestinal kanama, bronkospazm, pulmoner ödem, azalmış işitme, solunum alkalozu, artmış Topuz, azalmış HDL, pansitopeni ve atipik lenfositler.
Laboratuvar Anormallikleri
Serum transaminazlarında (ALT veya AST) tersinir yükselmeler) karvedilol ile tedavi sırasında gözlenmiştir. Transaminaz oranları kontrol sırasında gözlenen yükselmeler (normalin üst sınırının 2 ila 3 katı) klinik çalışmalar genellikle tedavi edilen denekler arasında benzer olmuştur karvedilol ve plasebo ile tedavi edilenler. Bununla birlikte, transaminaz yükselmeleri, rechallenge ile teyit edildi, karvedilol ile gözlemlendi. Uzun vadede, şiddetli kalp yetmezliğinde plasebo kontrollü çalışma, tedavi edilen denekler Allegra konularda daha hepatik transaminaz alt değerleri tedavi vardı plasebo ile, muhtemelen kalpte karvedilol kaynaklı gelişmeler nedeniyle fonksiyon daha az hepatik tıkanıklığa ve/veya daha iyi hepatik kan akışına yol açtı
Karvedilol tedavisi ile ilişkili değildir serum potasyumunda klinik olarak anlamlı değişiklikler, total trigliseritler, total kolesterol, HDL kolesterol, ürik asit, kan üre azotu veya kreatinin. Hayır hipertansif hastalarda açlık serum glikozunda klinik olarak anlamlı değişiklikler kaydedildi denekler, açlık serum glukozu kalp yetmezliği klinik değerlendirilmedi denemeler.
Pazarlama Sonrası Deneyim
Aşağıdaki ADVERS REAKSİYONLAR tespit edilmiştir COREG ® veya COREG CR'NİN onay sonrası kullanımı sırasında. Çünkü bu reaksiyonlar belirsiz büyüklükteki bir nüfustan gönüllü olarak rapor edildi, her zaman değil sıklıklarını güvenilir bir şekilde tahmin etmek veya nedensel bir sonuç oluşturmak mümkündür uyuşturucuya maruz kalma ile ilişki.
Kan ve lenfatik sistem bozuklukları
Aplastik anemi.
Bağışıklık Sistemi Bozuklukları
Aşırı duyarlılık (örneğin, anafilaktik reaksiyonlar, anjiyoödem, ürtiker).
Böbrek ve idrar bozuklukları
Üriner inkontinans.
Solunum, torasik ve Mediastinal bozukluklar
İnterstisyel pnömoni.
Deri ve deri altı doku bozuklukları
Stevens-Johnson sendromu, toksik epidermal nekroliz, eritema multiforme.
İLAÇ ETKİLEŞİMLERİ
CYP2D6 inhibitörleri ve zayıf Metabolizörler
Karvedilolün güçlü inhibitörleri ile etkileşimleri CYP2D6 izoenzimi (kinidin, fluoksetin, paroksetin ve propafenon gibi) henüz çalışılmamıştır, ancak bu ilaçların kan dolaşımını arttırması beklenir karvedilolün R( ) enantiyomerinin seviyeleri. Klinik çalışmalarda yan etkilerin retrospektif analizi, zayıf 2D6'NIN metabolizörler, muhtemelen titrasyon sırasında daha yüksek bir baş dönmesi oranına sahipti daha yüksek konsantrasyonlarda vazodilatasyon etkilerinden kaynaklanan α-bloke edici R( ) enantiyomeri.
Hipotansif Ajanlar
Her iki ilacı da β-blokaj ile alan hastalar özellikleri ve katekolaminleri (örneğin, reserpin ve monoamin oksidaz inhibitörleri) belirtileri için yakından gözlemlenmelidir hipotansiyon ve / veya şiddetli bradikardi.
Klonidin ile birlikte ajanlarla birlikte uygulanması β-bloke edici özellikler kan basıncını güçlendirebilir ve kalp atış hızı düşürücü etkiler. Ajanlarla birlikte tedavi edildiğinde β-bloke edici özellikler ve klonidin sonlandırılmalıdır, β-bloke edici ajan önce kesilmelidir. Klonidin tedavisi daha sonra dozajı kademeli olarak azaltarak birkaç gün sonra kesilmelidir.
Siklosporin
Ortalama yalak siklosporinde mütevazı artışlar 21 hastada karvedilol tedavisinin başlamasından sonra konsantrasyonlar gözlendi kronik vasküler reddi olan böbrek nakli denekleri. Yaklaşık olarak Deneklerin %30'unda siklosporin dozu azaltılmalıdır siklosporin konsantrasyonlarını terapötik aralıkta tutun, kalan hiçbir ayar gerekli değildi. Grup için ortalama olarak, doz bu deneklerde siklosporin yaklaşık %20 oranında azalmıştır. Geniş bireyler arası özellikler nedeniyle gerekli doz ayarlamasında değişkenlik, tavsiye edilir karvedilolün başlamasından sonra siklosporin konsantrasyonları yakından izlenmelidir tedavi ve siklosporin dozunun uygun şekilde ayarlanması
Digitalis Glikozitler
Hem digitalis glikozitleri hem de β-blokerleri yavaşlar atriyoventriküler iletim ve kalp atış hızını azaltır. Eşzamanlı kullanım olabilir bradikardi riskini arttırın. Digoksin konsantrasyonları yaklaşık olarak artar Digoksin ve karvedilol eşzamanlı olarak uygulandığında %15. Bu nedenle, digoksin artan takibi başlatan, ayarlarken tavsiye edilir, ya da COREG CR'Yİ durduruyor.
Karaciğer Metabolizmasının İndükleyicileri / İnhibitörleri
Rifampin, karvedilolün plazma konsantrasyonlarını azalttı yaklaşık %70. Simetidin altında artan alan eğri (AUC) yaklaşık %30'dur, ancak Cmaksım'da herhangi bir değişikliğe neden olmamıştır.
Amiodaron
Amiodaron ve metaboliti desetil amiodaron, CYP2C9 inhibitörleri ve P-glikoprotein S konsantrasyonlarını arttırdı(-) karvedilolün enantiyomeri en az 2 kat. Amiodaron veya diğer CYP2C9 inhibitörlerinin birlikte uygulanması COREG CR ile flukonazol, β-bloke edici özelliklerini artırabilir Allegra kalp hızı ya da kalp daha da yavaşlaması sonucu iletim. Hastalar bradikardi veya kalp belirtileri için gözlemlenmelidir blok, özellikle önceden var olan tedaviye bir ajan eklendiğinde diğer.
Kalsiyum Kanal Blokerleri
İletim bozukluğu (nadiren hemodinamik ile karvedilol diltiazem ile birlikte kullanıldığında uzlaşma gözlenmiştir. Β-bloke edici özelliklere sahip diğer ajanlarda olduğu gibi, COREG CR Verapamil veya diltiazem kalsiyum kanal blokerleri ile oral olarak uygulanır buna ek olarak, EKG ve kan basıncını izlemeniz önerilir.
İnsülin Veya Oral Hipoglisemik
Β-bloke edici özelliklere sahip ajanlar insülin ve oral hipoglisemiklerin kan şekeri azaltıcı etkisi. Bu nedenle, içinde insülin veya oral hipoglisemik alan hastalar, kanın düzenli olarak izlenmesi glikoz tavsiye edilir.
Proton Pompa İnhibitörleri
AUC ve Cmaksimum seviyelerinde klinik olarak anlamlı bir artış yoktur karvedilol genişletilmiş salımlı kapsüllerin eşzamanlı uygulanması ile pantoprazol.
Anestezi
COREG CR ile tedaviye devam edilecekse perioperatif olarak, anestezik ajanlar olduğunda özel dikkat gösterilmelidir eter, siklopropan ve diğerleri gibi miyokard fonksiyonunu inhibe edin. trikloroetilen kullanılır.

Gebelik Kategorisi C
Hamile sıçanlarda ve tavşanlarda yapılan çalışmalar karvedilol, sıçanlarda 300 mg dozlarında implantasyon sonrası kayıpların arttığını gösterdi günde kg başına (m2 başına mg olarak önerilen maksimum insan dozunun [MRHD] 50 katı) ve tavşanlarda günde kg başına 75 mg dozlarda (m2 başına mg olarak MRHD'NİN 25 katı). Sıçanlarda, maternal olarak fetal vücut ağırlığında da bir azalma vardı toksik doz günde kg başına 300 mg'dır (m2 başına mg olarak MRHD'NİN 50 katı). gecikmiş iskelet ile fetüslerin sıklığında bir artış eşlik eder geliştirme (eksik veya bodur 13. kaburga). Sıçanlarda gözlemlenmemiş etki seviyesi gelişimsel toksisite için günde kg başına 60 mg (mg olarak MRHD'NİN 10 katı m2 başına), tavşanlarda günde kg başına 15 mg idi (m2 başına mg olarak MRHD'NİN 5 katı). Gebe kadınlarda yeterli ve iyi kontrol edilen çalışmalar yoktur. ÇEKİRDEK CR hamilelik sırasında sadece potansiyel fayda haklı çıkarsa kullanılmalıdır. fetus için potansiyel risk

Klinik Denemeler Deneyimi
Karvedilol ile deneklerde güvenlik açısından değerlendirilmiştir sol ventrikülü olan hastalarda kalp yetmezliği (hafif, orta ve şiddetli) miyokard enfarktüsü sonrası disfonksiyon ve hipertansif hastalarda. Bu gözlenen advers olay profili ilacın farmakolojisi ile tutarlıydı ve klinik çalışmalarda deneklerin sağlık durumu. Yan etkiler bu popülasyonların her biri için COREG CR veya COREG Cr kullanımını yansıtan rapor edilmiştir. karvedilolün hemen salınması aşağıda verilmiştir. Hariç tutulan advers olaylar bilgilendirici olmak için çok genel olarak kabul edilir ve makul bir şekilde ilişkili olmayanlar bu durum ile ilişkili olduğu için ilacın kullanımı ile tedavi edilen veya tedavi edilen popülasyonda çok yaygındır. Advers olayların oranları genel olarak demografik alt kümeler arasında benzerdi (erkekler ve kadınlar, yaşlılar ve yaşlılar). yaşlı olmayan, siyahlar ve siyahlar). COREG CR güvenlik açısından değerlendirildi 4 Hafta (2 hafta hemen serbest bırakma karvedilol ve 2 hafta çekirdek CR) stabil hafif hastalığı olan 157 deneği içeren klinik çalışma (n = 187) , orta veya şiddetli kronik kalp yetmezliği ve sol ventrikül ile 30 denekler akut miyokard enfarktüsü sonrası disfonksiyon. Olumsuz profil bu küçük, kısa süreli çalışmada COREG CR ile gözlenen olaylar genellikle hemen salınan karvedilol ile gözlemlenene benzer. Farklılıklar çekirdek için plazma seviyelerindeki benzerliğe bağlı olarak güvenlik beklenmez CR ve hemen serbest bırakma karvedilol
Kalp Yetmezliği
Aşağıdaki bilgiler Güvenlik deneyimini açıklar hemen salınan karvedilol ile kalp yetmezliğinde.
Karvedilol kalp yetmezliğinde güvenlik açısından değerlendirildi dünya çapında 4.500'den fazla konuda 2.100'den fazla kişi katıldı plasebo kontrollü klinik çalışmalar. Tedavi edilen toplamın yaklaşık %60'ı plasebo kontrollü klinik çalışmalarda popülasyon at için karvedilol aldı en az 6 ay ve %30'u en az 12 ay boyunca karvedilol aldı. KUYRUKLUYILDIZIN içinde hafif ila orta derecede kalp yetmezliği olan 1511 denek ile tedavi edildi 5'e kadar karvedilol.9 yıl (ortalama: 4.8 yıl). Her ikisi de ABD'de klinik çalışmalarda günlük dozlarda karvedilol ile karşılaştırıldığında hafif ila orta derecede kalp yetmezliği Plasebo (n = 437) ile 100 mg (n = 765) ve çok uluslu bir klinik çalışmada şiddetli kalp yetmezliğinde (COPERNİCUS), günlük dozlarda karvedilolü karşılaştırdı plasebo (n = 1,133) ile 50 mg'a (n = 1,156) kadar, olumsuz deneyimler karvedilol ve plasebo deneklerinde benzerdi. İçinde plasebo kontrollü klinik çalışmalar, ilacın kesilmesinin tek nedeni daha büyüktür. %1'den fazla ve karvedilol üzerinde daha sık meydana gelen baş dönmesi (1.% 3 açık carvedilol, 0.COPERNİCUS denemesinde plaseboda %6)
Tablo 2, deneklerde bildirilen advers olayları göstermektedir ABD plasebo kontrollü klinikte kayıtlı hafif ila orta derecede kalp yetmezliği çalışmalar ve COPERNİCUS denemesinde kayıtlı ciddi kalp yetmezliği ile. Gösterilen ilaçla tedavi edilen deneklerde daha sık meydana gelen advers olaylar deneklerde insidansı %3'ten fazla olan plasebo ile tedavi edilen denekler nedensellikten bağımsız olarak karvedilol ile tedavi edilir. Medyan deneme ilaç maruz kalma 6 idi.Denemelerde hem karvedilol hem de plasebo denekleri için 3 ay hafif ila orta derecede kalp yetmezliği ve 10.Deneklerin yargılanmasında 4 ay şiddetli kalp yetmezliği ile. Karvedilolün advers olay profili KUYRUKLUYILDIZIN uzun vadeli çalışması genellikle ABD'de gözlemlenene benziyordu Kalp Yetmezliği Denemeleri.11
Tablo 2: Daha Sık Meydan Gelen Advers Olaylar (%)
Karvedilolün plasebodan hemen salınması ile denekler
(HF) hafif-Orta Kalp yeterliği BİZİ Kalp Yetmezliği Denemeler veya Kayıtlı
COPERNİCUS çalışmasında ciddi kalp yetmezliği olan denekler (insidans > %3
Nedensellikten bağımsız olarak karvedilol ile tedavi edilen denekler)
| Vücut Sistemi / Olumsuz Olay | Hafif ila orta derecede HF | Şiddetli HF | ||
| Karvedilol (n = 765) |
Plasebo (n = 437) |
Karvedilol (n = 1,156) |
Plasebo (n = 1,133) |
|
| Bir bütün olarak vücut | ||||
| Asteni | 7 | 7 | 11 | 9 |
| Yorgunluk | 24 | 22 | — | — |
| Digoksin seviyesi arttı | 5 | 4 | 2 | 1 |
| Ödeme genelleştirildi | 5 | 3 | 6 | 5 |
| Ödemeli | 4 | 2 | — | — |
| Kardiyovasküler sistem | ||||
| Bradikardi | 9 | 1 | 10 | 3 |
| Hipotansiyon | 9 | 3 | 14 | 8 |
| Senkop | 3 | 3 | 8 | 5 |
| Anjina pektoris | 2 | 3 | 6 | 4 |
| Merkezi Sinir Sistemi | ||||
| Baş dönmesi | 32 | 19 | 24 | 17 |
| Ağrı | 8 | 7 | 5 | 3 |
| Gastrointestinal sistem | ||||
| Ishal | 12 | 6 | 5 | 3 |
| Bulantı | 9 | 5 | 4 | 3 |
| Kusan | 6 | 4 | 1 | 2 |
| Metabolizma | ||||
| Hiperglisemi | 12 | 8 | 5 | 3 |
| Ağırlık artışı | 10 | 7 | 12 | 11 |
| Topuz arttı | 6 | 5 | — | — |
| NPN arttı | 6 | 5 | — | — |
| Hiperkolesterolemi | 4 | 3 | 1 | 1 |
| Periferik ödeme | 2 | 1 | 7 | 6 |
| Iskelet | ||||
| Artralji | 6 | 5 | 1 | 1 |
| Solunum | ||||
| Öksürük arttı | 8 | 9 | 5 | 4 |
| Hırıltı | 4 | 4 | 4 | 2 |
| Görüş | ||||
| Görme anormal | 5 | 2 | — | — |
Bu hastalarda kalp yetmezliği ve nefes darlığı da bildirilmiştir ancak plasebo alan deneklerde oranlar eşit veya daha yüksekti.
Aşağıdaki advers olaylar bir frekans %1'den fazla, ancak %3'ten az veya eşit ve daha sık deneklerde ABD plasebo kontrollü çalışmalarda karvedilol ile hafif ila orta derecede kalp yetmezliği veya şiddetli kalp yetmezliği olan deneklerde COPERNİCUS davası.
İnsidans %1'den Fazla Veya 3'e Eşit%
Bir bütün olarak vücut: Alerji, halsizlik, hipovolemi, ateş, bacak ödemi.
Kardiyovasküler sistem: Sıvı aşırı yük, postural hipotansiyon, ağırlaştırılmış anjina pektoris, av blokajı, çarpıntı, hipertansiyon.
Merkezi ve çevre sinir sistemi: Hipestezi, vertigo, parestezi.
Gastrointestinal sistem: Melena, periodontitis.
Karaciger ve safra sistemi: SGPT arttı, SGOT artmak.
Metabolik ve beslenme: Hiperürisemi, hipoglisemi, hiponatremi, artmış alkalin fosfataz, glikozüri, hipervolemi, diabetes mellitus, GGT artışı, kilo kaybı, hiperkalemi, kreatinin arttı.
Iskelet: Kas krampları.
Trombosit, kanama ve sıkıştırma: Protrombin azalmış, purpura, trombositopeni.
Psikiyatri: Uyku hali.
Üreme, erkek: İktidarsızlık.
Özel Duyular: Bulanık görme.
Ürün Sistemi: Böbrek yetmezliği, albüminüri, hematüri.
Miyokard sonrası sol ventrikül disfonksiyonu Enfarktüs
Aşağıdaki bilgiler Güvenlik deneyimini açıklar akut miyokard enfarktüsü sonrası sol ventrikül disfonksiyonu ile hemen serbest bırakma karvedilol.
Karvedilol, hayatta kalanlarda güvenlik açısından değerlendirildi sol ventrikül disfonksiyonu ile akut miyokard enfarktüsü Karvedilol alan 969 denek ve 980 denek içeren Oğlak davası plasebo aldı. Deneklerin yaklaşık %75'i at için karvedilol aldı en az 6 ay ve %53'ü en az 12 ay boyunca karvedilol aldı. Konulular ortalama 12.9 ay ve 12.8 ay boyunca karvedilol ve sırasıyla plasebo.
Karvedilol ile bildirilen en yaygın advers olaylar Oğlak denemesinde ABD'de ilacın profili ile tutarlıydı kalp yetmezliği denemeleri ve COPERNİCUS denemesi. Tek ek olumsuz Oğlak burcunda bildirilen olaylar, deneklerin %3'ünden fazlası ve daha fazlası genellikle karvedilol üzerinde dispne, anemi ve akciğer ödemi vardı. Aşağıdaki olumsuz olaylara daha az %1 den daha büyük bir frekans ile bildirildi ama veya karvedilol ile %3'e eşit ve daha sık: grip sendromu, serebrovasküler kaza, periferik vasküler bozukluk, hipotoni, depresyon, gastrointestinal ağrı, artrit ve gut. Genel oranlar advers olaylara bağlı süreksizlikler her iki grupta da benzerdi. Bu veritabanında, ilacın kesilmesinin tek nedeni %1'den fazladır ve karvedilolde daha sık görülen hipotansiyon (1.Karvedilol üzerinde %5, 0.2 % açık plasebo)
Hipertansiyon
COREG CR, 8 haftada güvenlik açısından değerlendirildi esansiyel hipertansiyonu olan 337 denekte çift kör deneme. Profil COREG CR ile gözlenen advers olaylar genellikle gözlemlenene benzerdi hemen serbest bırakılan karvedilol ile. Nedeniyle süreksizliklerin genel oranları coreg CR ve plasebo arasında advers olaylar benzerdi.
Tablo 3: Daha Sık Meydan Gelen Advers Olaylar (%)
arteriyel hipertansiyon olan deneklerde plaseboya göre COREG CR ile (ınsidans ≥ 1%
Nedensellikten bağımsız olarak karvedilol ile tedavi edilen deneklerde)
| Olumsuz Olay | ÇEKİRDEK CR (n = 253) |
Plasebo (n = 84) |
| Nazofarenjit | 4 | 0 |
| Baş dönmesi | 2 | 1 |
| Bulantı | 2 | 0 |
| Periferik ödeme | 2 | 1 |
| Burun tıkanı | 1 | 0 |
| Parestezi | 1 | 0 |
| Sinüs tıkanığı | 1 | 0 |
| Ishal | 1 | 0 |
| Uykusuzluk | 1 | 0 |
Aşağıdaki bilgiler Güvenlik deneyimini açıklar hemen salınan karvedilol ile hipertansiyonda.
Karvedilol hipertansiyonda güvenlik açısından değerlendirildi ABD klinik çalışmalarında 2.193 denek ve 2.976 denek uluslararası klinik çalışmalar. Tedavi edilen toplamın yaklaşık %36'sı nüfus en az 6 ay boyunca karvedilol aldı. Genel olarak, karvedilol günde 50 mg'a kadar olan dozlarda iyi tolere edildi. Bildirilen yan etkilerin çoğu karvedilol tedavisi sırasında hafif ila orta şiddette idi. ABD'de kontrollü 50 mg'a kadar olan dozlarda karvedilol monoterapisini doğrudan karşılaştıran klinik çalışmalar plasebo ile (n = 1.142) (n = 462), 4.Karvedilol deneklerinin %9'u durduruldu 5'e karşı advers olaylar için.Plasebo deneklerin %2'si. Hiçbir olmasına rağmen süreksizlik oranlarındaki genel fark, süreksizlikler daha yaygındı postural hipotansiyon için karvedilol grubunda (%1'e karşı 0). Genel ABD plasebo kontrollü çalışmalarda advers olayların insidansı bulundu artan karvedilol dozu ile artış. Bireysel advers olaylar için bu sadece 2'den sıklık olarak artan baş dönmesi için ayırt edilebilir% toplam günlük doz 6'dan arttıkça %5'e kadar.Tek veya bölünmüş olarak 25 mg ila 50 mg dozlar
Tablo 4, plasebo kontrollü ABD'deki advers olayları göstermektedir daha büyük bir insidans ile ortaya çıkan hipertansiyon için klinik çalışmalar nedensellik ne olursa olsun %1'e eşit veya daha fazla ve bu daha sıktı plasebo ilaç-tedavi konular-konular ele.
Tablo 4: ABD plasebo kontrol advers olaylar (% oluşumu)
Hemen salınan karvedilol ile hipertansion denemeleri (insidans ≥ 1%
Nedensellikten bağımsız olarak karvedilol ile tedavi edilen deneklerde)*
| Olumsuz Olay | Karvedilol (n = 1.142) |
Plasebo (n = 462) |
| Kardiyovasküler sistem | ||
| Bradikardi | 2 | — |
| Postural hipotansiyon | 2 | — |
| Periferik ödeme | 1 | — |
| Merkezi Sinir Sistemi | ||
| Baş dönmesi | 6 | 5 |
| Uykusuzluk | 2 | 1 |
| Gastrointestinal sistem | ||
| Ishal | 2 | 1 |
| Hematolojik | ||
| Trombositopeni | 1 | — |
| Metabolizma | ||
| Hipertrigliseridemi | 1 | — |
| * Gösterilen oran > %1 ile olaylar en yakın yuvarlanır tamsayi'yi. | ||
Bu çalışmalarda nefes darlığı ve yorgunluk da bildirilmiştir, ancak plasebo alan deneklerde oranlar eşit veya daha yüksekti.
Yukarıda açıklanmayan aşağıdaki yan etkiler şunlardı dünya çapında açık veya açık olarak karvedilol ile ilgili olarak rapor edilmiştir. hipertansiyon ya da kalp ile konularda Allegra ile kontrollü deneyler başarısızlık.
İnsidans %0.1'den Büyük Veya 1'e Eşit%
Kardiyovasküler sistem: Periferik iskemi, taşikardi.
Merkezi ve çevre sinir sistemi: Hipokinezi.
Gastrointestinal sistem: Bilirubinemi, artmış karaciğer enzimler (hipertansiyon hastalarının %0.2'si ve kalp yetmezliği hastalarının %0.4'ü) hepatik enzimlerdeki artışlar nedeniyle tedaviden çıkarıldı).
Psikiyatri: Sinirlilik, uyku bozukluğu, ağırlaştırılmış depresyon, konsantrasyon bozukluğu, anormal düşünme, paroniria, duygusal kararsızlık.
Solunum Sistemi: Astma.
Üreme, erkek: Libido azaldı.
Cilt ve ekler: Kaşıntı, eritematöz döküntü, döküntü makülopapüler, döküntü sedef formu, ışığa duyarlılık reaksiyonu.
Özel Duyular: Kulak çınlaması.
Ürün Sistemi: İşeme sıklığı arttı.
Otonom Sinir Sistemi: Ağız kuruluğu, terleme artmak.
Metabolik ve beslenme: Hipokalemi, hipertrigliseridemi.
Hematolojik: Anemi, aşırı üretimi.
Aşağıdaki olaylar eşit veya daha az rapor edildi deneklerin %0.1'ine kadar ve potansiyel olarak önemlidir: tam AV bloğu, paket dal blokajı, miyokardiyal iskemi, serebrovasküler bozukluk, konvülsiyonlar, migren, nevralji, parezi, anafilaktoid reaksiyon, alopesi, eksfolyatif dermatit, amnezi, gastrointestinal kanama, bronkospazm, pulmoner ödem, azalmış işitme, solunum alkalozu, artmış Topuz, azalmış HDL, pansitopeni ve atipik lenfositler.
Laboratuvar Anormallikleri
Serum transaminazlarında (ALT veya AST) tersinir yükselmeler) karvedilol ile tedavi sırasında gözlenmiştir. Transaminaz oranları kontrol sırasında gözlenen yükselmeler (normalin üst sınırının 2 ila 3 katı) klinik çalışmalar genellikle tedavi edilen denekler arasında benzer olmuştur karvedilol ve plasebo ile tedavi edilenler. Bununla birlikte, transaminaz yükselmeleri, rechallenge ile teyit edildi, karvedilol ile gözlemlendi. Uzun vadede, şiddetli kalp yetmezliğinde plasebo kontrollü çalışma, tedavi edilen denekler Allegra konularda daha hepatik transaminaz alt değerleri tedavi vardı plasebo ile, muhtemelen kalpte karvedilol kaynaklı gelişmeler nedeniyle fonksiyon daha az hepatik tıkanıklığa ve/veya daha iyi hepatik kan akışına yol açtı
Karvedilol tedavisi ile ilişkili değildir serum potasyumunda klinik olarak anlamlı değişiklikler, total trigliseritler, total kolesterol, HDL kolesterol, ürik asit, kan üre azotu veya kreatinin. Hayır hipertansif hastalarda açlık serum glikozunda klinik olarak anlamlı değişiklikler kaydedildi denekler, açlık serum glukozu kalp yetmezliği klinik değerlendirilmedi denemeler.
Pazarlama Sonrası Deneyim
Aşağıdaki ADVERS REAKSİYONLAR tespit edilmiştir COREG ® veya COREG CR'NİN onay sonrası kullanımı sırasında. Çünkü bu reaksiyonlar belirsiz büyüklükteki bir nüfustan gönüllü olarak rapor edildi, her zaman değil sıklıklarını güvenilir bir şekilde tahmin etmek veya nedensel bir sonuç oluşturmak mümkündür uyuşturucuya maruz kalma ile ilişki.
Kan ve lenfatik sistem bozuklukları
Aplastik anemi.
Bağışıklık Sistemi Bozuklukları
Aşırı duyarlılık (örneğin, anafilaktik reaksiyonlar, anjiyoödem, ürtiker).
Böbrek ve idrar bozuklukları
Üriner inkontinans.
Solunum, torasik ve Mediastinal bozukluklar
İnterstisyel pnömoni.
Deri ve deri altı doku bozuklukları
Stevens-Johnson sendromu, toksik epidermal nekroliz, eritema multiforme.

Doz aşımı şiddetli hipotansiyon, bradikardi neden olabilir, kalp yetmezliği, kardiyojenik şok ve kalp durması. Solunum sorunlar, bronkospazmlar, kusma, bilinç kaybı ve genelleştirilmiş nöbetler de oluşabilir.
Hasta sırtüstü bir pozisyona yerleştirilmeli ve, gerekirse, gözlem altında tutulur ve yoğun bakım altında tedavi edilir koşullar. Aşağıdaki ilaçlar reçete edilebilir:
Aşık bradikardi için: atropin, 2 mg IV.
Kardiyovasküler fonksiyonu desteklemek için: glukagon, 5 için 10 mg IV hızlı 30 saniye, 5 sürekli bir infüzyon başına mg izledi saat, dozlarda sempatomimetikler (dobutamin, izoprenalin, adrenalin) vücut ağırlığına ve etkisine bağlı olarak.
Periferik vazodilatasyon hakim ise, gerekli olabilir sürekli izleme ile adrenalin veya noradrenalin uygulamak için dolaşım koşulları. Tedaviye dirençli bradikardi, kalp pili tedavisi için yapılmalıdır. Bronkospazm için β-sempatomimetikler (aerosol veya IV) veya AMİNOFİLİN IV verilmelidir. Nöbet durumunda, yavaş IV diazepam veya klonazepam enjeksiyonu önerilir.
DEĞİL: Şiddetli zehirlenme durumunda nerede şok belirtileri vardır, panzehir tedavisi uzun süre devam etmelidir. 7 ila 10 saatlik Yarılanma ömrüne karşılık gelen yeterince uzun bir süre. carvedilol.
COREG CR ile doz aşımı deneyimi yoktur. Durumlar tek başına veya diğer ilaçlarla kombinasyon halinde karvedilol ile aşırı doz edildiğini bildirdi. Bazı durumlarda yutulan miktarlar 1.000 miligramı aştı. Semptomlar düşük tansiyon ve kalp atış hızını içeriyordu. Standart destekleyici tedavi sağlandı ve bireyler iyileşti.

Kalp Yetmezliği ve Sol Ventrikül fonksiyon Bozukluğu aşağıdaki Miyokard Enfarktüsü
Karvedilolün yararlı etkilerinin temeli kalp yetmezliği olan hastalar ve sol ventrikül disfonksiyonu olan hastalar akut miyokard enfarktüsünün ardından bilinmemektedir. Bu β1-blokaj için konsantrasyon-yanıt ilişkisi COREG CR'NİN uygulanması, karvedilolün derhal salınmasına eşdeğerdir (±%20). tabletler.
Hipertansiyon
Β-blokajın bir antihipertansif ürettiği mekanizma etki kurulmamıştır.
β-adrenoreseptör bloke edici aktivite olmuştur karvedilolün (1) azaldığını gösteren hayvan ve insan çalışmalarında gösterilmiştir normal deneklerde kardiyak output, (2) egzersizi azaltır-ve / veya izoproterenol kaynaklı taşikardi ve (3) refleks ortostatik azaltır taşikardi. Önemli β-adrenoreseptör bloke edici etki genellikle görülür ilaç uygulamasından sonra 1 saat içinde.
α1-adrenoreseptör bloke edici aktivite olmuştur insan ve hayvan çalışmalarında gösterilen, karvedilol (1) fenilefrinin basınç etkilerini zayıflatır, (2) vazodilatasyona neden olur ve (3) periferik vasküler direnci azaltır. Bu etkiler Aşağıdakilere katkıda bulunur kan basıncında bir azalma ve genellikle ilacın alınmasından sonraki 30 dakika içinde görülür yönetim.
Α1 reseptör bloke edici aktivitesi nedeniyle karvedilol, kan basıncı ayakta yatarken yatarken olduğundan daha fazla azalır pozisyon ve nadir vakalar da dahil olmak üzere postural hipotansiyon belirtileri (%1.8) senkop oluşabilir. Postural hipotansiyon ile oral uygulamadan sonra meydana geldi, geçici oldu ve hemen serbest bırakıldığında nadirdir karvedilol, önerilen başlangıç dozunda gıda ile birlikte uygulanır ve titrasyon artışları yakından takip edilir.
Bir rasgele, çift kör, plasebo-kontrollü deneme , kalp atış hızı yanıtı ile ölçülen coreg CR'NİN β1 bloke edici etkisi submaksimal bisiklet ergometrisinin, gerekli olan yetişkin deneklerde kararlı durumda karvedilolün derhal salınması hipertansiyon.
Normal böbrek fonksiyonu olan hipertansif hastalarda, terapötik karvedilol dozları böbrek vasküler direncini azalttı glomerüler filtrasyon hızında veya renal plazma akışında değişiklik. Atılımdaki değişiklikler hipertansif hastalarda sodyum, potasyum, ürik asit ve fosfor normal böbrek fonksiyonu karvedilol ve plasebodan sonra benzerdi.
Karvedilolün plazma katekolaminleri üzerinde çok az etkisi vardır, plazma aldosteron veya elektrolit seviyeleri, ancak önemli ölçüde azalır en az 4 hafta boyunca verildiğinde plazma renin aktivitesi. Aynı zamanda seviyeleri artırır atriyal natriüretik peptid.

Emilme
Karvedilol aşağıdaki gibi hızlı ve yoğun bir şekilde emilir mutlak salımlı karvedilol tabletlerinin oral uygulaması önemli derecede biyoyararlanım nedeniyle yaklaşık %25 ila %35 arasında ilk geçiş metabolizması. COREG Cr genişletilmiş salımlı kapsüller yaklaşık olarak Anında salınan karvedilol tabletlerinin biyoyararlanımının %85'i. İçin karşılık gelen dozajlar, maruz kalma (AUC, Cmaksimum, çukur konsantrasyonu) COREG Cr genişletilmiş salımlı olarak karvedilol kapsüller, şu anda serbest bırakılan karvedilol tabletlerine eşdeğerdir her ikisi de gıda ile uygulanır. KARVEDİLOLÜN çekirdek CR'DEN emilimi hemen salınan karvedilol tabletine kıyasla daha yavaş ve daha uzun süreli uygulamadan yaklaşık 5 saat sonra elde edilen tepe konsantrasyonları ile. Kan plazmasındaki karvedilol konsantrasyonu, aşırı dozda orantılı olarak artar. COREG CR 10 ila 80 mg dozaj aralığı. Konu içinde ve konu arasında AUC ve Cmax için değişkenlik, COREG CR ve anında serbest bırakma için benzerdir karvedilol
Gıdanın etkisi: COREG CR'NİN a ile uygulanması yüksek yağlı yemek, AUC ve Cmax'ta çekirdek ile karşılaştırıldığında artışa (~%20) neden oldu CR standart bir yemek ile uygulanır. AUC (%27) ve Cmaksimum (43%) COREG CR'NİN açlık durumunda uygulanmasıyla karşılaştırıldığında gözlendi standart bir yemekten sonra uygulama. COREG CR gıda ile alınmalıdır.
Yetişkin deneklerle yapılan bir denemede, içeriği serpme elma püresi üzerindeki COREG CR kapsülünün önemli bir özelliği yoktu. bozulmamış uygulama ile karşılaştırıldığında genel maruz kalma (AUC) üzerindeki etki kapsül standart bir yemekten sonra, ancak Cmaksimum (%18) bir düşüşe neden oldu.
Dağıtım
Karvedilol, plazma proteinlerine %98'den fazla bağlanır, öncelikle albümin ile. Plazma-protein bağlanması bağımsızdır terapötik aralıkta konsantrasyon. Karvedilol temel, lipofiliktir yaklaşık 115 L'lik sabit bir dağılım hacmine sahip bileşik, ekstravasküler dokulara önemli bir dağılım gösterir.
Metabolizma ve atılım
Karvedilol yoğun olarak metabolize edilir. Oral takip radyo etiketli karvedilolün sağlıklı gönüllülere uygulanması, karvedilol kan plazmasındaki toplam radyoaktivitenin sadece %7'sini oluşturuyordu. AUC. Dozun %2'sinden azı idrarda değişmeden atıldı. Karvedilol esas olarak aromatik halka oksidasyonu ve glukuronidasyon ile metabolize edilir. Bu oksidatif metabolitler, konjugasyon yoluyla daha da metabolize edilir glukuronidasyon ve sülfasyon. Karvedilol metabolitleri vücuttan atılır öncelikle safra yoluyla dışkıya. Demetilasyon ve hidroksilasyon fenol halkası, β-reseptör bloke edici aktiviteye sahip 3 aktif metabolit üretir. Preklinik çalışmalara dayanarak, 4 ' - hidroksifenil metaboliti yaklaşık olarak Β-blokaj için karvedilolden 13 kat daha güçlü
Karvedilol ile karşılaştırıldığında, 3 aktif metabolit zayıf vazodilatasyon aktivitesi sergiler. Aktif plazma konsantrasyonları metabolitler, karvedilol için gözlemlenenlerin yaklaşık onda biridir ve farmakokinetik ebeveynlere benzer.
Carvedilol stereoselective ilk geçişten geçer plazma r( )-karvedilol seviyeleri ile metabolizma yaklaşık 2 ila 3 kat COREG CR'NİN oral uygulamasından sonra S (-) - karvedilolden daha yüksek sağlıklı denekler. Görünür boşluk h başına 90 L ve R için h başına 213 l'dir( )- ve S(-)-sırasıyla karvedilol.
Metabolizmadan sorumlu birincil P450 enzimleri insan karaciğer mikrozomlarında hem R () hem de S (-) - karvedilolün CYP2D6 ve CYP2C9 ve daha az ölçüde CYP3A4, 2C19, 1a2 ve 2E1. CYP2D6 düşünülüyor karvedilolün 4' - ve 5 ' - hidroksilasyonunda ana enzim olun 3a4'ten potansiyel katkı. CYP2C9 birincil öneme sahip olduğu düşünülmektedir S (-)-karvedilolün O-metilasyon yolunda.
Karvedilol genetik etkilere maruz kalır debrisokinin zayıf metabolizörleri ile polimorfizm (sitokrom için bir işaretleyici P450 2d6) 2 ila 3 kat daha yüksek plazma konsantrasyonları sergiliyor R( )-karvedilol, geniş metabolizörlerle karşılaştırıldığında. Buna karşılık, plazma s(-)-karvedilol seviyeleri zayıf insanlarda sadece %20 ila %25 arasında artar. metabolizers, bu sodium salt belirten bir dereceye kadar tarafından metabolize edilir sitokrom P450 2d6, R( )-karvedilolden daha fazladır. Karvedilolün farmakokinetiği s-mefenitoinin zayıf metabolizörlerinde (hastalar) farklı görünmüyor sitokrom P450 2c19'da eksik).

Ekim 2015

-

-


