









Componentes:
Opção de tratamento:
Medicamente revisado por Oliinyk Elizabeth Ivanovna, Farmácia Última atualização em 25.03.2022

Atenção! As informações na página são apenas para profissionais de saúde! As informações são coletadas em fontes abertas e podem conter erros significativos! Tenha cuidado e verifique novamente todas as informações desta página!

Coreg CR

Apresentações E Dosagens
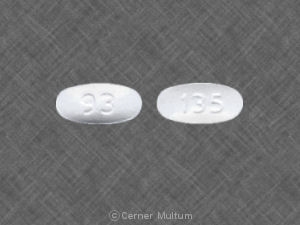
As cápsulas de gelatina são recheadas de cor branca a micropartículas esbranquiçadas e disponíveis nas seguintes dosagens::
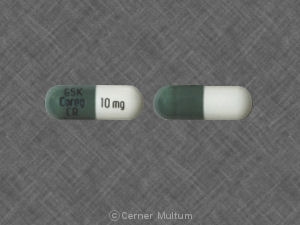
- 10 mg – cápsula branca e verde imprensa com " GSK COREG CR " e " 10 mg”
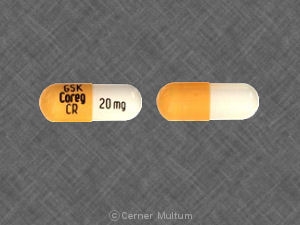
- 20 mg – cápsula branca e amarela imprensa com " GSK COREG CR " e " 20 mg”
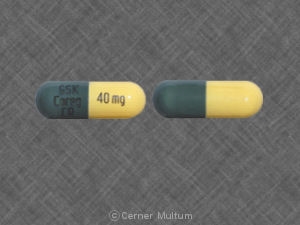
- 40 mg-cápsula amarela e verde imprensa com " GSK COREG CR " e " 40 mg”
- Cápsula de 80 mg-branca impressa com " GSK COREG CR” e " 80 mg”
Armazenagem E Manuseamento
As cápsulas de gelatina estão disponíveis nos seguintes potencialidade:
- 10 mg – cápsula branca e verde imprensa com " GSK COREG CR " e " 10 mg”
- 20 mg – cápsula branca e amarela imprensa com " GSK COREG CR " e " 20 mg”
- 40 mg-cápsula amarela e verde imprensa com " GSK COREG CR " e " 40 mg”
- Cápsula de 80 mg-branca impressa com " GSK COREG CR” e " 80 mg”
Frascos de 10 mg de 30: NDC 0007-3370-13
Frascos de 20 mg de 30: NDC 0007-3371-13
Frascos de 40 mg de 30: NDC 0007-3372-13
Frascos de 80 mg de 30: NDC 0007-3373-13
Conservar a 25 ° C (77°F), excursões de 15 ° a 30 ° C (59 ° a 86 ° F). Dispense num recipiente apertado e resistente à luz.
GlaxoSmithKline, Investigação Triangle Park, NC 27709. Revisto: Outubro De 2015

cardiaco
COREG CR® é indicado para a tratamento da insuficiência cardíaca crónica ligeira a grave de isquémia ou origem cardiomiopática, normalmente em adição aos diuréticos, inibidores da ECA e digitálicos, para aumentar a sobrevivência e, também, para reduzir o risco de hospitalizacao.
Disfunção Ventricular Esquerda Enfarte Do Miocárdio
COREG CR está indicado para reduzir mortalidade cardiovascular em doentes clinicamente estáveis que sobreviveram a fase aguda de enfarte do miocárdio e ejecção ventricular esquerda fracção inferior ou igual a 40% (com ou sem coração sintomático falha).
Hipertensao
COREG CR é indicado para a tratamento da hipertensão essencial. Pode ser utilizado isoladamente ou em associação com outros fármacos anti-hipertensores, especialmente diuréticos tipo-tiazida.

COREG CR é um extended-release cápsula destinada a administração única diária. Doentes controlados com placebo carvedilol comprimidos de libertação imediata, em monoterapia ou em associação com outros medicamentos podem ser mudados para COREG CR cápsulas de libertação prolongada com base na doses diárias totais indicadas na Tabela 1.
Tabela 1: Conversa Da Época
| Dose diária de comprimidos de Carvedilol de liberdade imediata | Dose diária de COREG CR cápsulasa |
| 6, 25 mg (3, 125 mg duas vezes por dia) | 10 mg uma vez por dia |
| 12, 5 mg (6, 25 mg duas vezes por dia) | 20 mg uma vez por dia |
| 25 mg (12, 5 mg duas vezes por dia) | 40 mg uma vez por dia |
| 50 mg (25 mg duas vezes por dia) | 80 mg uma vez por dia |
| a Quando se muda de carvedilol 12, 5 mg ou 25 mg duas vezes por dia, uma dose inicial de COREG CR 20 mg ou 40 mg uma vez por dia, os passos ou os que apresentaram um risco aumentado podem, respeitosamente, ser considerados hipotenso, tonturas ou sincope. Titulação subsequente para doses mais elevadas se necessário, deve ser feito um intervalo de, pelo menos, 2 semanas. |
COREG CR deve ser tomado uma vez por dia de manhã com alimento. COREG CR deve ser engolido como uma cápsula inteira. COREG CR e / ou its o conteúdo não deve ser esmagado, mastigado ou tomado em doses divididas.
Administração Alternativa
As cápsulas podem ser abertas cuidadosamente e as contas polvilhado sobre uma colher cheia de molho de maçã. O molho de maçã não deve estar quente. porque pode afectar as propriedades de libertação modificada desta formulação. A mistura de droga e puré de maçã deve ser consumida imediatamente na sua totalidade. O medicamento e a mistura de puré de maçã não devem ser armazenados para uso futuro. A absorção das esferas aspergidas noutros alimentos não foi testada.
cardiaco
A DOSE DEVE SER INDIVIDUALIZADA E CUIDADOSAMENTE MONITORIZADA POR UM MÉDICO DURANTE A TITULAÇÃO. Antes do início da COREG CR, é recomenda-se que a retenção de líquidos seja minimizada. A dose inicial recomendada de COREG CR é de 10 mg uma vez por dia durante 2 semanas. Doentes que toleram uma dose de 10 mg uma vez ao dia, a sua dose pode ser aumentada para 20, 40 e 80 mg ao longo de intervalos de pelo menos 2 semanas. Os doentes devem ser mantidos com doses mais baixas se: doses mais elevadas não são toleradas.
Os doentes devem ser avisados de que o início do tratamento e (em menor grau) aumentos posológicos podem estar associados a sintomas de tonturas ou vertigens (e raramente síncope) na primeira hora após a administração. Assim, durante estes períodos, devem evitar situações como a condução ou tarefas perigosas, em que os sintomas podem resultar em lesões. Os sintomas vasodilatadores frequentemente não requerem tratamento, mas pode ser útil separar o tempo de administração de COREG CR do do inibidor da ECA ou reduzir temporariamente a dose do inibidor da ECA. A dose de COREG CR deve não deve ser aumentado até que os sintomas de agravamento da insuficiência cardíaca ou vasodilatação tenham estabilizado
Retenção de líquidos (com ou sem agravamento transitório sintomas de insuficiência cardíaca) devem ser tratados por um aumento da dose de diuréticos.
A dose de COREG CR deve ser reduzida se os doentes sentir bradicardia (frequência cardíaca inferior a 55 batimentos por minuto).
Episódios de tonturas ou retenção de líquidos durante o início de COREG CR pode geralmente ser controlado sem interrupção de tratamento e não excluam a posterior titulação bem sucedida de, ou resposta favorável à COREG CR.
Disfunção Ventricular Esquerda Após Enfarte Do Miocárdio Miocardio
A DOSE DEVE SER INDIVIDUALIZADA E MONITORIZADA DURANTE AUMENTO DA TITULAÇÃO. O tratamento com COREG CR pode ser iniciado como ambulatório e deve ser iniciado após o paciente estar hemodinamicamente estável e a retenção de líquidos foi minimizada. Recomenda - se que COREG CR seja iniciada com 20 mg uma vez por dia e aumentada após 3 a 10 dias, com base em tolerabilidade, até 40 mg uma vez por dia, e depois novamente até à dose alvo de 80 mg uma vez diario. Pode ser utilizada uma dose inicial mais baixa (10 mg uma vez por dia) e / ou a taxa de a titulação aumentada pode ser retardada se clinicamente indicado (e.g., devido ao baixo nível de sangue pressão ou frequência cardíaca, ou retenção de fluidos). Os doentes devem ser doses mais baixas se não forem toleradas doses mais elevadas. O regime posológico recomendado não é necessário alterar a dose em doentes que receberam tratamento por via intravenosa ou oral. bloqueador beta durante a fase aguda do enfarte do miocárdio
Hipertensao
A DOSE DEVE SER INDIVIDUALIZADA. O início recomendado a dose de COREG CR é de 20 mg uma vez por dia. Se esta dose for tolerada, utilize standing a pressão sistólica medida cerca de 1 hora após a administração, Guia, da dose deve ser mantido durante 7 a 14 dias, e depois aumentado para 40 mg uma vez por dia se necessário, com base na pressão arterial no Vale, novamente usando a sistólica de pé pressão 1 hora após a dosagem como guia de tolerância. Esta dose deve também ser mantida durante 7 a 14 dias e pode então ser ajustada para cima até 80 mg uma vez por dia se tolerado e necessário. Embora não especificamente estudado, prevê-se que o efeito antihipertensor total de COREG CR seria observado dentro de 7 a 14 dias tal como foi demonstrado com carvedilol de libertação imediata. Dose diária Total não deve exceder 80 mg
Pode esperar-se a administração concomitante com um diurético para produzir efeitos aditivos e exagerar o componente ortostático de acção carvedilol.
hepatica
COREG CR não deve ser administrado a doentes com hepatica.
Uso Geriátrico
Quando os doentes idosos mudam de idade (idade igual ou superior a 65 anos)) que estão a tomar as doses mais elevadas dos comprimidos de libertação imediata de carvedilol (25 mg duas vezes por dia) até COREG CR, uma dose inicial mais baixa (40 mg) de COREG CR é recomendado para minimizar o potencial para tonturas, síncope ou hipotensão. Pacientes que trocaram e que toleram COREG CR deve, conforme apropriado, aumentar a sua dose após um intervalo de pelo menos duas semanas.

COREG CR está contra-indicado nas seguintes condições::
- Asma brônquica ou broncospasmo relacionado. Foram notificadas mortes devido ao estado asmático após administração de doses únicas de libertação imediata de carvedilol.
- Bloqueio AV de segundo ou terceiro grau.
- Sondrome do nódulo sinusal.
- Bradicardia grave (a menos que um pacemaker permanente esteja lugar).
- Doentes com choque cardiogénico ou que tenham descompensado insinuação cardíaca que requer a utilização de uma terapia inotrópica intraventosa. Doente primeiro deve ser desmamado da terapia intraventosa antes de iniciar COREG CR.
- Doentes com compromisso hepático grave.
- Doentes com história de hipersensibilidade grave reacção (P. ex. resumo de Stevens-Johnson, reacção anafilática, angioedema) a carvedilol ou qualquer um dos componentes da COREG CR.

AVISO
Incluído como parte da PRECAUCAO seccao.
PRECAUCAO
Em ensaios clínicos de COREG CR em indivíduos com hipertensão (338 indivíduos) e em indivíduos com disfunção ventricular esquerda após um enfarte do miocárdio ou insuficiência cardíaca( 187 indivíduos), o perfil os efeitos adversos observados com o fosfato de carvedilol foram geralmente semelhantes aos observados com o fosfato de carvedilol. o que foi observado com a administração de carvedilol de libertação imediata. Por conseguinte, a informação incluída nesta secção baseia-se em dados de ensaios clínicos controlados com COREG CR, bem como de libertação imediata carvedilol.
Cessação Da Terapêutica
Doentes com doença arterial coronária, que está a ser tratamento com COREG CR, deve ser aceite contra a interrupção abrupta da terapêutica com COREG CR. terapia. Exacerbação grave da angina de peito e dificuldade de enfarte do miocárdio enfarte e arritmias ventriculares forçadas forçadas em dentes com angina de peito. após a interrupção abrupta da terapêutica com bloqueadores β. As últimas 2 complicações podem ocorrer com ou sem exacerbação prévia de angina. Tal como com outros beta-bloqueadores, quando é COREG CR está planeado, os doentes devem ser cuidadamente observados e aconselhados a limitar ao mínimo a actividade física. COREG CR deve ser interrompido durante 1 a 2 semanas sempre que possível. Se a angina agravar ou se caso se verificique insuficiencia, recomendação-se que COREG CR seja prontamente reinstituído, pelo menos temporariamente. Porque a doença arterial coronária é comum e pode não ser reconhecido, pode ser prudente não continuar a terapêutica com COREG CR abruptamente mesmo mesmo em dias tratados apenas para hipertensão ou coração falha
Bradicardia
Em ensaios clínicos com carvedilol de libertação imediata, foi notificada bradicardia em cerca de 2% dos indivíduos hipertensos, 9% do coração indivíduos com falência hepática e 6, 5% indivíduos com enfarte do miocárdio com esquerda disfunção ventricular. A bradicardia foi notificada em 0, 5% dos indivíduos tratados com COREG CR num ensaio de indivíduos com insuficiência cardíaca e enfarte do miocárdio indivíduos com disfunção ventricular esquerda. Não houve relatórios de bradicardia no ensaio clínico de COREG CR em hipertensão. No entanto, se a frequência cardíaca desce abaixo dos 55 batimentos por minuto, a dose de COREG CR deve ser reduzido.
Hipotensao
Em ensaios clínicos com coração principalmente ligeiro a moderado falência com carvedilol de libertação imediata, hipotensão e hipotensão postural ocorreu em 9.7% e síncope em 3.4% dos indivíduos que receberam carvedilol comparativamente com 3.6% e 2%.5% dos doentes tratados com placebo, respectivamente. O risco para estes acontecimentos foi mais elevada durante os primeiros 30 dias de aumento da titulação e foi uma causa para a descontinuação da terapêutica em 0.7% de número de indivíduos tratados com carvedilol, em comparação com 0.4% dos doentes tratados com placebo. A longo prazo, ensaio controlado com placebo na insuficiência cardíaca grave (COPERNICUS), hipotensão e ocorreu hipotensão postural em 15.1% e síncope em 2.9% dos indivíduos com insuficiência cardíaca a receber carvedilol em comparação com 8.7% e 2.3% do placebo indivíduos, respectivamente. Estes acontecimentos foram uma causa para a descontinuação da terapêutica com Viraferon. terapêutica em 1.1% dos indivíduos tratados com carvedilol, em comparação com 0.8% dos doentes tratados com placebo
Num ensaio que comparou indivíduos com insuficiência cardíaca com para coagir CR ou manter com carvedilol de libertação imediata, houve um 2 vezes aumento da incidência combinada de hipotensão, síncope ou tonturas os idosos (com mais de 65 anos) mudaram da dose mais elevada de carvedilol (25 mg duas vezes por dia) a COREG CR 80 mg uma vez por dia.
No ensaio clínico de COREG CR em doentes hipertensos doentes, foi notificada síncope em 0, 3% dos doentes tratados com COREG CR comparativamente com com 0% dos indivíduos a receber placebo. Não houve relatos de posturas hipotensão neste ensaio. Ocorreu hipotensão Postural em 1, 8% e síncope em 0, 1% dos indivíduos hipertensos a receber carvedilol de libertação imediata, principalmente após a dose inicial ou no momento do aumento da dose e foi uma causa para interrupção da terapêutica em 1% dos indivíduos.
No ensaio de Capricórnio de sobreviventes de um agudo enfarte do miocárdio com disfunção ventricular esquerda, hipotensão ou ocorreu hipotensão postural em 20, 2% dos indivíduos tratados com carvedilol em comparação com 12, 6% dos indivíduos que receberam placebo. A síncope foi notificada em 3, 9% e 1, 9%.% de indivíduos, respectivamente. Estes acontecimentos foram uma causa para a descontinuação da terapêutica com Viraferon. terapêutica em 2, 5% dos indivíduos que receberam carvedilol, em comparação com 0, 2% dos indivíduos que receberam placebo item.
A partir de uma dose baixa, a administração com alimentos, e a titulação gradual deve diminuir a probabilidade de síncope ou excesso de hipotensao.
Durante o início da terapêutica, o doente deve ser advertido para evitar situações como a condução ou tarefas perigosas, onde a lesão pode resultar em síncope.
Insuficiência Cardíaca/Retenção De Líquidos
Pode ocorrer agravamento da insuficiência cardíaca ou retenção de líquidos durante a titulação do carvedilol. Se estes sintomas ocorrerem, os diuréticos deverão ser não deve ser avançada a dose de COREG CR até à estabilidade clínica. retomar. Ocasionalmente, é necessário baixar a dose de COREG CR ou descontinuar temporariamente a dose.. Estes episódios não impedir a posterior titulação bem sucedida de, ou uma resposta favorável a, COREG CR. Num ensaio controlado com placebo em indivíduos com insuficiência cardíaca grave, o agravamento da insuficiência cardíaca durante os primeiros 3 meses foi relatado para uma grau com carvedilol de libertação imediata e com placebo. Quando o tratamento foi mantida após 3 meses, o agravamento da insuficiência cardíaca foi notificado menos frequentemente em indivíduos tratados com carvedilol do que com placebo. Agravamento a insuficiência cardíaca observada durante a terapêutica a longo prazo é mais susceptível de estar relacionada com doença subjacente dos doentes do que ao tratamento com carvedilol
Broncospasmo não alérgico
Doentes com doença broncospástica (p. ex., doença crónica) bronquite e enfisema) não devem, em geral, receber bloqueadores beta. COREG CR pode ser utilizado com precaução, no entanto, em doentes que não respondem a, ou não pode tolerar outros agentes antihipertensores. É prudente, se COREG CR é utilizado, para utilizar a menor dose eficaz, de modo a que a inibição da ou os agonistas β exógenos são minimizados.
Em ensaios clínicos em indivíduos com insuficiência cardíaca, doentes com doença broncospástica foram incluídos caso não necessitassem de administração oral. ou medicação inalada para tratar a doença broncospástica. Nestes doentes, recomenda-se que COREG CR seja utilizado com precaução. A dose as recomendações devem ser seguidas cuidadosamente e a dose deve ser reduzida se: qualquer evidência de broncospasmo é observada durante a titulação.
Controlo Glicémico Da Diabetes Tipo 2
De um modo geral, Os β-bloqueadores podem mascarar parte da manifestações de hipoglicemia, particularmente taquicardia. Selectivo os bloqueadores β podem potenciar a hipoglicemia induzida e atrasar a recuperação. dos níveis séricos de glucose. Doentes sujeitos a hipoglicemia espontânea, ou os doentes diabéticos que recebem insulina ou agentes hipoglicemiantes, devem ser diabéticos. advertiu sobre essas possibilidades.
Em doentes com insuficiência cardíaca com diabetes, carvedilol a terapêutica pode levar a um agravamento da hiperglicemia, que responde à intensificação. de terapia hipoglicémica. Recomenda-se que a glicemia seja monitorizada quando a dosagem com COREG CR é iniciada, ajustada ou descontinuada. Ensaios concebidos para examinar os efeitos do carvedilol no controlo glicémico em doentes com a diabetes e a insuficiência cardíaca não foram conduzidas.
Num ensaio concebido para examinar os efeitos da carvedilol de libertação imediata no controlo glicémico, numa população com ligeiro a moderado hipertensão e diabetes mellitus de tipo 2 bem controlada, o carvedilol não teve efeito adverso no controlo glicémico, com base em medições da HbA1c.
Doença Vascular Periférica
os bloqueadores beta podem precipitar ou agravar os sintomas de insuficiência arterial em doentes com doença vascular periférica. Cuidado deve ser exercido em tais indivíduos.
Deterioração Da Função Renal
Raramente, a utilização de carvedilol em doentes com insuficiência cardíaca resultou na deterioração da função renal. Os doentes em risco parecem estar aqueles com pressão arterial baixa (pressão arterial sistólica inferior a 100 mm Hg), cardiopatia isquémica e doença vascular difusa e / ou renal subjacente insuficiência. A função Renal voltou aos valores basais quando o carvedilol foi parada. Em doentes com estes factores de risco recomenda-se que a função deve ser monitorizada durante a titulação de COREG CR e o fármaco deve ser descontinuado. redução da dose se ocorrer agravamento da função renal.
cirurgiao
A terapêutica beta-bloqueante administrada cronicamente não deve ser no entanto, a o coração para responder a estímulos adrenérgicos reflexos pode aumentar os riscos de anestesia geral e procedimentos cirúrgicos.
Tirotoxicose
o bloqueio β-adrenérgico pode mascarar os sinais clínicos de hipertiroidismo, tal como taquicardia. A retirada abrupta do β-bloqueio pode deve ser seguida de uma exacerbação dos sintomas de hipertiroidismo ou precipitar tempestade tiroideia.
Feocromocitoma
Em doentes com feocromocitoma, um o agente deve ser iniciado antes da utilização de qualquer bloqueador beta. Embora carvedilol tenha ambos α-e β-bloqueantes farmacológicos atividades, não houve experiência com o seu uso nesta condição. Assim, deve ter-se precaução na administração de doentes suspeitos de terem feocromocitoma.
Angina variante de Prinzmetal
Os agentes com actividade bloqueadora Beta não selectiva podem provocar dor no peito em doentes com angina variante de Prinzmetal. Houve não existe experiência clínica com o carvedilol nestes doentes, embora a a actividade de bloqueio alfa pode prevenir estes sintomas. No entanto, tomado na administração de COREG CR a doentes suspeitos de terem Angina variante de Prinzmetal.
Risco De Reacção Anafiláctica
Durante o tratamento com β-bloqueadores, doentes com história de a reacção anafiláctica grave a uma variedade de alergénios pode ser mais reactiva a desafio repetido, acidental, diagnóstico ou terapêutico. Tal os doentes podem não responder às doses habituais de epinefrina utilizadas para o tratamento da doença. alergico.
Síndrome Intraoperacional Da Íris Flexível
A síndrome intraoperatória da Floppy Iris (IFIS) foi observado durante a cirurgia da catarata em alguns doentes tratados com bloqueadores alfa-1 (COREG CR é um bloqueador alfa / beta). Esta variante da síndrome das pupilas pequenas é caracterizada pela combinação de uma íris flácida que se ondula em resposta a correntes de irrigação intraoperativas, miose intraoperatória progressiva apesar dilatação pré-operatória com fármacos midráticos padrão, e prolapso potencial de a íris em direcção às incisões de phacoemulsificação. Paciente oftalmologista deve ser preparado para possíveis modificações na cirurgia técnica, como a utilização de ganchos da íris, anéis dilatadores da íris, ou substâncias viscoelásticas. Não parece haver um benefício de parar terapêutica com bloqueadores alfa-1 antes da cirurgia de catarata
Informação Do Aconselhamento Do Doente
Aconselhar o paciente a ler o paciente aprovado pela FDA rotulagem (informação do doente).
Os doentes a tomar COREG CR devem ser avisados da seguinte:
- Os agentes não devem interferir ou continuar a utilizar de COREG CR sem o conselho de um médico.
- Os doentes com insinuação cardíaca devem o médico se sentir sinais ou sintomas de agravamento da insubficiência cardíaca tais como como aumento de peso ou aumento da falta de ar.
- Os doentes podem sentir uma diminuição da impressão arterial quando de pé, resultando em tonturas e, raramente, desmaias. Os doentes devem deite-se quando ocorrerem estes sintomas de diminuição da impressão arterial.
- Se sentir tonturas ou fadiga, os doentes devem evitar a condução ou tarefas perigosas.
- Os doentes devem consultar um médico se sentem tonturas ou desmaio, não caso de uma dose ser ajustada.
- Os dentes não devem esmagar ou mastigar as cápsulas COREG CR.
- Os doentes devem tomar COREG CR com alimentos.
- Os doentes diabéticos devem comunicar quaisquer alterações no sangue níveis de açúcar no sangue para o seu médico.
- Os utilizadores de dentes de contacto podem sentir diminuição lacrimação.
Toxicologia Não Clínica
Carcinogénese, Mutagénese, Diminuição Da Fertilidade
Em estudos de 2 anos realizados em ratos aos quais foi administrado carvedilol a doses até 75 mg por kg por dia (12 vezes a DMRH quando comparadas com mg por m2 nos ratinhos administrados até 200 mg por kg por dia (16 vezes a dose de MRHD em mg) ou em ratinhos administrados até 200 mg por kg por dia (16 vezes a dose de MRHD em mg). por m2), o carvedilol não teve qualquer efeito carcinogénico.
O Carvedilol foi negativo quando testado numa bateria de ensaios de genotoxicidade, incluindo os ensaios de Ames e CHO / HGPRT para Mutagenicidade e a in vitro micronúcleos de hamster e in vivo linfócitos humanos testes de clastogenicidade nas células.
Em doses iguais ou superiores a 200 mg por kg por dia (superior ou igual a 32 vezes a dose de MRHD em mg por m2) o carvedilol foi tóxico em ratos adultos (sedação, aumento de peso reduzido) e foi associada a uma redução número de acasalamentos bem sucedidos, tempo prolongado de acasalamento, significativamente menor corpora lutea e Implantes por barragem, e reabsorção completa de 18% do maca. O nível de dose sem efeito observado para a toxicidade evidente e para a a fertilidade foi de 60 mg por kg por dia (10 vezes a dose de MRHD em mg por m2).
Utilização Em Populações Específicas
Gravidez
Gravidez Categoria C
Estudos realizados em ratos e coelhos fêmeas gestantes aos quais foi administrado carvedilol revelou um aumento da perda pós-implantação em ratos com doses de 300 mg por kg por dia (50 vezes a dose máxima recomendada no ser humano [DMRH] em mg por m2) e em coelhos com doses de 75 mg por kg por dia (25 vezes a dose de MRHD em mg por m2). Nos ratos, verificou-se também uma diminuição do peso corporal fetal na mãe. dose tóxica de 300 mg por kg por dia( 50 vezes a dose de MRHD em mg por m2), que foi acompanhado por uma elevação na frequência de fetos com atraso no esqueleto desenvolvimento (falta ou falha da 13ª costela). Nos ratos, o nível sem efeito observado para a toxicidade para o desenvolvimento foi de 60 mg por kg por dia (10 vezes a dose de MRHD em mg). por m2), em coelhos foi de 15 mg por kg por dia (5 vezes a dose de MRHD em mg por m2).). Não existem estudos adequados e bem controlados em mulheres grávidas.. COREG CR deve ser utilizado durante a gravidez apenas se os potenciais benefícios justificarem a risco potencial para o feto
mae
Desconhece-se se este fármaco é excretado no ser humano. leite. Estudos em ratos demonstraram que o carvedilol e / ou os seus metabolitos (como 4. 5 interacções medicamentosas e outras formas de interacção leite. Verificou - se um aumento da mortalidade 1 semana após o parto em recém-nascidos de ratos tratados com 60 mg por kg por dia (10 vezes a dose de MRHD em mg por m2) e superior durante o último trimestre da gestação até ao dia 22 do aleitamento. Porque muitos os medicamentos são excretados no leite humano e devido ao potencial para reacções adversas em lactentes dos bloqueadores β, especialmente bradicárdia, deve ser tomada a decisão de interromper a amamentação ou de interromper a amamentação. a droga, levando em conta a importância da droga para a mãe. O os efeitos de outros agentes bloqueadores α e β incluíram perinatais e insuficiência neonatal
Uso Pediátrico
Eficácia do carvedilol em doentes com menos de 18 anos anos não foram estabelecidos.
Num ensaio de dupla ocultação, 161 Crianças (Idade Média: 6 anos), intervalo: 2 meses a 17 anos, 45% mais jovem do que 2 anos) com coração crónico falência [classe II-IV da NYHA, fracção de ejecção ventricular esquerda inferior a 40% para crianças com ventrículo esquerdo Sistémico( LV) e ventricular moderado-grave disfunção qualitativa por ECO para aqueles com um ventrículo sistémico que foi não um LV] que estavam a receber tratamento padrão de base foram aleatorizados para placebo ou para 2 doses de carvedilol. Estes níveis de dose produzidos redução da frequência cardíaca corrigida pelo placebo de 4 a 6 batimentos cardíacos por minuto, indicativo de actividade β-bloqueio. A exposição pareceu ser mais baixa em doentes pediátricos do que adultos. Após 8 meses de acompanhamento, não houve efeito significativo do tratamento nos resultados clínicos. Reacções adversas ensaio clínico que ocorreu em mais de 10% dos indivíduos tratados com carvedilol de libertação imediata e ao dobro da taxa de indivíduos tratados com placebo incluindo dor torácica (17% versus 6%), tonturas (13% versus 2%) e dispneia (11% versus 0%)
Uso Geriátrico
Os ensaios clínicos iniciais de COREG CR em indivíduos com hipertensão, insuficiência cardíaca e disfunção ventricular esquerda após enfarte do miocárdio não incluiu número suficiente de indivíduos com 65 anos de idade anos ou mais para determinar se eles respondem de forma diferente do mais jovem paciente.
Um ensaio aleatorizado (n = 405) comparando indivíduos com indivíduos ligeiros para insuficiência cardíaca grave mudou para COREG CR ou manteve-se em libertação imediata o carvedilol incluiu 220 indivíduos com idade igual ou superior a 65 anos.. Neste subgrupo idoso, a incidência combinada de tonturas, hipotensão ou síncope foi de 24% (18 / 75) nos indivíduos que mudaram da dose mais elevada de libertação imediata. carvedilol (25 mg duas vezes por dia) até à dose mais elevada de COREG CR (80 mg uma vez por dia) dia) comparado com 11% (4 / 36) em indivíduos mantidos em libertação imediata carvedilol (25 mg duas vezes por dia). Quando se muda das doses mais elevadas de libertação imediata carvedilol a COREG CR, recomenda-se uma dose inicial mais baixa para idosos paciente
A informação que se segue está disponível para ensaios com carvedilol de libertação imediata. Dos 765 indivíduos com insuficiência cardíaca aleatorizados ao carvedilol nos ensaios clínicos dos EUA, 31% (235) tinham idade igual ou superior a 65 anos, e 7.3% (56) tinham idade igual ou superior a 75 anos. Dos 1.156 indivíduos aleatorizados para carvedilol num ensaio a longo prazo, controlado com placebo, na insuficiência cardíaca grave, 47% (547) tinham 65 anos ou mais e 15% (174) tinham 75 anos ou idoso. Dos 3. 025 indivíduos que receberam carvedilol em ensaios de insuficiência cardíaca em todo o mundo, 42% tinham idade igual ou superior a 65 anos. Dos 975 indivíduos com enfarte do miocárdio no estudo do Capricórnio, 48% (468) foram doentes com 65 anos ou mais e 11% (111) tinham idade igual ou superior a 75 anos. Da 2,065 indivíduos hipertensos nos ensaios clínicos de eficácia ou segurança dos EUA que foram tratados com carvedilol, 21% (436) tinham idade igual ou superior a 65 anos. De 3,722 indivíduos a receber carvedilol de libertação imediata em ensaios clínicos de hipertensão realizado em todo o mundo, 24% tinham idade igual ou superior a 65 anos
Com excepção de tonturas em indivíduos hipertensos (incidência 8, 8% nos idosos versus 6% nos indivíduos mais jovens), nà foram observadas diferenças na segurança ou eficácia (ver figuras 2 e 4). entre os indivíduos mais velhos e os indivíduos mais jovens em cada uma destas populações. Do mesmo modo, a experiência clínica notificada não identificou diferenças na respostas entre os indivíduos idosos e os indivíduos mais jovens, mas maior sensibilidade alguns indivíduos mais velhos não podem ser descartados.

SECUNDARIO
Experiência Em Ensaios Clínicos
O Carvedilol foi avaliado quanto à segurança em indivíduos com insuficiência cardíaca (ligeira, moderada e grave), em indivíduos com ventrículo esquerdo disfunção após enfarte do miocárdio e em indivíduos hipertensos. O o perfil de acontecimentos adversos observados foi consistente com a farmacologia do fármaco. e o estado de saúde dos indivíduos nos ensaios clínicos. Acontecimentos adversos comunicado para cada uma destas populações, reflectindo a utilização de COREG CR ou o carvedilol de libertação imediata é fornecido a seguir.. Os acontecimentos adversos estão excluídos. considerado demasiado geral para ser informativo, e aqueles não razoavelmente associados com o uso da droga porque eles estavam associados com a condição de ser tratados ou são muito comuns na população tratada. Taxas de acontecimentos adversos foram geralmente semelhantes em todos os subconjuntos demográficos (homens e mulheres, idosos e não idosos, negros e não Negros). COREG CR foi avaliado quanto à segurança em 4 semanas (2 semanas de libertação imediata de carvedilol e 2 semanas de COREG CR) ensaios clínicos (n = 187) que incluíram 157 indivíduos com, insuficiência cardíaca crónica moderada ou grave e 30 indivíduos com ventrículo esquerdo disfunção após enfarte agudo do miocárdio. O perfil de os acontecimentos observados com COREG CR neste pequeno ensaio clínico de curta duração foram geralmente semelhante ao observado com carvedilol de libertação imediata. Diferenças na não seria de esperar segurança com base na semelhança dos níveis plasmáticos de COREG CR e carvedilol de libertação imediata
cardiaco
A informação que se segue descreve a experiência de segurança na insuficiência cardíaca com carvedilol de libertação imediata.
O Carvedilol foi avaliado quanto à segurança na insuficiência cardíaca. em mais de 4.500 temas em todo o mundo, dos quais mais de 2.100 participaram ensaios clínicos controlados com placebo. Aproximadamente 60% do total tratado a população em ensaios clínicos controlados com placebo recebeu carvedilol para pelo menos 6 meses e 30% receberam carvedilol durante pelo menos 12 meses. No cometa no ensaio, 1. 511 indivíduos com insuficiência cardíaca ligeira a moderada foram tratados com carvedilol até 5.9 anos (média: 4.8 anos). Ambos os ensaios clínicos nos Estados Unidos da América insuficiência cardíaca ligeira a moderada que comparou o carvedilol em doses diárias até 100 mg (n = 765) com placebo (n = 437) e num ensaio clínico multinacional na insuficiência cardíaca grave (COPERNICUS) que comparou o carvedilol em doses diárias to 50 mg (n = 1. 156) com placebo (n = 1. 133), taxas de descontinuação para os efeitos adversos foram semelhantes nos indivíduos tratados com carvedilol e placebo.. Em nos ensaios clínicos controlados com placebo, a única causa de descontinuação é maior do que nos ensaios clínicos controlados com placebo. mais de 1%, e ocorrendo mais frequentemente em carvedilol foram tonturas (1.3% em carvedilol, 0.6% com placebo no ensaio COPERNICUS)
A tabela 2 mostra os acontecimentos adversos notificados em indivíduos com insuficiência cardíaca ligeira a moderada incluída nos ensaios clínicos controlados com placebo ensaios clínicos e com insuficiência cardíaca grave incluída no ensaio COPERNICUS. Figurar os acontecimentos adversos que ocorreram mais frequentemente em indivíduos tratados com indivíduos tratados com placebo com uma incidência superior a 3% em indivíduos tratado com carvedilol independentemente da causalidade. Median trial medication a exposição foi de 6.3 meses para os indivíduos que receberam carvedilol e placebo nos ensaios de insuficiência cardíaca ligeira a moderada e 10.4 meses no ensaio clínico de indivíduos com insuficiência cardíaca grave. O perfil de acontecimentos adversos de carvedilol observado em o ensaio a longo prazo cometas foi geralmente semelhante ao observado nos EUA. Ensaios De Insuficiência Cardíaca.11
Quadro 2: Contactos Adversários ( % ) Que Ocorrem Mais Frequentemente
com Carvedilol de libertação imediata do que com Placebo em índios com
Insuficiência cardíaca ligeira a moderada (HF) inclui nos ensalos de insufficiência cardíaca dos EUA ou
Doentes com insinuação cardíaca grave no ensaio COPERNICUS (incidência > 3% em doentes com insuficiência cardíaca grave)
Índios tratados com Carvedilol, independente da causalidade)
| Sistema Corporal / Acontecimento Adverso | HF ligeiro a moderado | Campa HF | ||
| Carvedilol (n = 765) |
Placebo (n = 437) |
Carvedilol (n = 1, 156)) |
Placebo (n = 1,133) |
|
| Corpo como um todo | ||||
| Astenia | 7 | 7 | 11 | 9 |
| Fadiga | 24 | 22 | — | — |
| Aumento do nível de digoxina | 5 | 4 | 2 | 1 |
| Edema generalizado | 5 | 3 | 6 | 5 |
| Dependente de Edema | 4 | 2 | — | — |
| Cardiovascular | ||||
| Bradicardia | 9 | 1 | 10 | 3 |
| Hipotensao | 9 | 3 | 14 | 8 |
| Sincope | 3 | 3 | 8 | 5 |
| Angina | 2 | 3 | 6 | 4 |
| Sistema Nervoso Central | ||||
| Tontura | 32 | 19 | 24 | 17 |
| Dor | 8 | 7 | 5 | 3 |
| Gastrintestinal | ||||
| Diarréia | 12 | 6 | 5 | 3 |
| Nausea | 9 | 5 | 4 | 3 |
| Vomito | 6 | 4 | 1 | 2 |
| Metabolico | ||||
| Hiperglicemia | 12 | 8 | 5 | 3 |
| Aumento de peso | 10 | 7 | 12 | 11 |
| Aumento do pão | 6 | 5 | — | — |
| NPN aumentada | 6 | 5 | — | — |
| Hipercolesterolemia | 4 | 3 | 1 | 1 |
| Edema periférico | 2 | 1 | 7 | 6 |
| Esqueletico | ||||
| Artralgia | 6 | 5 | 1 | 1 |
| Respiratório | ||||
| Aumento da tosse | 8 | 9 | 5 | 4 |
| Rales | 4 | 4 | 4 | 2 |
| Visao | ||||
| Perturbações da visão | 5 | 2 | — | — |
Foram também notificados casos de insuficiência cardíaca e dispneia nestes doentes. ensaios clínicos, mas as taxas foram iguais ou superiores nos indivíduos que receberam placebo.
Os seguintes acontecimentos adversos foram notificados com uma frequência superior a 1% mas inferior ou igual a 3% e com maior frequência com carvedilol nos ensaios controlados com placebo nos EUA em indivíduos com insuficiência cardíaca ligeira a moderada, ou em indivíduos com insuficiência cardíaca grave Julgamento de Copérnico.
Incidência Superior A 1% Para Inferior Ou Igual A 3%
Corpo como um todo: Alergia, mal-estar, hipovolemia, febre, edema da perna.
Cardiovascular: Sobrecarga de fluidos, postural hipotensão, angina de peito agravada, bloqueio AV, palpitações, hipertensão.
Sistema nervoso central e periférico: Hipestesia, vertigens, parestesia.
Gastrintestinal: Melena, periodontite.
Sistema hepático e biliar: Aumento da SGPT, SGOT aumento.
Metabolismo e nutrição: Hiperuricemia, hipoglicemia, hiponatremia, aumento da fosfatase alcalina, glicosúria, hipervolemia, diabetes mellitus, GGT aumentada, perda de peso, hipercaliemia, aumento da creatinina.
Esqueletico: Cãibras musculares.
Plaquetas, hemorragia e coagulação: Protrombina diminuição da púrpura, trombocitopenia.
Psiquiatrico: Sonolência.
Reprodutivo masculino: Impotência.
Sentidos Especiais: Turvar.
Sistema Urinário: Insuficiência Renal, albuminúria, hematúria.
Disfunção Ventricular esquerda após enfarte do miocárdio Miocardio
A informação que se segue descreve a experiência de segurança na disfunção ventricular esquerda após enfarte agudo do miocárdio com libertação imediata de carvedilol.
O Carvedilol foi avaliado quanto à segurança em sobreviventes de um enfarte agudo do miocárdio com disfunção ventricular esquerda na O estudo do Capricórnio, que envolveu 969 indivíduos que receberam carvedilol e 980 que recebeu placebo. Aproximadamente 75% dos indivíduos receberam carvedilol para pelo menos 6 meses e 53% receberam carvedilol durante pelo menos 12 meses. Item foram tratados durante uma média de 12, 9 meses e 12, 8 meses com carvedilol e placebo, respectivamente.
Os acontecimentos adversos mais frequentes notificados com carvedilol no caso do Capricórnio, foram consistentes com o perfil da droga nos EUA. ensaios de insuficiência cardíaca e o ensaio COPERNICUS. O único acontecimentos notificados em Capricórnio em mais de 3% dos indivíduos e mais frequentemente tratados com carvedilol apresentavam dispneia, anemia e edema pulmonar.. Seguinte os acontecimentos adversos foram notificados com uma frequência superior a 1% mas inferior a ou igual a 3% e mais frequentemente com carvedilol: síndrome gripal, acidente vascular cerebral, doença vascular periférica, hipotonia, depressão, dor gastrointestinal, artrite e gota. As taxas globais de a interrupção devido a acontecimentos adversos foi semelhante em ambos os grupos de indivíduos. Nesta base de dados, a única causa de interrupção superior a 1%, e a ocorrência mais frequente de carvedilol foi hipotensão (1.5% em carvedilol, 0.2% sobre placebo)
Hipertensao
COREG CR foi avaliado para a segurança em 8 semanas. ensaio com dupla ocultação em 337 indivíduos com hipertensão essencial. O perfil de os acontecimentos adversos observados com COREG CR foram geralmente semelhantes aos observados com o COREG CR. com carvedilol de libertação imediata. As taxas globais de desistências devidas a os acontecimentos adversos foram semelhantes entre COREG CR e placebo.
Quadro 3: Contactos Adversos ( % ) Que Ocorrem Mais Frequentemente
com COREG CR do que com Placebo em indívidos com hipertensão (incidência ≥ 1%
em índios tratados com Carvedilol, independente da causalidade)
| Contexto Adverso | COREG CR (n = 253) |
Placebo (n = 84) |
| Nasofaringite | 4 | 0 |
| Tontura | 2 | 1 |
| Nausea | 2 | 0 |
| Edema periférico | 2 | 1 |
| Nasal De Congestão | 1 | 0 |
| Parestesia | 1 | 0 |
| Congestão sinusal | 1 | 0 |
| Diarréia | 1 | 0 |
| Insónia | 1 | 0 |
A informação que se segue descreve a experiência de segurança na hipertensão com carvedilol de libertação imediata.
Carvedilol foi avaliado quanto à segurança na hipertensão. em mais de 2. 193 indivíduos nos ensaios clínicos nos EUA e em 2. 976 indivíduos nos ensaios clínicos nos EUA. ensaios clínicos internacionais. Aproximadamente 36% do total tratado a população recebeu carvedilol durante pelo menos 6 meses. Em geral, carvedilol foi bem tolerado em doses até 50 mg por dia. A maioria dos acontecimentos adversos notificados durante a terapêutica com carvedilol foram de gravidade ligeira a moderada.. Nos EUA controlados ensaios clínicos que compararam directamente carvedilol em monoterapia em doses até 50 mg (n = 1. 142) com placebo( n = 462), 4.9% dos indivíduos tratados com carvedilol interromperam o tratamento. para efeitos adversos versus 5.2% dos doentes tratados com placebo. Apesar de não haver diferença global nas taxas de descontinuação, as interrupções foram mais frequentes no grupo do carvedilol para hipotensão postural (1% versus 0). Geral a incidência de acontecimentos adversos nos ensaios controlados com placebo nos EUA foi aumento com o aumento da dose de carvedilol. Para os acontecimentos adversos individuais: apenas se distinguiram as tonturas, que aumentaram em frequência de 2% para 5% Como dose diária total aumentada de 6.25 mg a 50 mg em monoterapia ou em associação dose
A tabela 4 mostra acontecimentos adversos nos EUA controlados com placebo ensaios clínicos para a hipertensão que ocorreram com uma incidência de de 1%, independentemente da causalidade, e que foram mais frequentes em indivíduos tratados com fármaco do que indivíduos tratados com placebo.
Quadro 4: acontecimentos adversos (gravura) nos EUA controlados com Placebo
Grupos de hipertensão com Carvedilol de libertação imediata (incidência ≥ 1%
em índios tratados com Carvedilol, independente da causalidade)*
| Contexto Adverso | Carvedilol (n = 1. 142) |
Placebo (n = 462) |
| Cardiovascular | ||
| Bradicardia | 2 | — |
| Hipotensa Postural | 2 | — |
| Edema periférico | 1 | — |
| Sistema Nervoso Central | ||
| Tontura | 6 | 5 |
| Insónia | 2 | 1 |
| Gastrintestinal | ||
| Diarréia | 2 | 1 |
| Hematológico | ||
| Trombocitopenia | 1 | — |
| Metabolico | ||
| Hipertrigliceridemia | 1 | — |
| * São apresentados eventos com uma taxa > 1% atrasada para a inteiro. | ||
Dispneia e fadiga também foram notificados nestes ensaios, mas as taxas foram iguais ou superiores nos indivíduos que receberam placebo.
Os seguintes acontecimentos adversos Não descritos acima foram: reportado como possível ou provavelmente relacionado com carvedilol em worldwide open ou ensaios controlados com carvedilol em indivíduos com hipertensão ou coração falha.
Incidência Superior A 0,1% Para Inferior Ou Igual A 1%
Cardiovascular: Isquemia periférica, taquicardia.
Sistema nervoso central e periférico: Hipocinésia.
Gastrintestinal: Bilirrubinemia, aumento da função hepática enzimas (0, 2% dos doentes com hipertensão e 0, 4% dos doentes com insuficiência cardíaca foram interrompeu a terapêutica devido a aumentos das enzimas hepáticas).
Psiquiatrico: Nervosismo, perturbação do sono, agravamento depressão, diminuição da concentração, pensamentos anormais, paroniria, labilidade.
Sistema Respiratório: Asma.
Reprodutivo masculino: Diminuição da libido.
Pelé e anexos: Prurido, erupção cutânea eritematosa, erupção cutânea maculopapular, erupção cutânea psoriaforme, reacção de fotossensibilidade.
Sentidos Especiais: Zumbido.
Sistema Urinário: Aumento da frequência na micção.
Sistema Nervoso Autónomo: Secura de boca, sudação aumento.
Metabolismo e nutrição: Hipocaliemia, hipertrigliceridemia.
Hematológico: Anemia, leucopenia.
Os seguintes acontecimentos foram relatados em menor ou igual to 0, 1% dos indivíduos e são potencialmente importantes: bloco AV completo, pacote bloqueio de ramo, isquemia do miocárdio, alterações cerebrovasculares, convulsões, enxaqueca, nevralgia, paresia, reacção anafilactóide, alopécia, esfoliativa dermatite, amnésia, hemorragia gastrointestinal, broncospasmo, edema pulmonar, diminuição audição, alcalose respiratória, aumento do BUN, diminuição das HDL, pancitopenia, e linfócitos atípicos.
Alterações Laboratoriais
Elevação reversível das transaminases séricas (ALT ou AST) foram observados durante o tratamento com carvedilol. Taxas de transaminase elevações (2 a 3 vezes o limite superior do normal) observadas durante o os ensaios clínicos têm sido geralmente semelhantes entre indivíduos tratados com carvedilol e os tratados com placebo. No entanto, aumentos das transaminases, foram observados com carvedilol. A longo prazo, ensaio controlado com placebo na insuficiência cardíaca grave, indivíduos tratados com o carvedilol apresentou valores mais baixos para as transaminases hepáticas do que para os indivíduos tratados. com placebo, possivelmente porque o carvedilol induziu melhorias na a função conduziu a uma menor congestão hepática e / ou melhoria do fluxo sanguíneo hepático
A terapêutica com Carvedilol não foi associada a alterações clinicamente significativas no potássio sérico, triglicéridos totais, total colesterol, colesterol HDL, ácido úrico, azoto ureico sanguíneo ou creatinina. Não foram observadas alterações clinicamente relevantes nos níveis séricos de glucose em jejum nos doentes hipertensos. indivíduos, a glucose sérica em jejum não foi avaliada na insuficiência cardíaca clínica. ensaio.
Frequente (≥1 / 10)
Foram identificadas as seguintes reacções adversas: durante a utilização pós-aprovação de COREG® ou COREG CR. Estas reacções são: reportado voluntariamente a partir de uma população de tamanho incerto, nem sempre é possível estimar de forma fiável a sua frequência ou estabelecer um nexo de causalidade relação com a exposição a drogas.
Doenças do sangue e do sistema linfático
Anemia aplástica.
Doenças Do Sistema Imunitário
Hipersensibilidade (por ex., reacções anafilácticas), angioedema e urticária).
Doenças renais e urinárias
Incontinência urinária.
Doenças respiratórias, torácicas e do mediastino
Pneumonite intersticial.
Afecções dos tecidos cutâneos e subcutâneas
Síndrome de Stevens-Johnson, necrólise epidérmica tóxica, eritema multiforme.
INTERACCAO
Inibidores e metabolizadores fracos do CYP2D6
Interacções do carvedilol com inibidores potentes da Isoenzima CYP2D6 (tal como quinidina, fluoxetina, paroxetina e propafenona)) não foram estudados, mas seria de esperar que estes medicamentos aumentassem o sangue níveis do enantiómero R( ) do carvedilol. A análise retrospectiva dos efeitos secundários em ensaios clínicos mostrou que o 2D6 é fraco. os metabolizadores tiveram uma maior taxa de tonturas durante a titulação, presumivelmente resultante dos efeitos vasodilatadores das concentrações mais elevadas da enantiómero α-bloqueador R ().
Agentes Hipotensores
Doentes a tomar ambos os fármacos com bloqueio beta as propriedades e uma droga que pode diminuir as catecolaminas (por exemplo, reserpina e os inibidores da monoamino oxidase) devem ser cuidadosamente observados para detecção de sinais de hipotensão e / ou bradicardia grave.
Administração concomitante de clonidina com agentes com as propriedades de bloqueio beta podem potenciar a pressão arterial e efeitos de redução da frequência cardíaca. Quando o tratamento concomitante com agentes com as propriedades de bloqueio β e a clonidina devem ser terminadas, o agente β-bloqueante deve ser interrompido primeiro. A terapêutica com clonidina pode então ser descontinuado vários dias depois, diminuindo gradualmente a dose.
Ciclosporina
Aumentos modestos da ciclosporina média foram observadas concentrações após o início do tratamento com carvedilol em 21 doentes com transplante renal com rejeição vascular crónica. Em cerca de 30% dos indivíduos, a dose de ciclosporina teve de ser reduzida de modo a manter as concentrações de ciclosporina dentro dos limites terapêuticos, enquanto na quanto ao restante, não foi necessário qualquer ajustamento. Em média, para o grupo, a dose de a ciclosporina foi reduzida cerca de 20% nestes indivíduos.. Devido à grande interindividual devido à variabilidade da dose, recomenda-se que seja as concentrações de ciclosporina devem ser cuidadosamente monitorizadas após o início do carvedilol. tratamento e que a dose de ciclosporina seja ajustada conforme apropriado
Glicósidos Digitálicos
Os glicosídeos digitálicos e os bloqueadores β são lentos. condução auriculoventricular e diminuição da frequência cardíaca. O uso concomitante pode aumentar o risco de bradicardia. As concentrações de digoxina são aumentadas em cerca de 15% quando a digoxina e o carvedilol são administrados concomitantemente. Assim, recomenda-se uma monitorização aumentada da digoxina quando se inicia, ajusta ou supressão da COREG CR.
Indutores/Inibidores Do Metabolismo Hepático
A rifampina reduziu as concentrações plasmáticas de carvedilol por cerca de 70%. Aumento da área sob a curva (AUC) em cerca de 30% mas não causou alteração na Cmax.
Amiodarona
Amiodarona e seu metabolito desetil amiodarona, os inibidores da CYP2C9 e glicoproteína-P aumentaram as concentrações da S(-) enantiómero de carvedilol pelo menos 2 vezes. A administração concomitante de amiodarona ou de outros inibidores da CYP2C9, tais como: fluconazol com COREG CR pode aumentar as propriedades de bloqueio β Do carvedilol resultando numa maior diminuição da frequência cardíaca ou cardíaca conducao. Os doentes devem ser observados para detecção de sinais de bradicardia ou coração bloquear, particularmente quando um agente é adicionado ao tratamento pré-existente com o restante.
Bloqueadores Dos Canais De Cálcio
Perturbação da condução (raramente com hemodinâmica) compromisso) foi observado quando o carvedilol é co-administrado com diltiazem. Tal como acontece com outros agentes com propriedades de bloqueio β, se COREG CR deve ser administrado por via oral com bloqueadores dos canais de cálcio do verapamilo ou diltiazem. recomenda-se a monitorização do ECG e da pressão arterial.
Insulina Ou Hipoglicemiantes Orais
Os agentes com propriedades de bloqueio β podem aumentar a açúcar no sangue-efeito redutor da insulina e hipoglicemiantes orais. Por conseguinte, em doentes que tomam insulina ou hipoglicemiantes orais, monitorização regular do sangue recomenda-se glucose.
Inibidores Da Bomba De Protões
Não existe aumento clinicamente significativo na AUC e Cmax. com a administração concomitante de cápsulas de libertação prolongada de carvedilol com pantoprazol.
Anestesia
Se for necessário continuar o tratamento com COREG CR perioperativamente, deve ter-se especial cuidado quando os agentes anestésicos que despressurizar a função do miocárdio, tais como éter, ciclopropano, e tricloroetileno, são usados.

Gravidez Categoria C
Estudos realizados em ratos e coelhos fêmeas gestantes aos quais foi administrado carvedilol revelou um aumento da perda pós-implantação em ratos com doses de 300 mg por kg por dia (50 vezes a dose máxima recomendada no ser humano [DMRH] em mg por m2) e em coelhos com doses de 75 mg por kg por dia (25 vezes a dose de MRHD em mg por m2). Nos ratos, verificou-se também uma diminuição do peso corporal fetal na mãe. dose tóxica de 300 mg por kg por dia( 50 vezes a dose de MRHD em mg por m2), que foi acompanhado por uma elevação na frequência de fetos com atraso no esqueleto desenvolvimento (falta ou falha da 13ª costela). Nos ratos, o nível sem efeito observado para a toxicidade para o desenvolvimento foi de 60 mg por kg por dia (10 vezes a dose de MRHD em mg). por m2), em coelhos foi de 15 mg por kg por dia (5 vezes a dose de MRHD em mg por m2).). Não existem estudos adequados e bem controlados em mulheres grávidas.. COREG CR deve ser utilizado durante a gravidez apenas se os potenciais benefícios justificarem a risco potencial para o feto

Experiência Em Ensaios Clínicos
O Carvedilol foi avaliado quanto à segurança em indivíduos com insuficiência cardíaca (ligeira, moderada e grave), em indivíduos com ventrículo esquerdo disfunção após enfarte do miocárdio e em indivíduos hipertensos. O o perfil de acontecimentos adversos observados foi consistente com a farmacologia do fármaco. e o estado de saúde dos indivíduos nos ensaios clínicos. Acontecimentos adversos comunicado para cada uma destas populações, reflectindo a utilização de COREG CR ou o carvedilol de libertação imediata é fornecido a seguir.. Os acontecimentos adversos estão excluídos. considerado demasiado geral para ser informativo, e aqueles não razoavelmente associados com o uso da droga porque eles estavam associados com a condição de ser tratados ou são muito comuns na população tratada. Taxas de acontecimentos adversos foram geralmente semelhantes em todos os subconjuntos demográficos (homens e mulheres, idosos e não idosos, negros e não Negros). COREG CR foi avaliado quanto à segurança em 4 semanas (2 semanas de libertação imediata de carvedilol e 2 semanas de COREG CR) ensaios clínicos (n = 187) que incluíram 157 indivíduos com, insuficiência cardíaca crónica moderada ou grave e 30 indivíduos com ventrículo esquerdo disfunção após enfarte agudo do miocárdio. O perfil de os acontecimentos observados com COREG CR neste pequeno ensaio clínico de curta duração foram geralmente semelhante ao observado com carvedilol de libertação imediata. Diferenças na não seria de esperar segurança com base na semelhança dos níveis plasmáticos de COREG CR e carvedilol de libertação imediata
cardiaco
A informação que se segue descreve a experiência de segurança na insuficiência cardíaca com carvedilol de libertação imediata.
O Carvedilol foi avaliado quanto à segurança na insuficiência cardíaca. em mais de 4.500 temas em todo o mundo, dos quais mais de 2.100 participaram ensaios clínicos controlados com placebo. Aproximadamente 60% do total tratado a população em ensaios clínicos controlados com placebo recebeu carvedilol para pelo menos 6 meses e 30% receberam carvedilol durante pelo menos 12 meses. No cometa no ensaio, 1. 511 indivíduos com insuficiência cardíaca ligeira a moderada foram tratados com carvedilol até 5.9 anos (média: 4.8 anos). Ambos os ensaios clínicos nos Estados Unidos da América insuficiência cardíaca ligeira a moderada que comparou o carvedilol em doses diárias até 100 mg (n = 765) com placebo (n = 437) e num ensaio clínico multinacional na insuficiência cardíaca grave (COPERNICUS) que comparou o carvedilol em doses diárias to 50 mg (n = 1. 156) com placebo (n = 1. 133), taxas de descontinuação para os efeitos adversos foram semelhantes nos indivíduos tratados com carvedilol e placebo.. Em nos ensaios clínicos controlados com placebo, a única causa de descontinuação é maior do que nos ensaios clínicos controlados com placebo. mais de 1%, e ocorrendo mais frequentemente em carvedilol foram tonturas (1.3% em carvedilol, 0.6% com placebo no ensaio COPERNICUS)
A tabela 2 mostra os acontecimentos adversos notificados em indivíduos com insuficiência cardíaca ligeira a moderada incluída nos ensaios clínicos controlados com placebo ensaios clínicos e com insuficiência cardíaca grave incluída no ensaio COPERNICUS. Figurar os acontecimentos adversos que ocorreram mais frequentemente em indivíduos tratados com indivíduos tratados com placebo com uma incidência superior a 3% em indivíduos tratado com carvedilol independentemente da causalidade. Median trial medication a exposição foi de 6.3 meses para os indivíduos que receberam carvedilol e placebo nos ensaios de insuficiência cardíaca ligeira a moderada e 10.4 meses no ensaio clínico de indivíduos com insuficiência cardíaca grave. O perfil de acontecimentos adversos de carvedilol observado em o ensaio a longo prazo cometas foi geralmente semelhante ao observado nos EUA. Ensaios De Insuficiência Cardíaca.11
Quadro 2: Contactos Adversários ( % ) Que Ocorrem Mais Frequentemente
com Carvedilol de libertação imediata do que com Placebo em índios com
Insuficiência cardíaca ligeira a moderada (HF) inclui nos ensalos de insufficiência cardíaca dos EUA ou
Doentes com insinuação cardíaca grave no ensaio COPERNICUS (incidência > 3% em doentes com insuficiência cardíaca grave)
Índios tratados com Carvedilol, independente da causalidade)
| Sistema Corporal / Acontecimento Adverso | HF ligeiro a moderado | Campa HF | ||
| Carvedilol (n = 765) |
Placebo (n = 437) |
Carvedilol (n = 1, 156)) |
Placebo (n = 1,133) |
|
| Corpo como um todo | ||||
| Astenia | 7 | 7 | 11 | 9 |
| Fadiga | 24 | 22 | — | — |
| Aumento do nível de digoxina | 5 | 4 | 2 | 1 |
| Edema generalizado | 5 | 3 | 6 | 5 |
| Dependente de Edema | 4 | 2 | — | — |
| Cardiovascular | ||||
| Bradicardia | 9 | 1 | 10 | 3 |
| Hipotensao | 9 | 3 | 14 | 8 |
| Sincope | 3 | 3 | 8 | 5 |
| Angina | 2 | 3 | 6 | 4 |
| Sistema Nervoso Central | ||||
| Tontura | 32 | 19 | 24 | 17 |
| Dor | 8 | 7 | 5 | 3 |
| Gastrintestinal | ||||
| Diarréia | 12 | 6 | 5 | 3 |
| Nausea | 9 | 5 | 4 | 3 |
| Vomito | 6 | 4 | 1 | 2 |
| Metabolico | ||||
| Hiperglicemia | 12 | 8 | 5 | 3 |
| Aumento de peso | 10 | 7 | 12 | 11 |
| Aumento do pão | 6 | 5 | — | — |
| NPN aumentada | 6 | 5 | — | — |
| Hipercolesterolemia | 4 | 3 | 1 | 1 |
| Edema periférico | 2 | 1 | 7 | 6 |
| Esqueletico | ||||
| Artralgia | 6 | 5 | 1 | 1 |
| Respiratório | ||||
| Aumento da tosse | 8 | 9 | 5 | 4 |
| Rales | 4 | 4 | 4 | 2 |
| Visao | ||||
| Perturbações da visão | 5 | 2 | — | — |
Foram também notificados casos de insuficiência cardíaca e dispneia nestes doentes. ensaios clínicos, mas as taxas foram iguais ou superiores nos indivíduos que receberam placebo.
Os seguintes acontecimentos adversos foram notificados com uma frequência superior a 1% mas inferior ou igual a 3% e com maior frequência com carvedilol nos ensaios controlados com placebo nos EUA em indivíduos com insuficiência cardíaca ligeira a moderada, ou em indivíduos com insuficiência cardíaca grave Julgamento de Copérnico.
Incidência Superior A 1% Para Inferior Ou Igual A 3%
Corpo como um todo: Alergia, mal-estar, hipovolemia, febre, edema da perna.
Cardiovascular: Sobrecarga de fluidos, postural hipotensão, angina de peito agravada, bloqueio AV, palpitações, hipertensão.
Sistema nervoso central e periférico: Hipestesia, vertigens, parestesia.
Gastrintestinal: Melena, periodontite.
Sistema hepático e biliar: Aumento da SGPT, SGOT aumento.
Metabolismo e nutrição: Hiperuricemia, hipoglicemia, hiponatremia, aumento da fosfatase alcalina, glicosúria, hipervolemia, diabetes mellitus, GGT aumentada, perda de peso, hipercaliemia, aumento da creatinina.
Esqueletico: Cãibras musculares.
Plaquetas, hemorragia e coagulação: Protrombina diminuição da púrpura, trombocitopenia.
Psiquiatrico: Sonolência.
Reprodutivo masculino: Impotência.
Sentidos Especiais: Turvar.
Sistema Urinário: Insuficiência Renal, albuminúria, hematúria.
Disfunção Ventricular esquerda após enfarte do miocárdio Miocardio
A informação que se segue descreve a experiência de segurança na disfunção ventricular esquerda após enfarte agudo do miocárdio com libertação imediata de carvedilol.
O Carvedilol foi avaliado quanto à segurança em sobreviventes de um enfarte agudo do miocárdio com disfunção ventricular esquerda na O estudo do Capricórnio, que envolveu 969 indivíduos que receberam carvedilol e 980 que recebeu placebo. Aproximadamente 75% dos indivíduos receberam carvedilol para pelo menos 6 meses e 53% receberam carvedilol durante pelo menos 12 meses. Item foram tratados durante uma média de 12, 9 meses e 12, 8 meses com carvedilol e placebo, respectivamente.
Os acontecimentos adversos mais frequentes notificados com carvedilol no caso do Capricórnio, foram consistentes com o perfil da droga nos EUA. ensaios de insuficiência cardíaca e o ensaio COPERNICUS. O único acontecimentos notificados em Capricórnio em mais de 3% dos indivíduos e mais frequentemente tratados com carvedilol apresentavam dispneia, anemia e edema pulmonar.. Seguinte os acontecimentos adversos foram notificados com uma frequência superior a 1% mas inferior a ou igual a 3% e mais frequentemente com carvedilol: síndrome gripal, acidente vascular cerebral, doença vascular periférica, hipotonia, depressão, dor gastrointestinal, artrite e gota. As taxas globais de a interrupção devido a acontecimentos adversos foi semelhante em ambos os grupos de indivíduos. Nesta base de dados, a única causa de interrupção superior a 1%, e a ocorrência mais frequente de carvedilol foi hipotensão (1.5% em carvedilol, 0.2% sobre placebo)
Hipertensao
COREG CR foi avaliado para a segurança em 8 semanas. ensaio com dupla ocultação em 337 indivíduos com hipertensão essencial. O perfil de os acontecimentos adversos observados com COREG CR foram geralmente semelhantes aos observados com o COREG CR. com carvedilol de libertação imediata. As taxas globais de desistências devidas a os acontecimentos adversos foram semelhantes entre COREG CR e placebo.
Quadro 3: Contactos Adversos ( % ) Que Ocorrem Mais Frequentemente
com COREG CR do que com Placebo em indívidos com hipertensão (incidência ≥ 1%
em índios tratados com Carvedilol, independente da causalidade)
| Contexto Adverso | COREG CR (n = 253) |
Placebo (n = 84) |
| Nasofaringite | 4 | 0 |
| Tontura | 2 | 1 |
| Nausea | 2 | 0 |
| Edema periférico | 2 | 1 |
| Nasal De Congestão | 1 | 0 |
| Parestesia | 1 | 0 |
| Congestão sinusal | 1 | 0 |
| Diarréia | 1 | 0 |
| Insónia | 1 | 0 |
A informação que se segue descreve a experiência de segurança na hipertensão com carvedilol de libertação imediata.
Carvedilol foi avaliado quanto à segurança na hipertensão. em mais de 2. 193 indivíduos nos ensaios clínicos nos EUA e em 2. 976 indivíduos nos ensaios clínicos nos EUA. ensaios clínicos internacionais. Aproximadamente 36% do total tratado a população recebeu carvedilol durante pelo menos 6 meses. Em geral, carvedilol foi bem tolerado em doses até 50 mg por dia. A maioria dos acontecimentos adversos notificados durante a terapêutica com carvedilol foram de gravidade ligeira a moderada.. Nos EUA controlados ensaios clínicos que compararam directamente carvedilol em monoterapia em doses até 50 mg (n = 1. 142) com placebo( n = 462), 4.9% dos indivíduos tratados com carvedilol interromperam o tratamento. para efeitos adversos versus 5.2% dos doentes tratados com placebo. Apesar de não haver diferença global nas taxas de descontinuação, as interrupções foram mais frequentes no grupo do carvedilol para hipotensão postural (1% versus 0). Geral a incidência de acontecimentos adversos nos ensaios controlados com placebo nos EUA foi aumento com o aumento da dose de carvedilol. Para os acontecimentos adversos individuais: apenas se distinguiram as tonturas, que aumentaram em frequência de 2% para 5% Como dose diária total aumentada de 6.25 mg a 50 mg em monoterapia ou em associação dose
A tabela 4 mostra acontecimentos adversos nos EUA controlados com placebo ensaios clínicos para a hipertensão que ocorreram com uma incidência de de 1%, independentemente da causalidade, e que foram mais frequentes em indivíduos tratados com fármaco do que indivíduos tratados com placebo.
Quadro 4: acontecimentos adversos (gravura) nos EUA controlados com Placebo
Grupos de hipertensão com Carvedilol de libertação imediata (incidência ≥ 1%
em índios tratados com Carvedilol, independente da causalidade)*
| Contexto Adverso | Carvedilol (n = 1. 142) |
Placebo (n = 462) |
| Cardiovascular | ||
| Bradicardia | 2 | — |
| Hipotensa Postural | 2 | — |
| Edema periférico | 1 | — |
| Sistema Nervoso Central | ||
| Tontura | 6 | 5 |
| Insónia | 2 | 1 |
| Gastrintestinal | ||
| Diarréia | 2 | 1 |
| Hematológico | ||
| Trombocitopenia | 1 | — |
| Metabolico | ||
| Hipertrigliceridemia | 1 | — |
| * São apresentados eventos com uma taxa > 1% atrasada para a inteiro. | ||
Dispneia e fadiga também foram notificados nestes ensaios, mas as taxas foram iguais ou superiores nos indivíduos que receberam placebo.
Os seguintes acontecimentos adversos Não descritos acima foram: reportado como possível ou provavelmente relacionado com carvedilol em worldwide open ou ensaios controlados com carvedilol em indivíduos com hipertensão ou coração falha.
Incidência Superior A 0,1% Para Inferior Ou Igual A 1%
Cardiovascular: Isquemia periférica, taquicardia.
Sistema nervoso central e periférico: Hipocinésia.
Gastrintestinal: Bilirrubinemia, aumento da função hepática enzimas (0, 2% dos doentes com hipertensão e 0, 4% dos doentes com insuficiência cardíaca foram interrompeu a terapêutica devido a aumentos das enzimas hepáticas).
Psiquiatrico: Nervosismo, perturbação do sono, agravamento depressão, diminuição da concentração, pensamentos anormais, paroniria, labilidade.
Sistema Respiratório: Asma.
Reprodutivo masculino: Diminuição da libido.
Pelé e anexos: Prurido, erupção cutânea eritematosa, erupção cutânea maculopapular, erupção cutânea psoriaforme, reacção de fotossensibilidade.
Sentidos Especiais: Zumbido.
Sistema Urinário: Aumento da frequência na micção.
Sistema Nervoso Autónomo: Secura de boca, sudação aumento.
Metabolismo e nutrição: Hipocaliemia, hipertrigliceridemia.
Hematológico: Anemia, leucopenia.
Os seguintes acontecimentos foram relatados em menor ou igual to 0, 1% dos indivíduos e são potencialmente importantes: bloco AV completo, pacote bloqueio de ramo, isquemia do miocárdio, alterações cerebrovasculares, convulsões, enxaqueca, nevralgia, paresia, reacção anafilactóide, alopécia, esfoliativa dermatite, amnésia, hemorragia gastrointestinal, broncospasmo, edema pulmonar, diminuição audição, alcalose respiratória, aumento do BUN, diminuição das HDL, pancitopenia, e linfócitos atípicos.
Alterações Laboratoriais
Elevação reversível das transaminases séricas (ALT ou AST) foram observados durante o tratamento com carvedilol. Taxas de transaminase elevações (2 a 3 vezes o limite superior do normal) observadas durante o os ensaios clínicos têm sido geralmente semelhantes entre indivíduos tratados com carvedilol e os tratados com placebo. No entanto, aumentos das transaminases, foram observados com carvedilol. A longo prazo, ensaio controlado com placebo na insuficiência cardíaca grave, indivíduos tratados com o carvedilol apresentou valores mais baixos para as transaminases hepáticas do que para os indivíduos tratados. com placebo, possivelmente porque o carvedilol induziu melhorias na a função conduziu a uma menor congestão hepática e / ou melhoria do fluxo sanguíneo hepático
A terapêutica com Carvedilol não foi associada a alterações clinicamente significativas no potássio sérico, triglicéridos totais, total colesterol, colesterol HDL, ácido úrico, azoto ureico sanguíneo ou creatinina. Não foram observadas alterações clinicamente relevantes nos níveis séricos de glucose em jejum nos doentes hipertensos. indivíduos, a glucose sérica em jejum não foi avaliada na insuficiência cardíaca clínica. ensaio.
Frequente (≥1 / 10)
Foram identificadas as seguintes reacções adversas: durante a utilização pós-aprovação de COREG® ou COREG CR. Estas reacções são: reportado voluntariamente a partir de uma população de tamanho incerto, nem sempre é possível estimar de forma fiável a sua frequência ou estabelecer um nexo de causalidade relação com a exposição a drogas.
Doenças do sangue e do sistema linfático
Anemia aplástica.
Doenças Do Sistema Imunitário
Hipersensibilidade (por ex., reacções anafilácticas), angioedema e urticária).
Doenças renais e urinárias
Incontinência urinária.
Doenças respiratórias, torácicas e do mediastino
Pneumonite intersticial.
Afecções dos tecidos cutâneos e subcutâneas
Síndrome de Stevens-Johnson, necrólise epidérmica tóxica, eritema multiforme.

Sobredosagem pode causar hipotensão grave, bradicardia, insuficiência cardíaca, choque cardiogénico e paragem cardíaca. Respiratorio problemas, broncospasmos, vómitos, lapsos de consciência e generalização podem também ocorrer convulsões.
O doente deve ser colocado em decúbito dorsal e, se necessário, mantidos sob observação e tratados sob cuidados intensivos condicao. Podem ser administrados os seguintes agentes::
Em caso de bradicardia excessiva: atropina, 2 mg por via intravenosa.
Para apoiar a função cardiovascular: glucagom, 5 a 10 mg IV rapidamente durante 30 segundos, seguido de uma perfusão contínua de 5 mg por horas, simpaticomiméticos (dobutamina, isoprenalina, adrenalina) em doses de acordo com o peso corporal e efeito.
Se a vasodilatação periférica dominar, pode ser necessário para administrar adrenalina ou noradrenalina com monitorização contínua de condições circulatórias. Para bradicardia resistente à terapêutica, terapia com pacemaker deve ser realizado. Para broncospasmo, simpaticomiméticos β (como aerossol ou IV)ou deve ser administrada a aminofilina IV. Em caso de convulsões, recomenda-se a injecção de diazepam ou clonazepam.
NOTAR: Em caso de intoxicação grave, quando existem sintomas de choque, o tratamento com antídotos deve ser continuado para uma período de tempo suficientemente longo, compatível com a semi - vida de 7 a 10 horas carvedilol.
Não existe experiência de sobredosagem com COREG CR. Vez de sobredosagem com carvedilol em monoterapia ou em associação com outros medicamentos, têm foi relatado. As quantidades ingeridas em alguns casos excederam 1000 miligramas. Os sintomas experimentados incluíram pressão arterial baixa e frequência cardíaca. Padrao foi fornecido tratamento de suporte e os indivíduos recuperaram.

Insuficiência cardíaca e disfunção Ventricular esquerda após Enfarte Do Miocárdio
A base para os efeitos benéficos do carvedilol em doentes com insuficiência cardíaca e em doentes com disfunção ventricular esquerda após um enfarte agudo do miocárdio não é conhecido. O relação concentração-resposta para o β1-bloqueio após a administração de COREG CR é equivalente (±20%) ao carvedilol de libertação imediata comprimido.
Hipertensao
O mecanismo através do qual o β-bloqueio produz um antihipertensor não foi estabelecido qualquer efeito.
a actividade de Bloqueio Do β-adrenoreceptor foi demonstrado em estudos em animais e em seres humanos que demonstram que o carvedilol (1) reduz a a produção cardíaca em indivíduos normais, (2) reduz o exercício e/ou taquicardia induzida pelo isoproterenol e (3) reduz a ortostática reflexa taquicardia. Efeito bloqueador significativo do β-adrenoreceptor é geralmente observado 1 hora após a administração do medicamento.
a actividade de bloqueio do α1-adrenoreceptor foi demonstrado em estudos em humanos e animais, que demonstram que o carvedilol (1) atenua os efeitos pressores da fenilefrina, (2) causa vasodilatação, e (3) reduz a resistência vascular periférica. Estes efeitos contribuem para a redução da pressão arterial e geralmente são observados dentro de 30 minutos do fármaco administracao.
Devido à actividade bloqueadora dos receptores α1 carvedilol, a pressão arterial está mais baixa em pé do que em decúbito dorsal. situação e sintomas de hipotensão postural( 1, 8%), incluindo casos raros pode ocorrer síncope. Após administração oral, quando hipotensão postural ocorreu, foi transitório e é pouco frequente quando a libertação imediata carvedilol é administrado com alimentos na dose inicial recomendada e os incrementos de titulação são seguidos de perto.
Num ensaio aleatorizado, em dupla ocultação, controlado com placebo, o efeito de bloqueio β1 do COREG CR, medido pela resposta da frequência cardíaca a a ergometria de bicicleta submaximal mostrou ser equivalente à observada com carvedilol de libertação imediata no estado estacionário em indivíduos adultos com hipertensao.
Em indivíduos hipertensos com função renal normal, as doses terapêuticas de carvedilol diminuíram a resistência vascular renal, sem alteração da taxa de filtração glomerular ou do fluxo plasmático renal. Alterações na excreção de sódio, potássio, ácido úrico e fósforo em doentes hipertensos com a função renal normal foi semelhante após o carvedilol e o placebo.
O Carvedilol tem pouco efeito nas catecolaminas de plasma., aldosterona plasmática, ou níveis electrolíticos, mas reduz significativamente actividade da renina plasmática durante pelo menos 4 semanas. Também aumenta os níveis de peptídeo atriurético natriurético.

Absorcao
O Carvedilol é rápida e extensivamente absorvido após administração oral dos comprimidos de carvedilol de libertação imediata, com uma dose biodisponibilidade de aproximadamente 25% a 35% devido a um grau significativo de metabolismo de primeira passagem. COREG CR cápsulas de libertação prolongada têm aproximadamente 85% da biodisponibilidade dos comprimidos de carvedilol de libertação imediata. Para as dosagens correspondentes, a exposição (AUC, Cmax, concentração mínima) de carvedilol sob a forma de COREG CR de libertação prolongada as cápsulas são equivalentes às dos comprimidos de carvedilol de libertação imediata quando ambos são administrados com alimentos. A absorção de carvedilol a partir de COREG CR é mais lento e mais prolongado em comparação com o comprimido de carvedilol de libertação imediata com concentrações máximas atingidas aproximadamente 5 horas após a administração. As concentrações plasmáticas de carvedilol aumentam de forma proporcional à dose durante o tratamento. o intervalo posológico de COREG CR 10 a 80 mg. Assunto interno e entre assuntos a variabilidade da AUC e Cmax é semelhante para COREG CR e libertação imediata carvedilol
Efeito dos alimentos: Administração de COREG CR com a a refeição rica em gorduras resultou em aumentos (~20%) da AUC e Cmax em comparação com COREG CR administrado com uma refeição padrão. Diminuição da AUC (27%) e Cmax (43%) observou-se quando COREG CR foi administrado em jejum em comparação com administração após uma refeição padrão. COREG CR deve ser tomado com alimentos.
Num ensaio com indivíduos adultos, aspergir o conteúdo da cápsula COREG CR em puré de maçã não pareceu ter uma efeito na exposição global (AUC) em comparação com a administração do fármaco intacto cápsula após uma refeição padrão, mas resultou numa diminuição na Cmax (18%).
Distribuicao
O Carvedilol liga-se em mais de 98% às proteínas plasmáticas, principalmente com albumina. A ligação às proteínas plasmáticas é independente da concentração no intervalo terapêutico. O Carvedilol é um lipofílico básico. composto com um volume de distribuição no estado estacionário de aproximadamente 115 L, o que indica uma distribuição substancial nos tecidos extravasculares.
Metabolismo e excreção
O Carvedilol é extensivamente metabolizado. Após administração oral administração de carvedilol marcado radioactivamente a voluntários saudáveis, carvedilol foram responsáveis por apenas cerca de 7% da radioactividade total no plasma, tal como medida pelo AUC. Menos de 2% da dose foi excretada inalterada na urina.. Carvedilol é metabolizada principalmente por oxidação de anel aromático e glucuronidação.. O os metabolitos oxidativos são ainda metabolizados por conjugação via glucuronidação e sulfação. Os metabolitos de carvedilol são excretados principalmente através da bílis nas fezes. Desmetilação e hidroxilação no o anel fenol produz 3 metabolitos activos com actividade bloqueadora dos receptores β. Com base em estudos pré-clínicos, o metabolito 4'-hidroxifenilo é aproximadamente 13 vezes mais potente do que o carvedilol para o β-bloqueio
Em comparação com o carvedilol, os 3 metabolitos activos prova fraca actividade vasodilatadora. Concentrações plasmáticas da substância activa os metabolitos são cerca de um décimo dos observados para o carvedilol e têm farmacocinética semelhante à do progenitor.
O Carvedilol passa por uma primeira passagem estereosselectiva metabolismo com níveis plasmáticos de R( )-carvedilol aproximadamente 2 a 3 vezes superior a S(-)-carvedilol após administração oral de COREG CR em sujeitos saudáveis. A depuração aparente é de 90 L por h e 213 L por h para R( )- E S ( - ) - carvedilol, respectivamente.
As principais enzimas P450 responsáveis pelo metabolismo tanto o R( ) como o S(-)-carvedilol em microssomas hepáticos humanos foram CYP2D6 e CYP2C9 e em menor extensão CYP3A4, 2C19, 1A2 e 2E1. Pensa-se que o CYP2D6 ser a principal enzima na 4' - e 5 ' -hidroxilação do carvedilol, com uma contribuição potencial da 3A4. Pensa-se que o CYP2C9 tem uma importância primária na Via de o-metilação do S ( - ) - carvedilol.
O Carvedilol está sujeito aos efeitos da genética. polimorfismo com metabolizadores fracos de debrisoquina (um marcador para o citocromo P450 2D6) exibindo concentrações plasmáticas 2 a 3 vezes mais elevadas do que as do P450 2D6. R () - carvedilol comparado com metabolizadores extensos. Em contraste, o plasma os níveis de S (-) - carvedilol são aumentados apenas cerca de 20% a 25% nos pobres metabolizadores, indicando que este enantiómero é metabolizado em menor extensão por citocromo P450 2D6 than R () - carvedilol. A farmacocinética do carvedilol do não parecem ser diferentes nos metabolizadores fracos da S-mefenitoína (doentes deficiência no citocromo P450 2C19).

Outubro de 2015

-

-


