



Komposition:
Wird bei der Behandlung verwendet:
Medizinisch geprüft von Kovalenko Svetlana Olegovna, Apotheke Zuletzt aktualisiert am 27.03.2022

Achtung! Die Informationen auf der Seite sind nur für medizinisches Fachpersonal! Die Informationen werden in öffentlichen Quellen gesammelt und können aussagekräftige Fehler enthalten! Seien Sie vorsichtig und überprüfen Sie alle Informationen auf dieser Seite!
Top 20 Medikamente mit den gleichen Inhaltsstoffen:


Dosierungsformen und Stärken
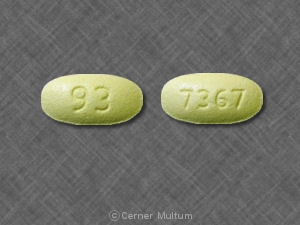
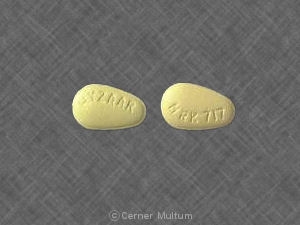
- HYZAAR 50 / 12.5 sind gelbe, ovale, filmbeschichtete Tabletten mit Code 717 auf einer Seite.
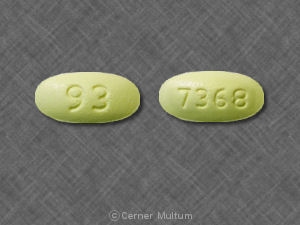
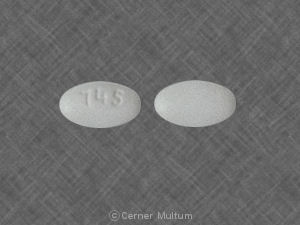
- HYZAAR 100 / 12.5 sind weiße, ovale, filmbeschichtete Tabletten mit Code 745 auf einer Seite.
- HYZAAR 100/25 sind hellgelb, oval, filmbeschichtet Tabletten mit dem Code 747 auf einer Seite.
Lagerung und Handhabung
HYZAAR wird als filmbeschichtete Tablette geliefert.
| Losartan / Hydrochlorothiazid | Farbe | Form | Gravur | NDC 0006-xxxx-xx | ||
| Flasche / 30 | Flasche / 90 | Flasche / 1000 | ||||
| 50 / 12,5 mg | gelb | oval | 717 | 0717-31 | 0717-54 | 0717-82 |
| 100 / 12,5 mg | weiß | oval | 745 | 0745-31 | 0745-54 | 0745-82 |
| 100/25 mg | hellgelb | oval | 747 | 0747-31 | 0747-54 | n / a |
Bei 25 ° C lagern; Ausflüge bis 15-30 ° C (59-86 ° F) erlaubt. Behälter fest verschlossen halten. Vor Licht schützen.
Hergestellt für: Merck Sharp & Dohme Corp., ein Tochtergesellschaft von MERCK & CO., INC., Whitehouse Station, NJ 08889, USA . Überarbeitet: Dezember 2015

Hypertonie
HYZAAR® ist angezeigt zur Behandlung von Bluthochdruck, um den Blutdruck zu senken. Blut senken Druck senkt das Risiko tödlicher und nicht tödlicher kardiovaskulärer Ereignisse (CV) hauptsächlich Schlaganfälle und Myokardinfarkt. Diese Vorteile wurden in gesehen kontrollierte Studien mit blutdrucksenkenden Arzneimitteln aus einer Vielzahl von pharmakologische Klassen einschließlich Losartan und Hydrochlorothiazid.
Kontrolle des Bluthochdrucks sollte Teil eines umfassenden kardiovaskulären Risikomanagements sein, einschließlich as geeignete Lipidkontrolle, Diabetesmanagement, antithrombotische Therapie, Raucherentwöhnung, Bewegung und begrenzte Natriumaufnahme. Viele Patienten werden Benötigen Sie mehr als 1 Medikament, um Blutdruckziele zu erreichen. Für spezifische Beratung zu Zielen und Management siehe veröffentlichte Richtlinien, wie die der Gemeinsames nationales Komitee des Nationalen Programms für Hochblutdruckbildung am Prävention, Erkennung, Bewertung und Behandlung von Bluthochdruck (JNC).
Zahlreiche blutdrucksenkende Mittel Medikamente aus verschiedenen pharmakologischen Klassen und mit unterschiedlichen Mechanismen von In randomisierten kontrollierten Studien wurde gezeigt, dass Maßnahmen reduziert werden kardiovaskuläre Morbidität und Mortalität, und es kann geschlossen werden, dass dies der Fall ist Blutdrucksenkung und keine andere pharmakologische Eigenschaft der Drogen, die maßgeblich für diese Vorteile verantwortlich sind. Der größte und der größte Ein konsistenter kardiovaskulärer Ergebnisvorteil war eine Verringerung des Risikos von Schlaganfall, aber Verringerung des Myokardinfarkts und der kardiovaskulären Mortalität wurden auch regelmäßig gesehen.
Erhöht systolisch oder diastolisch Druck verursacht ein erhöhtes kardiovaskuläres Risiko und den absoluten Risikoanstieg pro mmHg ist bei höheren Blutdrucken größer, so dass auch bescheidene Reduzierungen auftreten von schwerer Hypertonie kann einen erheblichen Nutzen bringen. Relative Risikominderung Die Blutdrucksenkung ist in verschiedenen Populationen ähnlich absolutes Risiko, daher ist der absolute Nutzen bei Patienten mit höherem Risiko größer Risiko unabhängig von ihrer Hypertonie (z. B. Patienten mit Diabetes oder Hyperlipidämie), und von solchen Patienten wird erwartet, dass sie von mehr profitieren aggressive Behandlung eines niedrigeren Blutdruckziels.
Einige blutdrucksenkende Medikamente bei schwarzen Patienten kleinere Blutdruckeffekte (als Monotherapie) haben und Viele blutdrucksenkende Medikamente haben zusätzliche zugelassene Indikationen und Wirkungen (z.B.bei Angina, Herzinsuffizienz oder diabetischer Nierenerkrankung). Diese Überlegungen können die Auswahl der Therapie leiten.
Diese Kombination mit fester Dosis ist nicht für die anfängliche Therapie der Hypertonie angezeigt, außer wenn die Hypertonie ist so schwerwiegend, dass der Wert einer sofortigen Blutdruckkontrolle übersteigt das Risiko, bei diesen Patienten eine Kombinationstherapie einzuleiten.
HYZAAR kann verabreicht werden mit andere blutdrucksenkende Mittel.
Hypertensive Patienten mit Links Ventrikuläre Hypertrophie
HYZAAR soll reduzieren das Schlaganfallrisiko bei Patienten mit Bluthochdruck und linksventrikulär Hypertrophie, aber es gibt Hinweise darauf, dass dieser Vorteil nicht für Schwarz gilt Patienten.

Hypertonie
Die übliche Anfangsdosis von HYZAAR beträgt 50 / 12,5 (Losartan 50) mg / Hydrochlorothiazid 12,5 mg) einmal täglich. Die Dosierung kann nach 3 erhöht werden Wochen Therapie bis maximal 100/25 (Losartan 100 mg / Hydrochlorothiazid 25 mg) einmal täglich nach Bedarf zur Kontrolle des Blutdrucks.
Initiieren Sie einen Patienten, dessen Blutdruck nicht ausreichend ist einmal täglich mit Losartan 50 mg Monotherapie mit HYZAAR 50 / 12.5 kontrolliert. Wenn Der Blutdruck bleibt nach etwa 3 Wochen Therapie, der Dosierung, unkontrolliert kann einmal täglich auf zwei Tabletten HYZAAR 50 / 12.5 oder eine Tablette erhöht werden HYZAAR 100/25 einmal täglich.
Initiieren Sie einen Patienten, dessen Blutdruck nicht ausreichend ist kontrolliert mit Losartan 100 mg Monotherapie mit HYZAAR 100 / 12,5 (Losartan 100 mg / Hydrochlorothiazid 12,5 mg) einmal täglich. Wenn der Blutdruck bleibt Erhöhen Sie die Dosis nach etwa 3 Wochen Therapie unkontrolliert auf zwei Tabletten von HYZAAR 50 / 12.5 einmal täglich oder eine Tablette von HYZAAR 100/25 einmal täglich.
Initiieren Sie einen Patienten, dessen Blutdruck unzureichend ist einmal täglich mit Hydrochlorothiazid 25 mg kontrolliert werden oder wird kontrolliert, aber wer tritt mit diesem Regime einmal täglich eine Hypokaliämie auf HYZAAR 50 / 12.5 auf Reduzierung der Hydrochlorothiazid-Dosis, ohne den erwarteten Gesamtwert zu verringern blutdrucksenkende Reaktion. Bewerten Sie das klinische Ansprechen auf HYZAAR 50 / 12.5 und wenn der Blutdruck nach etwa 3 Wochen Therapie unkontrolliert bleibt, Erhöhen Sie die Dosis einmal täglich auf zwei Tabletten HYZAAR 50 / 12.5 oder eine Tablette davon HYZAAR 100/25 einmal täglich.
Hypertensive Patienten mit linksventrikulärer Hypertrophie
Bei Patienten, deren Blutdruck nicht ausreichend ist kontrolliert auf 50 mg Losartan-Kalium, Behandlung mit HYZAAR 50 / 12.5 einleiten. Wenn eine zusätzliche Blutdrucksenkung erforderlich ist, erhöhen Sie die Dosis auf HYZAAR 100 / 12,5, gefolgt von HYZAAR 100/25. Für weitere Blutdrucksenkungen hinzufügen andere blutdrucksenkende Mittel.

HYZAAR ist kontraindiziert:
- Bei Patienten, die überempfindlich gegen eine Komponente von sind dieses Produkt.
- Bei Patienten mit Anurie
- Zur gleichzeitigen Anwendung mit Aliskiren bei Patienten mit Diabetes

WARNHINWEISE
Im Rahmen der enthalten VORSICHTSMASSNAHMEN Sektion.
VORSICHTSMASSNAHMEN
Fetale Toxizität
Verwendung von Medikamenten, die auf das Renin-Angiotensin-System wirken während des zweiten und dritten Schwangerschaftstrimesters reduziert die fetale Niere Funktion und erhöht die Morbidität und den Tod des Fötus und des Neugeborenen. Resultierend Oligohydramnios können mit fetaler Lungenhypoplasie und Skelett assoziiert sein Verformungen. Mögliche Nebenwirkungen bei Neugeborenen sind Schädelhypoplasien Anurie, Hypotonie, Nierenversagen und Tod. Wenn eine Schwangerschaft festgestellt wird, Stellen Sie HYZAAR so schnell wie möglich ein.
Thiazide überqueren die Plazentaschranke und erscheinen in der Schnur Blut. Nebenwirkungen sind fetale oder neonatale Gelbsucht, Thrombozytopenie.
Hypotonie bei Patienten mit Volumen- oder Salzmangel
Bei Patienten mit aktiviertem Renin-Angiotensin-System wie Patienten mit Volumen- oder Salzmangel (z., diejenigen, die mit hohen behandelt werden Dosen von Diuretika), symptomatische Hypotonie kann nach Beginn von auftreten Behandlung mit HYZAAR. Korrigieren Sie das Volumen oder den Salzmangel vor der Verabreichung von HYZAAR. Verwenden Sie HYZAAR nicht als Ersttherapie bei Patienten mit intravaskulärer Behandlung Volumenverarmung.
Beeinträchtigte Nierenfunktion
Veränderungen der Nierenfunktion einschließlich akutem Nierenversagen kann durch Medikamente verursacht werden, die das Reninangiotensin-System hemmen, und durch Diuretika. Patienten, deren Nierenfunktion teilweise von der Aktivität der Renin-Angiotensin-System (z.Patienten mit chronischer Nierenarterienstenose Nierenerkrankungen, schwere Herzinsuffizienz oder Volumenverarmung können auftreten besonderes Risiko für akutes Nierenversagen bei HYZAAR. Nieren überwachen Funktionieren Sie bei diesen Patienten regelmäßig. Erwägen Sie das Zurückhalten oder Absetzen Therapie bei Patienten, die eine klinisch signifikante Abnahme der Niere entwickeln Funktion auf HYZAAR .
Überempfindlichkeit
Überempfindlichkeitsreaktionen auf Hydrochlorothiazid können treten bei Patienten mit oder ohne Allergie oder Asthma bronchiale in der Vorgeschichte auf, jedoch sind wahrscheinlicher bei Patienten mit einer solchen Vorgeschichte.
Elektrolyt- und Stoffwechseleffekte
In doppelblinden klinischen Studien mit verschiedenen Dosen von Losartan-Kalium und Hydrochlorothiazid, die Inzidenz von Hypertensiv Patienten, die eine Hypokaliämie (Serumkalium <3,5 mÄq / l) entwickelten, betrugen 6,7% gegenüber 3,5% für Placebo; die Inzidenz von Hyperkaliämie (Serumkalium> 5,7 mEq / L) betrug 0,4% gegenüber 0% für Placebo.
HYZAAR enthält Hydrochlorothiazid, das verursachen kann Hypokaliämie, Hyponatriämie und Hypomagnesiämie. Hypomagnesiämie kann dazu führen Hypokaliämie, die trotz Kaliumrepletion möglicherweise schwer zu behandeln ist. HYZAAR enthält auch Losartan, das Hyperkaliämie verursachen kann. Serumelektrolyte überwachen regelmäßig.
Hydrochlorothiazid kann die Glukosetoleranz verändern und erhöhen Serumspiegel von Cholesterin und Triglyceriden.
Eine Hyperurikämie kann auftreten oder eine offene Gicht kann ausgefällt werden bei Patienten, die eine Thiazidtherapie erhalten. Weil Losartan Harnsäure senkt Losartan in Kombination mit Hydrochlorothiazid schwächt das Diuretikum-induzierte Hyperurikämie.
Hydrochlorothiazid verringert die Calciumausscheidung im Urin und kann Erhöhungen des Serumcalciums verursachen. Kalziumspiegel überwachen.
Akute Myopie und Glaukom zur Schließung des Sekundärwinkels
Hydrochlorothiazid, ein Sulfonamid, kann eine verursachen eigenwillige Reaktion, die zu akuter vorübergehender Myopie und akuter Wirkung führt Winkelschlussglaukom. Zu den Symptomen gehört das akute Auftreten einer verminderten Sehschärfe oder Augenschmerzen und treten typischerweise innerhalb von Stunden bis Wochen nach der Einleitung des Arzneimittels auf. Unbehandeltes Glaukom mit akuter Winkelschließung kann zu einem dauerhaften Sehverlust führen. Das Die Hauptbehandlung besteht darin, Hydrochlorothiazid so schnell wie möglich abzusetzen. Bei intraokularen Behandlungen müssen möglicherweise schnelle medizinische oder chirurgische Behandlungen in Betracht gezogen werden Druck bleibt unkontrolliert. Risikofaktoren für die Entwicklung einer akuten Winkelschließung Das Glaukom kann eine Sulfonamid- oder Penicillinallergie in der Vorgeschichte enthalten.
Systemischer Lupus Erythematodes
Es wurde berichtet, dass Thiaziddiuretika verursachen Verschlimmerung oder Aktivierung des systemischen Lupus erythematodes.
Postsympathektomie-Patienten
Die blutdrucksenkende Wirkung des Arzneimittels kann verstärkt werden bei der Postsympathektomie-Patientin.
Informationen zur Patientenberatung
Weisen Sie den Patienten an, den von der FDA zugelassenen Patienten zu lesen Kennzeichnung (PATIENTE INFORMATIONEN).
Schwangerschaft
Beraten Sie Patientinnen von der Geburt Alter über die Folgen der Exposition gegenüber HYZAAR während der Schwangerschaft. Diskutieren Behandlungsoptionen mit Frauen, die eine Schwangerschaft planen. Sagen Sie es den Patienten Melden Sie Schwangerschaften so schnell wie möglich ihren Ärzten.
Symptomatische Hypotonie
Beraten Sie die Patienten darüber Benommenheit kann auftreten, insbesondere in den ersten Tagen der Therapie, und zu Melden Sie dieses Symptom einem Gesundheitsdienstleister. Informieren Sie die Patienten über Dehydration durch unzureichende Flüssigkeitsaufnahme, übermäßigen Schweiß, Erbrechen oder Durchfall zu einem übermäßigen Blutdruckabfall führen. Wenn eine Synkope auftritt, raten Sie den Patienten ihren Gesundheitsdienstleister zu kontaktieren.
Kaliumzusätze
Weisen Sie die Patienten darauf hin, nicht zu verwenden Kaliumpräparate oder kaliumhaltige Salzersatzstoffe ohne Beratung ihres Gesundheitsdienstleisters.
Akute Myopie und Glaukom zur Schließung des Sekundärwinkels
Weisen Sie die Patienten an, HYZAAR abzusetzen, und suchen Sie sofort einen Arzt auf, wenn Es treten Symptome einer akuten Myopie oder eines Glaukoms mit sekundärem Winkelverschluss auf.
Nichtklinische Toxikologie
Karzinogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
Losartan-Kaliumhydrochlorothiazid
Mit dem wurden keine Kanzerogenitätsstudien durchgeführt Losartan-Kaliumhydrochlorothiazid-Kombination.
Losartan-Kaliumhydrochlorothiazid beim Testen an einem Gewichtsverhältnis von 4: 1, war im Ames-Mikrobiellen Mutagenese-Assay negativ und der V-79 China Hamster Lungenzellmutagenese Assay. Außerdem gab es keine Hinweise auf direkte Genotoxizität in der in vitro alkalischer Elutionstest bei Ratten Hepatozyten und in vitro Chromosomenaberrationstest im Eierstock des chinesischen Hamsters Zellen in nichtzytotoxischen Konzentrationen.
Losartan-Kalium, zusammen mit Hydrochlorothiazid hatte keinen Einfluss auf die Fruchtbarkeit oder das Paarungsverhalten des Mannes Ratten in Dosierungen von bis zu 135 mg / kg / Tag Losartan und 33,75 mg / kg / Tag von Hydrochlorothiazid. Es wurde gezeigt, dass diese Dosierungen jeweils liefern systemische Exposition (AUCs) für Losartan, seinen aktiven Metaboliten und Hydrochlorothiazid, die ungefähr 60-, 60- und 30-mal höher sind als diejenigen, die beim Menschen mit 100 mg Losartan-Kalium in Kombination mit erreicht werden 25 mg Hydrochlorothiazid. Bei weiblichen Ratten jedoch die gleichzeitige Anwendung von Dosen von nur 10 mg / kg / Tag Losartan und 2,5 mg / kg / Tag von Hydrochlorothiazid war mit einem leichten, aber statistisch signifikanten assoziiert Abnahme der Fruchtbarkeits- und Fruchtbarkeitsindizes. AUC-Werte für Losartan, es ist aktiver Metabolit und Hydrochlorothiazid, extrapoliert aus Daten, die mit erhalten wurden Losartan, das Ratten in einer Dosis von 50 mg / kg / Tag in Kombination mit verabreicht wurde 12,5 mg / kg / Tag Hydrochlorothiazid waren ungefähr 6, 2 und 2 Mal größer als diejenigen, die beim Menschen mit 100 mg Losartan in Kombination erreicht wurden mit 25 mg Hydrochlorothiazid.
Losartan Kalium
Losartan-Kalium war bei Verabreichung nicht krebserregend bei maximal tolerierten Dosierungen für Ratten und Mäuse für 105 und 92 Wochen beziehungsweise. Weibliche Ratten, denen die höchste Dosis (270 mg / kg / Tag) verabreicht wurde, hatten eine leichte höhere Inzidenz von Pankreas-Azinar-Adenomen. Die maximal tolerierten Dosierungen (270 mg / kg / Tag bei Ratten, 200 mg / kg / Tag bei Mäusen) lieferten systemische Expositionen für Losartan und sein pharmakologisch aktiver Metabolit, die ungefähr waren 160- und 90-mal (Ratten) und 30- und 15-mal (mäuse) die Exposition von 50 kg Mensch 100 mg pro Tag gegeben.
Losartan-Kalium war im Mikrobiellen negativ Mutagenese- und V-79-Mutagenese-Assays für Säugetierzellen und in der in vitro alkalisch elution und in vitro und in vivo Chromosomenaberrationstests. Zusätzlich, Der aktive Metabolit zeigte keine Hinweise auf Genotoxizität im mikrobiellen Mittel Mutagenese, in vitro alkalische Elution und in vitro Chromosomenaberration Assays.
Fruchtbarkeit und Reproduktionsleistung waren nicht betroffen in Studien mit männlichen Ratten, denen orale Dosen von Losartan-Kalium bis zu verabreicht wurden ca. 150 mg / kg / Tag. Die Verabreichung toxischer Dosierungen in Frauen (300/200 mg / kg / Tag) waren mit einem signifikanten assoziiert (p <0,05) Abnahme der Anzahl der Corpora lutea / weiblich, Implantate / weiblich und leben Feten / Frauen im Kaiserschnitt. Bei 100 mg / kg / Tag nur eine Abnahme der Anzahl von Corpora lutea / weiblich wurde beobachtet. Das Verhältnis dieser Ergebnisse zu Die medikamentöse Behandlung ist ungewiss, da bei diesen Dosierungen keine Wirkung auf diese aufgetreten ist Implantate / schwangere Frau, Prozent nach Implantationsverlust oder leben Tiere / Wurf bei Geburt. Bei nicht schwangeren Ratten wurde 7 mg / kg / Tag verabreicht Tage waren systemische Exposition (AUCs) für Losartan und seinen aktiven Metaboliten maximal das 66- und 26-fache der beim Menschen erreichten Exposition empfohlene Tagesdosis beim Menschen (100 mg).
Hydrochlorothiazid
Zweijährige Fütterungsstudien an Mäusen und Ratten, die unter durchgeführt wurden Die Schirmherrschaft des National Toxicology Program (NTP) ergab keine Beweise dafür ein krebserzeugendes Potenzial von Hydrochlorothiazid bei weiblichen Mäusen (in Dosen von bis bis ungefähr 600 mg / kg / Tag) oder bei männlichen und weiblichen Ratten (in Dosen von bis zu ca. 100 mg / kg / Tag). Das NTP fand jedoch zweideutige Beweise dafür Hepatokarzinogenität bei männlichen Mäusen.
Hydrochlorothiazid war nicht genotoxisch in vitro in der Ames-Mutagenitätstest von Salmonella typhimurium-Stämmen TA 98, TA 100, TA 1535, TA 1537 und TA 1538 und im chinesischen Hamster-Ovarialtest (CHO) für Chromosomenaberrationen oder in vivo in Assays mit Mauskeimzelle Chromosomen, Knochenmarkchromosomen des chinesischen Hamsters und die Drosophila-Geschlechtskraw rezessives tödliches Merkmalgen. Positive Testergebnisse wurden nur im in erhalten vitro CHO Schwester Chromatid Exchange (Klastogenität) und im Mauslymphom Zelltests (Mutagenität) unter Verwendung von Hydrochlorothiazidkonzentrationen von 43 bis 1300 mcg / ml und im Aspergillus nidulans Nicht-Disjunktions-Assay an einem nicht spezifizierte Konzentration.
Hydrochlorothiazid hatte keine nachteiligen Auswirkungen auf die Fruchtbarkeit von Mäusen und Ratten beiderlei Geschlechts in Studien, in denen sich diese Arten befanden über ihre Ernährung zuvor Dosen von bis zu 100 bzw. 4 mg / kg ausgesetzt zu paaren und während der Schwangerschaft.
Verwendung in bestimmten Populationen
Schwangerschaft
Schwangerschaftskategorie D
Verwendung von Medikamenten, die auf das Renin-Angiotensin-System wirken während des zweiten und dritten Schwangerschaftstrimesters reduziert die fetale Niere Funktion und erhöht die Morbidität und den Tod des Fötus und des Neugeborenen. Resultierend Oligohydramnios können mit fetaler Lungenhypoplasie und Skelett assoziiert sein Verformungen. Mögliche Nebenwirkungen bei Neugeborenen sind Schädelhypoplasien Anurie, Hypotonie, Nierenversagen und Tod. Wenn eine Schwangerschaft festgestellt wird, Losartan so schnell wie möglich absetzen. Diese nachteiligen Ergebnisse sind normalerweise verbunden mit der Verwendung dieser Medikamente im zweiten und dritten Trimester der Schwangerschaft. Die meisten epidemiologische Studien, in denen fetale Anomalien nach Exposition untersucht wurden blutdrucksenkender Gebrauch im ersten Trimester hat keine Medikamente unterschieden Beeinflussung des Renin-Angiotensin-Systems durch andere blutdrucksenkende Mittel. Eine angemessene Behandlung der mütterlichen Hypertonie während der Schwangerschaft ist wichtig Ergebnisse für Mutter und Fötus zu optimieren.
In dem ungewöhnlichen Fall, dass es keine angemessene gibt Alternative zur Therapie mit Arzneimitteln, die das Reninangiotensin-System für a beeinflussen Bei einem bestimmten Patienten sollten Sie die Mutter über das potenzielle Risiko für den Fötus informieren. Führen Sie serielle Ultraschalluntersuchungen durch, um das Intraamniotikum zu bewerten Umgebung. Wenn Oligohydramnios beobachtet werden, setzen Sie HYZAAR ab, es sei denn, dies ist der Fall als lebensrettend für die Mutter angesehen. Fetale Tests können angemessen sein, basierend in der Woche der Schwangerschaft. Patienten und Ärzte sollten sich jedoch bewusst sein dass Oligohydramnios möglicherweise erst nach dem Anhalten des Fötus auftreten irreversible Verletzung. Beobachten Sie Säuglinge mit einer Vorgeschichte von Uterusexposition genau an HYZAAR für Hypotonie, Oligurie und Hyperkaliämie.
Es gab keine Hinweise auf Teratogenität bei Ratten oder Kaninchen, die mit einer maximalen Losartan-Kaliumdosis von 10 mg / kg / Tag in behandelt wurden Kombination mit 2,5 mg / kg / Tag Hydrochlorothiazid. Bei diesen Dosierungen jeweilige Exposition (AUCs) von Losartan, seinem aktiven Metaboliten und Hydrochlorothiazid bei Kaninchen waren ungefähr 5-, 1,5- und 1,0-mal so viel wie beim Menschen mit 100 mg Losartan in Kombination mit 25 mg Hydrochlorothiazid. AUC-Werte für Losartan sein aktiver Metabolit und Hydrochlorothiazid, extrapoliert aus Daten, die mit Losartan erhalten wurden, das Ratten in einer Dosis von 50 mg / kg / Tag in verabreicht wurde Kombination mit 12,5 mg / kg / Tag Hydrochlorothiazid betrug ungefähr 6, 2- und 2-mal höher als beim Menschen mit 100 mg Losartan in Kombination mit 25 mg Hydrochlorothiazid. Fetale Toxizität bei Ratten als nachgewiesen durch einen leichten Anstieg der überzähligen Rippen, wurde bei Frauen beobachtet wurden vor und während der Schwangerschaft mit 10 mg / kg / Tag Losartan in behandelt Kombination mit 2,5 mg / kg / Tag Hydrochlorothiazid. Wie auch in Studien beobachtet mit Losartan allein, nachteiligen fetalen und neonatalen Wirkungen, einschließlich verringert Körpergewicht, Nierentoxizität und Mortalität traten auf, wenn trächtige Ratten waren während der späten Schwangerschaft und / oder Stillzeit mit 50 mg / kg / Tag Losartan in behandelt Kombination mit 12,5 mg / kg / Tag Hydrochlorothiazid. Entsprechende AUCs für Losartan, sein aktiver Metabolit und Hydrochlorothiazid bei diesen Dosierungen in Ratten waren ungefähr 35-, 10- und 10-mal höher als die in erreichten Menschen mit der Verabreichung von 100 mg Losartan in Kombination mit 25 mg Hydrochlorothiazid. Bei Verabreichung von Hydrochlorothiazid ohne Losartan an trächtige Mäuse und Ratten während ihrer jeweiligen Hauptperioden Organogenese in Dosen von bis zu 3000 bzw. 1000 mg / kg / Tag Keine Hinweise auf eine Schädigung des Fötus.
Thiazide überqueren die Plazentaschranke und erscheinen in der Schnur Blut. Es besteht die Gefahr von fetalem oder neonatalem Gelbsucht, Thrombozytopenie und möglicherweise andere Nebenwirkungen, die bei Erwachsenen aufgetreten sind.
Stillende Mütter
Es ist nicht bekannt, ob Losartan beim Menschen ausgeschieden wird Milch, aber signifikante Mengen an Losartan und seinem aktiven Metaboliten wurden gezeigt in Rattenmilch präsent sein. Thiazide erscheinen in der Muttermilch. Wegen der Möglicherweise für nachteilige Auswirkungen auf das stillende Kind sollte eine Entscheidung getroffen werden ob die Pflege abgebrochen oder das Medikament unter Berücksichtigung des Medikaments abgesetzt werden soll Bedeutung der Droge für die Mutter.
Pädiatrische Anwendung
Sicherheit und Wirksamkeit von HYZAAR bei pädiatrischen Patienten wurden nicht gegründet.
Neugeborene mit einer Uterusexposition in der Vorgeschichte von HYZAAR: Wenn Oligurie oder Hypotonie auftritt, direkte Aufmerksamkeit für die Unterstützung des Blutes Druck und Nierenperfusion. Möglicherweise ist eine Austauschtransfusion oder Dialyse erforderlich als Mittel zur Umkehrung der Hypotonie und / oder zum Ersatz einer gestörten Niere Funktion.
Geriatrische Anwendung
In einer kontrollierten klinischen Studie zur Reduktion der kombiniertes Risiko für kardiovaskulären Tod, Schlaganfall und Myokardinfarkt hypertensive Patienten mit linksventrikulärer Hypertrophie, 2857 Patienten (62%) waren 65 Jahre und älter, während 808 Patienten (18%) 75 Jahre und älter waren. In einem In dieser Studie wurden die Patienten zusammen verabreicht, um den Blutdruck zu kontrollieren Losartan und Hydrochlorothiazid 74% der Gesamtzeit, in der sie ein Studienmedikament erhielten. Zwischen diesen Patienten wurden keine allgemeinen Unterschiede in der Wirksamkeit beobachtet und jüngere Patienten. Unerwünschte Ereignisse waren bei älteren Menschen etwas häufiger im Vergleich zu nicht älteren Patienten sowohl für das Losartanhydrochlorothiazid als auch für die Kontrollgruppen.
Rennen
In der Losartan Intervention für Endpunktreduzierung in Hypertonie-Studie (LIFE), Schwarze Patienten mit Hypertonie und links Mit Atenolol behandelte ventrikuläre Hypertrophie hatte ein geringeres Schlaganfallrisiko primärer zusammengesetzter Endpunkt im Vergleich zu schwarzen Patienten, die mit behandelt wurden Losartan (beide mit Hydrochlorothiazid bei der Mehrzahl der Patienten behandelt). In der Untergruppe der schwarzen Patienten (n = 533, 6% der Patienten der LIFE-Studie) dort waren 29 primäre Endpunkte unter 263 Patienten unter Atenolol (11%, 26 pro 1000) Patientenjahre) und 46 primäre Endpunkte bei 270 Patienten (17%, 42 pro 1000) Patientenjahre) auf Losartan. Dieser Befund konnte nicht auf der Grundlage von erklärt werden Unterschiede in der Bevölkerung außer der Rasse oder bei Ungleichgewichten zwischen Behandlungsgruppen. Zusätzlich Blutdrucksenkungen in beiden Behandlungen Gruppen waren konsistent zwischen schwarzen und nicht schwarzen Patienten. Gegeben die Schwierigkeiten bei der Interpretation von Untersetzungsunterschieden in großen Versuchen können es nicht sein bekannt, ob der beobachtete Unterschied das Ergebnis des Zufalls ist. Das Die LIFE-Studie liefert keine Hinweise darauf, dass die Vorteile von Losartan bei der Reduzierung der Risiko von kardiovaskulären Ereignissen bei hypertensiven Patienten mit linksventrikulärem Licht Hypertrophie gilt für schwarze Patienten.
Leberfunktionsstörung
Die Einleitung von HYZAAR wird bei Patienten mit nicht empfohlen Leberfunktionsstörung, da die geeignete Anfangsdosis von Losartan (25 mg) beträgt nicht verfügbar.
Nierenfunktionsstörung
Veränderungen der Nierenfunktion wurden in berichtet anfällige Personen. Sicherheit und Wirksamkeit von HYZAAR bei Patienten mit schwerer Nierenfunktionsstörung (Kreatin-Clearance <30) ml / min) wurden nicht eingerichtet.

Hydrochlorothiazid
Alkohol, Barbiturate oder Betäubungsmittel - Potenzierung einer orthostatischen Hypotonie kann auftreten.
Andere blutdrucksenkende Medikamente - additive Wirkung oder Potenzierung.
Skelettmuskelrelaxantien, nicht depolarisierend (z., Tubocurarin) - mögliche erhöhte Reaktionsfähigkeit auf das Muskelrelaxans.
Kortikosteroide, ACTH oder Glycyrrhizin (gefunden in Lakritz) - verstärkte Elektrolytverarmung, insbesondere Hypokaliämie.
Pressoramine (z., Noradrenalin) - möglich verminderte Reaktion auf Druckamine, aber nicht ausreichend, um ihre Verwendung auszuschließen.

Schwangerschaftskategorie D
Verwendung von Medikamenten, die auf das Renin-Angiotensin-System wirken während des zweiten und dritten Schwangerschaftstrimesters reduziert die fetale Niere Funktion und erhöht die Morbidität und den Tod des Fötus und des Neugeborenen. Resultierend Oligohydramnios können mit fetaler Lungenhypoplasie und Skelett assoziiert sein Verformungen. Mögliche Nebenwirkungen bei Neugeborenen sind Schädelhypoplasien Anurie, Hypotonie, Nierenversagen und Tod. Wenn eine Schwangerschaft festgestellt wird, Losartan so schnell wie möglich absetzen. Diese nachteiligen Ergebnisse sind normalerweise verbunden mit der Verwendung dieser Medikamente im zweiten und dritten Trimester der Schwangerschaft. Die meisten epidemiologische Studien, in denen fetale Anomalien nach Exposition untersucht wurden blutdrucksenkender Gebrauch im ersten Trimester hat keine Medikamente unterschieden Beeinflussung des Renin-Angiotensin-Systems durch andere blutdrucksenkende Mittel. Eine angemessene Behandlung der mütterlichen Hypertonie während der Schwangerschaft ist wichtig Ergebnisse für Mutter und Fötus zu optimieren.
In dem ungewöhnlichen Fall, dass es keine angemessene gibt Alternative zur Therapie mit Arzneimitteln, die das Reninangiotensin-System für a beeinflussen Bei einem bestimmten Patienten sollten Sie die Mutter über das potenzielle Risiko für den Fötus informieren. Führen Sie serielle Ultraschalluntersuchungen durch, um das Intraamniotikum zu bewerten Umgebung. Wenn Oligohydramnios beobachtet werden, setzen Sie HYZAAR ab, es sei denn, dies ist der Fall als lebensrettend für die Mutter angesehen. Fetale Tests können angemessen sein, basierend in der Woche der Schwangerschaft. Patienten und Ärzte sollten sich jedoch bewusst sein dass Oligohydramnios möglicherweise erst nach dem Anhalten des Fötus auftreten irreversible Verletzung. Beobachten Sie Säuglinge mit einer Vorgeschichte von Uterusexposition genau an HYZAAR für Hypotonie, Oligurie und Hyperkaliämie.
Es gab keine Hinweise auf Teratogenität bei Ratten oder Kaninchen, die mit einer maximalen Losartan-Kaliumdosis von 10 mg / kg / Tag in behandelt wurden Kombination mit 2,5 mg / kg / Tag Hydrochlorothiazid. Bei diesen Dosierungen jeweilige Exposition (AUCs) von Losartan, seinem aktiven Metaboliten und Hydrochlorothiazid bei Kaninchen waren ungefähr 5-, 1,5- und 1,0-mal so viel wie beim Menschen mit 100 mg Losartan in Kombination mit 25 mg Hydrochlorothiazid. AUC-Werte für Losartan sein aktiver Metabolit und Hydrochlorothiazid, extrapoliert aus Daten, die mit Losartan erhalten wurden, das Ratten in einer Dosis von 50 mg / kg / Tag in verabreicht wurde Kombination mit 12,5 mg / kg / Tag Hydrochlorothiazid betrug ungefähr 6, 2- und 2-mal höher als beim Menschen mit 100 mg Losartan in Kombination mit 25 mg Hydrochlorothiazid. Fetale Toxizität bei Ratten als nachgewiesen durch einen leichten Anstieg der überzähligen Rippen, wurde bei Frauen beobachtet wurden vor und während der Schwangerschaft mit 10 mg / kg / Tag Losartan in behandelt Kombination mit 2,5 mg / kg / Tag Hydrochlorothiazid. Wie auch in Studien beobachtet mit Losartan allein, nachteiligen fetalen und neonatalen Wirkungen, einschließlich verringert Körpergewicht, Nierentoxizität und Mortalität traten auf, wenn trächtige Ratten waren während der späten Schwangerschaft und / oder Stillzeit mit 50 mg / kg / Tag Losartan in behandelt Kombination mit 12,5 mg / kg / Tag Hydrochlorothiazid. Entsprechende AUCs für Losartan, sein aktiver Metabolit und Hydrochlorothiazid bei diesen Dosierungen in Ratten waren ungefähr 35-, 10- und 10-mal höher als die in erreichten Menschen mit der Verabreichung von 100 mg Losartan in Kombination mit 25 mg Hydrochlorothiazid. Bei Verabreichung von Hydrochlorothiazid ohne Losartan an trächtige Mäuse und Ratten während ihrer jeweiligen Hauptperioden Organogenese in Dosen von bis zu 3000 bzw. 1000 mg / kg / Tag Keine Hinweise auf eine Schädigung des Fötus.
Thiazide überqueren die Plazentaschranke und erscheinen in der Schnur Blut. Es besteht die Gefahr von fetalem oder neonatalem Gelbsucht, Thrombozytopenie und möglicherweise andere Nebenwirkungen, die bei Erwachsenen aufgetreten sind.

Erfahrung in klinischen Studien
Weil klinische Studien unter weit verbreitet sind unterschiedliche Bedingungen, in den klinischen Studien von a beobachtete Nebenwirkungsraten Arzneimittel kann nicht direkt mit den Raten in den klinischen Studien eines anderen verglichen werden Medikament und spiegelt möglicherweise nicht die in der Praxis beobachteten Raten wider.
Losartan-Kaliumhydrochlorothiazid wurde bewertet zur Sicherheit bei 858 Patienten, die wegen essentieller Hypertonie behandelt wurden, und 3889 Patienten wegen Bluthochdruck und linksventrikulärer Hypertrophie behandelt. Am nachteiligsten Reaktionen waren milder und vorübergehender Natur und nicht erforderlich Absetzen der Therapie. In kontrollierten klinischen Studien das Absetzen von Eine Therapie aufgrund klinischer unerwünschter Ereignisse war nur in 2,8% und 2,3% von erforderlich Patienten, die mit der Kombination bzw. Placebo behandelt wurden.
In diesen doppelblinden kontrollierten klinischen Studien nachteilig Reaktionen bei mehr als 2% der mit behandelten Probanden Losartan-Hydrochlorothiazid und häufiger als Placebo waren: Rückenschmerzen (2,1% gegenüber 0,6%), Schwindel (5,7% gegenüber 2,9%) und Infektion der oberen Atemwege (6,1%) gegenüber 4,6%). Die folgenden zusätzlichen Nebenwirkungen wurden in berichtet klinische Studien mit HYZAAR und / oder den einzelnen Komponenten:
Störungen des Blut- und Lymphsystems: Anämie, aplastische Anämie, hämolytische Anämie, Leukopenie, Agranulozytose.
Stoffwechsel- und Ernährungsstörungen: Magersucht, Hyperglykämie, Hyperurikämie, Elektrolytungleichgewicht einschließlich Hyponatriämie und Hypokaliämie.
Psychiatrische Störungen: Schlaflosigkeit, Unruhe.
Störungen des Nervensystems: Dysgeusie, Kopfschmerzen Migräne, Parästhesien.
Augenerkrankungen: Xanthopsie, vorübergehend verschwommen Vision.
Herzerkrankungen: Herzklopfen, Tachykardie.
Gefäßerkrankungen: Dosisbezogener Orthostatik Wirkungen, nekrotisierende Angiitis (Vaskulitis, kutane Vaskulitis).
Atemwegserkrankungen, Erkrankungen des Brustraums und des Mediastinums: Nasal Verstopfung, Pharyngitis, Sinusstörung, Atemnot (einschließlich Pneumonitis und Lungenödem).
Magen-Darm-Erkrankungen: Dyspepsie, Bauch Schmerzen, Magenreizungen, Krämpfe, Durchfall, Verstopfung, Übelkeit, Erbrechen, Pankreatitis, Sialoadenitis.
Hepato-Gallenstörungen: Gelbsucht (intrahepatisch cholestatischer Gelbsucht).
Haut- und Unterhautstörungen: Hautausschlag, Juckreiz, Purpura, toxische epidermale Nekrolyse, Urtikaria, Lichtempfindlichkeit, Hautlupus erythematodes.
Erkrankungen des Bewegungsapparates und des Bindegewebes: Muskel Krämpfe, Muskelkrämpfe, Myalgie, Arthralgie.
Nieren- und Harnwegserkrankungen: Glykosurie, Niere Dysfunktion, interstitielle Nephritis, Nierenversagen.
Störungen des Fortpflanzungssystems und der Brust: Erektil Dysfunktion / Impotenz.
Allgemeine Störungen und Bedingungen am Verabreichungsort: Brustschmerzen, Ödeme / Schwellungen, Unwohlsein, Fieber, Schwäche.
Untersuchungen: Leberfunktionsstörungen.
Husten
Anhaltender trockener Husten wurde in Verbindung gebracht Die Verwendung von ACE-Hemmern und in der Praxis kann eine Ursache für die Einstellung von sein ACE-Hemmertherapie. Zwei prospektive, parallele Gruppe, doppelblind, randomisierte, kontrollierte Studien wurden durchgeführt, um die Auswirkungen von Losartan zu bewerten über die Inzidenz von Husten bei hypertensiven Patienten, bei denen Husten aufgetreten war während der ACE-Hemmertherapie. Patienten mit typischem ACE-Hemmer Husten bei Anfechtung mit Lisinopril, dessen Husten unter Placebo verschwand, waren randomisiert auf Losartan 50 mg, Lisinopril 20 mg oder entweder Placebo (eine Studie, n = 97) oder 25 mg Hydrochlorothiazid (n = 135). Die doppelblinde Behandlungsdauer dauerte bis zu 8 Wochen. Die Inzidenz von Husten ist in der folgenden Tabelle 1 dargestellt.
Tabelle 1
| Studie 1 * | HCTZ | Losartan | Lisinopril |
| Husten | 25% | 17% | 69% |
| Studie 2 † | Placebo | Losartan | Lisinopril |
| Husten | 35% | 29% | 62% |
| * Demografie = (89%
Kaukasier, 64% weiblich) † Demografie = (90% Kaukasier, 51% Frauen) |
Diese Studien zeigen das die Häufigkeit von Husten im Zusammenhang mit einer Losartan-Therapie in einer Population, die Alle hatten Husten im Zusammenhang mit einer ACE-Hemmer-Therapie, ist ähnlich verbunden mit Hydrochlorothiazid oder Placebo-Therapie.
Fälle von Husten, einschließlich Bei der Verwendung von Losartan in wurden positive Neuherausforderungen gemeldet Postmarketing-Erfahrung.
Postmarketing-Erfahrung
Die folgenden Nebenwirkungen wurden während der Verwendung von HYZAAR nach der Zulassung identifiziert. Weil diese Reaktionen werden freiwillig von einer Population ungewisser Größe gemeldet nicht immer möglich, ihre Häufigkeit zuverlässig abzuschätzen oder eine Kausal festzustellen Beziehung zur Arzneimittelexposition.
Verdauungsstörungen: Hepatitis war selten bei mit Losartan behandelten Patienten berichtet.
Hämatologisch: Thrombozytopenie.
Überempfindlichkeit: Angioödem, einschließlich Schwellung des Kehlkopfes und der Stimmritze, die eine Verstopfung der Atemwege und / oder eine Schwellung verursacht von Gesicht, Lippen, Rachen und / oder Zunge wurde bei Patienten selten berichtet mit Losartan behandelt; Bei einigen dieser Patienten trat zuvor ein Angioödem auf mit anderen Arzneimitteln einschließlich ACE-Hemmern. Vaskulitis, einschließlich Henoch-Schönlein Purpura wurde mit Losartan berichtet. Anaphylaktische Reaktionen waren gemeldet.
Bewegungsapparat: Rhabdomyolyse
Haut: Erythroderma

Losartan Kalium
Bei Mäusen und Ratten wurde danach eine signifikante Letalität beobachtet orale Verabreichung von 1000 mg / kg bzw. 2000 mg / kg, ca. 44 und 170-fache der empfohlenen Höchstdosis beim Menschen auf mg / m²-Basis.
In Bezug auf Überdosierung in liegen nur begrenzte Daten vor Menschen. Die wahrscheinlichste Manifestation einer Überdosierung wäre Hypotonie und Tachykardie; Bradykardie kann durch parasympathische (vagale) Stimulation auftreten. Sollte eine symptomatische Hypotonie auftreten, sollte eine unterstützende Behandlung erfolgen eingeführt.
Weder Losartan noch sein aktiver Metabolit können entfernt werden durch Hämodialyse.
Hydrochlorothiazid
Die orale LD 50 von Hydrochlorothiazid ist mehr als 10 g / kg sowohl bei Mäusen als auch bei Ratten. Die häufigsten Anzeichen und Symptome beobachtet werden diejenigen, die durch Elektrolytmangel (Hypokaliämie, Hypochlorenämie) verursacht werden Hyponatriämie) und Dehydration infolge übermäßiger Diurese. Wenn digitalis wurde auch verabreicht, Hypokaliämie kann Herzrhythmusstörungen verstärken. Das Grad, in dem Hydrochlorothiazid durch Hämodialyse entfernt wird, war nicht etabliert.

Losartan Kalium
Losartan hemmt die Druckereffekt von Angiotensin II (sowie Angiotensin I) Infusionen. Eine Dosis von 100 mg hemmt den Druckbehälter Wirkung um etwa 85% in der Spitze, wobei die 25-40% ige Hemmung 24 Stunden lang anhält. Die Entfernung der negativen Rückkopplung von Angiotensin II führt zu einer Verdoppelung von Verdreifachung der Plasma-Renin-Aktivität und daraus resultierender Anstieg des Angiotensin-II-Plasmas Konzentration bei hypertensiven Patienten. Losartan hat keinen Einfluss auf die Reaktion zu Bradykinin, während ACE-Hemmer die Reaktion auf Bradykinin erhöhen. Aldosteron Die Plasmakonzentrationen fallen nach Losartan-Verabreichung. Trotz der Wirkung von Losartan auf die Aldosteronsekretion, sehr geringe Auswirkung auf das Serum Kalium wurde beobachtet.
Die Wirkung von Losartan ist im Wesentlichen vorhanden eine Woche, aber in einigen Studien trat der maximale Effekt in 3-6 Wochen auf. Im Langzeit-Follow-up-Studien (ohne Placebo-Kontrolle) die Wirkung von Losartan schien bis zu einem Jahr instand gehalten zu sein. Es gibt keinen offensichtlichen Rebound-Effekt nach abruptem Rückzug von Losartan. Im Durchschnitt gab es im Wesentlichen keine Veränderung Herzfrequenz bei mit Losartan behandelten Patienten in kontrollierten Studien.
Hydrochlorothiazid
Nach oraler Verabreichung von Hydrochlorothiazid Die Diurese beginnt innerhalb von 2 Stunden, erreicht ihren Höhepunkt in etwa 4 Stunden und dauert etwa 6 bis 12 Stunden Stunden.
Arzneimittelwechselwirkungen
Hydrochlorothiazid
Alkohol, Barbiturate oder Betäubungsmittel - Potenzierung einer orthostatischen Hypotonie kann auftreten.
Andere blutdrucksenkende Medikamente - additive Wirkung oder Potenzierung.
Skelettmuskelrelaxantien, nicht depolarisierend (z., Tubocurarin) - mögliche erhöhte Reaktionsfähigkeit auf das Muskelrelaxans.
Kortikosteroide, ACTH oder Glycyrrhizin (gefunden in Lakritz) - verstärkte Elektrolytverarmung, insbesondere Hypokaliämie.
Pressoramine (z., Noradrenalin) - möglich verminderte Reaktion auf Druckamine, aber nicht ausreichend, um ihre Verwendung auszuschließen.

Losartan Kalium
Absorption
Nach oraler Verabreichung wird Losartan gut resorbiert und unterliegt einem erheblichen First-Pass-Metabolismus. Die systemische Bioverfügbarkeit von Losartan sind ungefähr 33%. Mittlere Spitzenkonzentrationen von Losartan und seinen aktiver Metabolit wird in 1 Stunde bzw. in 3-4 Stunden erreicht. Während Die maximalen Plasmakonzentrationen von Losartan und seinem aktiven Metaboliten betragen ungefähr gleich ist die AUC (Fläche unter der Kurve) des Metaboliten etwa viermal so hoch wie großartig wie das von Losartan. Eine Mahlzeit verlangsamt die Aufnahme von Losartan und nimmt ab sein C max hat aber nur geringfügige Auswirkungen auf die Losartan AUC oder auf die AUC der Metabolit (~ 10% Abnahme). Die Pharmakokinetik von Losartan und seiner aktiven Metaboliten sind linear mit oralen Losartan-Dosen von bis zu 200 mg und ändern sich nicht im Laufe der Zeit.
Verteilung
Das Verteilungsvolumen von Losartan und dem aktiven Der Metabolit beträgt etwa 34 Liter bzw. 12 Liter. Sowohl Losartan als auch sein aktiver Metabolit ist stark an Plasmaproteine gebunden, hauptsächlich an Albumin mit plasmafreien Fraktionen von 1,3% bzw. 0,2%. Plasmaprotein Die Bindung ist über den mit den empfohlenen Werten erreichten Konzentrationsbereich konstant Dosen. Studien an Ratten zeigen, dass Losartan die Blut-Hirn-Schranke überschreitet schlecht, wenn überhaupt.
Stoffwechsel
Losartan ist ein oral aktiver Agent, der durchmacht wesentlicher First-Pass-Metabolismus durch Cytochrom P450-Enzyme. Es wird konvertiert, teilweise zu einem aktiven Carbonsäuremetaboliten, der für die meisten verantwortlich ist des Angiotensin-II-Rezeptorantagonismus, der auf die Losartan-Behandlung folgt. Etwa 14% einer oral verabreichten Losartan-Dosis werden in die aktive umgewandelt Metabolit. Neben dem aktiven Carbonsäuremetaboliten mehrere inaktive Metaboliten werden gebildet. In vitro Studien zeigen, dass Cytochrom P450 2C9 und 3A4 sind an der Biotransformation von Losartan beteiligt Metaboliten.
Beseitigung
Gesamtplasma-Clearance von Losartan und dem aktiven Der Metabolit beträgt etwa 600 ml / min bzw. 50 ml / min bei Nieren Abstand von ca. 75 ml / min bzw. 25 ml / min. Das Terminal Die Halbwertszeit von Losartan beträgt ca. 2 Stunden und der Metabolit ca. 6-9 Stunden. Nach oraler Verabreichung von Losartan-Einzeldosen etwa 4% der Dosis wird unverändert im Urin ausgeschieden und etwa 6% werden als aktiv im Urin ausgeschieden Metabolit. Die biliäre Ausscheidung trägt zur Eliminierung von Losartan und bei seine Metaboliten. Nach dem Mündlichen 14C-markierter Losartan, etwa 35% von Radioaktivität wird im Urin und etwa 60% im Kot zurückgewonnen. Folgen eine intravenöse Dosis von 14C-markierter Losartan, etwa 45% von Radioaktivität wird im Urin und zu 50% im Kot zurückgewonnen. Weder Losartan Bei wiederholter einmal täglicher Dosierung reichert sich weder sein Metabolit noch sein Metabolit im Plasma an.
Hydrochlorothiazid
Hydrochlorothiazid wird nicht metabolisiert, sondern eliminiert schnell an der Niere. Wenn die Plasmaspiegel mindestens 24 Jahre lang eingehalten wurden Es wurde beobachtet, dass die Plasma-Halbwertszeit zwischen 5,6 und 14,8 variiert Stunden. Mindestens 61 Prozent der oralen Dosis werden innerhalb von 24 unverändert eliminiert Stunden. Hydrochlorothiazid passiert das Plazenta, aber nicht das Bluthirn Barriere und wird in die Muttermilch ausgeschieden.
However, we will provide data for each active ingredient


