









コンポーネント:
Kovalenko Svetlana Olegovna 、薬局による医学的評価、 最終更新日:05.04.2022

アテンション! そのこのページの情報は医療専門家のみを対象としています! その情報が収集したオープン源を含めることが可能である重大な誤差! 注意して、このページ上のすべての情報を再確認してください!


投薬形態と強さ。
オレプトロ錠は、次の強さで入手できます。
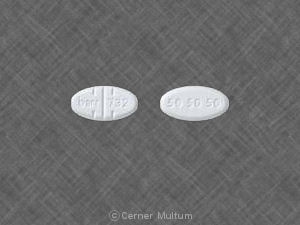
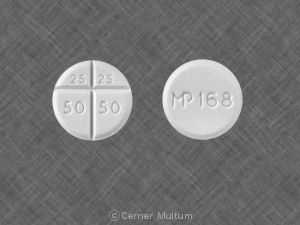
- 150 mgのトラゾドンを含むオレプトロ二等分錠。 塩酸塩(黄 ⁇ 色、カプセル型の錠剤、コーティングおよびスコアリング。 両面にDDS 080が片面に印刷されています)。
- 300 mgのトラゾドンを含むオレプトロ二等分錠。 塩酸塩(ベージュオレンジ、カプセル型タブレット、コーティングされ、両方でスコアリングされます。 DDS 081が片面に印刷された側面)。
保管と取り扱い。
オレプロ150 mg。 黄色がかったベージュのカプセル型です。 徐放錠、DDS 080が印刷された両面がコーティングおよびスコアリング。 片側。. 次のように提供されます。
30錠のボトル。 NDC。 43595-080-03。
オレプロ300 mg。 ベージュオレンジのカプセル型です。 DDS 081が印刷された状態で両面がコーティングおよびスコアリングされた徐放錠。 片側。. 次のように提供されます。
30錠のボトル。 NDC。 43595-081-03。
室温(15〜30°C)でしっかりと保管してください。 耐光容器。.
Angelini Pharma Inc. ゲーサーズバーグ、MD 20877。. ⁇ 改訂:2014年7月。

Oleptro™はメジャーの治療に使用されます。 成人のうつ病性障害(MDD)。. オレプトロの有効性はされています。 MDDによる外来患者の試験およびとの試験で確立された。 トラゾドンの即時放出製剤。.

線量選択。
オレプトロの推奨開始用量は1回150 mgです。 大人で毎日。. 用量は3日ごとに75 mg /日増加する可能性があります(つまり、.、。 治療の4日目に225 mgを開始します)。. 最大日用量は375を超えてはなりません。 mg。.
- オレプトロ錠は同時に経口摂取する必要があります。 毎日、夕方遅く、できれば就寝時に、空腹時に。.
- 適切な反応が得られたら、投与量も可能です。 治療に応じて調整しながら、徐々に減らします。 応答。.
- 患者は離脱症状がないか監視する必要があります。 塩酸トラゾドンによる治療の中止。. 投与量はあるべきです。 可能な限り徐々に減少しました。.
メンテナンス処理。
の維持療法に対するオレプトロの有効性。 MDDは評価されていません。. 利用可能な証拠の本体はありませんが。 オレプロで治療された患者がどのくらい続くべきかという質問に答えてください。 薬物、治療はいくつかのために継続することが一般的に推奨されます。 最初の応答の数か月後。. 患者は最低限に維持されるべきです。 有効用量および継続的な必要性を決定するために定期的に再評価されます。 メンテナンス治療用。.
患者をモノアミンオキシダーゼに切り替える。 精神障害を治療することを目的とした阻害剤(MAOI)。
中止の間に少なくとも14日が経過するはずです。 精神障害の治療と治療の開始を目的としたMAOI。 オレプロ。. 逆に、オレプトロを止めた後、少なくとも14日間は許可されるべきです。 精神障害の治療を目的としたMAOIを開始する前に。.
オレプトロとリネゾリドやメチレンなどの他のMAOIの使用。 青い。
治療を受けている患者でオレプトロを開始しないでください。 リスクが高いため、リネゾリドまたは静脈内メチレンブルーを使用します。 セロトニン症候群の。. より緊急の治療を必要とする患者。 精神状態、入院を含む他の介入は、すべきです。 考慮されます。.
場合によっては、すでにオレプトロを投与されている患者。 治療には、リネゾリドまたは静脈内メチレンによる緊急治療が必要な場合があります。 青い。. ラインゾリドまたは静脈内メチレンブルーの許容できる代替物。 治療は利用できず、リネゾリドまたはの潜在的な利点。 静脈内メチレンブルー処理は、リスクを上回ると判断されます。 特定の患者のセロトニン症候群、オレプトロは迅速に停止されるべきです。 リネゾリドまたは静脈内メチレンブルーを投与できます。. 患者。 セロトニン症候群の症状がないか2週間またはそれまで監視する必要があります。 リネゾリドまたは静脈内メチレンブルーの最終投与から24時間後。 どちらが先か。. オレプロによる治療は、24時間後に再開される場合があります。 リネゾリドまたは静脈内メチレンブルーの最後の投与量。.
メチレンブルーを投与するリスク。 非静脈内経路(経口錠剤や局所注射など)または内。 オレプトロで1 mg / kgをはるかに下回る静脈内投与量は不明です。. 。 それにもかかわらず、臨床医は緊急の可能性を認識している必要があります。 そのような使用によるセロトニン症候群の症状(参照。 警告と注意。].
重要な管理手順。
Oleptroタブレットは、柔軟性を提供するためにスコアリングされます。 投薬。.
オレプトロは丸ごと飲み込むか、半分として投与することができます。 スコアラインに沿ってタブレットを壊すことによってタブレット。. タブレットを半分に壊します。 タブレットの放出制御特性には影響しません。.
制御リリースプロパティを維持するために。 オレプトロは噛んだり砕いたりしないでください。.

モノアミンオキシダーゼ阻害剤(MAOI)。
MAOIの使用は、精神障害の治療を目的としています。 オレプロを使用するか、オレプロによる治療を中止してから14日以内です。 セロトニン症候群のリスクが高いため禁 ⁇ 。. の使用。 精神科の治療を目的としたMAOIを停止してから14日以内のオレプトロ。 障害も禁 ⁇ です。..
治療を受けている患者でオレプトロを始めます。 リネゾリドや静脈内メチレンブルーなどのMAOIも禁 ⁇ です。 セロトニン症候群のリスクが高いため。.

警告。
の一部として含まれています。 注意。 セクション。.
注意。
臨床的悪化と自殺のリスク。
大うつ病性障害(MDD)の患者、どちらも成人。 小児は、うつ病やうつ病の悪化を経験する可能性があります。 自殺念慮と行動(自殺)の出現または異常な変化。 彼らが抗うつ薬を服用しているかどうかにかかわらず、行動、そしてこれ。 リスクは、重大な寛解が発生するまで持続する可能性があります。. 自殺は既知のリスクです。 うつ病および他の特定の精神障害およびこれらの障害。 彼ら自身が自殺の最も強い予測因子です。. 長い間ありました。 しかし、抗うつ薬が誘発に役割を果たす可能性があることへの懸念。 うつ病の悪化と特定の患者における自殺の出現。 治療の初期段階。. 短期的なプールされた分析。 抗うつ薬(SSRIなど)のプラセボ対照試験が示した。 これらの薬は自殺念慮と行動のリスクを高めること。 (自殺)子供、青年、および若者(18〜24歳)と一緒に。 MDDおよびその他の精神障害。. 短期研究では示されませんでした。 プラセボと比較して抗うつ薬による自殺のリスクの増加。 24歳以上の成人;と比較して抗うつ薬の減少がありました。 65歳以上の成人のプラセボ。.
プラセボ対照試験のプールされた分析。 MDD、強迫性障害(OCD)の子供および青年、または。 その他の精神障害には、合計24件の短期試験9件が含まれていました。 4,400人以上の患者における抗うつ薬。. のプールされた分析。 MDDまたはその他の精神障害のある成人を対象としたプラセボ対照試験。 合計295件の短期試験(期間中央値2か月)11件が含まれています。 77,000人以上の患者における抗うつ薬。. かなりのばらつきがありました。 薬物間の自殺のリスクがあるが、増加する傾向。 研究されたほとんどすべての薬物の若い患者。. 違いがありました。 さまざまな適応症にわたる自殺の絶対リスク、最高。 MDDの発生率。リスクの違い(薬物対. プラセボ)は、しかし、そうでした。 年齢層内および適応症全体で比較的安定しています。. これらのリスク。 違い(自殺の症例数ごとの薬物プラセボの違い。 1,000人の治療を受けた患者)を表1に示します。.
表1。
| 年齢範囲。 | 治療された患者1,000人あたりの自殺の症例数の薬物プラセボの違い。 |
| プラセボと比較して増加します。 | |
| <18。 | 14の追加ケース。 |
| 18-24。 | 5つの追加ケース。 |
| プラセボと比較して減少。 | |
| 25-64。 | 1少ないケース。 |
| ≥65。 | 6件少ないケース。 |
自殺は発生しなかった。 小児試験。. 成人裁判では自殺がありましたが、その数です。 自殺への薬物影響についての結論に達するには十分ではなかった。.
かどうかは不明です。 自殺リスクは長期使用にまで及びます。.、数か月を超えて。. ただし、プラセボ対照維持からの実質的な証拠があります。 抗うつ薬の使用が遅れる可能性があるうつ病のある成人での試験。 うつ病の再発。.
治療されているすべての患者。 抗うつ薬を使用して、あらゆる適応症を適切に監視する必要があります。 臨床的悪化、自殺、および異常な変化について密接に観察されました。 行動、特に薬物療法のコースの最初の数か月の間。 または、用量変更時に、増加または減少する。.
以下の症状。 不安、興奮、パニック発作、不眠症、イライラ、敵意、 攻撃性、衝動性、アカシジア(精神運動不穏)、低 ⁇ 病、。 そして ⁇ 病は、治療されている成人および小児患者で報告されています。 大うつ病性障害やその他の抗うつ薬。 適応症、精神医学および非精神医学の両方。. 因果関係ですが。 そのような症状の出現とうつ病の悪化の間に。 および/または自殺衝動の出現は確立されていません、あります。 そのような症状が新たな自殺の前兆となる可能性があるという懸念。.
考慮すべきです。 中止の可能性を含め、治療計画を変更する。 うつ病が持続的に悪化している患者、または持続している患者の薬物療法。 新たな自殺または前駆体である可能性のある症状を経験している。 うつ病または自殺の悪化、特にこれらの症状が重度の場合。 突然の発症、または患者の症状の一部ではありませんでした。.
家族と介護者。 大うつ病性障害または抗うつ薬で治療されている患者。 精神医学と非精神医学の両方の他の適応症について警告されるべきです。 興奮、過敏性の出現について患者を監視する必要性。 異常な行動の変化、および上記のその他の症状、ならびに。 自殺の出現、およびそのような症状を直ちに健康に報告すること。 ケアプロバイダー。. そのような監視はすべきです。 家族や介護者による毎日の観察を含みます。. オレプトロの処方箋は、のために書かれるべきです。 順番に、良好な患者管理と一致する錠剤の最小量。 過剰摂取のリスクを減らすため。.
セロトニン症候群。
aの開発。 生命を脅かす可能性のあるセロトニン症候群がSNRIで報告されています。 オレプトロを含むSSRIのみですが、特に併用されます。 その他のセロトニン作動薬(トリプタン、三環系抗うつ薬など)。 フェンタニル、リチウム、トラマドール、トリプトファン、ブシピロン、セント. ジョンの麦 ⁇ )と。 セロトニンの代謝を損なう薬物(特にMAOI、両方)。 精神障害を治療することを目的としたもの、およびその他のもの。 リネゾリドと静脈内メチレンブルー)。.
セロトニン症候群の症状はあるかもしれません。 メンタルステータスの変更を含める(例:.、興奮、幻覚、せん妄、そして。 ⁇ 睡)、自律神経不安定性(例:.、頻脈、不安定な血圧、 めまい、発汗、紅潮、高体温症)、神経筋症状(例:.、。 振戦、硬直、ミオクローヌス、過反射、協調不全)、発作、および/または。 胃腸症状(例:.、吐き気、 ⁇ 吐、下 ⁇ )。. 患者はすべきです。 セロトニン症候群の出現を監視する。.
オレプトロの併用。 精神障害の治療を目的としたMAOIは禁 ⁇ です。. オレプロ。 また、次のようなMAOIで治療されている患者で開始しないでください。 リネゾリドまたは静脈内メチレンブルー。. メチレンブルーのすべてのレポート。 静脈内投与を含む投与経路に関する情報を提供した。 1 mg / kgから8 mg / kgの用量範囲での投与。. 報告はありません。 他の経路(経口錠剤や 局所組織注射)または低用量。. 状況があるかもしれません。 ラインゾリドやMAOIなどの治療を開始するために必要です。 オレプトロを服用している患者の静脈内メチレンブルー。. オレプトロはそうあるべきです。 MAOIによる治療を開始する前に中止されました。.
オレプロと他のセロトニン作動性を併用する場合。 薬物、トリプタン、三環系抗うつ薬、フェンタニル、リチウム、トラマドール、 ブスピロン、トリプトファン、セント. ジョンズワートは臨床的に正当化されている患者です。 セロトニン症候群のリスクの増加の可能性を認識しておく必要があります。 特に治療の開始時と用量の増加時。.
オレプロと併用セロトニン作動薬による治療。 エージェントは、上記のイベントが発生した場合、直ちに中止する必要があります。 支持的な対症療法を開始する必要があります。.
アングルクロージャー緑内障。
多くの使用後に発生する ⁇ 拡張。 オレプロを含む抗うつ薬は、アングル閉鎖攻撃を引き起こす可能性があります。 特許 ⁇ 彩切除術を受けていない解剖学的に狭い角度の患者。.
双極性障害とモニタリングのための患者のスクリーニング。 マニア/ヒポマニア。
大きなうつ病エピソードが最初の可能性があります。 双極性障害の提示。. それは一般的に信じられています(そうではありません。 対照試験で確立された)そのようなエピソードをで扱うこと。 抗うつ薬だけでも、aの沈殿の可能性が高まることがあります。 双極性障害のリスクがある患者の混合/ ⁇ 病エピソード。. どれか。 臨床的悪化と自殺リスクについて説明されている症状は、そのようなものです。 変換は不明です。. ただし、治療を開始する前に。 抗うつ薬、うつ病症状のある患者は適切にスクリーニングされるべきです。 それらが双極性障害のリスクがあるかどうかを判断するため。そのようなスクリーニングはすべきです。 自殺の家族歴を含む詳細な精神医学の歴史を含みます。 双極性障害、うつ病。. オレプトロはそうではないことに注意してください。 双極性うつ病の治療での使用が承認されています。.
QT延長と突然死のリスク。
トラゾドンはQT / QTc間隔を延長することが知られています。. いくつか。 QT / QTc間隔を延長する薬物は、トルサードドポワントを引き起こす可能性があります。 突然、原因不明の死。. QT延長の関係は最も明確です。 大幅な増加(20ミリ秒以上)ですが、QT / QTcが小さい可能性があります。 延長はまた、特に影響を受けやすい個人において、リスクを増大させる可能性があります。 低カリウム血症、低マグネシウム血症、または遺伝的素因のある人など。 QT / QTcの延長。.
トルサードドポワントは観察されていませんが。 市販前試験での推奨用量でのオレプトロの使用は、経験です。 リスクの増加を除外するには制限が多すぎます。. しかし、ありました。 Torsades de Pointesの市販後レポート。 トラゾドン(複数の交絡因子が存在する場合)、たとえ投与量でも。 1日あたり100 mg以下。.
心臓病の患者での使用。
塩酸トラゾドンは、使用中の使用は推奨されません。 心筋 ⁇ 塞の最初の回復段階。.
Oleptroを投与する場合は注意が必要です。 心臓病の患者およびそのような患者は注意深く監視されるべきです。 抗うつ薬(塩酸トラゾドンを含む)が引き起こす可能性があるため。 不整脈。.
QT延長はトラゾドン療法で報告されています。. 患者の臨床試験。 既存の心臓病は、塩酸トラゾドンがそうである可能性があることを示しています。 その集団の一部の患者では不整脈。. 不整脈が確認されました。 孤立したPVC、心室カプレット、失神を伴う頻脈、および トルサードドポワント。. 市販後のイベントは100 mgの用量で報告されています。 トラゾドンの即時放出型以下。.
QTを延長する薬物の併用投与。 間隔またはCYP3A4の阻害剤であるものは、心臓のリスクを高める可能性があります。 不整脈。.
起立性低血圧と失神。
起立性低血圧を含む低血圧および。 失神は、塩酸トラゾドンを投与されている患者で報告されています。. 降圧剤と併用する場合は、用量を減らす必要がある場合があります。 降圧薬。.
異常な出血。
市販後データは、使用間の関連を示しています。 セロトニンの再取り込みと発生を妨げる薬物の。 消化管(GI)出血。. トラゾドンと 出血イベント、特にGI出血が示され、患者は示されるべきです。 併用に関連する出血の潜在的なリスクについて警告。 トラゾドンおよびNSAID、アスピリン、または凝固に影響を与えるその他の薬物の 出血。. SSRIおよびSNRIに関連する他の出血イベントには、さまざまなものがあります。 斑状出血、血腫、鼻出血、および点状出血から生命にかかわる出血。.
MAOIとの相互作用。
セロトニン作動薬を組み合わせて投与されている患者。 モノアミンオキシダーゼ阻害剤(MAOI)を使用すると、深刻な報告があります。 時には高体温、硬直、ミオクローヌスなどの致命的な反応。 バイタルサインの急速な変動と精神的状態を伴う自律神経の不安定性。 せん妄や ⁇ 睡への極端な興奮を含む変化。. これら。 最近中止した患者でも反応が報告されています。 抗うつ薬治療とMAOIで開始されました。いくつかのケースが提示されました。 神経遮断薬悪性症候群に似た特徴があります。. さらに、制限されています。 セロトニン作動性抗うつ薬の併用効果に関する動物データ。 MAOIは、これらの薬物が相乗的に作用して血圧を上昇させる可能性があることを示唆しています。 行動興奮を呼び起こします。. したがって、オレプトロをお勧めします。 MAOIと組み合わせて、または14日以内に使用しないでください。 MAOIによる治療の中止。同様に、少なくとも14日はする必要があります。 MAOIを開始する前にOleptroを停止した後に許可されます。
持続勃起症。
持続勃起症のまれなケース(痛みを伴う勃起が6より大きい)。 持続時間の時間)は、トラゾドンを受けている男性で報告されました。. そうでない場合、プリアピズム。 迅速に処理すると、勃起組織に不可逆的な損傷をもたらす可能性があります。. 男性。 痛みを伴うかどうかにかかわらず、勃起が6時間を超えて続く人。 すぐに薬を中止し、緊急の医療処置を求める必要があります。.
トラゾドンは、持っている男性には注意して使用する必要があります。 それらを持続可能にする可能性のある条件(例:.、 ⁇ 状赤血球貧血、。 多発性骨髄腫、または白血病)、または解剖学的変形を伴う男性。 ペニス(例:.、角形成、海綿体線維症、またはペイロニー病)。.
低ナトリウム血症。
低ナトリウム血症は、治療の結果として発生する可能性があります。 抗うつ薬。. 多くの場合、この低ナトリウム血症はその結果であると思われます。 不適切な抗利尿ホルモン分 ⁇ 症候群(SIADH)。. ケース。 血清ナトリウムが110 mmol / L未満であることが報告されています。. 高齢患者。 抗うつ薬による低ナトリウム血症を発症するリスクが高い可能性があります。. また、。 利尿薬を服用している患者、またはその他の方法で体調が消耗している患者は、 より大きなリスク。. オレプトロの中止は、患者で考慮されるべきです。 症候性低ナトリウム血症と適切な医療介入が必要です。 制定された。.
低ナトリウム血症の兆候と症状には頭痛が含まれます。 集中困難、記憶障害、混乱、弱さ、そして。 落胆につながる可能性のある不安定さ。. 兆候と症状はもっと関連しています。 重度および/または急性の症例には、幻覚、失神、発作、 ⁇ 睡などがあります。 呼吸停止、そして死。.
認知障害と運動障害の可能性。
オレプトロは傾眠または鎮静を引き起こし、障害を引き起こす可能性があります。 潜在的なパフォーマンスに必要な精神的および/または身体的能力。 危険なタスク。. 危険な操作については、患者に注意する必要があります。 自動車を含む機械は、それが合理的に確実になるまで。 薬物治療はそれらに悪影響を及ぼしません。.
中止の症状。
不安、興奮などの離脱症状。 睡眠障害は、トラゾドンで報告されています。. 臨床経験。 完了する前に用量を徐々に減らすべきであることを示唆しています。 治療の中止。.
患者カウンセリング情報。
見る。 薬。 ガイド。.
患者さんのための情報。
処方者または他の医療専門家は通知する必要があります。 患者、その家族、および介護者は、利益とリスクについて考えます。 オレプロによる治療に関連しており、その上で彼らに助言する必要があります。 適切な使用。.
患者はそれに警告されるべきです。
- 自殺のリスクが高まる可能性があります。 特に子供、ティーンエイジャー、若者での考え。.
- 以下の症状を報告する必要があります。 医師:不安、興奮、パニック発作、不眠症、過敏症、 敵意、攻撃性、衝動性、アカシジア、低 ⁇ 病、 ⁇ 病。.
- 歴史がある場合は医師に通知する必要があります。 双極性障害、心臓病または心筋 ⁇ 塞の。.
- セロトニン症候群が発生する可能性があり、症状が含まれる場合があります。 精神状態の変化(例:.、興奮、幻覚、 ⁇ 睡)、自律神経。 不安定性(例:.、頻脈、不安定な血圧、高体温)、。 神経筋異常(例:.、過反射、協調不全)および/または消化管。 症状(例:.、吐き気、 ⁇ 吐、下 ⁇ )。.
- オレプトロを服用すると原因となる可能性があることを患者に通知する必要があります。 影響を受けやすい個人では、軽度の ⁇ 孔拡張が 角閉鎖緑内障のエピソード。. 既存の緑内障はほとんど常にです。 角度閉鎖緑内障は、診断されたときに緑内障が診断される可能性があるためです。 ⁇ 摘出術で確実に治療。. 開放隅角緑内障は危険因子ではありません。 角閉鎖緑内障用。. 患者は、決定するために検査されることを望むかもしれません。 それらが角度閉鎖の影響を受けやすく、予防的であるかどうか。 手順(例:.、 ⁇ 摘出術)、影響を受けやすい場合。.
- 塩酸トラゾドンは、 持続勃起症の発生。.
- を含む低血圧の可能性があります。 起立性低血圧と失神。.
- 出血のリスクがある可能性があります(含む。 生命にかかわる出血)および出血関連のイベント(含む。 斑状出血、血腫、鼻出血、点状出血)の併用。 塩酸トラゾドンおよびNSAID、アスピリン、または影響を与えるその他の薬物。 凝固または出血。.
- 不安、興奮などの離脱症状。 睡眠障害は、トラゾドンで報告されています。. 臨床経験。 用量を徐々に減らすべきであることを示唆しています。.
患者はそれをカウンセリングされるべきです。
- オレプトロは傾眠または鎮静を引き起こし、障害を引き起こす可能性があります。 潜在的なパフォーマンスに必要な精神的および/または身体的能力。 危険なタスク。. 危険な操作については、患者に注意する必要があります。 自動車を含む機械は、それが合理的に確実になるまで。 薬物治療はそれらに影響を与えません。.
- トラゾドンはアルコールに対する反応を高めるかもしれません。 バルビツール酸塩、およびその他のCNS抑制剤。.
- 妊娠するつもりの女性。 母乳育児は、彼らが継続すべきかどうか医師と話し合うべきです。 妊娠中および授乳中の女性での使用は推奨されないため、オレプロを使用します。.
重要な管理手順。
- オレプトロは丸ごと飲み込むか、半分ずつ壊す必要があります。 スコアライン。.
- 制御リリースプロパティを維持するために。 噛んだりつぶしたりしないでください。.
- オレプトロは毎日同時に服用する必要があります。 夕方遅く、できれば就寝時、空腹時。.
非臨床毒性学。
発がん、変異誘発、生殖能力の障害。
発がんの薬物または用量に関連した発生はありませんでした。 18日間300 mg / kgまでの毎日の経口投与でトラゾドンを投与されているラットで明らか。 月。.
特定の集団で使用します。
妊娠。
妊娠カテゴリーC
塩酸トラゾドンは増加を引き起こすことが示されています。 使用する2つの研究で胎児吸収と胎児へのその他の悪影響。 提案された約30〜50倍の用量レベルで投与した場合のラット。 最大ヒト用量。. 先天性異常も1つ増加しました。 最大ヒト用量の約15〜50倍での3つのウサギの研究の。. 妊娠中の女性を対象とした適切で適切に管理された研究はありません。. オレプロ。 潜在的な利益が正当化する場合にのみ、妊娠中に使用する必要があります。 胎児への潜在的なリスク。.
授乳中の母親。
トラゾドンおよび/またはその代謝産物は、 授乳中のラットの乳。この薬は母乳に分 ⁇ される可能性があることを示唆しています。. オレプロを授乳中の女性に投与する場合は注意が必要です。.
小児用。
小児集団の安全性と有効性があります。 確立されていません。. オレプトロは子供や青年には使用しないでください。.
老人用。
臨床でオレプトロで治療された202人の患者のうち。 試験では、65歳以上の患者は9人でした。. 安全性に全体的な違いはありません。 これらの被験者と若い被験者の間で有効性が観察されました。 他の報告された臨床文献とトラゾドンの経験はそうではありません。 高齢者と若年患者の反応の違いを特定しました。. ただし、オレプトロでの高齢者の経験は限られているため、そうする必要があります。 老人患者には注意して使用。.
抗うつ薬は以下の症例と関連しています。 高齢患者の臨床的に有意な低ナトリウム血症。 この副作用のリスク。
腎障害。
オレプトロは腎患者で研究されていません。 障害。. この集団ではトラゾドンを注意して使用する必要があります。.
肝障害。
オレプトロは肝臓の患者では研究されていません。 障害。. この集団ではトラゾドンを注意して使用する必要があります。.

副作用。
以下の深刻な副作用が説明されています。 ラベルの他の場所:。
- 臨床的悪化と自殺のリスク。
- セロトニン症候群またはNMS様反応。
- QT延長と突然死のリスク。
- 起立性低血圧。
- 異常な出血イベント。
- 持続勃起症。
- 低ナトリウム血症。
- 認知障害と運動障害。
- 中止症状。
最も一般的な副作用(5%以上と報告されています。 プラセボの2倍の割合)は、傾眠/鎮静、めまいです。 便秘、視力障害。.
表2は、有害事象(AE)の概要を示しています。 少なくとも発生率でオレプトロ治療の中止につながります。 プラセボの1%と少なくとも2倍。.
表2:AEあり。
取られた措置としての中止(≥1%の発生率と2xプラセボの発生率)。
| オレプロ。 N = 202。 |
|
| 傾眠/鎮静。 | 8(4.0%)。 |
| めまい。 | 7(3.5%)。 |
| 混乱状態。 | 2(1.0%)。 |
| 異常な調整。 | 2(1.0%)。 |
| 頭痛。 | 2(1.0%)。 |
| 吐き気。 | 2(1.0%)。 |
| バランス障害/歩行障害。 | 2(1.0%)。 |
臨床研究の経験。
以下に説明するデータ。 暴露された204人を含む406人の患者の臨床試験における暴露を反映している。 プラセボと202をオレプトロに曝露。. 患者は18〜80歳でした。 患者の69.3%と67.5%は、以前にうつ病のエピソードを少なくとも1回経験しました。 プラセボ群とアクティブ治療群の過去24か月間。. に。 個々の患者、用量は柔軟で、1日あたり150〜375 mgの範囲でした。. 6週間の治療期間中の平均1日量は310 mgでした。. タブレット。 経口投与され、1日1回、合計8日間投与されました。 滴定期間を含む週。.
臨床試験があるからです。 大きく異なる条件下で実施され、副作用率が観察されました。 薬物の臨床試験は、その割合と直接比較することはできません。 別の薬物の臨床試験であり、観察された率を反映していない可能性があります。 練習。.
表3は、その概要を示しています。 5%以上の発生率で発生したすべての治療緊急AE。 Oleptroグループ、臨床研究者が関連していると見なしたかどうか。 研究薬かどうか。.
表3:最も一般的。
治療緊急有害事象(アクティブ治療を受けている患者の5%以上)。
| 優先用語。 | プラセボ。 N = 204。 |
オレプロ。 N = 202。 |
| 傾眠/鎮静。 | 39(19%)。 | 93(46%)。 |
| 頭痛。 | 55(27%)。 | 67(33%)。 |
| 口渇。 | 26(13%)。 | 51(25%)。 |
| めまい。 | 25(12%)。 | 50(25%)。 |
| 吐き気。 | 26(13%)。 | 42(21%)。 |
| 疲労。 | 17(8%)。 | 30(15%)。 |
| 下 ⁇ 。 | 23(11%)。 | 19(9%)。 |
| 便秘。 | 4(2%)。 | 16(8%)。 |
| 腰痛。 | 7(3%)。 | 11(5%)。 |
| 視力がぼやけている。 | 0(0%)。 | 11(5%)。 |
性機能不全。
関連する有害事象。 性的機能障害(因果関係に関係なく)は4.9%と1.5%報告されました。 オレプトロとプラセボでそれぞれ治療された患者。. オレプログループでは、 射精障害は患者の1.5%で発生し、性欲の減少が発生しました。 患者の1.5%、勃起不全と異常なオルガスム<1%。 患者。.
バイタルサインと重量。
バイタルサイン(血液)に顕著な変化はありませんでした。 圧力、呼吸数、脈拍)またはいずれかの治療グループの体重。.
以下は、治療に伴う有害性のリストです。 発生率が1%以上5%未満の反応(つまり、.、あまり一般的ではない)で。 オレプロで治療された患者。. このリストは、含めることを意図していません。 反応(i)以前の表またはラベルの他の場所にすでにリストされている。 (ii)治療との関連が遠い、(iii)そうだった。 一般的ではないこと、および(iv)持っているとは見なされなかった。 重大な臨床的影響。. 反応は身体系によって分類されます。 次の定義を使用します。頻繁な副作用が発生しています。 少なくとも1/100人の患者; まれ。 副作用はそれらです。 1/100未満の患者で発生します。.
耳と迷路の障害—。 まれ。:。 視力低下、耳鳴り、めまい。
眼疾患—。 頻繁。:視覚障害;。 まれ。:ドライアイ、目の痛み、恐怖症。
胃腸障害—。 頻繁。:。 腹痛、 ⁇ 吐;。 まれ。:逆流性食道炎。
一般的な障害と管理サイトの条件—。 頻繁。:浮腫;。 まれ。:歩行障害。
免疫系障害—。 まれ。:。 過敏症。
筋骨格系および結合組織障害—。 頻繁。:筋骨格系の苦情、筋肉痛;。 まれ。:筋肉。 けいれん。
神経系障害—。 頻繁。:調整。 異常、味覚異常、記憶障害、片頭痛、感覚異常、振戦; まれ。:。 健忘症、失語症、知覚低下、言語障害。
精神障害—。 頻繁。:興奮、。 混乱状態、見当識障害。
腎障害と尿障害— 頻繁。:。 排尿の緊急性;。 まれ。: ⁇ の痛み、尿失禁。
呼吸器、胸部および縦隔障害— 頻繁。:呼吸困難。
皮膚および皮下組織障害—。 頻繁。:。 寝汗;。 まれ。:にきび、多汗症、光線過敏症反応。
血管障害—。 まれ。:紅潮。
市販後の経験。
塩酸トラゾドンに関する自発的報告。 市販後の経験から受け取ったものには、次のものがあります。 興奮、脱毛症、不安症、失語症、無呼吸、乳房肥大または。 充血、心 ⁇ 、脳血管障害、悪寒、胆 ⁇ うっ滞。 陰核、うっ血性心不全、複視、浮腫、 ⁇ 体外路症状、 壮大な発作、幻覚、溶血性貧血、多毛症、。 高ビリルビン血症、アミラーゼの増加、 ⁇ 液分 ⁇ の増加、不眠症。 白血球増加症、白血球減少症、黄 ⁇ 、授乳、肝酵素の変化、 メテモグロビン血症、吐き気/ ⁇ 吐(最も頻繁に)、感覚異常、妄想。 反応、持続勃起症、そう ⁇ 、乾 ⁇ 、精神病、発疹、 ⁇ 睡、。 不適切なADH症候群、遅発性ジスキネジア、原因不明の死、尿。 失禁、尿閉、じんま疹、血管拡張、めまい、および。 弱点。.
報告されている心血管系の影響。 以下を含めます:伝導ブロック、起立性低血圧および失神、。 動 ⁇ 、徐脈、心房細動、心筋 ⁇ 塞、心臓。 逮捕、不整脈、心室を含む心室異所性活動。 頻脈とQT延長。. 市販後調査では、QTが延長されました。 間隔、トルサードドポワント、心室頻脈が報告されています。 1日あたり100 mg以下の用量でトラゾドンの即時放出型を使用。 .
薬物相互作用。
モノアミンオキシダーゼ阻害剤(MAOI)。
セロトニン作動薬。
中央神経系(CNS)抑制剤。
トラゾドンはアルコールに対する反応を高めるかもしれません。 バルビツール酸塩、およびその他のCNS抑制剤。.
チトクロームP450 3A4阻害剤。
In vitroの薬物代謝研究は、あることを示唆しています。 トラゾドンがチトクロームP450とともに投与された場合の薬物相互作用の可能性。 3A4(CYP3A4)阻害剤。. リトナビルの短期投与の影響。 (200 mgを1日2回、4回投与)単回投与の薬物動態について。 トラゾドン(50 mg)は10人の健康な被験者で研究されています。. のCmax。 トラゾドンは34%増加し、AUCは2.4倍に増加し、半減期は増加しました。 2.2倍、クリアランスは52%減少しました。. を含む悪影響。 リトナビルとトラゾドンの場合、吐き気、低血圧、失神が見られました。 同時投与されました。. ケトコナゾール、インジナビル、その他の可能性があります。 イトラコナゾールなどのCYP3A4阻害剤は、大幅な増加につながる可能性があります。 悪影響の可能性があるトラゾドン血漿濃度。. もし。 トラゾドンは強力なCYP3A4阻害剤とともに使用されます。これは心臓のリスクです。 不整脈は増加し、低下する可能性があります。 トラゾドンの投与量を検討する必要があります。.
チトクロームP450インデューサー(例:.、カルバマゼピン)。
カルバマゼピンはCYP3A4を誘発します。. 共同投与後。 カルバマゼピン400 mg /日、トラゾドン100 mg〜300 mg毎日。 カルバマゼピンはトラゾドンの血漿中濃度を低下させた。 mクロロフェンリピペラジン(活性代謝物)はそれぞれ76%と60%です。 プレカルバマゼピン値と比較。. 患者は注意深く監視されるべきです。 両方を服用するときにトラゾドンの用量を増やす必要があるかどうかを確認します。 薬物。.
ジゴキシンとフェニトイン。
血清ジゴキシンまたはフェニトインレベルの上昇がありました。 これらのいずれかと同時にトラゾドンを投与されている患者で報告されています。 薬物。. 血清レベルを監視し、必要に応じて投与量を調整します。.
NSAID、アスピリン、または凝固または出血に影響を与えるその他の薬物。
セロトニンの関連の可能性のため。 薬物と消化管出血を調節する患者は監視されるべきです。 に関連する出血の潜在的なリスクについて警告しました。 トラゾドンとNSAID、アスピリン、または影響を与えるその他の薬物の併用。 凝固または出血。.
ワルファリン。
変更された(増加または。 減少)ワルファリンとトラゾドンの両方を服用した場合のプロトロンビン時間。.
薬物乱用と依存。
規制物質。
オレプトロは規制物質ではありません。.
虐待。
塩酸トラゾドンはそうではありません。 その可能性について前臨床または臨床試験で体系的に研究されています。 乱用、薬物探索行動の兆候は臨床試験で見られませんでした。 オレプロと。. ただし、aの範囲を予測することは困難です。 CNS活性薬は誤用、転用、乱用されます。. その結果、医師。 薬物乱用の病歴について患者を注意深く評価し、それに従う必要があります。 患者は密接に観察し、トラゾドンの誤用または乱用の兆候がないか観察します。 塩酸塩(例:.、耐性の発達、用量の増加、。 薬物探索行動)。.

妊娠カテゴリーC
塩酸トラゾドンは増加を引き起こすことが示されています。 使用する2つの研究で胎児吸収と胎児へのその他の悪影響。 提案された約30〜50倍の用量レベルで投与した場合のラット。 最大ヒト用量。. 先天性異常も1つ増加しました。 最大ヒト用量の約15〜50倍での3つのウサギの研究の。. 妊娠中の女性を対象とした適切で適切に管理された研究はありません。. オレプロ。 潜在的な利益が正当化する場合にのみ、妊娠中に使用する必要があります。 胎児への潜在的なリスク。.

以下の深刻な副作用が説明されています。 ラベルの他の場所:。
- 臨床的悪化と自殺のリスク。
- セロトニン症候群またはNMS様反応。
- QT延長と突然死のリスク。
- 起立性低血圧。
- 異常な出血イベント。
- 持続勃起症。
- 低ナトリウム血症。
- 認知障害と運動障害。
- 中止症状。
最も一般的な副作用(5%以上と報告されています。 プラセボの2倍の割合)は、傾眠/鎮静、めまいです。 便秘、視力障害。.
表2は、有害事象(AE)の概要を示しています。 少なくとも発生率でオレプトロ治療の中止につながります。 プラセボの1%と少なくとも2倍。.
表2:AEあり。
取られた措置としての中止(≥1%の発生率と2xプラセボの発生率)。
| オレプロ。 N = 202。 |
|
| 傾眠/鎮静。 | 8(4.0%)。 |
| めまい。 | 7(3.5%)。 |
| 混乱状態。 | 2(1.0%)。 |
| 異常な調整。 | 2(1.0%)。 |
| 頭痛。 | 2(1.0%)。 |
| 吐き気。 | 2(1.0%)。 |
| バランス障害/歩行障害。 | 2(1.0%)。 |
臨床研究の経験。
以下に説明するデータ。 暴露された204人を含む406人の患者の臨床試験における暴露を反映している。 プラセボと202をオレプトロに曝露。. 患者は18〜80歳でした。 患者の69.3%と67.5%は、以前にうつ病のエピソードを少なくとも1回経験しました。 プラセボ群とアクティブ治療群の過去24か月間。. に。 個々の患者、用量は柔軟で、1日あたり150〜375 mgの範囲でした。. 6週間の治療期間中の平均1日量は310 mgでした。. タブレット。 経口投与され、1日1回、合計8日間投与されました。 滴定期間を含む週。.
臨床試験があるからです。 大きく異なる条件下で実施され、副作用率が観察されました。 薬物の臨床試験は、その割合と直接比較することはできません。 別の薬物の臨床試験であり、観察された率を反映していない可能性があります。 練習。.
表3は、その概要を示しています。 5%以上の発生率で発生したすべての治療緊急AE。 Oleptroグループ、臨床研究者が関連していると見なしたかどうか。 研究薬かどうか。.
表3:最も一般的。
治療緊急有害事象(アクティブ治療を受けている患者の5%以上)。
| 優先用語。 | プラセボ。 N = 204。 |
オレプロ。 N = 202。 |
| 傾眠/鎮静。 | 39(19%)。 | 93(46%)。 |
| 頭痛。 | 55(27%)。 | 67(33%)。 |
| 口渇。 | 26(13%)。 | 51(25%)。 |
| めまい。 | 25(12%)。 | 50(25%)。 |
| 吐き気。 | 26(13%)。 | 42(21%)。 |
| 疲労。 | 17(8%)。 | 30(15%)。 |
| 下 ⁇ 。 | 23(11%)。 | 19(9%)。 |
| 便秘。 | 4(2%)。 | 16(8%)。 |
| 腰痛。 | 7(3%)。 | 11(5%)。 |
| 視力がぼやけている。 | 0(0%)。 | 11(5%)。 |
性機能不全。
関連する有害事象。 性的機能障害(因果関係に関係なく)は4.9%と1.5%報告されました。 オレプトロとプラセボでそれぞれ治療された患者。. オレプログループでは、 射精障害は患者の1.5%で発生し、性欲の減少が発生しました。 患者の1.5%、勃起不全と異常なオルガスム<1%。 患者。.
バイタルサインと重量。
バイタルサイン(血液)に顕著な変化はありませんでした。 圧力、呼吸数、脈拍)またはいずれかの治療グループの体重。.
以下は、治療に伴う有害性のリストです。 発生率が1%以上5%未満の反応(つまり、.、あまり一般的ではない)で。 オレプロで治療された患者。. このリストは、含めることを意図していません。 反応(i)以前の表またはラベルの他の場所にすでにリストされている。 (ii)治療との関連が遠い、(iii)そうだった。 一般的ではないこと、および(iv)持っているとは見なされなかった。 重大な臨床的影響。. 反応は身体系によって分類されます。 次の定義を使用します。頻繁な副作用が発生しています。 少なくとも1/100人の患者; まれ。 副作用はそれらです。 1/100未満の患者で発生します。.
耳と迷路の障害—。 まれ。:。 視力低下、耳鳴り、めまい。
眼疾患—。 頻繁。:視覚障害;。 まれ。:ドライアイ、目の痛み、恐怖症。
胃腸障害—。 頻繁。:。 腹痛、 ⁇ 吐;。 まれ。:逆流性食道炎。
一般的な障害と管理サイトの条件—。 頻繁。:浮腫;。 まれ。:歩行障害。
免疫系障害—。 まれ。:。 過敏症。
筋骨格系および結合組織障害—。 頻繁。:筋骨格系の苦情、筋肉痛;。 まれ。:筋肉。 けいれん。
神経系障害—。 頻繁。:調整。 異常、味覚異常、記憶障害、片頭痛、感覚異常、振戦; まれ。:。 健忘症、失語症、知覚低下、言語障害。
精神障害—。 頻繁。:興奮、。 混乱状態、見当識障害。
腎障害と尿障害— 頻繁。:。 排尿の緊急性;。 まれ。: ⁇ の痛み、尿失禁。
呼吸器、胸部および縦隔障害— 頻繁。:呼吸困難。
皮膚および皮下組織障害—。 頻繁。:。 寝汗;。 まれ。:にきび、多汗症、光線過敏症反応。
血管障害—。 まれ。:紅潮。
市販後の経験。
塩酸トラゾドンに関する自発的報告。 市販後の経験から受け取ったものには、次のものがあります。 興奮、脱毛症、不安症、失語症、無呼吸、乳房肥大または。 充血、心 ⁇ 、脳血管障害、悪寒、胆 ⁇ うっ滞。 陰核、うっ血性心不全、複視、浮腫、 ⁇ 体外路症状、 壮大な発作、幻覚、溶血性貧血、多毛症、。 高ビリルビン血症、アミラーゼの増加、 ⁇ 液分 ⁇ の増加、不眠症。 白血球増加症、白血球減少症、黄 ⁇ 、授乳、肝酵素の変化、 メテモグロビン血症、吐き気/ ⁇ 吐(最も頻繁に)、感覚異常、妄想。 反応、持続勃起症、そう ⁇ 、乾 ⁇ 、精神病、発疹、 ⁇ 睡、。 不適切なADH症候群、遅発性ジスキネジア、原因不明の死、尿。 失禁、尿閉、じんま疹、血管拡張、めまい、および。 弱点。.
報告されている心血管系の影響。 以下を含めます:伝導ブロック、起立性低血圧および失神、。 動 ⁇ 、徐脈、心房細動、心筋 ⁇ 塞、心臓。 逮捕、不整脈、心室を含む心室異所性活動。 頻脈とQT延長。. 市販後調査では、QTが延長されました。 間隔、トルサードドポワント、心室頻脈が報告されています。 1日あたり100 mg以下の用量でトラゾドンの即時放出型を使用。 .

人間の経験。
関連する健康リスクが予想されます。 オレプトロの過剰摂取は、おそらくトラゾドンのそれに似ています。 即時放出製剤。.
過剰摂取による死亡は、摂取した患者で発生しています。 トラゾドンと他のCNS抑制薬(アルコール、アルコール、 水酸クロラールとジアゼパム;アモバルビタール;クロルジアゼポキシド;またはメプロバメート)。.
報告された最も深刻な反応は、 トラゾドンだけの過剰摂取は、持続勃起症、呼吸停止、発作でした。 QT延長を含むECGの変更。. 反応が最も多く報告された。 眠気と ⁇ 吐が頻繁にありました。. 過剰摂取は増加を引き起こす可能性があります。 報告された副作用の発生率または重症度。.
過剰摂取の管理。
オレプトロの過剰摂取に対する特定の解毒剤はありません。.
治療はそれらの一般的な対策で構成されるべきです。 に有効な薬物による過剰摂取の管理に採用されています。 大うつ病性障害の治療。. 適切な気道、酸素化を確保します。 と換気。. 心臓のリズムとバイタルサインを監視します。.
一般的な支援的および対症療法もです。 おすすめ。. ⁇ 吐の誘発は推奨されません。. 胃洗浄液。 必要に応じて、適切な気道保護を備えた大口径の ⁇ 体チューブを使用できます。 摂取直後に、または症候性患者で実施された場合に示されます。. 活性炭を投与する必要があります。. 強制利尿は有用かもしれません。 薬物の排除を促進する。.
過剰摂取の管理では、その可能性を検討してください。 複数の薬物関与。. 医師は毒との接触を検討する必要があります。 過剰摂取の治療に関する追加情報のためのコントロールセンター。.

前臨床試験では、そのトラゾドンが選択的に示されています。 セロトニンの神経再取り込みを阻害し、5-HT-2A / 2Cで ⁇ 抗薬として機能します。 セロトニン受容体。.
トラゾドンはモノアミンオキシダーゼ阻害剤ではありません。 アンフェタミンタイプの薬とは異なり、中枢神経系を刺激しません。.
トラゾドンはアルファ1アドレナリン受容体に ⁇ 抗します。 姿勢性低血圧に関連している可能性のあるプロパティ。.

トラゾドンの定常状態のAUCは、その後も同等です。 トラゾドン100 mg即時放出(IR)を1日3回投与。 (平均±SD AUCss = 33058±8006 ng * h / mL)およびOleptro 300 mgを1日1回(平均±。 SD AUCss = 29131±9931 ng * h / mL)1週間。. 定常状態のCmaxとCmin。 トラゾドン100 mg IR 3の投与後、トラゾドンは同等ではありませんでした。 1日1回(平均±SD Cmax、ss = 3118±758 ng / mL、Cmin、ss = 843±274 ng / mL)。 オレプロ300 mgを1日1回(平均±SD Cmax、ss = 1812±621 ng / mL、Cmin、ss =。 674±355 ng / mL)1週間。.
吸収。
トラゾドンは経口投与後によく吸収されます。 組織に選択的な局在なし。. 単回投与後。 空腹時条件下でのオレプトロ300 mg錠剤の投与、平均ピーク。 1188±362 ng / mLのトラゾドン血漿濃度(Cmax)はaで報告されました。 投与後9時間の中央値Tmax。. Oleptro 300 mg錠剤を間もなく服用する場合。 高脂肪食の摂取後、Cmaxはと比較して約86%増加します。 空腹時にそれを取る。. ただし、AUC0-∞とTmaxはそうではありません。 食物の影響を大幅に受けます。.
オレプトロ錠は、投与量に比例します。 無傷または75 mgから375 mgの範囲の用量の単回投与。 二等分された錠剤。.
代謝。
In vitro。 ヒト肝ミクロソームの研究が示しています。 トラゾドンは、酸化的切断を介して代謝され、活性代謝物になります。 CYP3A4によるm-クロロフェニルピペラジン(mCPP)。. かもしれない他の代謝経路。 トラゾドンの代謝に関与することは十分に特徴付けられていません。. トラゾドンは広範囲に代謝されます。経口投与量の1%未満が排 ⁇ されます。 尿中で変化なし。.
除去。
排 ⁇ は主に腎臓であり、70〜75%のanです。 経口投与量は、摂取後72時間以内に尿中に回収されます。. Oleptro 300 mg錠剤の単回投与後、平均は明らかです。 10時間の最終半減期が報告されました。.
タンパク質結合。
トラゾドンは89〜95%のタンパク質結合です。 in vitro。 で。 ヒトの治療用量で達成された濃度。.
However, we will provide data for each active ingredient


