









Komposition:
Anwendung:
Medizinisch geprüft von Kovalenko Svetlana Olegovna, Apotheke Zuletzt aktualisiert am 05.04.2022

Achtung! Die Informationen auf der Seite sind nur für medizinisches Fachpersonal! Die Informationen werden in öffentlichen Quellen gesammelt und können aussagekräftige Fehler enthalten! Seien Sie vorsichtig und überprüfen Sie alle Informationen auf dieser Seite!
Top 20 Medikamente mit den gleichen Inhaltsstoffen:


Dosierungsformen und Stärken
Oleptro-Tabletten sind in folgenden Stärken erhältlich:
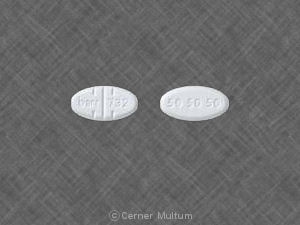
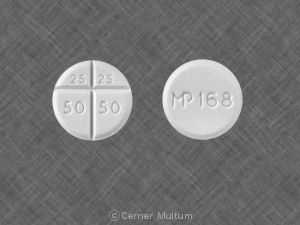
- Oleptro-Bisectable-Tabletten mit 150 mg Trazodon Hydrochlorid (gelblich-beige, kapselförmige Tablette, beschichtet und bewertet beide Seiten mit DDS 080 auf einer Seite gedruckt)
- Oleptro-Bisectable-Tabletten mit 300 mg Trazodon Hydrochlorid (beige-orange, kapselförmige Tablette, beschichtet und auf beiden geritzt Seiten mit DDS 081 auf einer Seite gedruckt)
Lagerung und Handhabung
Oleptro 150 mg ist gelblich-beige, kapselförmig Tablette mit verlängerter Freisetzung, beidseitig beschichtet und mit DDS 080 bedruckt auf einer Seite. Es wird wie folgt geliefert:
Flaschen mit 30 Tabletten NDC 43595-080-03
Oleptro 300 mg ist beige-orange, kapselförmig Tablette mit verlängerter Freisetzung, beidseitig beschichtet und mit DDS 081 bedruckt auf einer Seite. Es wird wie folgt geliefert:
Flaschen mit 30 Tabletten NDC 43595-081-03
Bei Raumtemperatur (15 - 30 ° C) fest lagern lichtbeständige Behälter.
Angelini Pharma Inc. Gaithersburg, MD 20877. Überarbeitet: Juli 2014

Oleptro ™ ist zur Behandlung von Major indiziert depressive Störung (MDD) bei Erwachsenen. Die Wirksamkeit von Oleptro war in einem Versuch von ambulanten Patienten mit MDD sowie in Versuchen mit dem Formulierung von Trazodon mit sofortiger Freisetzung.

Dosisauswahl
Die empfohlene Anfangsdosis von Oleptro beträgt 150 mg einmal täglich bei Erwachsenen. Die Dosis kann alle drei Tage um 75 mg / Tag erhöht werden (d. H., Beginnen Sie 225 mg am Tag 4 der Therapie. Die maximale Tagesdosis sollte 375 nicht überschreiten mg.
- Oleptro-Tabletten sollten gleichzeitig oral eingenommen werden jeden Tag, am späten Abend, vorzugsweise vor dem Schlafengehen, auf nüchternen Magen.
- Sobald eine angemessene Reaktion erreicht ist, kann die Dosierung erreicht werden schrittweise reduziert werden, wobei die anschließende Anpassung vom Therapeutikum abhängt Antwort.
- Die Patienten sollten wann auf Entzugssymptome überwacht werden Absetzen der Behandlung mit Trazodonhydrochlorid. Die Dosis sollte sein nach Möglichkeit schrittweise reduziert.
Erhaltungsbehandlung
Die Wirksamkeit von Oleptro bei der Erhaltungstherapie von MDD wurde nicht bewertet. Es gibt zwar keine Beweise dafür Beantworten Sie die Frage, wie lange ein mit Oleptro behandelter Patient fortfahren soll Für das Medikament wird allgemein empfohlen, die Behandlung für mehrere fortzusetzen Monate nach einer ersten Antwort. Die Patienten sollten auf dem niedrigsten Stand gehalten werden wirksame Dosis und regelmäßig überprüft werden, um den anhaltenden Bedarf zu bestimmen zur Erhaltungstherapie.
Wechseln eines Patienten zu oder von einer Monoaminoxidase Inhibitor (MAOI) zur Behandlung von psychiatrischen Störungen
Zwischen dem Absetzen von sollten mindestens 14 Tage vergehen ein MAOI zur Behandlung von psychiatrischen Störungen und zum Beginn der Therapie mit Oleptro. Umgekehrt sollten nach dem Absetzen von Oleptro mindestens 14 Tage zulässig sein vor Beginn eines MAOI zur Behandlung von psychiatrischen Störungen.
Verwendung von Oleptro mit anderen MAOs wie Linezolid oder Methylen Blau
Starten Sie Oleptro nicht bei einem behandelten Patienten mit linezolid oder intravenösem Methylenblau, da ein erhöhtes Risiko besteht des Serotonin-Syndroms. Bei einem Patienten, der eine dringlichere Behandlung von a benötigt psychiatrische Erkrankung, andere Interventionen, einschließlich Krankenhausaufenthalt, sollten berücksichtigt werden.
In einigen Fällen erhält ein Patient bereits Oleptro Die Therapie kann eine dringende Behandlung mit Linezolid oder intravenösem Methylen erfordern blau. Wenn akzeptable Alternativen zu Linezolid oder intravenösem Methylenblau Behandlung sind nicht verfügbar und die potenziellen Vorteile von Linezolid oder Die intravenöse Behandlung mit Methylenblau überwiegt das Risiko von Das Serotonin-Syndrom bei einem bestimmten Patienten, Oleptro, sollte sofort gestoppt werden und linezolid oder intravenös Methylenblau kann verabreicht werden. Der Patient sollte zwei Wochen oder bis auf Symptome des Serotonin-Syndroms überwacht werden 24 Stunden nach der letzten Dosis von Linezolid oder intravenösem Methylenblau was auch immer zuerst kommt. Die Therapie mit Oleptro kann 24 Stunden nach dem letzte Dosis von Linezolid oder intravenösem Methylenblau.
Das Risiko der Verabreichung von Methylenblau durch nicht intravenöse Wege (wie orale Tabletten oder durch lokale Injektion) oder in intravenöse Dosen von viel weniger als 1 mg / kg mit Oleptro sind unklar. Das Der Kliniker sollte sich jedoch der Möglichkeit eines Auftretens bewusst sein Symptome des Serotonin-Syndroms bei einer solchen Anwendung (siehe WARNHINWEISE UND VORSICHTSMASSNAHMEN].
Wichtige Anweisungen zur Verwaltung
Oleptro-Tabletten werden bewertet, um Flexibilität zu bieten Dosierung.
Oleptro kann ganz geschluckt oder zur Hälfte verabreicht werden Tablette durch Brechen des Tablets entlang der Score-Linie. Das Tablet halbieren hat keinen Einfluss auf die Eigenschaften des Tablets mit kontrollierter Freisetzung.
Um seine Eigenschaften mit kontrollierter Freisetzung aufrechtzuerhalten, Oleptro darf nicht gekaut oder zerkleinert werden.

Monoaminoxidasehemmer (MAOIs)
Die Verwendung von MAOI zur Behandlung von psychiatrischen Störungen mit Oleptro oder innerhalb von 14 Tagen nach Beendigung der Behandlung mit Oleptro ist kontraindiziert wegen eines erhöhten Risikos des Serotonin-Syndroms. Die Verwendung von Oleptro innerhalb von 14 Tagen nach Absetzen eines MAOI zur Behandlung von psychiatrischen Behandlungen Störungen sind ebenfalls kontraindiziert..
Beginn von Oleptro bei einem Patienten, mit dem behandelt wird MAOs wie Linezolid oder intravenöses Methylenblau sind ebenfalls kontraindiziert wegen eines erhöhten Risikos für ein Serotonin-Syndrom.

WARNHINWEISE
Im Rahmen der enthalten VORSICHTSMASSNAHMEN Sektion.
VORSICHTSMASSNAHMEN
Klinische Verschlechterung und Suizidrisiko
Patienten mit Major Depression (MDD), beide erwachsen und pädiatrisch können eine Verschlechterung ihrer Depression und / oder der Entstehung von Selbstmordgedanken und -verhalten (Suizidalität) oder ungewöhnlichen Veränderungen in Verhalten, unabhängig davon, ob sie Antidepressiva einnehmen oder nicht, und dies Das Risiko kann bestehen bleiben, bis eine signifikante Remission auftritt. Selbstmord ist ein bekanntes Risiko für Depressionen und bestimmte andere psychiatrische Störungen und diese Störungen selbst sind die stärksten Prädiktoren für Selbstmord. Es hat lange gedauert ständige Besorgnis darüber, dass Antidepressiva eine Rolle bei der Induktion spielen könnten Verschlechterung der Depression und Auftreten von Suizidalität bei bestimmten Patienten während der frühen Behandlungsphasen. Gepoolte kurzfristige Analysen placebokontrollierte Studien mit Antidepressiva (SSRIs und andere) zeigten dass diese Medikamente das Risiko von Selbstmorddenken und -verhalten erhöhen (Suizidalität) bei Kindern, Jugendlichen und jungen Erwachsenen (18 - 24 Jahre) mit MDD und andere psychiatrische Störungen. Kurzzeitstudien zeigten keine Erhöhung des Suiziditätsrisikos mit Antidepressiva im Vergleich zu Placebo in Erwachsene über 24 Jahre; Es gab eine Reduktion mit Antidepressiva im Vergleich zu Placebo bei Erwachsenen ab 65 Jahren.
Die gepoolten Analysen placebokontrollierter Studien in Kinder und Jugendliche mit MDD, Zwangsstörung (OCD) oder Weitere psychiatrische Störungen umfassten insgesamt 24 Kurzzeitstudien von 9 Antidepressiva bei über 4.400 Patienten. Die gepoolten Analysen von placebokontrollierte Studien bei Erwachsenen mit MDD oder anderen psychiatrischen Störungen umfasste insgesamt 295 Kurzzeitstudien (Mediandauer von 2 Monaten) von 11 Antidepressiva bei über 77.000 Patienten. Es gab erhebliche Unterschiede im Risiko der Suizidalität unter Drogen, aber eine Tendenz zu einer Zunahme der jüngere Patienten für fast alle untersuchten Medikamente. Es gab Unterschiede in absolutes Suiziditätsrisiko über die verschiedenen Indikationen hinweg mit dem höchsten Inzidenz in MDD. Die Risikounterschiede (Arzneimittel vs. Placebo) waren jedoch relativ stabil innerhalb der Altersschichten und zwischen den Indikationen. Dieses Risiko Unterschiede (Drogen-Placebo-Unterschied in der Anzahl der Fälle von Suizidalität pro 1.000 behandelte Patienten) sind in Tabelle 1 aufgeführt.
Tabelle 1
| Altersspanne | Arzneimittel-Placebo-Unterschied in der Anzahl der Fälle von Suizidalität pro 1.000 behandelten Patienten |
| Erhöht sich im Vergleich zu Placebo | |
| <18 | 14 weitere Fälle |
| 18 - 24 | 5 zusätzliche Fälle |
| Verringert sich im Vergleich zu Placebo | |
| 25 - 64 | 1 Fall weniger |
| ≥ 65 | 6 weniger Fälle |
In keinem von ihnen traten Selbstmorde auf die pädiatrischen Studien. Es gab Selbstmorde in den Erwachsenenversuchen, aber die Anzahl reichte nicht aus, um eine Schlussfolgerung über die Drogenwirkung auf den Selbstmord zu ziehen.
Es ist nicht bekannt, ob die Das Suizidalitätsrisiko erstreckt sich auf die längerfristige Verwendung, d.h.über mehrere Monate hinaus. Es gibt jedoch wesentliche Hinweise auf eine placebokontrollierte Wartung Studien bei Erwachsenen mit Depressionen, bei denen die Verwendung von Antidepressiva die verzögern kann Wiederauftreten von Depressionen.
Alle behandelten Patienten mit Antidepressiva für jede Indikation sollte angemessen überwacht werden und eng beobachtet auf klinische Verschlechterung, Suizidalität und ungewöhnliche Veränderungen in Verhalten, insbesondere in den ersten Monaten eines medikamentösen Therapieverlaufs oder zu Zeiten von Dosisänderungen entweder erhöht oder verringert.
Die folgenden Symptome Angst, Unruhe, Panikattacken, Schlaflosigkeit, Reizbarkeit, Feindseligkeit Aggressivität, Impulsivität, Akathisie (psychomotorische Unruhe), Hypomanie, und Manie wurden bei behandelten erwachsenen und pädiatrischen Patienten berichtet mit Antidepressiva bei Major Depression sowie bei anderen Indikationen, sowohl psychiatrisch als auch nichtpsychiatrisch. Obwohl ein Kausalzusammenhang zwischen dem Auftreten solcher Symptome und entweder der Verschlechterung der Depression und / oder die Entstehung von Selbstmordimpulsen wurde dort nicht festgestellt Bedenken, dass solche Symptome Vorläufer einer aufkommenden Suizidalität darstellen könnten.
Überlegungen sollten angestellt werden das therapeutische Regime zu ändern, einschließlich möglicherweise das Absetzen des Medikamente bei Patienten, deren Depression anhaltend schlimmer ist oder die es sind Auftreten einer aufkommenden Suizidalität oder von Symptomen, die Vorläufer sein könnten Verschlechterung der Depression oder Suizidalität, insbesondere wenn diese Symptome schwerwiegend sind, abrupt zu Beginn oder nicht Teil der Symptome des Patienten.
Familien und Betreuer von Patienten, die mit Antidepressiva wegen einer Major Depression behandelt werden oder andere psychiatrische und nichtpsychiatrische Indikationen sollten beachtet werden die Notwendigkeit, Patienten auf das Auftreten von Unruhe, Reizbarkeit zu überwachen, ungewöhnliche Verhaltensänderungen und die anderen oben beschriebenen Symptome sowie das Auftreten von Suizidalität und solche Symptome sofort der Gesundheit zu melden Pflegedienstleister. Eine solche Überwachung sollte beinhalten die tägliche Beobachtung durch Familien und Betreuer. Rezepte für Oleptro sollten für die geschrieben werden kleinste Menge Tabletten, die mit einem guten Patientenmanagement vereinbar ist das Risiko einer Überdosierung zu verringern.
Serotonin-Syndrom
Die Entwicklung eines Bei SNRIs wurde über ein möglicherweise lebensbedrohliches Serotonin-Syndrom berichtet und SSRIs, einschließlich Oleptro, allein, insbesondere aber bei gleichzeitiger Anwendung von andere serotonerge Arzneimittel (einschließlich Triptane, trizyklische Antidepressiva) Fentanyl, Lithium, Tramadol, Tryptophan, Busipiron und St. Johanniskraut) und mit Arzneimitteln, die den Metabolismus von Serotonin beeinträchtigen (insbesondere MAOs, beide diejenigen, die psychiatrische Störungen behandeln sollen, und auch andere, wie z linezolid und intravenös Methylenblau).
Symptome des Serotonin-Syndroms können mentale Statusänderungen einschließen (z.Agitation, Halluzinationen, Delir und Koma), autonome Instabilität (z.Tachykardie, labiler Blutdruck Schwindel, Diaphorese, Spülung, Hyperthermie), neuromuskuläre Symptome (z., Zittern, Steifigkeit, Myoklonus, Hyperreflexie, Inkoordination), Krampfanfälle und / oder gastrointestinale Symptome (z.Übelkeit, Erbrechen, Durchfall). Patienten sollten auf das Auftreten des Serotonin-Syndroms überwacht werden.
Die gleichzeitige Anwendung von Oleptro mit MAOs zur Behandlung von psychiatrischen Störungen ist kontraindiziert. Oleptro sollte auch nicht bei einem Patienten begonnen werden, der mit MAOs wie behandelt wird linezolid oder intravenös Methylenblau. Alle Berichte mit Methylenblau das lieferte Informationen zum Verabreichungsweg intravenös Verabreichung im Dosisbereich von 1 mg / kg bis 8 mg / kg. Keine Berichte beteiligt die Verabreichung von Methylenblau auf anderen Wegen (wie oralen Tabletten oder lokale Gewebeinjektion) oder in niedrigeren Dosen. Es kann Umstände geben, unter denen es ist notwendig, um die Behandlung mit einem MAOI wie Linezolid oder zu beginnen intravenöses Methylenblau bei einem Patienten, der Oleptro einnimmt. Oleptro sollte sein vor Beginn der Behandlung mit dem MAOI abgebrochen ..
Bei gleichzeitiger Anwendung von Oleptro mit anderen serotonergen Medikamente, Triptane, trizyklische Antidepressiva, Fentanyl, Lithium, Tramadol, Buspiron, Tryptophan und St. Johns Wort ist klinisch gerechtfertigt, Patienten sollte auf ein potenziell erhöhtes Risiko für das Serotonin-Syndrom aufmerksam gemacht werden insbesondere während des Behandlungsbeginns und Dosiserhöhungen.
Behandlung mit Oleptro und allen damit einhergehenden Serotonergen Agenten sollten sofort abgesetzt werden, wenn die oben genannten Ereignisse auftreten und Eine unterstützende symptomatische Behandlung sollte eingeleitet werden.
Winkelverschluss Glaukom
Die Pupillardilatation, die nach Verwendung vieler auftritt Antidepressiva, einschließlich Oleptro, können einen Winkelverschlussangriff in a auslösen Patient mit anatomisch engen Winkeln, der keine patentierte Iridektomie hat.
Screening von Patienten auf bipolare Störung und Überwachung auf Manie / Hypomanie
Eine Major Depression Episode kann die Initiale sein Darstellung der bipolaren Störung. Es wird allgemein angenommen (wenn auch nicht in kontrollierten Studien festgestellt), dass die Behandlung einer solchen Episode mit einem Antidepressivum allein kann die Wahrscheinlichkeit eines Niederschlags von a erhöhen gemischte / manische Episode bei Patienten mit Risiko für bipolare Störungen. Ob einer von Die für die klinische Verschlechterung und das Suizidrisiko beschriebenen Symptome stellen eine solche dar Konvertierung ist unbekannt. Vor Beginn der Behandlung mit einem Antidepressivum, Patienten mit depressiven Symptomen sollten angemessen untersucht werden um festzustellen, ob sie einem Risiko für eine bipolare Störung ausgesetzt sind; ein solches Screening sollte eine detaillierte psychiatrische Vorgeschichte enthalten, einschließlich einer Familiengeschichte von Selbstmord, bipolare Störung und Depression. Es ist zu beachten, dass Oleptro dies nicht ist zugelassen zur Behandlung von bipolaren Depressionen.
QT-Verlängerung und Risiko eines plötzlichen Todes
Es ist bekannt, dass Trazodon das QT / QTc-Intervall verlängert. Etwas Medikamente, die das QT / QTc-Intervall verlängern, können Torsades de Pointes mit verursachen plötzlicher, ungeklärter Tod. Die Beziehung der QT-Verlängerung ist am deutlichsten größere Erhöhungen (20 ms und mehr), aber es ist möglich, dass kleinere QT / QTc Verlängerungen können auch das Risiko erhöhen, insbesondere bei anfälligen Personen wie diejenigen mit Hypokaliämie, Hypomagnesiämie oder einer genetischen Veranlagung zu verlängerte QT / QTc.
Obwohl Torsades de Pointes nicht beobachtet wurde Die Verwendung von Oleptro in empfohlenen Dosen in Vormarketing-Studien ist eine Erfahrung zu begrenzt, um ein erhöhtes Risiko auszuschließen. Es gab jedoch Postmarketing-Berichte von Torsades de Pointes mit der Form der sofortigen Veröffentlichung von Trazodon (in Gegenwart mehrerer Störfaktoren), auch bei Dosen von 100 mg pro Tag oder weniger.
Anwendung bei Patienten mit Herzerkrankungen
Trazodonhydrochlorid wird während der Anwendung nicht empfohlen die anfängliche Erholungsphase des Myokardinfarkts.
Bei der Verabreichung von Oleptro ist Vorsicht geboten Patienten mit Herzerkrankungen und solchen Patienten sollten engmaschig überwacht werden da Antidepressiva (einschließlich Trazodonhydrochlorid) verursachen können Herzrhythmusstörungen.
Bei der Trazodontherapie wurde über eine QT-Verlängerung berichtet. Klinische Studien bei Patienten mit bereits bestehende Herzerkrankungen weisen darauf hin, dass Trazodonhydrochlorid sein kann arrhythmogen bei einigen Patienten in dieser Population. Arrhythmien identifiziert Dazu gehören isolierte PVCs, ventrikuläre Couplets, Tachykardie mit Synkope und Torsades de Pointes. Postmarketing-Ereignisse wurden in Dosen von 100 mg berichtet oder weniger mit der Form von Trazodon mit sofortiger Freisetzung.
Gleichzeitige Verabreichung von Arzneimitteln, die die QT verlängern Intervall oder das CYP3A4-Inhibitoren sind, kann das Herzrisiko erhöhen Arrhythmie.
Orthostatische Hypotonie und Synkope
Hypotonie, einschließlich orthostatischer Hypotonie und Bei Patienten, die Trazodonhydrochlorid erhielten, wurde über eine Synkope berichtet. Die gleichzeitige Anwendung mit einem blutdrucksenkenden Mittel kann eine Reduzierung der Dosis von erfordern das blutdrucksenkende Medikament.
Abnormale Blutungen
Postmarketing-Daten haben einen Zusammenhang zwischen der Verwendung gezeigt von Arzneimitteln, die das Wiederauftreten von Serotonin und das Auftreten von stören gastrointestinale (GI) Blutungen. Während keine Assoziation zwischen Trazodon und Blutungsereignisse, insbesondere GI-Blutungen, wurden gezeigt, Patienten sollten es sein gewarnt über das potenzielle Blutungsrisiko im Zusammenhang mit der gleichzeitigen Anwendung von Trazodon und NSAIDs, Aspirin oder anderen Arzneimitteln, die die Gerinnung beeinflussen, oder Blutung. Andere Blutungsereignisse im Zusammenhang mit SSRIs und SNRIs reichten von Ekchymose, Hämatom, Nasenbluten und Petechien zu lebensbedrohlichen Blutungen.
Interaktion mit MAOIs
Bei Patienten, die in Kombination serotonerge Medikamente erhalten Bei einem Monoaminoxidasehemmer (MAOI) wurde über schwerwiegende Berichte berichtet manchmal tödliche Reaktionen wie Hyperthermie, Steifigkeit, Myoklonus autonome Instabilität mit schnellen Schwankungen der Vitalfunktionen und des mentalen Status Änderungen, die extreme Erregung beinhalten, die zu Delir und Koma führt. Diese Reaktionen wurden auch bei Patienten berichtet, die kürzlich abgesetzt haben Antidepressivum-Behandlung und wurde mit einem MAOI begonnen. Einige Fälle vorgestellt mit Merkmalen, die dem malignen neuroleptischen Syndrom ähneln. Darüber hinaus begrenzt Tierdaten zu den Auswirkungen der kombinierten Verwendung von serotonergen Antidepressiva und MAOs schlagen vor, dass diese Medikamente synergistisch wirken können, um den Blutdruck zu erhöhen und Verhaltensanregung hervorrufen. Daher wird Oleptro empfohlen sollte nicht in Kombination mit einem MAOI oder innerhalb von 14 Tagen nach verwendet werden Absetzen der Behandlung mit einem MAOI. Ebenso sollten mindestens 14 Tage sein erlaubt nach dem Stoppen von Oleptro vor dem Starten eines MAOI .
Priapismus
Seltene Fälle von Priapismus (schmerzhafte Erektionen größer als 6 Stunden Dauer) wurden bei Männern gemeldet, die Trazodon erhielten. Priapismus, wenn nicht sofort behandelt, kann zu irreversiblen Schäden am erektilen Gewebe führen. Männer die eine Erektion von mehr als 6 Stunden haben, ob schmerzhaft oder nicht, sollte das Medikament sofort absetzen und einen Arzt aufsuchen.
Trazodon sollte bei Männern mit Vorsicht angewendet werden Bedingungen, die sie für Priapismus prädisponieren könnten (z.Sichelzellenanämie multiple Myelome oder Leukämie) oder bei Männern mit anatomischer Verformung der Penis (z.Angulation, Kavernosfibrose oder Peyronie-Krankheit).
Hyponatriämie
Hyponatriämie kann als Ergebnis der Behandlung mit auftreten Antidepressiva. In vielen Fällen scheint diese Hyponatriämie das Ergebnis zu sein das Syndrom der unangemessenen antidiuretischen Hormonsekretion (SIADH). Fälle mit Serumnatrium unter 110 mmol / l wurden berichtet. Ältere Patienten kann ein höheres Risiko für die Entwicklung einer Hyponatriämie mit Antidepressiva haben. Ebenfalls Patienten, die Diuretika einnehmen oder auf andere Weise volumenarm sind, können sich an höheres Risiko. Das Absetzen von Oleptro sollte bei Patienten mit in Betracht gezogen werden symptomatische Hyponatriämie und geeignete medizinische Intervention sollten sein eingeführt.
Anzeichen und Symptome einer Hyponatriämie sind Kopfschmerzen Konzentrationsschwierigkeiten, Gedächtnisstörungen, Verwirrung, Schwäche und Unstetigkeit, die zu Stürzen führen kann. Anzeichen und Symptome im Zusammenhang mit mehr Zu den schweren und / oder akuten Fällen gehörten Halluzinationen, Synkopen, Anfälle, Koma Atemstillstand und Tod.
Potenzial für kognitive und motorische Beeinträchtigungen
Oleptro kann Schläfrigkeit oder Sedierung verursachen und beeinträchtigen die geistigen und / oder körperlichen Fähigkeiten, die für die Leistung von potenziell erforderlich sind gefährliche Aufgaben. Patienten sollten vor gefährlichen Operationen gewarnt werden Maschinen, einschließlich Autos, bis sie einigermaßen sicher sind, dass die Die medikamentöse Behandlung wirkt sich nicht nachteilig auf sie aus.
Abbruchsymptome
Entzugssymptome wie Angst, Unruhe und Schlafstörungen wurden mit Trazodon gemeldet. Klinische Erfahrung schlägt vor, die Dosis vor Abschluss schrittweise zu reduzieren Absetzen der Behandlung.
Informationen zur Patientenberatung
Sehen Medikamente Führen.
Informationen für Patienten
Verschreiber oder andere Angehörige der Gesundheitsberufe sollten informieren Patienten, ihre Familien und ihre Betreuer über die Vorteile und Risiken verbunden mit der Behandlung mit Oleptro und sollte sie in seiner beraten angemessene Verwendung.
Patienten sollten davor gewarnt werden
- Es besteht die Möglichkeit eines erhöhten Selbstmordrisikos Gedanken besonders bei Kindern, Jugendlichen und jungen Erwachsenen.
- Die folgenden Symptome sollten dem gemeldet werden Arzt: Angstzustände, Unruhe, Panikattacken, Schlaflosigkeit, Reizbarkeit, Feindseligkeit, Aggressivität, Impulsivität, Akathisie, Hypomanie und Manie.
- Sie sollten ihren Arzt informieren, wenn sie eine Vorgeschichte haben von bipolarer Störung, Herzerkrankung oder Myokardinfarkt.
- Das Serotonin-Syndrom kann auftreten und Symptome können sein Änderungen des mentalen Status (z., Unruhe, Halluzinationen und Koma), autonom Instabilität (z.Tachykardie, labiler Blutdruck und Hyperthermie) neuromuskuläre Aberrationen (z.Hyperreflexie, Inkoordination) und / oder Magen-Darm Symptome (z.Übelkeit, Erbrechen und Durchfall).
- Patienten sollten darauf hingewiesen werden, dass die Einnahme von Oleptro eine Ursache sein kann leichte Pupillardilatation, die bei anfälligen Personen zu einer führen kann Folge des Winkelverschlussglaukoms. Vorbestehendes Glaukom ist fast immer Offenwinkelglaukom, da bei Diagnose ein Winkelverschlussglaukom diagnostiziert werden kann endgültig mit Iridektomie behandelt. Offenwinkelglaukom ist kein Risikofaktor für Winkelverschlussglaukom. Patienten möchten möglicherweise untersucht werden, um festzustellen ob sie anfällig für Winkelschließungen sind und eine Prophylaxe haben Verfahren (z., Iridektomie), wenn sie anfällig sind.
- Trazodonhydrochlorid wurde mit dem assoziiert Auftreten von Priapismus.
- Es besteht die Möglichkeit einer Hypotonie, einschließlich orthostatische Hypotonie und Synkope.
- Es besteht ein potenzielles Blutungsrisiko (einschließlich lebensbedrohliche Blutungen) und blutungsbedingte Ereignisse (einschließlich Ekchymose, Hämatom, Nasenbluten und Petechien) bei gleichzeitiger Anwendung von Trazodonhydrochlorid und NSAIDs, Aspirin oder andere Arzneimittel, die diese betreffen Gerinnung oder Blutung.
- Entzugssymptome wie Angst, Unruhe und Schlafstörungen wurden mit Trazodon gemeldet. Klinische Erfahrung schlägt vor, die Dosis schrittweise zu reduzieren.
Patienten sollten das beraten werden
- Oleptro kann Schläfrigkeit oder Sedierung verursachen und beeinträchtigen die geistigen und / oder körperlichen Fähigkeiten, die für die Leistung von potenziell erforderlich sind gefährliche Aufgaben. Patienten sollten vor gefährlichen Operationen gewarnt werden Maschinen, einschließlich Autos, bis sie einigermaßen sicher sind, dass die medikamentöse Behandlung betrifft sie nicht.
- Trazodon kann die Reaktion auf Alkohol verbessern Barbiturate und andere ZNS-Depressiva.
- Frauen, die schwanger werden wollen oder die es sind Das Stillen sollte mit einem Arzt besprochen werden, ob sie fortfahren sollen Oleptro anwenden, da die Anwendung bei schwangeren und stillenden Frauen nicht empfohlen wird.
Wichtige Anweisungen zur Verwaltung
- Oleptro sollte ganz geschluckt oder halbiert werden die Score-Linie.
- Um seine Eigenschaften mit kontrollierter Freisetzung aufrechtzuerhalten, es sollte nicht gekaut oder zerquetscht werden.
- Oleptro sollte jeden Tag zur gleichen Zeit eingenommen werden am späten Abend vorzugsweise vor dem Schlafengehen auf nüchternen Magen.
Nichtklinische Toxikologie
Karzinogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
Es gab kein arzneimittel- oder dosisabhängiges Auftreten einer Karzinogenese offensichtlich bei Ratten, die Trazodon in täglichen oralen Dosen von bis zu 300 mg / kg für 18 erhalten Monate.
Verwendung in bestimmten Populationen
Schwangerschaft
Schwangerschaftskategorie C
Es wurde gezeigt, dass Trazodonhydrochlorid eine erhöhte Ursache darstellt fetale Resorption und andere nachteilige Auswirkungen auf den Fötus in zwei Studien unter Verwendung die Ratte, wenn sie in Dosierungen verabreicht wird, die ungefähr das 30- bis 50-fache des vorgeschlagenen Werts betragen maximale menschliche Dosis. Es gab auch eine Zunahme angeborener Anomalien in einem von drei Kaninchenstudien mit ungefähr dem 15- bis 50-fachen der maximalen menschlichen Dosis. Es gibt keine angemessenen und gut kontrollierten Studien bei schwangeren Frauen. Oleptro sollte während der Schwangerschaft nur angewendet werden, wenn der potenzielle Nutzen dies rechtfertigt potenzielles Risiko für den Fötus.
Stillende Mütter
Trazodon und / oder seine Metaboliten wurden in der gefunden Milch laktierender Ratten, was darauf hindeutet, dass das Medikament in die Muttermilch ausgeschieden werden kann. Vorsicht ist geboten, wenn Oleptro einer stillenden Frau verabreicht wird.
Pädiatrische Anwendung
Sicherheit und Wirksamkeit in der pädiatrischen Bevölkerung haben nicht etabliert. Oleptro darf nicht bei Kindern oder Jugendlichen angewendet werden.
Geriatrische Anwendung
Von 202 Patienten, die in der klinischen Behandlung mit Oleptro behandelt wurden In der Studie waren 9 Patienten älter als 65 Jahre. Keine allgemeinen Sicherheitsunterschiede oder Wirksamkeit wurde zwischen diesen Probanden und jüngeren Probanden beobachtet, und andere berichtete klinische Literatur und Erfahrungen mit Trazodon haben dies nicht getan identifizierte Unterschiede in den Reaktionen zwischen älteren und jüngeren Patienten. Da die Erfahrung älterer Menschen mit Oleptro jedoch begrenzt ist, sollte dies der Fall sein bei geriatrischen Patienten mit Vorsicht angewendet.
Antidepressiva wurden mit Fällen von assoziiert klinisch signifikante Hyponatriämie bei älteren Patienten, die möglicherweise höher sind Risiko für diese Nebenwirkung
Nierenfunktionsstörung
Oleptro wurde bei Patienten mit Nierenfunktion nicht untersucht Beeinträchtigung. Trazodon sollte in dieser Population mit Vorsicht angewendet werden.
Leberfunktionsstörung
Oleptro wurde bei Patienten mit Leber nicht untersucht Beeinträchtigung. Trazodon sollte in dieser Population mit Vorsicht angewendet werden.

SEITENWIRKUNGEN
Die folgenden schwerwiegenden Nebenwirkungen werden beschrieben an anderer Stelle in der Kennzeichnung:
- Klinische Verschlechterung und Suizidrisiko
- Serotonin-Syndrom oder NMS-ähnliche Reaktionen
- QT-Verlängerung und Risiko eines plötzlichen Todes
- Orthostatische Hypotonie
- Anormale Blutungsereignisse
- Priapismus
- Hyponatriämie
- Kognitive und motorische Beeinträchtigung
- Abbruchsymptome
Die häufigsten Nebenwirkungen (berichtet in ≥ 5% und mit der doppelten Rate von Placebo) sind: Schläfrigkeit / Sedierung, Schwindel, Verstopfung, Sehvermögen verschwommen.
Tabelle 2 enthält die Zusammenfassung der unerwünschten Ereignisse (UE) was zum Absetzen der Oleptro-Behandlung mit einer Inzidenz von mindestens 1% und mindestens doppelt so viel wie bei Placebo.
Tabelle 2: Nebenwirkungen mit
Absetzen als ergriffene Maßnahme (≥ 1% Inzidenz und Inzidenz 2x Placebo)
| Oleptro N = 202 |
|
| Schläfrigkeit / Sedierung | 8 (4,0%) |
| Schwindel | 7 (3,5%) |
| Verwirrungszustand | 2 (1,0%) |
| Koordination abnormal | 2 (1,0%) |
| Kopfschmerzen | 2 (1,0%) |
| Übelkeit | 2 (1,0%) |
| Gleichgewichtsstörung / Gangstörung | 2 (1,0%) |
Erfahrung in klinischen Studien
Die unten beschriebenen Daten spiegelt die Exposition in einer klinischen Studie mit 406 Patienten wider, darunter 204, denen sie ausgesetzt waren Placebo und 202 Oleptro ausgesetzt. Die Patienten waren zwischen 18 und 80 Jahre alt und 69,3% und 67,5% der Patienten hatten mindestens eine frühere Depressionsepisode in den letzten 24 Monaten in der Placebo- bzw. aktiv behandelten Gruppe. Im Bei einzelnen Patienten waren die Dosen flexibel und lagen zwischen 150 und 375 mg pro Tag. Die mittlere Tagesdosis während des 6-wöchigen Behandlungszeitraums betrug 310 mg. Die Tabletten wurden oral verabreicht und einmal täglich für eine Gesamtdauer von 8 gegeben Wochen einschließlich der Titrationsperiode.
Weil klinische Studien sind durchgeführt unter sehr unterschiedlichen Bedingungen, Nebenwirkungen beobachtet in Die klinischen Studien eines Arzneimittels können nicht direkt mit den Raten in der verglichen werden klinische Studien mit einem anderen Arzneimittel und spiegeln möglicherweise nicht die in beobachteten Raten wider üben.
Tabelle 3 enthält die Zusammenfassung von Alle behandlungsbedingten Nebenwirkungen, die in der Inzidenz bei ≥ 5% auftraten Oleptro-Gruppe, unabhängig davon, ob der klinische Prüfer mit ihm verwandt ist das Studienmedikament oder nicht.
Tabelle 3: Am häufigsten
Behandlungsereignisse (≥ 5% der Patienten unter aktiver Behandlung)
| Bevorzugte Laufzeit | Placebo N = 204 |
Oleptro N = 202 |
| Schläfrigkeit / Sedierung | 39 (19%) | 93 (46%) |
| Kopfschmerzen | 55 (27%) | 67 (33%) |
| Trockener Mund | 26 (13%) | 51 (25%) |
| Schwindel | 25 (12%) | 50 (25%) |
| Übelkeit | 26 (13%) | 42 (21%) |
| Müdigkeit | 17 (8%) | 30 (15%) |
| Durchfall | 23 (11%) | 19 (9%) |
| Verstopfung | 4 (2%) | 16 (8%) |
| Rückenschmerzen | 7 (3%) | 11 (5%) |
| Vision verschwommen | 0 (0%) | 11 (5%) |
Sexuelle Funktionsstörung
Unerwünschte Ereignisse im Zusammenhang mit Sexuelle Dysfunktion (unabhängig von der Kausalität) wurde von 4,9% und 1,5% von gemeldet Patienten, die mit Oleptro bzw. Placebo behandelt wurden. In der Oleptro-Gruppe Ejakulationsstörungen traten bei 1,5% der Patienten auf, es trat eine verminderte Libido auf bei 1,5% der Patienten und erektile Dysfunktion und abnormaler Orgasmus <1% von Patienten.
Vitalfunktionen und Gewicht
Es gab keine nennenswerten Veränderungen der Vitalfunktionen (Blut Druck, Atemfrequenz, Puls) oder Gewicht in beiden Behandlungsgruppen.
Es folgt eine Liste der behandlungsbedingten Nebenwirkungen Reaktionen mit einer Inzidenz von ≥ 1% bis <5% (d.h., weniger häufig) in mit Oleptro behandelte Patienten. Diese Auflistung soll nicht enthalten sein Reaktionen (i), die bereits in früheren Tabellen oder an anderer Stelle in der Kennzeichnung aufgeführt sind (ii) für die der Zusammenhang mit der Behandlung gering ist, (iii) die dies waren allgemein als nicht informativ und (iv) die nicht als vorhanden angesehen wurden signifikante klinische Implikationen. Reaktionen werden nach Körpersystemen klassifiziert unter Verwendung der folgenden Definitionen: Häufige Nebenwirkungen treten auf bei mindestens 1/100 Patienten; Selten Nebenwirkungen sind diese tritt bei weniger als 1/100 Patienten auf.
Ohren- und Labyrinthstörungen - Selten: Hypoakusis, Tinnitus, Schwindel
Augenerkrankungen - Häufig: Sehstörung; Selten: trockenes Auge, Augenschmerzen, Photophobie
Magen-Darm-Störungen - Häufig: Bauchschmerzen, Erbrechen; Selten: Refluxösophagitis
Allgemeine Störungen und Bedingungen auf der Verwaltungsstelle - Häufig: Ödeme; Selten: Gangstörung
Störungen des Immunsystems - Selten: Überempfindlichkeit
Erkrankungen des Bewegungsapparates und des Bindegewebes - Häufig: Beschwerden des Bewegungsapparates, Myalgie; Selten: Muskel zucken
Störungen des Nervensystems - Häufig: Koordination Anormalität, Dysgeusie, Gedächtnisstörung, Migräne, Parästhesie, Zittern; Selten: Amnesie, Aphasie, Hypästhesie, Sprachstörung
Psychiatrische Störungen - Häufig: Aufregung, Verwirrtheit, Orientierungslosigkeit
Nieren- und Harnwegserkrankungen - Häufig: Miktion Dringlichkeit; Selten: Blasenschmerzen, Harninkontinenz
Atemwegserkrankungen, Erkrankungen des Brustraums und des Mediastinums - Häufig: Atemnot
Haut- und subkutane Gewebestörungen - Häufig: Nachtschweiß; Selten: Akne, Hyperhidrose, Lichtempfindlichkeitsreaktion
Gefäßerkrankungen - Selten: Spülen
Postmarketing-Erfahrung
Spontane Berichte über Trazodonhydrochlorid aus Postmarketing-Erfahrung erhalten werden: abnormale Träume, Unruhe, Alopezie, Angst, Aphasie, Apnoe, Ataxie, Brustvergrößerung oder Verstopfung, Kardiospasmus, zerebrovaskulärer Unfall, Schüttelfrost, Cholestase, Klitoris, Herzinsuffizienz, Diplopie, Ödeme, extrapyramidale Symptome, Grand-Mal-Anfälle, Halluzinationen, hämolytische Anämie, Hirsutismus, Hyperbilirubinämie, erhöhte Amylase, erhöhte Speichelfluss, Schlaflosigkeit, Leukozytose, Leukonychie, Gelbsucht, Laktation, Leberenzymanipationen, Methämoglobinämie, Übelkeit / Erbrechen (am häufigsten), Parästhesie, Paranoid Reaktion, Priapismus, Juckreiz, Psoriasis, Psychose, Hautausschlag, Stupor, unangemessenes ADH-Syndrom, Spätdyskinesie, unerklärlicher Tod, Harn Inkontinenz, Harnverhaltung, Urtikaria, Vasodilatation, Schwindel und Schwäche.
Über kardiovaskuläre Systemeffekte wurde berichtet Folgendes umfassen: Leitungsblock, orthostatische Hypotonie und Synkope, Herzklopfen, Bradykardie, Vorhofflimmern, Myokardinfarkt, Herz Festnahme, Arrhythmie, ventrikuläre ektopische Aktivität, einschließlich ventrikulärer Tachykardie und QT-Verlängerung. Bei der Überwachung nach dem Inverkehrbringen verlängerte QT Intervall, Torsades de Pointes und ventrikuläre Tachykardie wurden berichtet mit der Form von Trazodon mit sofortiger Freisetzung in Dosen von 100 mg pro Tag oder weniger .
Drogeninteraktionen
Monoaminoxidasehemmer (MAOIs)
Serotonerge Drogen
Depressiva des Central Nervous System (CNS)
Trazodon kann die Reaktion auf Alkohol verbessern Barbiturate und andere ZNS-Depressiva.
Cytochrom P450 3A4 Inhibitoren
In-vitro-Studien zum Arzneimittelstoffwechsel legen nahe, dass es eine gibt Potenzial für Arzneimittelwechselwirkungen, wenn Trazodon mit Cytochrom P450 verabreicht wird 3A4 (CYP3A4) -Inhibitoren. Die Wirkung der kurzfristigen Verabreichung von Ritonavir (200 mg zweimal täglich, 4 Dosen) zur Pharmakokinetik einer Einzeldosis von Trazodon (50 mg) wurde an 10 gesunden Probanden untersucht. Die Cmax von Trazodon stieg um 34%, die AUC um das 2,4-fache und die Halbwertszeit erhöhte sich um das 2,2-fache und die Clearance um 52% verringert. Unerwünschte Wirkungen einschließlich Übelkeit, Hypotonie und Synkope wurden bei Ritonavir und Trazodon beobachtet wurden gemeinsam verwaltet. Es ist wahrscheinlich, dass Ketoconazol, Indinavir und andere CYP3A4-Inhibitoren wie Itraconazol können zu einem erheblichen Anstieg von führen Trazodon-Plasmakonzentrationen mit dem Potenzial für Nebenwirkungen. Wenn Trazodon wird zusammen mit einem wirksamen CYP3A4-Inhibitor angewendet, dem Risiko eines Herzinsuffizienzs Die Arrhythmie kann erhöht und niedriger sein Die Trazodon-Dosis sollte in Betracht gezogen werden.
Cytochrom P450-Induktoren (z., Carbamazepin)
Carbamazepin induziert CYP3A4. Nach der gleichzeitigen Verwaltung von Carbamazepin 400 mg pro Tag mit Trazodon 100 mg bis 300 mg täglich Carbamazepin reduzierte die Plasmakonzentrationen von Trazodon und Mchlorphenlypiperazin (ein aktiver Metabolit) um 76% bzw. 60% im Vergleich zu Precarbamazepinwerten. Die Patienten sollten engmaschig überwacht werden Überprüfen Sie, ob bei der Einnahme beider eine erhöhte Trazodon-Dosis erforderlich ist Drogen.
Digoxin und Phenytoin
Erhöhte Serumdigoxin- oder Phenytoinspiegel waren berichtet bei Patienten, die gleichzeitig mit einem dieser Patienten Trazodon erhielten Drogen. Überwachen Sie die Serumspiegel und passen Sie die Dosierungen nach Bedarf an.
NSAIDs, Aspirin oder andere Arzneimittel, die die Koagulation oder Blutungen beeinflussen
Aufgrund einer möglichen Assoziation zwischen Serotonin Patienten sollten modulieren und gastrointestinale Blutungen bekommen und überwacht werden für und gewarnt über das potenzielle Blutungsrisiko im Zusammenhang mit dem gleichzeitige Anwendung von Trazodon und NSAIDs, Aspirin oder anderen betroffenen Arzneimitteln Gerinnung oder Blutung.
Warfarin
Es gab Berichte über veränderte (entweder erhöhte oder verringerte) Prothrombinzeiten bei der Einnahme von Warfarin und Trazodon.
Drogenmissbrauch und Abhängigkeit
Kontrollierte Substanz
Oleptro ist keine kontrollierte Substanz.
Missbrauch
Obwohl Trazodonhydrochlorid nicht war systematisch in präklinischen oder klinischen Studien auf sein Potenzial für untersucht Missbrauch, in den klinischen Studien wurde kein Hinweis auf drogensuchendes Verhalten gesehen mit Oleptro. Es ist jedoch schwierig vorherzusagen, inwieweit a ZNS-aktives Medikament wird missbraucht, umgeleitet und missbraucht. Folglich Ärzte sollte Patienten sorgfältig auf eine Vorgeschichte von Drogenmissbrauch untersuchen und diesen folgen Patienten genau, beobachten sie auf Anzeichen von Missbrauch oder Missbrauch von Trazodon Hydrochlorid (z., Entwicklung der Toleranz, Erhöhung der Dosis, drogensuchendes Verhalten).

Schwangerschaftskategorie C
Es wurde gezeigt, dass Trazodonhydrochlorid eine erhöhte Ursache darstellt fetale Resorption und andere nachteilige Auswirkungen auf den Fötus in zwei Studien unter Verwendung die Ratte, wenn sie in Dosierungen verabreicht wird, die ungefähr das 30- bis 50-fache des vorgeschlagenen Werts betragen maximale menschliche Dosis. Es gab auch eine Zunahme angeborener Anomalien in einem von drei Kaninchenstudien mit ungefähr dem 15- bis 50-fachen der maximalen menschlichen Dosis. Es gibt keine angemessenen und gut kontrollierten Studien bei schwangeren Frauen. Oleptro sollte während der Schwangerschaft nur angewendet werden, wenn der potenzielle Nutzen dies rechtfertigt potenzielles Risiko für den Fötus.

Die folgenden schwerwiegenden Nebenwirkungen werden beschrieben an anderer Stelle in der Kennzeichnung:
- Klinische Verschlechterung und Suizidrisiko
- Serotonin-Syndrom oder NMS-ähnliche Reaktionen
- QT-Verlängerung und Risiko eines plötzlichen Todes
- Orthostatische Hypotonie
- Anormale Blutungsereignisse
- Priapismus
- Hyponatriämie
- Kognitive und motorische Beeinträchtigung
- Abbruchsymptome
Die häufigsten Nebenwirkungen (berichtet in ≥ 5% und mit der doppelten Rate von Placebo) sind: Schläfrigkeit / Sedierung, Schwindel, Verstopfung, Sehvermögen verschwommen.
Tabelle 2 enthält die Zusammenfassung der unerwünschten Ereignisse (UE) was zum Absetzen der Oleptro-Behandlung mit einer Inzidenz von mindestens 1% und mindestens doppelt so viel wie bei Placebo.
Tabelle 2: Nebenwirkungen mit
Absetzen als ergriffene Maßnahme (≥ 1% Inzidenz und Inzidenz 2x Placebo)
| Oleptro N = 202 |
|
| Schläfrigkeit / Sedierung | 8 (4,0%) |
| Schwindel | 7 (3,5%) |
| Verwirrungszustand | 2 (1,0%) |
| Koordination abnormal | 2 (1,0%) |
| Kopfschmerzen | 2 (1,0%) |
| Übelkeit | 2 (1,0%) |
| Gleichgewichtsstörung / Gangstörung | 2 (1,0%) |
Erfahrung in klinischen Studien
Die unten beschriebenen Daten spiegelt die Exposition in einer klinischen Studie mit 406 Patienten wider, darunter 204, denen sie ausgesetzt waren Placebo und 202 Oleptro ausgesetzt. Die Patienten waren zwischen 18 und 80 Jahre alt und 69,3% und 67,5% der Patienten hatten mindestens eine frühere Depressionsepisode in den letzten 24 Monaten in der Placebo- bzw. aktiv behandelten Gruppe. Im Bei einzelnen Patienten waren die Dosen flexibel und lagen zwischen 150 und 375 mg pro Tag. Die mittlere Tagesdosis während des 6-wöchigen Behandlungszeitraums betrug 310 mg. Die Tabletten wurden oral verabreicht und einmal täglich für eine Gesamtdauer von 8 gegeben Wochen einschließlich der Titrationsperiode.
Weil klinische Studien sind durchgeführt unter sehr unterschiedlichen Bedingungen, Nebenwirkungen beobachtet in Die klinischen Studien eines Arzneimittels können nicht direkt mit den Raten in der verglichen werden klinische Studien mit einem anderen Arzneimittel und spiegeln möglicherweise nicht die in beobachteten Raten wider üben.
Tabelle 3 enthält die Zusammenfassung von Alle behandlungsbedingten Nebenwirkungen, die in der Inzidenz bei ≥ 5% auftraten Oleptro-Gruppe, unabhängig davon, ob der klinische Prüfer mit ihm verwandt ist das Studienmedikament oder nicht.
Tabelle 3: Am häufigsten
Behandlungsereignisse (≥ 5% der Patienten unter aktiver Behandlung)
| Bevorzugte Laufzeit | Placebo N = 204 |
Oleptro N = 202 |
| Schläfrigkeit / Sedierung | 39 (19%) | 93 (46%) |
| Kopfschmerzen | 55 (27%) | 67 (33%) |
| Trockener Mund | 26 (13%) | 51 (25%) |
| Schwindel | 25 (12%) | 50 (25%) |
| Übelkeit | 26 (13%) | 42 (21%) |
| Müdigkeit | 17 (8%) | 30 (15%) |
| Durchfall | 23 (11%) | 19 (9%) |
| Verstopfung | 4 (2%) | 16 (8%) |
| Rückenschmerzen | 7 (3%) | 11 (5%) |
| Vision verschwommen | 0 (0%) | 11 (5%) |
Sexuelle Funktionsstörung
Unerwünschte Ereignisse im Zusammenhang mit Sexuelle Dysfunktion (unabhängig von der Kausalität) wurde von 4,9% und 1,5% von gemeldet Patienten, die mit Oleptro bzw. Placebo behandelt wurden. In der Oleptro-Gruppe Ejakulationsstörungen traten bei 1,5% der Patienten auf, es trat eine verminderte Libido auf bei 1,5% der Patienten und erektile Dysfunktion und abnormaler Orgasmus <1% von Patienten.
Vitalfunktionen und Gewicht
Es gab keine nennenswerten Veränderungen der Vitalfunktionen (Blut Druck, Atemfrequenz, Puls) oder Gewicht in beiden Behandlungsgruppen.
Es folgt eine Liste der behandlungsbedingten Nebenwirkungen Reaktionen mit einer Inzidenz von ≥ 1% bis <5% (d.h., weniger häufig) in mit Oleptro behandelte Patienten. Diese Auflistung soll nicht enthalten sein Reaktionen (i), die bereits in früheren Tabellen oder an anderer Stelle in der Kennzeichnung aufgeführt sind (ii) für die der Zusammenhang mit der Behandlung gering ist, (iii) die dies waren allgemein als nicht informativ und (iv) die nicht als vorhanden angesehen wurden signifikante klinische Implikationen. Reaktionen werden nach Körpersystemen klassifiziert unter Verwendung der folgenden Definitionen: Häufige Nebenwirkungen treten auf bei mindestens 1/100 Patienten; Selten Nebenwirkungen sind diese tritt bei weniger als 1/100 Patienten auf.
Ohren- und Labyrinthstörungen - Selten: Hypoakusis, Tinnitus, Schwindel
Augenerkrankungen - Häufig: Sehstörung; Selten: trockenes Auge, Augenschmerzen, Photophobie
Magen-Darm-Störungen - Häufig: Bauchschmerzen, Erbrechen; Selten: Refluxösophagitis
Allgemeine Störungen und Bedingungen auf der Verwaltungsstelle - Häufig: Ödeme; Selten: Gangstörung
Störungen des Immunsystems - Selten: Überempfindlichkeit
Erkrankungen des Bewegungsapparates und des Bindegewebes - Häufig: Beschwerden des Bewegungsapparates, Myalgie; Selten: Muskel zucken
Störungen des Nervensystems - Häufig: Koordination Anormalität, Dysgeusie, Gedächtnisstörung, Migräne, Parästhesie, Zittern; Selten: Amnesie, Aphasie, Hypästhesie, Sprachstörung
Psychiatrische Störungen - Häufig: Aufregung, Verwirrtheit, Orientierungslosigkeit
Nieren- und Harnwegserkrankungen - Häufig: Miktion Dringlichkeit; Selten: Blasenschmerzen, Harninkontinenz
Atemwegserkrankungen, Erkrankungen des Brustraums und des Mediastinums - Häufig: Atemnot
Haut- und subkutane Gewebestörungen - Häufig: Nachtschweiß; Selten: Akne, Hyperhidrose, Lichtempfindlichkeitsreaktion
Gefäßerkrankungen - Selten: Spülen
Postmarketing-Erfahrung
Spontane Berichte über Trazodonhydrochlorid aus Postmarketing-Erfahrung erhalten werden: abnormale Träume, Unruhe, Alopezie, Angst, Aphasie, Apnoe, Ataxie, Brustvergrößerung oder Verstopfung, Kardiospasmus, zerebrovaskulärer Unfall, Schüttelfrost, Cholestase, Klitoris, Herzinsuffizienz, Diplopie, Ödeme, extrapyramidale Symptome, Grand-Mal-Anfälle, Halluzinationen, hämolytische Anämie, Hirsutismus, Hyperbilirubinämie, erhöhte Amylase, erhöhte Speichelfluss, Schlaflosigkeit, Leukozytose, Leukonychie, Gelbsucht, Laktation, Leberenzymanipationen, Methämoglobinämie, Übelkeit / Erbrechen (am häufigsten), Parästhesie, Paranoid Reaktion, Priapismus, Juckreiz, Psoriasis, Psychose, Hautausschlag, Stupor, unangemessenes ADH-Syndrom, Spätdyskinesie, unerklärlicher Tod, Harn Inkontinenz, Harnverhaltung, Urtikaria, Vasodilatation, Schwindel und Schwäche.
Über kardiovaskuläre Systemeffekte wurde berichtet Folgendes umfassen: Leitungsblock, orthostatische Hypotonie und Synkope, Herzklopfen, Bradykardie, Vorhofflimmern, Myokardinfarkt, Herz Festnahme, Arrhythmie, ventrikuläre ektopische Aktivität, einschließlich ventrikulärer Tachykardie und QT-Verlängerung. Bei der Überwachung nach dem Inverkehrbringen verlängerte QT Intervall, Torsades de Pointes und ventrikuläre Tachykardie wurden berichtet mit der Form von Trazodon mit sofortiger Freisetzung in Dosen von 100 mg pro Tag oder weniger .

Menschliche Erfahrung
Es wird erwartet, dass die damit verbundenen Gesundheitsrisiken Eine Überdosierung von Oleptro ist höchstwahrscheinlich ähnlich wie bei Trazodon Formulierungen mit sofortiger Freisetzung.
Bei aufgenommenen Patienten ist der Tod durch Überdosierung aufgetreten Trazodon und andere ZNS-depressive Medikamente gleichzeitig (Alkohol, Alkohol und Chloralhydrat und Diazepam; Amobarbital; Chlordiazepoxid; oder Meprobamat).
Die schwersten Reaktionen, mit denen berichtet wurde, sind aufgetreten Eine Überdosierung von Trazodon allein war Priapismus, Atemstillstand, Krampfanfälle und EKG-Änderungen, einschließlich QT-Verlängerung. Die Reaktionen berichteten am meisten häufig waren Schläfrigkeit und Erbrechen. Eine Überdosierung kann zu einer Zunahme führen in Inzidenz oder Schweregrad einer der gemeldeten Nebenwirkungen.
Management von Überdosierung
Es gibt kein spezifisches Gegenmittel für eine Überdosierung mit Oleptro.
Die Behandlung sollte aus diesen allgemeinen Maßnahmen bestehen beschäftigt bei der Behandlung von Überdosierung mit jedem Medikament, das in der Behandlung von Major Depression. Stellen Sie eine angemessene Atemwege und Sauerstoff sicher und Belüftung. Überwachen Sie den Herzrhythmus und die Vitalfunktionen.
Allgemeine unterstützende und symptomatische Maßnahmen sind ebenfalls empfohlen. Die Induktion von Erbrechen wird nicht empfohlen. Magenspülung mit a Orogastrisches Rohr mit großer Bohrung und angemessenem Atemwegsschutz, falls erforderlich, kann angezeigt sein, wenn sie kurz nach der Einnahme oder bei symptomatischen Patienten durchgeführt werden. Aktivkohle sollte verabreicht werden. Erzwungene Diurese kann nützlich sein Erleichterung der Eliminierung des Arzneimittels.
Berücksichtigen Sie bei der Verwaltung von Überdosierungen die Möglichkeit von multiple Drogenbeteiligung. Der Arzt sollte erwägen, ein Gift zu kontaktieren Kontrollzentrum für zusätzliche Informationen zur Behandlung von Überdosierungen.

Präklinische Studien haben gezeigt, dass Trazodon selektiv ist hemmt die neuronale Wiederaufnahme von Serotonin und wirkt als Antagonist bei 5-HT-2A / 2C Serotoninrezeptoren.
Trazodon ist kein Monoaminoxidasehemmer und stimuliert im Gegensatz zu Medikamenten vom Amphetamintyp nicht das Zentralnervensystem.
Trazodon antagonisiert Alpha-1-adrenerge Rezeptoren, a Eigenschaft, die mit posturaler Hypotonie verbunden sein kann.

Die AUC von Trazodon im stationären Zustand ist danach äquivalent Verabreichung von Trazodon 100 mg sofortige Freisetzung (IR) drei (3) mal täglich (Mittelwert ± SD AUCss = 33058 ± 8006 ng * h / ml) und Oleptro 300 mg einmal täglich (Mittelwert ± SD AUCss = 29131 ± 9931 ng * h / ml) für eine Woche. Steady State Cmax und Cmin von Trazodon war nach Verabreichung von Trazodon 100 mg IR 3 nicht äquivalent mal täglich (Mittelwert ± SD Cmax, ss = 3118 ± 758 ng / ml, Cmin, ss = 843 ± 274 ng / ml) und Oleptro 300 mg einmal täglich (Mittelwert ± SD Cmax, ss = 1812 ± 621 ng / ml, Cmin, ss = 674 ± 355 ng / ml) für eine Woche.
Absorption
Trazodon wird nach oraler Verabreichung gut resorbiert ohne selektive Lokalisierung in einem Gewebe. Nach Einzeldosis Verabreichung von Oleptro 300 mg Tabletten unter Fastenbedingungen, ein mittlerer Peak Die Trazodon-Plasmakonzentration (Cmax) von 1188 ± 362 ng / ml wurde bei a angegeben mediane Tmax von 9 Stunden nach der Dosis. Wenn Oleptro 300 mg Tabletten in Kürze eingenommen werden Nach Einnahme einer fettreichen Mahlzeit steigt Cmax im Vergleich zu etwa 86% unter Fastenbedingungen nehmen. AUC0-∞ und Tmax sind dies jedoch nicht signifikant von Lebensmitteln betroffen.
Oleptro-Tabletten sind nachträglich dosisproportional Einzeldosis-Verabreichung von Dosen im Bereich von 75 mg bis 375 mg als intakt oder halbierte Tabletten.
Stoffwechsel
In vitro Studien an menschlichen Lebermikrosomen zeigen dass Trazodon über eine oxidative Spaltung zu einem aktiven Metaboliten metabolisiert wird m-Chlorphenylpiperazin (mCPP) durch CYP3A4. Andere Stoffwechselwege, die sein können am Metabolismus von Trazodon beteiligt, wurden nicht gut charakterisiert. Trazodon wird weitgehend metabolisiert; weniger als 1% einer oralen Dosis werden ausgeschieden unverändert im Urin.
Beseitigung
Die Elimination erfolgt überwiegend über die Niere mit 70 bis 75% von a Die orale Dosis wird innerhalb der ersten 72 Stunden nach der Einnahme im Urin zurückgewonnen. Nach einmaliger Verabreichung von Oleptro 300 mg Tabletten ist ein Mittelwert erkennbar Eine terminale Halbwertszeit von 10 Stunden wurde gemeldet.
Proteinbindung
Trazodon ist zu 89 bis 95% proteingebunden in vitro bei Konzentrationen, die mit therapeutischen Dosen beim Menschen erreicht wurden.
However, we will provide data for each active ingredient


