









Kompozisyon:
Uygulama:
Kovalenko Svetlana Olegovna tarafından tıbbi olarak gözden geçirilmiştir, Eczane Son güncelleme: 05.04.2022

Dikkat! Sayfadaki bilgiler sadece sağlık profesyonelleri içindir! Bilgi kamu kaynaklarında toplanır ve anlamlı hatalar içerebilir! Dikkatli olun ve bu sayfadaki tüm bilgileri tekrar kontrol edin!


Dozaj Formları ve Güçlü Yönleri
Oleptro tabletleri aşağıdaki güçlerde mevcuttur:
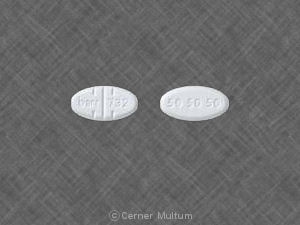
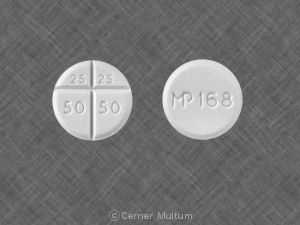
- 150 mg trazodon içeren Oleptro ikiye bölünebilir tabletler hidroklorür (sarımsı bej, kapsül şeklinde tablet, kaplanmış ve üzerinde puanlanmıştır her iki taraf da bir tarafta DDS 080 baskılı)
- 300 mg trazodon içeren Oleptro ikiye bölünebilir tabletler hidroklorür (bej-turuncu, kapsül şeklindeki tablet, her ikisinde de kaplanmış ve puanlanmıştır DDS 081'in bir tarafı baskılı kenarlar)
Depolama ve Taşıma
Oleptro 150 mg sarımsı bej, kapsül şeklindedir DDS 080 baskılı her iki tarafta kaplanmış ve puanlanmış genişletilmiş tablet bir tarafta. Aşağıdaki gibi sağlanır:
30 tabletlik şişeler NDC 43595-080-03
Oleptro 300 mg bej-turuncu, kapsül şeklindedir DDS 081 baskılı her iki tarafta kaplanmış ve puanlanmış genişletilmiş tablet bir tarafta. Aşağıdaki gibi sağlanır:
30 tabletlik şişeler NDC 43595-081-03
Oda sıcaklığında (15 - 30 ° C) sıkıca saklayın ışığa dayanıklı kaplar.
Angelini Pharma Inc. Gaithersburg, MD 20877. Â Revize: Temmuz 2014

Oleptro ™ majör tedavisi için endikedir yetişkinlerde depresif bozukluk (MDD). Oleptro'nun etkinliği olmuştur MDD ile ayakta tedavi denemesinde ve aynı zamanda trazodonun derhal salınım formülasyonu.

Doz Seçimi
Önerilen başlangıç Oleptro dozu bir kez 150 mg'dır yetişkinlerde günlük. Doz her üç günde bir 75 mg / gün artırılabilir (yani., tedavinin 4. gününde 225 mg'a başlayın). Maksimum günlük doz 375'i geçmemelidir mg.
- Oleptro tabletleri aynı anda ağızdan alınmalıdır her gün, akşam geç saatlerde tercihen yatmadan önce, aç karnına.
- Yeterli bir yanıt alındıktan sonra, dozaj olabilir terapötik bağlı olarak daha sonra ayarlanarak kademeli olarak azaltılmalıdır tepki.
- Hastalar ne zaman yoksunluk belirtileri açısından izlenmelidir trazodon hidroklorür ile tedavinin kesilmesi. Doz olmalıdır mümkün olduğunda yavaş yavaş azaldı.
Bakım Tedavisi
Oleptro'nun idame tedavisi için etkinliği MDB değerlendirilmedi. Hiçbir kanıt mevcut olmasa da Oleptro ile tedavi edilen bir hastanın ne kadar süre devam etmesi gerektiği sorusunu cevaplayın ilaç, genellikle tedavinin birkaç kişi için sürdürülmesi önerilir ilk yanıttan aylar sonra. Hastalar en düşük seviyede tutulmalıdır etkili doz ve devam eden ihtiyacı belirlemek için periyodik olarak yeniden değerlendirilmelidir bakım tedavisi için.
Bir Hastayı Monoamin Oksidaza Değiştirme İnhibitör (MAOI) Psikiyatrik Bozuklukları Tedavi Etmeyi Amaçladı
En az 14 gün, kesilmesi arasında geçmelidir psikiyatrik bozuklukları tedavi etmeyi ve tedaviye başlamayı amaçlayan bir MAOI Oleptro. Tersine, Oleptro'yu durdurduktan sonra en az 14 güne izin verilmelidir psikiyatrik bozuklukları tedavi etmeyi amaçlayan bir MAOI başlamadan önce.
Oleptro'nun Linezolid veya Metilen gibi diğer MAOI'lerle Kullanımı Mavi
Tedavi gören bir hastada Oleptro'yu başlatmayın linezolid veya intravenöz metilen mavisi ile çünkü artan bir risk vardır serotonin sendromu. Daha acil tedavi gerektiren bir hastada a psikiyatrik durum, hastaneye yatış da dahil olmak üzere diğer müdahaleler yapılmalıdır dikkate alınmalıdır.
Bazı durumlarda, zaten Oleptro alan bir hasta tedavi linezolid veya intravenöz metilen ile acil tedavi gerektirebilir mavi. Linezolid veya intravenöz metilen mavisine kabul edilebilir alternatifler varsa tedavi mevcut değildir ve linezolid veya potansiyel faydaları intravenöz metilen mavisi tedavisinin risklerinden daha ağır bastığı düşünülmektedir belirli bir hastada serotonin sendromu, Oleptro derhal durdurulmalıdır ve linezolid veya intravenöz metilen mavisi uygulanabilir. Hasta iki hafta veya daha uzun süre serotonin sendromu semptomları açısından izlenmelidir Son doz linezolid veya intravenöz metilen mavisinden 24 saat sonra hangisi önce gelirse. Oleptro ile tedaviye 24 saat sonra devam edilebilir son doz linezolid veya intravenöz metilen mavisi.
Metilen mavisini uygulama riski intravenöz olmayan yollar (oral tabletler veya lokal enjeksiyon gibi) veya Oleptro ile 1 mg / kg'dan çok daha düşük intravenöz dozlar belirsizdir. yine de klinisyen ortaya çıkma olasılığının farkında olmalıdır bu tür kullanımla serotonin sendromu belirtileri (bkz UYARILAR VE ÖNLEMLER].
Önemli Yönetim Talimatları
Oleptro tabletleri esneklik sağlamak için puanlanır dozlama.
Oleptro tamamen yutulabilir veya yarı olarak uygulanabilir tableti skor çizgisi boyunca kırarak. Tableti yarıya indirmek tabletin kontrollü salım özelliklerini etkilemez.
Kontrollü salım özelliklerini korumak için Oleptro çiğnenmemeli veya ezilmemelidir.

Monoamin Oksidaz İnhibitörleri (MAOI'ler)
Psikiyatrik bozuklukları tedavi etmek için MAOI kullanımı Oleptro ile veya Oleptro ile tedaviyi bıraktıktan sonraki 14 gün içinde serotonin sendromu riskinin artması nedeniyle kontrendikedir. Kullanımı Psikiyatrik tedavi amaçlı bir MAOI'yi durdurduktan sonraki 14 gün içinde Oleptro bozukluklar da kontrendikedir..
Tedavi gören bir hastada Oleptro'ya başlanması Linezolid veya intravenöz metilen mavisi gibi MAOI'ler de kontrendikedir serotonin sendromu riskinin artması nedeniyle.

UYARILAR
Bir parçası olarak dahil ÖNLEMLER Bölüm.
ÖNLEMLER
Klinik Kötüleşme ve İntihar Riski
Her ikisi de yetişkin olan majör depresif bozukluğu (MDD) olan hastalar ve pediatrik, depresyonlarında ve / veya intihar düşüncesi ve davranışının ortaya çıkması (intihar) veya olağandışı değişiklikler antidepresan ilaçlar alıp almadıklarına bakılmaksızın davranış ve bu önemli bir remisyon meydana gelene kadar risk devam edebilir. İntihar bilinen bir risktir depresyon ve diğer bazı psikiyatrik bozukluklar ve bu bozukluklar kendileri intiharın en güçlü yordayıcılarıdır. Uzun zaman oldu bununla birlikte, antidepresanların indüklemede bir rolü olabileceği endişesi depresyonun kötüleşmesi ve bazı hastalarda intihar eğilimi ortaya çıkması tedavinin erken aşamalarında. Kısa vadeli havuzlanmış analizler antidepresan ilaçların (SSRI'lar ve diğerleri) plasebo kontrollü çalışmaları göstermiştir bu ilaçların intihar düşünme ve davranış riskini arttırması (suçluluk) çocuklarda, ergenlerde ve genç yetişkinlerde (18-24 yaş) MDB ve diğer psikiyatrik bozukluklar. Kısa süreli çalışmalar göstermedi antidepresanlarla intihar riskinde plaseboya kıyasla artış 24 yaşın üzerindeki yetişkinler; antidepresanlarla karşılaştırıldığında bir azalma vardı 65 yaş ve üstü yetişkinlerde plasebo.
Plasebo kontrollü çalışmaların havuzlanmış analizleri MDB, obsesif kompulsif bozukluk (OKB) olan çocuklar ve ergenler veya diğer psikiyatrik bozukluklar arasında toplam 24 kısa süreli 9 çalışma yer almaktadır 4.400'den fazla hastada antidepresan ilaçlar. Toplanan analizleri MDB veya diğer psikiyatrik bozuklukları olan yetişkinlerde plasebo kontrollü çalışmalar toplam 295 kısa süreli deneme (ortalama 2 aylık süre) 11'i içeriyordu 77.000'den fazla hastada antidepresan ilaçlar. Önemli farklılıklar vardı ilaçlar arasında intihar riski, ancak bir artış eğilimi neredeyse tüm ilaçlar için genç hastalar çalışıldı. Farklılıklar vardı en yüksek endikasyonlarla farklı endikasyonlarda mutlak intihar riski MDB insidansı Risk farklılıkları (ilaç ve ilaç. plasebo) idi yaş katmanları içinde ve endikasyonlar arasında nispeten stabildir. Bu risk farklılıklar (her biri için intihar vakası sayısında ilaç-plasebo farkı Tedavi edilen 1.000 hasta) Tablo 1'de verilmiştir.
Tablo 1
| Yaş aralığı | Tedavi Edilen 1000 Hastada Suikidite Olgu Sayısında İlaç-Plasebo Farkı |
| Plasebo ile karşılaştırıldığında artar | |
| <18 | 14 ek vaka |
| 18-24 | 5 ek vaka |
| Plasebo ile karşılaştırıldığında azalır | |
| 25-64 | 1 daha az vaka |
| ≥ 65 | 6 daha az vaka |
Hiçbirinde intihar olmadı pediatrik denemeler. Yetişkin davalarında intiharlar vardı, ancak sayı intihar üzerindeki uyuşturucu etkisi hakkında herhangi bir sonuca varmak için yeterli değildi.
Bilinmiyor mu? intihar riski uzun süreli kullanıma, yani., birkaç aydan fazla. Bununla birlikte, plasebo kontrollü bakımdan önemli kanıtlar vardır depresyonu olan yetişkinlerde antidepresan kullanımının geciktirebileceği denemeler depresyonun tekrarlaması.
Tüm hastalar tedavi görüyor herhangi bir endikasyon için antidepresanlarla uygun şekilde izlenmeli ve izlenmelidir klinik kötüleşme, intihar eğilimi ve olağandışı değişiklikler açısından yakından gözlemlenmiştir davranış, özellikle ilaç tedavisinin ilk birkaç ayında veya doz değişiklikleri zamanlarında, artar veya azalır.
Aşağıdaki belirtiler, kaygı, ajitasyon, panik atak, uykusuzluk, sinirlilik, düşmanlık, saldırganlık, dürtüsellik, akatizi (psikomotor huzursuzluk), hipomani ve tedavi gören yetişkin ve pediatrik hastalarda mani bildirilmiştir majör depresif bozukluk için olduğu kadar diğerleri için de antidepresanlar ile hem psikiyatrik hem de psikiyatrik olmayan endikasyonlar. Her ne kadar nedensel bir bağlantı bu tür semptomların ortaya çıkması ile depresyonun kötüleşmesi arasında ve / veya intihar dürtülerinin ortaya çıkması tespit edilmemiştir bu tür semptomların ortaya çıkan intiharlığın öncüllerini temsil edebileceğinden endişe duymaktadır.
Dikkate alınmalıdır muhtemelen bırakılma da dahil olmak üzere terapötik rejimi değiştirmek depresyonu sürekli olarak daha kötü olan veya olan hastalarda ilaç ortaya çıkabilecek intihar veya semptomlar yaşamak özellikle bu semptomlar şiddetli ise, kötüleşen depresyon veya intihar eğilimi başlangıçta ani veya hastanın semptomlarının bir parçası değildi.
Aileleri ve bakıcıları majör depresif bozukluk nedeniyle antidepresanlarla tedavi edilen hastalar veya hem psikiyatrik hem de psikiyatrik olmayan diğer endikasyonlar hakkında uyarılmalıdır ajitasyon, sinirlilik, ortaya çıkması için hastaları izleme ihtiyacı davranışta olağandışı değişiklikler ve yukarıda açıklanan diğer semptomlar intiharlığın ortaya çıkması ve bu tür semptomları derhal sağlığa bildirmek bakım sağlayıcıları. Bu izleme yapılmalıdır aileler ve bakıcılar tarafından günlük gözlemleri içerir. Oleptro için reçeteler yazılmalıdır sırayla iyi hasta yönetimi ile tutarlı en az miktarda tablet aşırı doz riskini azaltmak.
Serotonin Sendromu
Gelişimi a SNRI'larda potansiyel olarak hayatı tehdit eden serotonin sendromu bildirilmiştir ve Oleptro dahil SSRI'lar tek başına, ancak özellikle eşzamanlı kullanımı ile diğer serotonerjik ilaçlar (triptanlar, trisiklik antidepresanlar dahil) fentanil, lityum, tramadol, triptofan, busipirone ve St. John's Wort) ve serotonin metabolizmasını bozan ilaçlarla (özellikle MAOI'ler, her ikisi de psikiyatrik bozuklukları tedavi etmeyi amaçlayanlar ve diğerleri gibi linezolid ve intravenöz metilen mavisi).
Serotonin sendromu semptomları olabilir zihinsel durum değişikliklerini içerir (ör.ajitasyon, halüsinasyonlar, deliryum ve koma), otonom instabilite (ör., taşikardi, kararsız kan basıncı, baş dönmesi, terleme, kızarma, hipertermi), nöromüsküler semptomlar (ör., titreme, sertlik, miyoklonus, hiperrefleksi, koordinasyon), nöbetler ve / veya gastrointestinal semptomlar (ör., bulantı, kusma, ishal). Hastalar yapmalıdır serotonin sendromunun ortaya çıkışı açısından izlenmelidir.
Oleptro'nun birlikte kullanımı psikiyatrik bozuklukları tedavi etmeyi amaçlayan MAOI'lerle kontrendikedir. Oleptro MAOI'lerle tedavi edilen bir hastada da başlatılmamalıdır linezolid veya intravenöz metilen mavisi. Metilen mavisi ile ilgili tüm raporlar intravenöz uygulama yolu hakkında bilgi verdi 1 mg / kg ila 8 mg / kg doz aralığında uygulama. Rapor yok metilen mavisinin diğer yollarla uygulanması (oral tabletler veya lokal doku enjeksiyonu) veya daha düşük dozlarda. Bunun ne zaman olduğu olabilir linezolid veya gibi bir MAOI ile tedaviyi başlatmak için gereklidir Oleptro alan bir hastada intravenöz metilen mavisi. Oleptro olmalı MAOI ile tedaviye başlamadan önce kesilir.
Oleptro'nun diğer serotonerjik ile birlikte kullanılması durumunda ilaçlar, triptanlar, trisiklik antidepresanlar, fentanil, lityum, tramadol, buspirone, triptofan ve St. John's Wort klinik olarak garantilidir, hastalar serotonin sendromu için potansiyel artmış bir risk hakkında bilgilendirilmelidir özellikle tedaviye başlandığında ve doz artar.
Oleptro ve eşlik eden serotonerjik ile tedavi ajanlar, yukarıdaki olaylar meydana gelirse derhal durdurulmalıdır ve destekleyici semptomatik tedavi başlatılmalıdır.
Açı Kapanışı Glaucoma
Birçoğunun kullanımından sonra ortaya çıkan pupiller dilatasyon Oleptro dahil antidepresan ilaçlar a'da bir açı kapanma saldırısını tetikleyebilir patent iridektomi olmayan anatomik olarak dar açıları olan hasta.
Hastaları Bipolar Bozukluk ve İzleme İçin Tarama Mania / Hipomanya
Başlıca depresif bir bölüm ilk olabilir bipolar bozukluğun sunumu. Genel olarak inanılır (ancak olmasa da) kontrollü çalışmalarda kurulmuş) böyle bir bölüme bir tek başına antidepresan a'nın çökme olasılığını artırabilir bipolar bozukluk riski taşıyan hastalarda karışık / manik dönem. Herhangi biri klinik kötüleşme ve intihar riski için tanımlanan semptomlar böyle bir şeyi temsil eder dönüşüm bilinmiyor. Bununla birlikte, bir ile tedaviye başlamadan önce antidepresan, depresif semptomları olan hastalar yeterince taranmalıdır bipolar bozukluk için risk altında olup olmadıklarını belirlemek; böyle bir tarama yapılmalıdır ailenin intihar öyküsü de dahil olmak üzere ayrıntılı bir psikiyatrik öykü içerir bipolar bozukluk ve depresyon. Oleptro'nun olmadığı belirtilmelidir bipolar depresyon tedavisinde kullanım için onaylanmıştır.
QT Uzatma ve Ani Ölüm Riski
Trazodonun QT / QTc aralığını uzattığı bilinmektedir. Biraz QT / QTc aralığını uzatan ilaçlar Torsades de Pointes'e neden olabilir ani, açıklanamayan ölüm. QT uzaması ilişkisi en açıktır daha büyük artışlar (20 ms ve daha büyük), ancak daha küçük QT / QTc olması mümkündür uzamalar, özellikle duyarlı bireylerde riski de artırabilir hipokalemi, hipomagnezemi veya genetik yatkınlığı olanlar gibi uzun QT / QTc.
Her ne kadar Torsades de Pointes ile gözlemlenmemiştir pazarlama öncesi çalışmalarda önerilen dozlarda Oleptro kullanımı, deneyimdir artan bir riski ortadan kaldıramayacak kadar sınırlı. Ancak, olmuştur Torsades de Pointes'in pazarlama sonrası raporları trazodon (çoklu karıştırıcı faktörlerin varlığında), dozlarında bile Günde 100 mg veya daha az.
Kalp Hastalığı Olan Hastalarda Kullanın
Trazodon hidroklorür sırasında kullanılması önerilmez miyokard enfarktüsünün ilk iyileşme aşaması.
Oleptro uygulanırken dikkatli olunmalıdır kalp hastalığı olan hastalar ve bu hastalar yakından izlenmelidir antidepresan ilaçlar (trazodon hidroklorür dahil) neden olabilir kardiyak aritmiler.
Trazodon tedavisi ile QT uzaması bildirilmiştir. Hastalarda klinik çalışmalar önceden var olan kalp hastalığı, trazodon hidroklorürün olabileceğini gösterir bu popülasyondaki bazı hastalarda aritmojenik. Aritmiler tanımlandı izole PVC'ler, ventriküler beyitler, senkoplu taşikardi ve içerir Torsades de Pointes. Pazarlama sonrası olaylar 100 mg'lık dozlarda bildirilmiştir veya daha az trazodonun derhal serbest bırakılması formuyla.
QT'yi uzatan ilaçların birlikte uygulanması CYP3A4 inhibitörleri olan aralık kardiyak riskini artırabilir aritmi.
Ortostatik Hipotansiyon ve Senkop
Ortostatik hipotansiyon dahil hipotansiyon ve trazodon hidroklorür alan hastalarda senkop bildirilmiştir. Bir antihipertansif ile birlikte kullanım, dozunda bir azalma gerektirebilir antihipertansif ilaç.
Anormal Kanama
Pazarlama sonrası veriler kullanım arasında bir ilişki olduğunu göstermiştir serotonin geri alımına müdahale eden ilaçların oluşumu gastrointestinal (GI) kanama. Trazodon ve arasında bir ilişki yok kanama olayları, özellikle GI kanaması gösterildi, hastalar olmalıdır eşzamanlı kullanımla ilişkili potansiyel kanama riski konusunda uyarıldı trazodon ve NSAID'lerin, aspirin veya pıhtılaşmayı etkileyen diğer ilaçların veya kanıyor. SSRI'lar ve SNRI'lar ile ilgili diğer kanama olayları arasında değişmektedir ekimoz, hematom, burun kanaması ve peteşiler hayatı tehdit eden kanamalara.
MAOI'lerle Etkileşim
Serotonerjik ilaçları birlikte alan hastalarda bir monoamin oksidaz inhibitörü (MAOI) ile ciddi raporlar vardır bazen hipertermi, sertlik, miyoklonus gibi ölümcül reaksiyonlar hayati belirtilerde hızlı dalgalanma ve zihinsel durum ile otonom istikrarsızlık deliryum ve komaya ilerleyen aşırı ajitasyon içeren değişiklikler. Bunlar son zamanlarda kesilen hastalarda da reaksiyonlar bildirilmiştir antidepresan tedavisi ve bir MAOI üzerinde başlatılmıştır. Bazı vakalar sunuldu nöroleptik malign sendromu andıran özelliklere sahiptir. Ayrıca, sınırlı serotonerjik antidepresanların kombine kullanımının etkileri üzerine hayvan verileri ve MAOI'ler, bu ilaçların kan basıncını yükseltmek için sinerjik olarak hareket edebileceğini düşündürmektedir ve davranışsal uyarımı çağrıştırır. Bu nedenle, Oleptro'nun tavsiye edilmesi MAOI ile kombinasyon halinde veya 14 gün içinde kullanılmamalıdır MAOI ile tedaviyi bırakmak. Benzer şekilde, en az 14 gün olmalıdır MAOI başlamadan önce Oleptro'yu durdurduktan sonra izin verilir .
Priapizm
Nadir priapizm vakaları (6'dan büyük ağrılı ereksiyonlar) saatlerce) trazodon alan erkeklerde bildirilmiştir. Priapizm, değilse derhal tedavi edilir, erektil dokuda geri dönüşü olmayan hasara neden olabilir. Erkekler ağrılı olsun ya da olmasın, 6 saatten fazla süren ereksiyonu olanlar ilacı derhal bırakmalı ve acil tıbbi yardım almalıdır.
Trazodon, sahip olan erkeklerde dikkatli kullanılmalıdır onları priapizme yatkın hale getirebilecek koşullar (ör.orak hücre anemisi multipl miyelom veya lösemi) veya anatomik deformasyonu olan erkeklerde penis (ör., angulasyon, kavernosal fibroz veya Peyronie hastalığı).
Hiponatremi
Hiponatremi, tedavinin bir sonucu olarak ortaya çıkabilir antidepresanlar. Birçok durumda, bu hiponatremi bunun sonucu gibi görünmektedir uygunsuz antidiüretik hormon salgısı sendromu (SIADH). Vakalar serum sodyum 110 mmol / L'den düşük olduğu bildirilmiştir. Yaşlı hastalar antidepresanlarla hiponatremi gelişme riski daha yüksek olabilir. Ayrıca, diüretik alan veya hacim tükenmiş olan hastalar olabilir daha büyük risk. Oleptro'nun kesilmesi, hastalarda düşünülmelidir semptomatik hiponatremi ve uygun tıbbi müdahale olmalıdır kurdu.
Hiponatremi belirtileri ve semptomları baş ağrısını içerir konsantre olma zorluğu, hafıza bozukluğu, karışıklık, halsizlik ve düşmelere yol açabilecek kararsızlık. Daha fazlası ile ilişkili belirti ve semptomlar şiddetli ve / veya akut vakalar halüsinasyon, senkop, nöbet, koma, içerir solunum durması ve ölüm.
Bilişsel ve Motor Bozukluğu Potansiyeli
Oleptro uyku hali veya sedasyona neden olabilir ve bozabilir potansiyel olarak performans için gerekli zihinsel ve / veya fiziksel yetenek tehlikeli görevler. Hastalar tehlikeli çalışma konusunda uyarılmalıdır otomobiller de dahil olmak üzere makineler, ilaç tedavisi onları olumsuz etkilemez.
Sonlandırma Belirtileri
Anksiyete, ajitasyon ve dahil olmak üzere yoksunluk belirtileri trazodon ile uyku bozuklukları bildirilmiştir. Klinik deneyim tamamlanmadan önce dozun kademeli olarak azaltılması gerektiğini düşündürmektedir tedavinin kesilmesi.
Hasta Danışmanlığı Bilgileri
Görmek İlaç Rehber.
Hastalar İçin Bilgi
Reçete yazanlar veya diğer sağlık profesyonelleri bilgilendirmelidir hastalar, aileleri ve bakıcıları faydalar ve riskler hakkında Oleptro ile tedavi ile ilişkili ve onlara danışmanlık yapmalıdır uygun kullanım.
Hastalar Buna Uyarılmalıdır
- İntihar riskinin artması potansiyeli vardır özellikle çocuklarda, gençlerde ve genç yetişkinlerde düşünceler.
- Aşağıdaki belirtiler bildirilmelidir doktor: kaygı, ajitasyon, panik atak, uykusuzluk, sinirlilik, düşmanlık, saldırganlık, dürtüsellik, akatizi, hipomani ve mani.
- Geçmişleri varsa doktorlarını bilgilendirmelidirler bipolar bozukluk, kalp hastalığı veya miyokard enfarktüsü.
- Serotonin sendromu ortaya çıkabilir ve semptomlar içerebilir zihinsel durumdaki değişiklikler (ör.ajitasyon, halüsinasyonlar ve koma), otonom kararsızlık (ör.taşikardi, kararsız kan basıncı ve hipertermi) nöromüsküler anormallikler (ör., hiperrefleksi, koordinasyon) ve / veya gastrointestinal belirtiler (ör., bulantı, kusma ve ishal).
- Hastalara Oleptro almanın neden olabileceği konusunda bilgilendirilmelidir duyarlı bireylerde hafif pupiller dilatasyon, bir açı kapatma glokomu bölümü. Önceden var olan glokom neredeyse her zaman vardır açık açılı glokom çünkü açı kapanması glokomu teşhis edildiğinde olabilir iridektomi ile kesin olarak tedavi edildi. Açık açılı glokom bir risk faktörü değildir açı kapatma glokomu için. Hastalar belirlemek için muayene edilmek isteyebilir açı kapanmasına duyarlı olup olmadıkları ve profilaktik olup olmadıkları prosedür (ör., iridektomi), eğer duyarlılarsa.
- Trazodon hidroklorür ile ilişkilendirilmiştir priapizmin ortaya çıkışı.
- Hipotansiyon için bir potansiyel vardır ortostatik hipotansiyon ve senkop.
- Potansiyel kanama riski vardır (dahil hayatı tehdit eden kanamalar) ve kanamayla ilgili olaylar (dahil ekimoz, hematom, burun kanaması ve peteşiler) trazodon hidroklorür ve NSAID'ler, aspirin veya etkileyen diğer ilaçlar pıhtılaşma veya kanama.
- Anksiyete, ajitasyon ve dahil olmak üzere yoksunluk belirtileri trazodon ile uyku bozuklukları bildirilmiştir. Klinik deneyim dozun kademeli olarak azaltılması gerektiğini düşündürmektedir.
Hastalar Buna Danışmanlık Etmelidir
- Oleptro uyku hali veya sedasyona neden olabilir ve bozabilir potansiyel olarak performans için gerekli zihinsel ve / veya fiziksel yetenek tehlikeli görevler. Hastalar tehlikeli çalışma konusunda uyarılmalıdır makul bir şekilde emin olana kadar otomobiller dahil makineler ilaç tedavisi onları etkilemez.
- Trazodon alkole yanıtı artırabilir barbitüratlar ve diğer CNS depresanları.
- Hamile kalmayı planlayan veya olan kadınlar emzirme, devam etmeleri gerekip gerekmediğini bir doktorla tartışmalıdır Oleptro kullanın, çünkü hamile ve emziren kadınlarda kullanılması önerilmez.
Önemli Yönetim Talimatları
- Oleptro tamamen yutulmalı veya yarıya kadar kırılmalıdır skor çizgisi.
- Kontrollü salım özelliklerini korumak için çiğnenmemeli veya ezilmemelidir.
- Oleptro her gün aynı saatte alınmalıdır akşam geç saatlerde tercihen yatmadan önce aç karnına.
Klinik Olmayan Toksikoloji
Kanserojenez, Mutajenez, Doğurganlığın Bozukluğu
İlaç veya doza bağlı karsinogenez oluşumu yoktu 18 mg için 300 mg / kg'a kadar günlük oral dozlarda trazodon alan sıçanlarda görülür aydır.
Belirli Popülasyonlarda Kullanın
Gebelik
Gebelik Kategorisi C
Trazodon hidroklorürün artmasına neden olduğu gösterilmiştir fetal rezorpsiyon ve fetus üzerindeki diğer olumsuz etkiler iki çalışmada kullanılmıştır doz seviyelerinde verildiğinde sıçan önerilenin yaklaşık 30-50 katıdır maksimum insan dozu. Birinde konjenital anomalilerde de bir artış oldu üç tavşan çalışmasının maksimum insan dozunun yaklaşık 15-50 katı. Gebe kadınlarda yeterli ve iyi kontrollü bir çalışma yoktur. Oleptro hamilelik sırasında sadece potansiyel fayda haklı çıkarsa kullanılmalıdır fetus için potansiyel risk.
Hemşirelik Anneler
Trazodon ve / veya metabolitleri emziren sıçanların sütü, ilacın anne sütünde salgılanabileceğini düşündürmektedir. Hemşirelik bir kadına Oleptro uygulandığında dikkatli olunmalıdır.
Pediatrik Kullanım
Pediyatrik popülasyonda güvenlik ve etkinlik vardır kurulmamış. Oleptro çocuklarda veya ergenlerde kullanılmamalıdır.
Geriatrik Kullanım
Klinikte Oleptro ile tedavi edilen 202 hastanın 65 yaşından büyük 9 hasta vardı. Güvenlik veya genel bir fark yok bu konular ve genç konular arasında etkinlik gözlenmiştir ve bildirilen diğer klinik literatür ve trazodon deneyimi yoktur yaşlı ve genç hastalar arasındaki yanıtlardaki farklılıkları tespit etti. Bununla birlikte, Oleptro'lu yaşlılarda deneyim sınırlı olduğundan, olmalıdır geriatrik hastalarda dikkatle kullanılır.
Antidepresanlar vakalarla ilişkilendirilmiştir daha büyük olabilecek yaşlı hastalarda klinik olarak anlamlı hiponatremi bu advers reaksiyon için risk
Böbrek Bozukluğu
Böbrek hastalarında Oleptro çalışılmamıştır değer düşüklüğü. Trazodon bu popülasyonda dikkatle kullanılmalıdır.
Karaciğer yetmezliği
Karaciğer hastalarında Oleptro çalışılmamıştır değer düşüklüğü. Trazodon bu popülasyonda dikkatle kullanılmalıdır.

YAN ETKİLER
Aşağıdaki ciddi advers reaksiyonlar açıklanmaktadır etiketlemenin başka bir yerinde :
- Klinik Kötüleşme ve İntihar Riski
- Serotonin Sendromu veya NMS benzeri Reaksiyonlar
- QT Uzatma ve Ani Ölüm Riski
- Ortostatik Hipotansiyon
- Anormal kanama olayları
- Priapizm
- Hiponatremi
- Bilişsel ve Motor Bozukluğu
- Sonlandırma belirtileri
En yaygın advers reaksiyonlar (≥% 5 olarak bildirilmiştir ve plasebo oranının iki katı): uyku hali / sedasyon, baş dönmesi, kabızlık, görme bulanık.
Tablo 2, advers olayların (AE) özetini göstermektedir en azından insidansla Oleptro tedavisinin kesilmesine yol açar Plasebo için% 1 ve en az iki kez.
Tablo 2: AE'ler
alınan eylem olarak kesilme (≥% 1 insidans ve insidans 2x plasebo)
| Oleptro N = 202 |
|
| Somnolans / Sedasyon | 8 (% 4.0) |
| Baş dönmesi | 7 (% 3.5) |
| Karışıklık durumu | 2 (% 1.0) |
| Koordinasyon anormal | 2 (% 1.0) |
| Baş ağrısı | 2 (% 1.0) |
| Bulantı | 2 (% 1.0) |
| Denge bozukluğu / Yürüyüş rahatsızlığı | 2 (% 1.0) |
Klinik Çalışmalar Deneyimi
Aşağıda açıklanan veriler 204'ü maruz kalan 406 hastanın klinik çalışmasında maruziyeti yansıtır plasebo ve 202 Oleptro'ya maruz kaldı. Hastalar 18-80 yaşları arasındaydı ve hastaların% 69.3'ünde ve% 67.5'inde en az bir önceki depresyon atağı vardı son 24 ayda plasebo ve aktif tedavi grubunda. İçinde bireysel hastalar, dozlar esnektir ve günde 150 ila 375 mg arasında değişmektedir. 6 haftalık tedavi süresi boyunca ortalama günlük doz 310 mg idi. Tabletler oral yoldan uygulandı ve günde bir kez toplam 8 süre verildi titrasyon süresi dahil haftalar.
Çünkü klinik çalışmalar çok çeşitli koşullar altında gerçekleştirilen advers reaksiyon oranları gözlenir bir ilacın klinik denemeleri, ilaçtaki oranlarla doğrudan karşılaştırılamaz başka bir ilacın klinik denemeleri ve gözlemlenen oranları yansıtmayabilir uygulama.
Tablo 3'ün özetini göstermektedir tüm tedavide ≥% 5 insidansla ortaya çıkan AE'ler Klinik araştırmacı tarafından ilişkili olduğu düşünülen Oleptro grubu çalışma ilacı ya da değil.
Tablo 3: En Yaygın
Tedavide Ortaya Çıkan Yan Etkiler (Aktif Tedavi Alan Hastaların ≥% 5'i)
| Tercih Edilen Terim | Plasebo N = 204 |
Oleptro N = 202 |
| Somnolans / Sedasyon | 39 (% 19) | 93 (% 46) |
| Baş ağrısı | 55 (% 27) | 67 (% 33) |
| Ağız kuruluğu | 26 (% 13) | 51 (% 25) |
| Baş dönmesi | 25 (% 12) | 50 (% 25) |
| Bulantı | 26 (% 13) | 42 (% 21) |
| Yorgunluk | 17 (% 8) | 30 (% 15) |
| İshal | 23 (% 11) | 19 (% 9) |
| Kabızlık | 4 (% 2) | 16 (% 8) |
| Sırt ağrısı | 7 (% 3) | 11 (% 5) |
| Görme bulanık | 0 (% 0) | 11 (% 5) |
Cinsel İşlev bozukluğu
İle ilgili olumsuz olaylar cinsel işlev bozukluğu (nedensellikten bağımsız olarak)% 4.9 ve% 1.5 oranında bildirilmiştir sırasıyla Oleptro ve plasebo ile tedavi edilen hastalar. Oleptro grubunda boşalma bozuklukları hastaların% 1.5'inde meydana geldi, libido azaldı hastaların% 1.5'inde erektil disfonksiyon ve anormal orgazm <% 1'dir hastalar.
Hayati İşaretler ve Ağırlık
Hayati belirtilerde (kan her iki tedavi grubunda da basınç, solunum hızı, nabız) veya ağırlık.
Aşağıda tedaviye bağlı advers bir liste bulunmaktadır insidansı ≥% 1 ila <% 5 olan reaksiyonlar (ör., daha az yaygın) Oleptro ile tedavi edilen hastalar. Bu listenin dahil edilmesi amaçlanmamıştır reaksiyonlar (i) önceki tablolarda veya etiketlemenin başka bir yerinde listelenmiş reaksiyonlar (ii) tedavi ile ilişkinin uzak olduğu, (iii) böyleydi genel olarak bilgilendirici olmayan ve (iv) sahip olmadığı düşünülen önemli klinik çıkarımlar. Reaksiyonlar vücut sistemine göre sınıflandırılır aşağıdaki tanımları kullanarak: sık görülen advers reaksiyonlar meydana gelir en az 1/100 hastada; Seyrek advers reaksiyonlar bunlar 1/100'den az hastada görülür.
Kulak ve Labirent Bozuklukları — Seyrek: hipoaküs, kulak çınlaması, baş dönmesi
Göz Bozuklukları- Sık: görme bozukluğu; Seyrek: kuru göz, göz ağrısı, fotofobi
Gastrointestinal Hastalıklar— Sık: karın ağrısı, kusma; Seyrek: reflü özofajit
Genel Bozukluklar ve Yönetim Sitesi Koşulları — Sık: ödem; Seyrek: yürüyüş rahatsızlığı
Bağışıklık Sistemi Bozuklukları— Seyrek: aşırı duyarlılık
Kas-iskelet sistemi ve Bağ Doku Bozuklukları — Sık: kas-iskelet şikayetler, kas ağrısı; Seyrek: kas seğirme
Sinir Sistemi Bozuklukları - Sık: koordinasyon anormal, disgeus, hafıza bozukluğu, migren, parestezi, titreme ; Seyrek: amnezi, afazi, hipoestezi, konuşma bozukluğu
Psikiyatrik Bozukluklar— Sık: ajitasyon, kafa karışıklığı, yönelim bozukluğu
Böbrek ve Üriner Bozukluklar - Sık: işeme aciliyeti; Seyrek: mesane ağrısı, idrar kaçırma
Solunum, Göğüs Hastalıkları ve Mediastinal Bozukluklar — Sık: dispne
Deri ve Deri Altı Doku Bozuklukları - Sık: gece terlemeleri; Seyrek: akne, hiperhidroz, ışığa duyarlılık reaksiyonu
Vasküler Bozukluklar - Seyrek: kızarma
Pazarlama Sonrası Deneyim
Trazodon hidroklorür ile ilgili spontan raporlar pazarlama sonrası deneyimlerden alınan aşağıdakileri içerir: anormal rüyalar, ajitasyon, alopesi, anksiyete, afazi, apne, ataksi, meme büyütme veya büyütme, kardiyospazm, serebrovasküler olay, titreme, kolestaz, klitorizm, konjestif kalp yetmezliği, diplopi, ödem, ekstrapiramidal semptomlar, büyük mal nöbetleri, halüsinasyonlar, hemolitik anemi, hirsutizm, hiperbilirubinemi, artmış amilaz, artmış tükürük salgısı, uykusuzluk, lökositoz, lökonyşi, sarılık, emzirme, karaciğer enzim değişiklikleri, methemoglobinemi, bulantı / kusma (en sık), parestezi, paranoyak reaksiyon, priapizm, kaşıntı, sedef hastalığı, psikoz, döküntü, stupor, uygunsuz ADH sendromu, geç diskinezi, açıklanamayan ölüm, idrar inkontinans, idrar retansiyonu, ürtiker, vazodilatasyon, vertigo ve zayıflık.
Bildirilen kardiyovasküler sistem etkileri aşağıdakileri içerir: iletim bloğu, ortostatik hipotansiyon ve senkop çarpıntı, bradikardi, atriyal fibrilasyon, miyokard enfarktüsü, kardiyak tutuklama, aritmi, ventriküler dahil ventriküler ektopik aktivite taşikardi ve QT uzaması. Pazarlama sonrası gözetimde, uzun süreli QT aralık, Torsades de Pointes ve ventriküler taşikardi bildirilmiştir günde 100 mg veya daha az dozlarda derhal serbest bırakılan trazodon formu ile .
İLAÇ ETKİLEŞİMLERİ
Monoamin Oksidaz İnhibitörleri (MAOI'ler)
Serotonerjik İlaçlar
Merkezi Sinir Sistemi (CNS) Depresanlar
Trazodon alkole yanıtı artırabilir barbitüratlar ve diğer CNS depresanları.
Sitokrom P450 3A4 İnhibitörleri
İn vitro ilaç metabolizması çalışmaları a olduğunu göstermektedir sitokrom P450 ile trazodon verildiğinde ilaç etkileşimi potansiyeli 3A4 (CYP3A4) inhibitörleri. Ritonavirin kısa süreli uygulanmasının etkisi (günde iki kez 200 mg, 4 doz) tek bir dozun farmakokinetiği üzerine 10 sağlıklı kişide trazodon (50 mg) çalışılmıştır. Cmax trazodon% 34 arttı, AUC 2.4 kat arttı, yarılanma ömrü arttı 2.2 kat azaldı ve açıklık% 52 azaldı. Olumsuz etkiler dahil ritonavir ve trazodon olduğunda bulantı, hipotansiyon ve senkop gözlendi birlikte uygulandı. Ketokonazol, indinavir ve diğerlerinin olması muhtemeldir İtrakonazol gibi CYP3A4 inhibitörleri, önemli ölçüde artışa neden olabilir yan etki potansiyeli olan trazodon plazma konsantrasyonları. Eğer trazodon, kardiyak riski olan güçlü bir CYP3A4 inhibitörü ile kullanılır aritmi artabilir ve daha düşük olabilir trazodon dozu dikkate alınmalıdır.
Sitokrom P450 İndükleyicileri (ör., karbamazepin)
Karbamazepin CYP3A4'ü indükler. Birlikte uygulamadan sonra günde 400 mg ila 300 mg trazodon ile günde 400 mg karbamazepin, karbamazepin, trazodonun plazma konsantrasyonlarını azalttı ve sırasıyla% 76 ve% 60 oranında mklorofenilipiperazin (aktif bir metabolit) precarbamazepine değerlerine kıyasla. Hastalar yakından izlenmelidir her ikisini de alırken artan bir trazodon dozuna ihtiyaç olup olmadığına bakın ilaçlar.
Digoksin ve Fenitoin
Artan serum digoksin veya fenitoin seviyeleri olmuştur bunlardan herhangi biriyle eşzamanlı olarak trazodon alan hastalarda bildirilmiştir ilaçlar. Serum seviyelerini izleyin ve dozajları gerektiği gibi ayarlayın.
NSAID'ler, Aspirin veya Pıhtılaşmayı veya Kanamayı Etkileyen Diğer İlaçlar
Serotonin arasındaki olası bir ilişki nedeniyle modüle edici ilaçlar ve gastrointestinal kanama, hastalar izlenmelidir ile ilişkili potansiyel kanama riski için ve bu konuda uyarılır trazodon ve NSAID'lerin, aspirin veya etkileyen diğer ilaçların birlikte kullanımı pıhtılaşma veya kanama.
Warfarin
Değiştirilmiş raporlar var (artmış ya da artmış hem warfarin hem de trazodon alırken protrombin süreleri azaldı.
Uyuşturucu Kullanımı ve Bağımlılığı
Kontrollü Madde
Oleptro kontrollü bir madde değildir.
Kötüye kullanım
Trazodon hidroklorür olmasa da klinik öncesi veya klinik çalışmalarda potansiyeli açısından sistematik olarak çalışılmıştır istismar, klinik çalışmalarda ilaç arama davranışı belirtisi görülmemiştir Oleptro ile. Ancak, ne ölçüde olduğunu tahmin etmek zordur CNS aktif ilaç kötüye kullanılacak, yönlendirilecek ve kötüye kullanılacaktır. Sonuç olarak, doktorlar hastaları uyuşturucu bağımlılığı öyküsü açısından dikkatle değerlendirmeli ve takip etmelidir hastaları yakından, trazodonun kötüye kullanılması veya kötüye kullanılması belirtileri açısından gözlemleyerek hidroklorür (ör., tolerans gelişimi, dozun artırılması, uyuşturucu arama davranışı).

Gebelik Kategorisi C
Trazodon hidroklorürün artmasına neden olduğu gösterilmiştir fetal rezorpsiyon ve fetus üzerindeki diğer olumsuz etkiler iki çalışmada kullanılmıştır doz seviyelerinde verildiğinde sıçan önerilenin yaklaşık 30-50 katıdır maksimum insan dozu. Birinde konjenital anomalilerde de bir artış oldu üç tavşan çalışmasının maksimum insan dozunun yaklaşık 15-50 katı. Gebe kadınlarda yeterli ve iyi kontrollü bir çalışma yoktur. Oleptro hamilelik sırasında sadece potansiyel fayda haklı çıkarsa kullanılmalıdır fetus için potansiyel risk.

Aşağıdaki ciddi advers reaksiyonlar açıklanmaktadır etiketlemenin başka bir yerinde :
- Klinik Kötüleşme ve İntihar Riski
- Serotonin Sendromu veya NMS benzeri Reaksiyonlar
- QT Uzatma ve Ani Ölüm Riski
- Ortostatik Hipotansiyon
- Anormal kanama olayları
- Priapizm
- Hiponatremi
- Bilişsel ve Motor Bozukluğu
- Sonlandırma belirtileri
En yaygın advers reaksiyonlar (≥% 5 olarak bildirilmiştir ve plasebo oranının iki katı): uyku hali / sedasyon, baş dönmesi, kabızlık, görme bulanık.
Tablo 2, advers olayların (AE) özetini göstermektedir en azından insidansla Oleptro tedavisinin kesilmesine yol açar Plasebo için% 1 ve en az iki kez.
Tablo 2: AE'ler
alınan eylem olarak kesilme (≥% 1 insidans ve insidans 2x plasebo)
| Oleptro N = 202 |
|
| Somnolans / Sedasyon | 8 (% 4.0) |
| Baş dönmesi | 7 (% 3.5) |
| Karışıklık durumu | 2 (% 1.0) |
| Koordinasyon anormal | 2 (% 1.0) |
| Baş ağrısı | 2 (% 1.0) |
| Bulantı | 2 (% 1.0) |
| Denge bozukluğu / Yürüyüş rahatsızlığı | 2 (% 1.0) |
Klinik Çalışmalar Deneyimi
Aşağıda açıklanan veriler 204'ü maruz kalan 406 hastanın klinik çalışmasında maruziyeti yansıtır plasebo ve 202 Oleptro'ya maruz kaldı. Hastalar 18-80 yaşları arasındaydı ve hastaların% 69.3'ünde ve% 67.5'inde en az bir önceki depresyon atağı vardı son 24 ayda plasebo ve aktif tedavi grubunda. İçinde bireysel hastalar, dozlar esnektir ve günde 150 ila 375 mg arasında değişmektedir. 6 haftalık tedavi süresi boyunca ortalama günlük doz 310 mg idi. Tabletler oral yoldan uygulandı ve günde bir kez toplam 8 süre verildi titrasyon süresi dahil haftalar.
Çünkü klinik çalışmalar çok çeşitli koşullar altında gerçekleştirilen advers reaksiyon oranları gözlenir bir ilacın klinik denemeleri, ilaçtaki oranlarla doğrudan karşılaştırılamaz başka bir ilacın klinik denemeleri ve gözlemlenen oranları yansıtmayabilir uygulama.
Tablo 3'ün özetini göstermektedir tüm tedavide ≥% 5 insidansla ortaya çıkan AE'ler Klinik araştırmacı tarafından ilişkili olduğu düşünülen Oleptro grubu çalışma ilacı ya da değil.
Tablo 3: En Yaygın
Tedavide Ortaya Çıkan Yan Etkiler (Aktif Tedavi Alan Hastaların ≥% 5'i)
| Tercih Edilen Terim | Plasebo N = 204 |
Oleptro N = 202 |
| Somnolans / Sedasyon | 39 (% 19) | 93 (% 46) |
| Baş ağrısı | 55 (% 27) | 67 (% 33) |
| Ağız kuruluğu | 26 (% 13) | 51 (% 25) |
| Baş dönmesi | 25 (% 12) | 50 (% 25) |
| Bulantı | 26 (% 13) | 42 (% 21) |
| Yorgunluk | 17 (% 8) | 30 (% 15) |
| İshal | 23 (% 11) | 19 (% 9) |
| Kabızlık | 4 (% 2) | 16 (% 8) |
| Sırt ağrısı | 7 (% 3) | 11 (% 5) |
| Görme bulanık | 0 (% 0) | 11 (% 5) |
Cinsel İşlev bozukluğu
İle ilgili olumsuz olaylar cinsel işlev bozukluğu (nedensellikten bağımsız olarak)% 4.9 ve% 1.5 oranında bildirilmiştir sırasıyla Oleptro ve plasebo ile tedavi edilen hastalar. Oleptro grubunda boşalma bozuklukları hastaların% 1.5'inde meydana geldi, libido azaldı hastaların% 1.5'inde erektil disfonksiyon ve anormal orgazm <% 1'dir hastalar.
Hayati İşaretler ve Ağırlık
Hayati belirtilerde (kan her iki tedavi grubunda da basınç, solunum hızı, nabız) veya ağırlık.
Aşağıda tedaviye bağlı advers bir liste bulunmaktadır insidansı ≥% 1 ila <% 5 olan reaksiyonlar (ör., daha az yaygın) Oleptro ile tedavi edilen hastalar. Bu listenin dahil edilmesi amaçlanmamıştır reaksiyonlar (i) önceki tablolarda veya etiketlemenin başka bir yerinde listelenmiş reaksiyonlar (ii) tedavi ile ilişkinin uzak olduğu, (iii) böyleydi genel olarak bilgilendirici olmayan ve (iv) sahip olmadığı düşünülen önemli klinik çıkarımlar. Reaksiyonlar vücut sistemine göre sınıflandırılır aşağıdaki tanımları kullanarak: sık görülen advers reaksiyonlar meydana gelir en az 1/100 hastada; Seyrek advers reaksiyonlar bunlar 1/100'den az hastada görülür.
Kulak ve Labirent Bozuklukları — Seyrek: hipoaküs, kulak çınlaması, baş dönmesi
Göz Bozuklukları- Sık: görme bozukluğu; Seyrek: kuru göz, göz ağrısı, fotofobi
Gastrointestinal Hastalıklar— Sık: karın ağrısı, kusma; Seyrek: reflü özofajit
Genel Bozukluklar ve Yönetim Sitesi Koşulları — Sık: ödem; Seyrek: yürüyüş rahatsızlığı
Bağışıklık Sistemi Bozuklukları— Seyrek: aşırı duyarlılık
Kas-iskelet sistemi ve Bağ Doku Bozuklukları — Sık: kas-iskelet şikayetler, kas ağrısı; Seyrek: kas seğirme
Sinir Sistemi Bozuklukları - Sık: koordinasyon anormal, disgeus, hafıza bozukluğu, migren, parestezi, titreme ; Seyrek: amnezi, afazi, hipoestezi, konuşma bozukluğu
Psikiyatrik Bozukluklar— Sık: ajitasyon, kafa karışıklığı, yönelim bozukluğu
Böbrek ve Üriner Bozukluklar - Sık: işeme aciliyeti; Seyrek: mesane ağrısı, idrar kaçırma
Solunum, Göğüs Hastalıkları ve Mediastinal Bozukluklar — Sık: dispne
Deri ve Deri Altı Doku Bozuklukları - Sık: gece terlemeleri; Seyrek: akne, hiperhidroz, ışığa duyarlılık reaksiyonu
Vasküler Bozukluklar - Seyrek: kızarma
Pazarlama Sonrası Deneyim
Trazodon hidroklorür ile ilgili spontan raporlar pazarlama sonrası deneyimlerden alınan aşağıdakileri içerir: anormal rüyalar, ajitasyon, alopesi, anksiyete, afazi, apne, ataksi, meme büyütme veya büyütme, kardiyospazm, serebrovasküler olay, titreme, kolestaz, klitorizm, konjestif kalp yetmezliği, diplopi, ödem, ekstrapiramidal semptomlar, büyük mal nöbetleri, halüsinasyonlar, hemolitik anemi, hirsutizm, hiperbilirubinemi, artmış amilaz, artmış tükürük salgısı, uykusuzluk, lökositoz, lökonyşi, sarılık, emzirme, karaciğer enzim değişiklikleri, methemoglobinemi, bulantı / kusma (en sık), parestezi, paranoyak reaksiyon, priapizm, kaşıntı, sedef hastalığı, psikoz, döküntü, stupor, uygunsuz ADH sendromu, geç diskinezi, açıklanamayan ölüm, idrar inkontinans, idrar retansiyonu, ürtiker, vazodilatasyon, vertigo ve zayıflık.
Bildirilen kardiyovasküler sistem etkileri aşağıdakileri içerir: iletim bloğu, ortostatik hipotansiyon ve senkop çarpıntı, bradikardi, atriyal fibrilasyon, miyokard enfarktüsü, kardiyak tutuklama, aritmi, ventriküler dahil ventriküler ektopik aktivite taşikardi ve QT uzaması. Pazarlama sonrası gözetimde, uzun süreli QT aralık, Torsades de Pointes ve ventriküler taşikardi bildirilmiştir günde 100 mg veya daha az dozlarda derhal serbest bırakılan trazodon formu ile .

İnsan Deneyimi
Sağlık risklerinin ilişkili olması beklenmektedir aşırı dozda Oleptro, büyük olasılıkla trazodon için olanlara benzer derhal serbest bırakılan formülasyonlar.
Yutma hastalarında aşırı dozdan ölüm meydana gelmiştir trazodon ve diğer CNS depresan ilaçları aynı anda (alkol; alkol ve kloral hidrat ve diazepam; amobarbital; klordiazepoksit; veya meprobamat).
En şiddetli reaksiyonların meydana geldiği bildirildi sadece trazodonun aşırı dozda priapizm, solunum durması, nöbetler olmuştur ve QT uzaması dahil EKG değişiklikleri. En çok bildirilen reaksiyonlar sık sık uyuşukluk ve kusma olmuştur. Doz aşımı artışa neden olabilir bildirilen advers reaksiyonların herhangi birinin insidansı veya ciddiyeti.
Doz aşımı yönetimi
Oleptro doz aşımı için spesifik bir antidot yoktur.
Tedavi bu genel önlemlerden oluşmalıdır doz aşımı yönetiminde, herhangi bir ilaçla etkili majör depresif bozukluğun tedavisi. Yeterli bir hava yolu, oksijenasyon sağlayın ve havalandırma. Kardiyak ritmi ve hayati belirtileri izleyin.
Genel destekleyici ve semptomatik önlemler de vardır tavsiye. Kusmanın indüksiyonu önerilmez. Gastrik lavaj a gerekirse uygun hava yolu korumalı büyük delikli orogastrik tüp olabilir yutulduktan hemen sonra veya semptomatik hastalarda yapılırsa endike olmalıdır. Aktif kömür uygulanmalıdır. Zorla diürez faydalı olabilir ilacın ortadan kaldırılmasını kolaylaştırmak.
Doz aşımı yönetiminde, olasılığını düşünün çoklu ilaç tutulumu. Doktor bir zehirle temas kurmayı düşünmelidir aşırı doz tedavisi hakkında ek bilgi için kontrol merkezi.

Klinik öncesi çalışmalar, trazodonun seçici olarak olduğunu göstermiştir nöronal serotoninin geri alımını inhibe eder ve 5-HT-2A / 2C'de bir antagonist görevi görür serotonin reseptörleri.
Trazodon bir monoamin oksidaz inhibitörü değildir ve amfetamin tipi ilaçların aksine, merkezi sinir sistemini uyarmaz.
Trazodon alfa 1-adrenerjik reseptörleri antagonize eder, a postüral hipotansiyon ile ilişkili olabilecek özellik.

Trazodone'un kararlı durum EAA değeri daha sonra eşdeğerdir günde üç (3) kez 100 mg derhal salınan (IR) Trazodon uygulaması (ortalama ± SD AUCss = 33058 ± 8006 ng * h / mL) ve Oleptro günde bir kez 300 mg (ortalama ± SD AUCss = 29131 ± 9931 ng * h / mL) bir hafta boyunca. Kararlı Durum Cmax ve Cmin trazodon 100 mg IR 3 trazodon uygulandıktan sonra eşdeğer değildi günde ortalama kez (ortalama ± SD Cmax, ss = 3118 ± 758 ng / mL, Cmin, ss = 843 ± 274 ng / mL) ve günde bir kez 300 mg Oleptro (ortalama ± SD Cmax, ss = 1812 ± 621 ng / mL, Cmin, ss = 674 ± 355 ng / mL) bir hafta boyunca.
Emilim
Trazodon oral uygulamadan sonra iyi emilir herhangi bir dokuda seçici lokalizasyon olmadan. Tek dozdan sonra Oleptro 300 mg tabletlerin açlık koşulları altında uygulanması, ortalama bir zirve a'da 1188 ± 362 ng / mL'lik trazodon plazma konsantrasyonu (Cmax) bildirilmiştir dozdan 9 saat sonra medyan Tmax. Oleptro 300 mg tabletler kısa süre içinde alındığında yüksek yağlı bir öğün yutulduktan sonra, Cmax buna kıyasla yaklaşık% 86 artar oruç koşullarında almak. Ancak, AUC0-∞ ve Tmax değildir gıdalardan önemli ölçüde etkilenir.
Oleptro tabletleri dozla orantılıdır bozulmamış olarak 75 mg ila 375 mg arasında değişen dozların tek doz uygulanması ikiye bölünmüş tabletler.
Metabolizma
İn vitro insan karaciğer mikrozomlarında yapılan çalışmalar göstermektedir trazodonun oksidatif bölünme yoluyla aktif bir metabolite metabolize olduğu CYP3A4 tarafından m-klorofenilpiperazin (MCPP). Olabilecek diğer metabolik yollar trazodonun metabolizmasında yer alan iyi karakterize edilmemiştir. Trazodon yoğun bir şekilde metabolize edilir; oral dozun% 1'inden azı atılır idrarda değişmedi.
Eliminasyon
Eliminasyon ağırlıklı olarak renaldir ve% 70 ila 75'i an oral doz, yutulduktan sonraki ilk 72 saat içinde idrarda geri kazanılır. Oleptro 300 mg tabletlerin tek doz uygulanmasını takiben, ortalama bir belirgindir 10 saatlik terminal yarılanma ömrü bildirilmiştir.
Protein Bağlama
Trazodon% 89 ila 95 proteine bağlıdır in vitro at insanlarda terapötik dozlarla elde edilen konsantrasyonlar.
However, we will provide data for each active ingredient


