









Composition:
Application:
Examiné médicalement par Kovalenko Svetlana Olegovna, Pharmacie Dernière mise à jour le 05.04.2022

Attention! Information sur la page est réservée aux professionnels de la santé! Les informations sont collectées dans des sources ouvertes et peuvent contenir des erreurs significatives! Soyez prudent et revérifiez toutes les informations de cette page!


Formes posologiques et forces
Les comprimés Oleptro sont disponibles dans les forces suivantes:
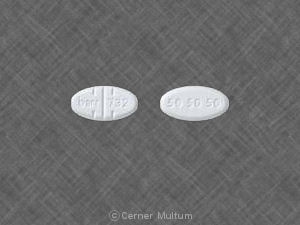
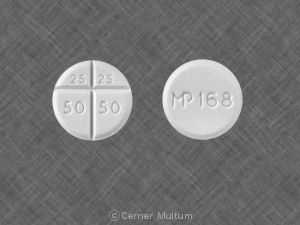
- Comprimés bissectables Oleptro contenant 150 mg de trazodone chlorhydrate (comprimé beige jaunâtre, en forme de capsule, enduit et marqué des deux côtés avec DDS 080 imprimé sur un côté)
- Comprimés bissectables Oleptro contenant 300 mg de trazodone chlorhydrate (comprimé beige-orange, en forme de capsule, enduit et sécable sur les deux côtés avec DDS 081 imprimé sur une face)
Stockage et manutention
Oleptro 150 mg est un beige jaunâtre, en forme de capsule comprimé à libération prolongée, enduit et marqué des deux côtés avec DDS 080 imprimé d'un côté. Il est fourni comme suit:
Bouteilles de 30 comprimés NDC 43595-080-03
Oleptro 300 mg est un beige-orange, en forme de capsule comprimé à libération prolongée, enduit et marqué des deux côtés avec DDS 081 imprimé d'un côté. Il est fourni comme suit:
Bouteilles de 30 comprimés NDC 43595-081-03
Conserver à température ambiante (15 - 30 ° C) serré conteneurs résistants à la lumière.
Angelini Pharma Inc. Gaithersburg, MD 20877. Révisé: juillet 2014

Oleptro ™ est indiqué pour le traitement du majeur trouble dépressif (TDM) chez l'adulte. L'efficacité d'Oleptro a été établi dans un essai de patients externes avec MDD ainsi que dans des essais avec le formulation à libération immédiate de trazodone.

Sélection de dose
La dose initiale recommandée d'Oleptro est de 150 mg une fois tous les jours chez l'adulte. La dose peut être augmentée de 75 mg / jour tous les trois jours (c.-à-d., commencer 225 mg le jour 4 du traitement). La dose quotidienne maximale ne doit pas dépasser 375 mg.
- Les comprimés d'Oleptro doivent être pris par voie orale en même temps tous les jours, en fin de soirée de préférence au coucher, à jeun.
- Une fois la réponse adéquate atteinte, la posologie peut être progressivement réduit, avec un ajustement ultérieur en fonction de la thérapeutique réponse.
- Les patients doivent être surveillés pour détecter les symptômes de sevrage lorsque arrêt du traitement par le chlorhydrate de trazodone. La dose doit être progressivement réduit autant que possible.
Traitement d'entretien
L'efficacité d'Oleptro pour le traitement d'entretien de Le MDD n'a pas été évalué. Bien qu'il n'y ait aucun ensemble de preuves à la disposition répondre à la question de savoir combien de temps un patient traité par Oleptro doit continuer le médicament, il est généralement recommandé de poursuivre le traitement pendant plusieurs mois après une première réponse. Les patients doivent être maintenus au plus bas dose efficace et être réévalué périodiquement pour déterminer le besoin continu pour le traitement d'entretien.
Passer un patient à ou à partir d'une monoamine oxydase Inhibiteur (IMAO) destiné à traiter les troubles psychiatriques
Au moins 14 jours devraient s'écouler entre l'arrêt de un IMAO destiné à traiter les troubles psychiatriques et l'initiation d'un traitement par Oleptro. Inversement, au moins 14 jours devraient être accordés après l'arrêt d'Oleptro avant de commencer un IMAO destiné à traiter les troubles psychiatriques.
Utilisation d'Oleptro avec d'autres IMAO tels que le linézolide ou le méthylène Bleu
Ne démarrez pas Oleptro chez un patient traité avec du bleu de méthylène linézolide ou intraveineux car il y a un risque accru du syndrome sérotoninergique. Chez un patient qui nécessite un traitement plus urgent d'un état psychiatrique, d'autres interventions, y compris l'hospitalisation, devraient être pris en considération.
Dans certains cas, un patient reçoit déjà Oleptro le traitement peut nécessiter un traitement urgent avec du linézolide ou du méthylène intraveineux bleu. Si des alternatives acceptables au linézolide ou au bleu de méthylène intraveineux le traitement n'est pas disponible et les avantages potentiels du linézolide ou le traitement intraveineux du bleu de méthylène est jugé supérieur aux risques de syndrome sérotoninergique chez un patient particulier, Oleptro doit être arrêté rapidement et du bleu de méthylène linézolide ou intraveineux peut être administré. Le patient doit être surveillé pour les symptômes du syndrome sérotoninergique pendant deux semaines ou jusqu'à 24 heures après la dernière dose de linézolide ou de bleu de méthylène intraveineux selon la première éventualité. La thérapie avec Oleptro peut être reprise 24 heures après le dernière dose de linézolide ou de bleu de méthylène intraveineux.
Le risque d'administrer du bleu de méthylène par voies non intraveineuses (telles que les comprimés oraux ou par injection locale) ou in les doses intraveineuses bien inférieures à 1 mg / kg avec Oleptro ne sont pas claires. Le le clinicien doit néanmoins être conscient de la possibilité d'émerger symptômes du syndrome sérotoninergique avec une telle utilisation (voir AVERTISSEMENTS ET PRÉCAUTIONS].
Instructions d'administration importantes
Les comprimés Oleptro sont notés pour offrir une flexibilité dosage.
Oleptro peut être avalé entier ou administré en deux comprimé en cassant le comprimé le long de la ligne de score. Briser le comprimé en deux n'affecte pas les propriétés de libération contrôlée du comprimé.
Afin de maintenir ses propriétés de libération contrôlée, Oleptro ne doit pas être mâché ou écrasé.

Inhibiteurs de la monoamine oxydase (IMAO)
L'utilisation des IMAO destinés à traiter les troubles psychiatriques avec Oleptro ou dans les 14 jours suivant l'arrêt du traitement par Oleptro contre-indiqué en raison d'un risque accru de syndrome sérotoninergique. L'utilisation de Oleptro dans les 14 jours suivant l'arrêt d'un IMAO destiné à traiter les soins psychiatriques les troubles sont également contre-indiqués..
Démarrage d'Oleptro chez un patient traité Les IMAO tels que le linézolide ou le bleu de méthylène intraveineux sont également contre-indiqués en raison d'un risque accru de syndrome sérotoninergique.

AVERTISSEMENTS
Inclus dans le cadre du PRÉCAUTIONS section.
PRÉCAUTIONS
Risque d'aggravation clinique et de suicide
Patients atteints d'un trouble dépressif majeur (TDM), tous deux adultes et pédiatrique, peut voir une aggravation de leur dépression et / ou du émergence d'idées et de comportements suicidaires (suicidalité) ou changements inhabituels comportement, qu'ils prennent ou non des antidépresseurs, et ce le risque peut persister jusqu'à ce qu'une rémission importante se produise. Le suicide est un risque connu de dépression et certains autres troubles psychiatriques et ces troubles eux-mêmes sont les plus grands prédicteurs du suicide. Il y a eu longtemps préoccupation permanente, cependant, que les antidépresseurs puissent jouer un rôle dans l'induction aggravation de la dépression et émergence de suicidalité chez certains patients pendant les premières phases du traitement. Analyses regroupées à court terme des essais contrôlés contre placebo de médicaments antidépresseurs (ISRS et autres) ont montré que ces médicaments augmentent le risque de pensée et de comportement suicidaires (suicidalité) chez les enfants, les adolescents et les jeunes adultes (âgés de 18 à 24 ans) avec MDD et autres troubles psychiatriques. Les études à court terme n'ont pas montré de augmentation du risque de suicidalité avec les antidépresseurs par rapport au placebo en adultes de plus de 24 ans; il y avait une réduction avec les antidépresseurs par rapport à placebo chez les adultes de 65 ans et plus.
Les analyses regroupées des essais contrôlés contre placebo en enfants et adolescents atteints de MDD, de trouble obsessionnel compulsif (TOC), ou les autres troubles psychiatriques comprenaient un total de 24 essais à court terme sur 9 antidépresseurs chez plus de 4 400 patients. Les analyses regroupées de essais contrôlés contre placebo chez des adultes atteints de MDD ou d'autres troubles psychiatriques comprenait un total de 295 essais à court terme (durée médiane de 2 mois) sur 11 antidépresseurs chez plus de 77 000 patients. Il y avait des variations considérables en risque de suicidalité chez les drogues, mais tendance à une augmentation de la patients plus jeunes pour presque tous les médicaments étudiés. Il y avait des différences dans risque absolu de suicidalité selon les différentes indications, avec le plus élevé incidence dans le MDD. Les différences de risque (drogue vs. placebo), cependant, l'étaient relativement stable dans les strates d'âge et dans toutes les indications. Ces risques différences (différence drogue-placebo dans le nombre de cas de suicidalité par 1 000 patients traités) sont fournis dans le tableau 1.
Tableau 1
| Age Range | Différence médicament-placebo dans le nombre de cas de suicidalité pour 1 000 patients traités |
| Augmente par rapport au placebo | |
| <18 | 14 cas supplémentaires |
| 18-24 | 5 cas supplémentaires |
| Diminue par rapport à Placebo | |
| 25 - 64 | 1 cas de moins |
| ≥ 65 | 6 cas de moins |
Aucun suicide n'est survenu dans aucun des cas les essais pédiatriques. Il y a eu des suicides dans les essais pour adultes, mais le nombre n'était pas suffisant pour parvenir à une conclusion sur l'effet de la drogue sur le suicide.
On ne sait pas si le le risque de suicidalité s'étend à une utilisation à plus long terme, c'est-à-dire., au-delà de plusieurs mois. Cependant, il existe des preuves substantielles de l'entretien contrôlé par placebo des essais chez l'adulte souffrant de dépression que l'utilisation d'antidépresseurs peut retarder le récidive de dépression.
Tous les patients traités avec des antidépresseurs pour toute indication doit être surveillée de manière appropriée et observé de près pour l'aggravation clinique, la suicidalité et les changements inhabituels comportement, en particulier pendant les premiers mois d'un cours de pharmacothérapie, ou en cas de changement de dose, augmente ou diminue.
Les symptômes suivants, anxiété, agitation, crises de panique, insomnie, irritabilité, hostilité, agressivité, impulsivité, akathisie (agitation psychomotrice), hypomanie , et la manie, ont été rapportées chez des patients adultes et pédiatriques traités avec des antidépresseurs pour les troubles dépressifs majeurs ainsi que pour les autres indications, à la fois psychiatriques et non psychiatriques. Bien qu'un lien de causalité entre l'émergence de tels symptômes et l'aggravation de la dépression et / ou l'émergence d'impulsions suicidaires n'a pas été établie, il y en a craignent que de tels symptômes ne représentent des précurseurs de suicidalité émergente.
Il faut réfléchir à changer le schéma thérapeutique, y compris éventuellement l'arrêt du médicaments, chez les patients dont la dépression est toujours pire, ou qui le sont éprouvant une suicidalité émergente ou des symptômes qui pourraient être des précurseurs aggravation de la dépression ou de la suicidalité, surtout si ces symptômes sont graves brusque au début ou ne faisait pas partie des symptômes de présentation du patient.
Familles et soignants de patients traités avec des antidépresseurs pour un trouble dépressif majeur ou d'autres indications, à la fois psychiatriques et non psychiatriques, doivent être alertées la nécessité de surveiller les patients pour l'émergence de l'agitation, de l'irritabilité les changements de comportement inhabituels et les autres symptômes décrits ci-dessus, ainsi que l'émergence de la suicidalité et de signaler immédiatement ces symptômes à la santé prestataires de soins. Cette surveillance devrait inclure l'observation quotidienne des familles et des soignants. Les prescriptions d'Oleptro doivent être écrites pour le plus petite quantité de comprimés compatible avec une bonne gestion du patient, dans l'ordre pour réduire le risque de surdosage.
Syndrome sérotoninergique
Le développement d'un un syndrome sérotoninergique potentiellement mortel a été signalé avec les ISRS et ISRS, y compris Oleptro, seuls mais particulièrement avec une utilisation concomitante de autres médicaments sérotoninergiques (y compris les triptans, les antidépresseurs tricycliques, fentanyl, lithium, tramadol, tryptophane, busipirone et St. John's Wort) et avec des médicaments qui altèrent le métabolisme de la sérotonine (en particulier, les IMAO, les deux ceux destinés à traiter les troubles psychiatriques et aussi d'autres, tels que linezolide et bleu de méthylène intraveineux).
Les symptômes du syndrome sérotoninergique peuvent inclure des changements d'état mental (par ex., agitation, hallucinations, délire, et coma), instabilité autonome (par ex., tachycardie, tension artérielle labile, étourdissements, diaphorèse, bouffées vasomotrices, hyperthermie), symptômes neuromusculaires (par ex., tremblements, rigidité, myoclonie, hyperréflexie, incoordination), convulsions et / ou symptômes gastro-intestinaux (par ex., nausées, vomissements, diarrhée). Les patients devraient être surveillé pour l'émergence du syndrome sérotoninergique.
L'utilisation concomitante d'Oleptro avec des IMAO destinés à traiter les troubles psychiatriques est contre-indiqué. Oleptro ne doit pas non plus être démarré chez un patient traité avec des IMAO tels que bleu de méthylène linézolide ou intraveineux. Tous les rapports avec du bleu de méthylène a fourni des informations sur la voie d'administration impliquée par voie intraveineuse administration dans la plage de doses de 1 mg / kg à 8 mg / kg. Aucun rapport impliqué l'administration de bleu de méthylène par d'autres voies (telles que les comprimés oraux ou injection de tissus locaux) ou à des doses plus faibles. Il peut y avoir des circonstances quand il est nécessaire pour initier un traitement avec un IMAO tel que le linézolide ou bleu de méthylène intraveineux chez un patient prenant Oleptro. Oleptro devrait l'être arrêté avant d'initier un traitement avec l'AMAI.
En cas d'utilisation concomitante d'Oleptro avec d'autres sérotoninergiques médicaments, triptans, antidépresseurs tricycliques, fentanyl, lithium, tramadol , buspirone, tryptophane et St. John's Wort est cliniquement justifié, patients doit être informé d'un risque potentiel accru de syndrome sérotoninergique en particulier pendant l'initiation du traitement et l'augmentation de la dose.
Traitement avec Oleptro et tout sérotoninergique concomitant les agents doivent être arrêtés immédiatement si les événements ci-dessus se produisent et un traitement symptomatique de soutien doit être instauré.
Glaucome à fermeture angulaire
La dilatation pupillaire qui se produit après l'utilisation de nombreuses personnes les antidépresseurs, y compris Oleptro, peuvent déclencher une attaque de fermeture d'angle dans a patient aux angles anatomiquement étroits qui n'a pas d'iridectomie brevetée.
Dépistage des patients pour un trouble bipolaire et surveillance Mania / Hypomania
Un épisode dépressif majeur peut être l'initiale présentation du trouble bipolaire. On le croit généralement (mais pas établi dans des essais contrôlés) qui traitent un tel épisode avec un l'antidépresseur seul peut augmenter la probabilité de précipitation d'un épisode mixte / maniaque chez les patients à risque de trouble bipolaire. Que ce soit les symptômes décrits pour l'aggravation clinique et le risque de suicide en représentent un tel la conversion est inconnue. Cependant, avant d'initier un traitement par un antidépresseur, les patients présentant des symptômes dépressifs doivent être correctement dépistés déterminer s'ils sont à risque de trouble bipolaire; un tel dépistage devrait inclure des antécédents psychiatriques détaillés, y compris des antécédents familiaux de suicide trouble bipolaire et dépression. Il convient de noter qu'Oleptro ne l'est pas approuvé pour une utilisation dans le traitement de la dépression bipolaire.
Prolongation QT et risque de mort subite
La trazodone est connue pour prolonger l'intervalle QT / QTc. Certains les médicaments qui prolongent l'intervalle QT / QTc peuvent provoquer des torsades de pointes avec mort subite et inexpliquée. La relation d'allongement de l'intervalle QT est la plus claire des augmentations plus importantes (20 ms et plus), mais il est possible que le QT / QTc plus petit les prolongations peuvent également augmenter le risque, en particulier chez les personnes sensibles tels que ceux souffrant d'hypokaliémie, d'hypomagnésémie ou d'une prédisposition génétique à QT / QTc prolongé.
Bien que Torsades de Pointes n'ait pas été observé avec l'utilisation d'Oleptro aux doses recommandées dans les essais de pré-commercialisation est une expérience trop limité pour exclure un risque accru. Cependant, il y en a eu rapports post-commercialisation de Torsades de Pointes avec la forme de libération immédiate de trazodone (en présence de multiples facteurs de confusion), même à des doses de 100 mg par jour ou moins.
Utilisation chez les patients atteints d'une maladie cardiaque
Le chlorhydrate de trazodone n'est pas recommandé pendant la phase de récupération initiale de l'infarctus du myocarde.
La prudence est de mise lors de l'administration d'Oleptro à les patients atteints d'une maladie cardiaque et ces patients doivent être étroitement surveillés car les antidépresseurs (y compris le chlorhydrate de trazodone) peuvent provoquer arythmies cardiaques.
Un allongement de l'intervalle QT a été rapporté avec un traitement par la trazodone. Études cliniques chez les patients atteints une maladie cardiaque préexistante indique que le chlorhydrate de trazodone peut l'être arythmogène chez certains patients de cette population. Arythmies identifiées comprennent les PVC isolés, les distiques ventriculaires, la tachycardie avec syncope, et Torsades de Pointes. Des événements post-commercialisation ont été rapportés à des doses de 100 mg ou moins avec la forme de libération immédiate de trazodone.
Administration concomitante de médicaments qui prolongent l'intervalle QT l'intervalle ou qui sont des inhibiteurs du CYP3A4 peut augmenter le risque cardiaque arythmie.
Hypotension et syncope orthostatiques
Hypotension, y compris hypotension orthostatique et une syncope a été rapportée chez des patients recevant du chlorhydrate de trazodone. L'utilisation concomitante avec un antihypertenseur peut nécessiter une réduction de la dose de le médicament antihypertenseur.
Saignement anormal
Les données post-commercialisation ont montré une association entre l'utilisation des médicaments qui interfèrent avec le recaptage de la sérotonine et la survenue de saignement gastro-intestinal (GI). Bien qu'il n'y ait aucune association entre la trazodone et des saignements, en particulier des saignements gastro-intestinaux, ont été observés, les patients devraient l'être mis en garde contre le risque potentiel de saignement associé à l'utilisation concomitante de trazodone et d'AINS, d'aspirine ou d'autres médicaments qui affectent la coagulation ou saignement. Les autres événements hémorragiques liés aux ISRS et aux IRS ont varié ecchymose, hématome, épistaxis et pétéchies à des hémorragies potentiellement mortelles.
Interaction avec les IMAO
Chez les patients recevant des médicaments sérotoninergiques en association avec un inhibiteur de la monoamine oxydase (IMAO), il a été signalé que grave réactions parfois fatales, y compris hyperthermie, rigidité, myoclonie instabilité autonome avec fluctuation rapide des signes vitaux et état mental les changements qui incluent l'agitation extrême progressant vers le délire et le coma. Ceux-ci des réactions ont également été rapportées chez des patients récemment arrêtés traitement antidépresseur et ont été lancés sur un IMAO. Certains cas ont été présentés avec des caractéristiques ressemblant au syndrome malin des neuroleptiques. De plus, limité données animales sur les effets de l'utilisation combinée d'antidépresseurs sérotoninergiques et Les IMAO suggèrent que ces médicaments peuvent agir en synergie pour augmenter la pression artérielle et évoquer l'excitation comportementale. Par conséquent, il est recommandé que Oleptro ne doit pas être utilisé en combinaison avec un IMAO ou dans les 14 jours suivant interrompre le traitement par un IMAO. De même, au moins 14 jours devraient être autorisé après avoir arrêté Oleptro avant de commencer un IMAO
Priapisme
Cas rares de priapisme (érections douloureuses supérieures à 6 heures) ont été signalés chez des hommes recevant de la trazodone. Le priapisme, sinon traité rapidement peut entraîner des dommages irréversibles au tissu érectile. Hommes qui ont une érection de plus de 6 heures, douloureuse ou non doit immédiatement arrêter le médicament et consulter un médecin d'urgence.
Trazodone doit être utilisé avec prudence chez les hommes qui en ont des conditions qui pourraient les prédisposer au priapisme (par ex., anémie falciforme , myélome multiple, ou leucémie), ou chez les hommes présentant une déformation anatomique du pénis (par ex., angulation, fibrose caverneuse ou maladie de Peyronie).
Hyponatrémie
Une hyponatrémie peut survenir à la suite du traitement par antidépresseurs. Dans de nombreux cas, cette hyponatrémie semble en résulter le syndrome de sécrétion inappropriée d'hormones antidiurétiques (SIADH). Cas avec du sodium sérique inférieur à 110 mmol / L ont été rapportés. Patients âgés peut être plus à risque de développer une hyponatrémie avec des antidépresseurs. Aussi, les patients prenant des diurétiques ou qui sont autrement épuisés en volume peuvent être à plus de risque. L'arrêt d'Oleptro doit être envisagé chez les patients atteints une hyponatrémie symptomatique et une intervention médicale appropriée doivent être institué.
Les signes et symptômes de l'hyponatrémie comprennent des maux de tête difficulté à se concentrer, troubles de la mémoire, confusion, faiblesse, et l'instabilité, qui peut entraîner des chutes. Signes et symptômes associés à plus les cas graves et / ou aigus ont inclus hallucination, syncope, convulsions, coma arrêt respiratoire et mort.
Potentiel de déficience cognitive et motrice
Oleptro peut provoquer une somnolence ou une sédation et peut altérer la capacité mentale et / ou physique requise pour l'exécution de potentiellement tâches dangereuses. Les patients doivent être avertis de l'utilisation dangereuse les machines, y compris les automobiles, jusqu'à ce qu'elles soient raisonnablement certaines que le le traitement médicamenteux ne les affecte pas négativement.
Symptômes d'arrêt
Symptômes de sevrage, y compris anxiété, agitation et des troubles du sommeil ont été signalés avec de la trazodone. Expérience clinique suggère que la dose soit progressivement réduite avant la fin arrêt du traitement.
Information sur le conseil aux patients
Voir Médicaments Guide.
Informations pour les patients
Les prescripteurs ou autres professionnels de la santé devraient en informer les patients, leurs familles et leurs soignants sur les avantages et les risques associé au traitement par Oleptro et devrait les conseiller dans son utilisation appropriée.
Les patients devraient être avertis de cela
- Il existe un risque accru de suicide pensées surtout chez les enfants, les adolescents et les jeunes adultes.
- Les symptômes suivants doivent être signalés au médecin: anxiété, agitation, crises de panique, insomnie, irritabilité, hostilité, agressivité, impulsivité, akathisie, hypomanie et manie.
- Ils devraient informer leur médecin s'ils ont des antécédents de trouble bipolaire, de maladie cardiaque ou d'infarctus du myocarde.
- Le syndrome sérotoninergique peut survenir et les symptômes peuvent inclure changements d'état mental (par ex., agitation, hallucinations et coma), autonome instabilité (par ex., tachycardie, tension artérielle labile et hyperthermie), aberrations neuromusculaires (par ex., hyperréflexie, incoordination) et / ou gastro-intestinale symptômes (par ex., nausées, vomissements et diarrhée).
- Les patients doivent être informés que la prise d'Oleptro peut provoquer une légère dilatation pupillaire, qui chez les individus sensibles, peut conduire à un épisode de glaucome à fermeture d'angle. Le glaucome préexistant est presque toujours glaucome à angle ouvert car le glaucome à fermeture d'angle, lorsqu'il est diagnostiqué, peut l'être traité définitivement par iridectomie. Le glaucome à angle ouvert n'est pas un facteur de risque pour le glaucome à fermeture d'angle. Les patients peuvent souhaiter être examinés pour déterminer s'ils sont sensibles à la fermeture d'angle et ont une prophylactique procédure (par ex., iridectomie), s'ils sont sensibles.
- Le chlorhydrate de trazodone a été associé à la occurrence du priapisme.
- Il existe un potentiel d'hypotension, y compris hypotension orthostatique et syncope.
- Il existe un risque potentiel de saignement (y compris hémorragies potentiellement mortelles) et événements liés aux saignements (y compris ecchymose, hématome, épistaxis et pétéchies) avec l'utilisation concomitante de chlorhydrate de trazodone et AINS, aspirine ou autres médicaments qui affectent coagulation ou saignement.
- Symptômes de sevrage, y compris anxiété, agitation et des troubles du sommeil ont été signalés avec de la trazodone. Expérience clinique suggère que la dose devrait être progressivement réduite.
Les patients devraient être conseillés
- Oleptro peut provoquer une somnolence ou une sédation et peut altérer la capacité mentale et / ou physique requise pour l'exécution de potentiellement tâches dangereuses. Les patients doivent être avertis de l'utilisation dangereuse les machines, y compris les automobiles, jusqu'à ce qu'elles soient raisonnablement certaines que le le traitement médicamenteux ne les affecte pas.
- La trazodone peut améliorer la réponse à l'alcool barbituriques et autres dépresseurs du SNC.
- Les femmes qui ont l'intention de devenir enceintes ou qui le sont l'allaitement doit discuter avec un médecin de l'opportunité de continuer utiliser Oleptro, car l'utilisation chez les femmes enceintes et allaitantes n'est pas recommandée.
Instructions d'administration importantes
- Oleptro doit être avalé entier ou cassé en deux la ligne de score.
- Afin de maintenir ses propriétés de libération contrôlée, il ne doit pas être mâché ou écrasé.
- Oleptro doit être pris à la même heure chaque jour, en le soir tardif de préférence au coucher, à jeun.
Toxicologie non clinique
Cancérogenèse, mutagenèse, altération de la fertilité
Aucune occurrence liée à la drogue ou à la dose de cancérogenèse ne l'était évident chez les rats recevant de la trazodone à des doses orales quotidiennes allant jusqu'à 300 mg / kg pendant 18 mois.
Utilisation dans des populations spécifiques
Grossesse
Catégorie de grossesse C
Il a été démontré que le chlorhydrate de trazodone provoque une augmentation résorption fœtale et autres effets indésirables sur le fœtus dans deux études utilisant le rat administré à des doses d'environ 30 à 50 fois supérieures à celles proposées dose humaine maximale. Il y a également eu une augmentation des anomalies congénitales en une seule de trois études sur le lapin à environ 15 à 50 fois la dose humaine maximale. Il n'y a pas d'études adéquates et bien contrôlées chez la femme enceinte. Oleptro ne doit être utilisé pendant la grossesse que si le bénéfice potentiel le justifie risque potentiel pour le fœtus.
Mères infirmières
La trazodone et / ou ses métabolites ont été trouvés dans le lait de rates allaitantes, ce qui suggère que le médicament peut être sécrété dans le lait maternel. La prudence s'impose lorsque Oleptro est administré à une femme qui allaite.
Utilisation pédiatrique
Sécurité et efficacité dans la population pédiatrique ont pas établi. Oleptro ne doit pas être utilisé chez les enfants ou les adolescents.
Utilisation gériatrique
Sur 202 patients traités par Oleptro dans la clinique essai, il y avait 9 patients de plus de 65 ans. Aucune différence globale de sécurité ou une efficacité a été observée entre ces sujets et les sujets plus jeunes, et aucune autre littérature clinique et expérience rapportée avec la trazodone ne l'ont pas fait les différences de réponses identifiées entre les patients âgés et les patients plus jeunes. Cependant, comme l'expérience chez les personnes âgées avec Oleptro est limitée, elle devrait l'être utilisé avec prudence chez les patients gériatriques.
Des antidépresseurs ont été associés à des cas de hyponatrémie cliniquement significative chez les patients âgés qui peuvent être plus importants risque de cet effet indésirable
Insuffisance rénale
Oleptro n'a pas été étudié chez les patients atteints de rein déficience. La trazodone doit être utilisée avec prudence dans cette population.
Insuffisance hépatique
Oleptro n'a pas été étudié chez les patients atteints de hépatique déficience. La trazodone doit être utilisée avec prudence dans cette population.

EFFETS CÔTÉ
Les effets indésirables graves suivants sont décrits ailleurs dans l'étiquetage:
- Risque d'aggravation clinique et de suicide
- Syndrome sérotoninergique ou réactions de type NMS
- Prolongation QT et risque de mort subite
- Hypotension orthostatique
- Événements hémorragiques anormaux
- Priapisme
- Hyponatrémie
- Cognitive et déficience motrice
- Symptômes d'arrêt
Les effets indésirables les plus courants (rapportés dans ≥ 5% et au double du taux de placebo) sont: somnolence / sédation, étourdissements, constipation, vision floue.
Le tableau 2 présente le résumé des événements indésirables (EI) conduisant à l'arrêt du traitement par Oleptro avec une incidence d'au moins 1% et au moins le double de celui du placebo.
Tableau 2: AE avec
arrêt comme action prise (incidence ≥ 1% et incidence 2x placebo)
| Oleptro N = 202 |
|
| Somnolence / Sédation | 8 (4,0%) |
| Vertiges | 7 (3,5%) |
| État confusionnel | 2 (1,0%) |
| Coordination anormale | 2 (1,0%) |
| Maux de tête | 2 (1,0%) |
| Nausées | 2 (1,0%) |
| Trouble de l'équilibre / Troubles de la marche | 2 (1,0%) |
Expérience en études cliniques
Les données décrites ci-dessous reflète l'exposition dans un essai clinique de 406 patients, dont 204 exposés placebo et 202 exposés à Oleptro. Les patients avaient entre 18 et 80 ans et 69,3% et 67,5% des patients avaient au moins un épisode de dépression précédent au cours des 24 derniers mois dans le groupe placebo et traité activement, respectivement. Dans patients individuels, les doses étaient flexibles et variaient de 150 à 375 mg par jour. La dose quotidienne moyenne pendant la période de traitement de 6 semaines était de 310 mg. Les comprimés ont été administrés par voie orale et ont été administrés une fois par jour pour une durée totale de 8 semaines, y compris la période de titration.
Parce que les essais cliniques le sont menée dans des conditions très variables, taux de réaction indésirable observés les essais cliniques d'un médicament ne peuvent pas être directement comparés aux taux du essais cliniques d'un autre médicament et ne peuvent pas refléter les taux observés dans pratique.
Le tableau 3 présente le résumé de tous les EI émergents liés au traitement qui se sont produits à une incidence ≥ 5% dans le Groupe Oleptro, considéré par l'investigateur clinique comme lié à le médicament à l'étude ou non.
Tableau 3: Le plus courant
Traitement des événements indésirables émergents (≥ 5% des patients sous traitement actif)
| Terme préféré | Placebo N = 204 |
Oleptro N = 202 |
| Somnolence / Sédation | 39 (19%) | 93 (46%) |
| Maux de tête | 55 (27%) | 67 (33%) |
| Bouche sèche | 26 (13%) | 51 (25%) |
| Vertiges | 25 (12%) | 50 (25%) |
| Nausées | 26 (13%) | 42 (21%) |
| Fatigue | 17 (8%) | 30 (15%) |
| Diarrhée | 23 (11%) | 19 (9%) |
| Constipation | 4 (2%) | 16 (8%) |
| Douleurs au dos | 7 (3%) | 11 (5%) |
| Vision floue | 0 (0%) | 11 (5%) |
Dysfonction sexuelle
Événements indésirables liés à les dysfonctionnements sexuels (quelle que soit la causalité) ont été signalés par 4,9% et 1,5% des patients traités respectivement par Oleptro et placebo. Dans le groupe Oleptro, des troubles de l'éjaculation sont survenus chez 1,5% des patients, une diminution de la libido s'est produite chez 1,5% des patients, dysfonction érectile et orgasme anormal <1% de patients.
Signes vitaux et poids
Il n'y a eu aucun changement notable dans les signes vitaux (sang pression, fréquence respiratoire, pouls) ou poids dans l'un ou l'autre groupe de traitement.
Voici une liste des indésirables liés au traitement réactions avec une incidence ≥ 1% à <5% (c.-à-d., moins commun) dans patients traités par Oleptro. Cette liste n'est pas destinée à inclure réactions (i) déjà répertoriées dans les tableaux précédents ou ailleurs dans l'étiquetage (ii) pour lesquels l'association avec le traitement est éloignée, (iii) qui l'étaient général comme non informatif, et (iv) qui n'étaient pas considérés comme ayant implications cliniques importantes. Les réactions sont classées par corps-système en utilisant les définitions suivantes: les effets indésirables fréquents sont ceux qui se produisent chez au moins 1/100 patients; Peu fréquent les effets indésirables sont ceux-là survenant chez moins de 1/100 patients.
Troubles de l'oreille et du labyrinthe — Peu fréquent: hypoacousie, acouphènes, vertiges
Troubles oculaires— Fréquent: perturbation visuelle; Peu fréquent: sécheresse oculaire, douleur oculaire, photophobie
Troubles gastro-intestinaux— Fréquent: douleurs abdominales, vomissements; Peu fréquent: œsophagite par reflux
Troubles généraux et conditions du site d'administration— Fréquent: œdème; Peu fréquent: perturbation de la marche
Troubles du système immunitaire— Peu fréquent: hypersensibilité
Troubles musculo-squelettiques et des tissus conjonctifs — Fréquent: plaintes musculo-squelettiques, myalgie ; Peu fréquent: muscle secousses
Troubles du système nerveux— Fréquent: coordination anormale, dysgueusie, troubles de la mémoire, migraine, paresthésie, tremblements ; Peu fréquent: amnésie, aphasie, hypoesthésie, troubles de la parole
Troubles psychiatriques— Fréquent: agitation, état confusionnel, désorientation
Troubles rénaux et urinaires— Fréquent: urgence de miction; Peu fréquent: douleur vésicale, incontinence urinaire
Troubles respiratoires, thoraciques et médiastinaux — Fréquent: dyspnée
Troubles de la peau et des tissus sous-cutanés— Fréquent: sueurs nocturnes; Peu fréquent: acné, hyperhidrose, réaction de photosensibilité
Troubles vasculaires— Peu fréquent: bouffées vasomotrices
Expérience post-commercialisation
Rapports spontanés concernant le chlorhydrate de trazodone reçus de l'expérience post-commercialisation sont les suivants: rêves anormaux , agitation, alopécie, anxiété, aphasie, apnée, ataxie, hypertrophie mammaire ou engorgement, cardiospasme, accident vasculaire cérébral, frissons, cholestase , clitorisme, insuffisance cardiaque congestive, diplopie, œdème, symptômes extrapyramidaux , convulsions de grand mal, hallucinations, anémie hémolytique, hirsutisme , hyperbilirubinémie, augmentation de l'amylase, augmentation de la salivation, insomnie , leucocytose, leuconychie, jaunisse, lactation, altérations des enzymes hépatiques , méthémoglobinémie, nausées / vomissements (le plus souvent), paresthésie, paranoïaque réaction, priapisme, prurit, psoriasis, psychose, éruption cutanée, stupeur , syndrome de la SDA inapproprié, dyskinésie tardive, mort inexpliquée, urinaire incontinence, rétention urinaire, urticaire, vasodilatation, vertiges, et faiblesse.
Effets sur le système cardiovasculaire qui ont été signalés inclure les éléments suivants: bloc de conduction, hypotension orthostatique et syncope, palpitations, bradycardie, fibrillation auriculaire, infarctus du myocarde, cardiaque arrêt, arythmie, activité ectopique ventriculaire, y compris ventriculaire tachycardie et allongement de l'intervalle QT. Dans la surveillance post-commercialisation, QT prolongé intervalle, torsades de pointes et tachycardie ventriculaire ont été rapportés avec la forme de trazodone à libération immédiate à des doses de 100 mg par jour ou moins .
INTERACTIONS DE DROGUES
Inhibiteurs de la monoamine oxydase (IMAO)
Médicaments sérotoninergiques
Dépresseurs du système nerveux central (SNC)
La trazodone peut améliorer la réponse à l'alcool barbituriques et autres dépresseurs du SNC.
Inhibiteurs du cytochrome P450 3A4
Des études in vitro sur le métabolisme des médicaments suggèrent qu'il existe un potentiel d'interactions médicamenteuses lorsque la trazodone est administrée avec le cytochrome P450 Inhibiteurs de 3A4 (CYP3A4). L'effet de l'administration à court terme du ritonavir (200 mg deux fois par jour, 4 doses) sur la pharmacocinétique d'une dose unique de la trazodone (50 mg) a été étudiée chez 10 sujets sains. La Cmax de la trazodone a augmenté de 34%, l'ASC a été multipliée par 2,4, la demi-vie a augmenté par 2,2 fois, et la clairance a diminué de 52%. Effets indésirables, y compris des nausées, une hypotension et une syncope ont été observées lorsque le ritonavir et la trazodone ont été co-administrés. Il est probable que le kétoconazole, l'indinavir et autres Les inhibiteurs du CYP3A4 tels que l'itraconazole peuvent entraîner des augmentations substantielles de concentrations plasmatiques de trazodone avec potentiel d'effets indésirables. Si la trazodone est utilisée avec un puissant inhibiteur du CYP3A4, le risque cardiaque l'arythmie peut être augmentée et plus faible la dose de trazodone doit être envisagée.
Inducteurs du cytochrome P450 (par ex., carbamazépine)
La carbamazépine induit le CYP3A4. Après la co-administration de carbamazépine 400 mg par jour avec 100 mg à 300 mg de trazodone par jour la carbamazépine a réduit les concentrations plasmatiques de trazodone et la mchlorophénylpipérazine (un métabolite actif) de 76% et 60% respectivement par rapport aux valeurs de précarbamazépine. Les patients doivent être étroitement surveillés voir s'il y a un besoin d'une dose accrue de trazodone lors de la prise des deux drogues.
Digoxine et phénytoïne
Des taux accrus de digoxine sérique ou de phénytoïne ont été signalé chez des patients recevant de la trazodone en même temps que l'un ou l'autre drogues. Surveillez les taux sériques et ajustez les doses au besoin.
AINS, aspirine ou autres médicaments affectant la coagulation ou le saignement
En raison d'une éventuelle association entre la sérotonine modulant les médicaments et les saignements gastro-intestinaux, les patients doivent être surveillés et mis en garde contre le risque potentiel de saignement associé au utilisation concomitante de trazodone et d'AINS, d'aspirine ou d'autres médicaments qui affectent coagulation ou saignement.
Warfarine
Des informations ont été modifiées (augmentées ou diminué) temps de prothrombine dans la prise de warfarine et de trazodone.
Abus de drogue et dépendance
Substance contrôlée
Oleptro n'est pas une substance contrôlée.
Abuser
Bien que le chlorhydrate de trazodone ne l'ait pas été systématiquement étudié dans les études précliniques ou cliniques pour son potentiel abus, aucune indication de comportement de recherche de médicaments n'a été observée dans les études cliniques avec Oleptro. Cependant, il est difficile de prédire dans quelle mesure a La drogue active du SNC sera utilisée à mauvais escient, détournée et maltraitée. Par conséquent, les médecins doit évaluer soigneusement les patients pour leurs antécédents d'abus de drogues et les suivre les patients de près, les observant pour détecter des signes d'abus ou d'abus de trazodone chlorhydrate (par ex., développement de la tolérance, incrémentation de la dose, comportement de recherche de drogue).

Catégorie de grossesse C
Il a été démontré que le chlorhydrate de trazodone provoque une augmentation résorption fœtale et autres effets indésirables sur le fœtus dans deux études utilisant le rat administré à des doses d'environ 30 à 50 fois supérieures à celles proposées dose humaine maximale. Il y a également eu une augmentation des anomalies congénitales en une seule de trois études sur le lapin à environ 15 à 50 fois la dose humaine maximale. Il n'y a pas d'études adéquates et bien contrôlées chez la femme enceinte. Oleptro ne doit être utilisé pendant la grossesse que si le bénéfice potentiel le justifie risque potentiel pour le fœtus.

Les effets indésirables graves suivants sont décrits ailleurs dans l'étiquetage:
- Risque d'aggravation clinique et de suicide
- Syndrome sérotoninergique ou réactions de type NMS
- Prolongation QT et risque de mort subite
- Hypotension orthostatique
- Événements hémorragiques anormaux
- Priapisme
- Hyponatrémie
- Cognitive et déficience motrice
- Symptômes d'arrêt
Les effets indésirables les plus courants (rapportés dans ≥ 5% et au double du taux de placebo) sont: somnolence / sédation, étourdissements, constipation, vision floue.
Le tableau 2 présente le résumé des événements indésirables (EI) conduisant à l'arrêt du traitement par Oleptro avec une incidence d'au moins 1% et au moins le double de celui du placebo.
Tableau 2: AE avec
arrêt comme action prise (incidence ≥ 1% et incidence 2x placebo)
| Oleptro N = 202 |
|
| Somnolence / Sédation | 8 (4,0%) |
| Vertiges | 7 (3,5%) |
| État confusionnel | 2 (1,0%) |
| Coordination anormale | 2 (1,0%) |
| Maux de tête | 2 (1,0%) |
| Nausées | 2 (1,0%) |
| Trouble de l'équilibre / Troubles de la marche | 2 (1,0%) |
Expérience en études cliniques
Les données décrites ci-dessous reflète l'exposition dans un essai clinique de 406 patients, dont 204 exposés placebo et 202 exposés à Oleptro. Les patients avaient entre 18 et 80 ans et 69,3% et 67,5% des patients avaient au moins un épisode de dépression précédent au cours des 24 derniers mois dans le groupe placebo et traité activement, respectivement. Dans patients individuels, les doses étaient flexibles et variaient de 150 à 375 mg par jour. La dose quotidienne moyenne pendant la période de traitement de 6 semaines était de 310 mg. Les comprimés ont été administrés par voie orale et ont été administrés une fois par jour pour une durée totale de 8 semaines, y compris la période de titration.
Parce que les essais cliniques le sont menée dans des conditions très variables, taux de réaction indésirable observés les essais cliniques d'un médicament ne peuvent pas être directement comparés aux taux du essais cliniques d'un autre médicament et ne peuvent pas refléter les taux observés dans pratique.
Le tableau 3 présente le résumé de tous les EI émergents liés au traitement qui se sont produits à une incidence ≥ 5% dans le Groupe Oleptro, considéré par l'investigateur clinique comme lié à le médicament à l'étude ou non.
Tableau 3: Le plus courant
Traitement des événements indésirables émergents (≥ 5% des patients sous traitement actif)
| Terme préféré | Placebo N = 204 |
Oleptro N = 202 |
| Somnolence / Sédation | 39 (19%) | 93 (46%) |
| Maux de tête | 55 (27%) | 67 (33%) |
| Bouche sèche | 26 (13%) | 51 (25%) |
| Vertiges | 25 (12%) | 50 (25%) |
| Nausées | 26 (13%) | 42 (21%) |
| Fatigue | 17 (8%) | 30 (15%) |
| Diarrhée | 23 (11%) | 19 (9%) |
| Constipation | 4 (2%) | 16 (8%) |
| Douleurs au dos | 7 (3%) | 11 (5%) |
| Vision floue | 0 (0%) | 11 (5%) |
Dysfonction sexuelle
Événements indésirables liés à les dysfonctionnements sexuels (quelle que soit la causalité) ont été signalés par 4,9% et 1,5% des patients traités respectivement par Oleptro et placebo. Dans le groupe Oleptro, des troubles de l'éjaculation sont survenus chez 1,5% des patients, une diminution de la libido s'est produite chez 1,5% des patients, dysfonction érectile et orgasme anormal <1% de patients.
Signes vitaux et poids
Il n'y a eu aucun changement notable dans les signes vitaux (sang pression, fréquence respiratoire, pouls) ou poids dans l'un ou l'autre groupe de traitement.
Voici une liste des indésirables liés au traitement réactions avec une incidence ≥ 1% à <5% (c.-à-d., moins commun) dans patients traités par Oleptro. Cette liste n'est pas destinée à inclure réactions (i) déjà répertoriées dans les tableaux précédents ou ailleurs dans l'étiquetage (ii) pour lesquels l'association avec le traitement est éloignée, (iii) qui l'étaient général comme non informatif, et (iv) qui n'étaient pas considérés comme ayant implications cliniques importantes. Les réactions sont classées par corps-système en utilisant les définitions suivantes: les effets indésirables fréquents sont ceux qui se produisent chez au moins 1/100 patients; Peu fréquent les effets indésirables sont ceux-là survenant chez moins de 1/100 patients.
Troubles de l'oreille et du labyrinthe — Peu fréquent: hypoacousie, acouphènes, vertiges
Troubles oculaires— Fréquent: perturbation visuelle; Peu fréquent: sécheresse oculaire, douleur oculaire, photophobie
Troubles gastro-intestinaux— Fréquent: douleurs abdominales, vomissements; Peu fréquent: œsophagite par reflux
Troubles généraux et conditions du site d'administration— Fréquent: œdème; Peu fréquent: perturbation de la marche
Troubles du système immunitaire— Peu fréquent: hypersensibilité
Troubles musculo-squelettiques et des tissus conjonctifs — Fréquent: plaintes musculo-squelettiques, myalgie ; Peu fréquent: muscle secousses
Troubles du système nerveux— Fréquent: coordination anormale, dysgueusie, troubles de la mémoire, migraine, paresthésie, tremblements ; Peu fréquent: amnésie, aphasie, hypoesthésie, troubles de la parole
Troubles psychiatriques— Fréquent: agitation, état confusionnel, désorientation
Troubles rénaux et urinaires— Fréquent: urgence de miction; Peu fréquent: douleur vésicale, incontinence urinaire
Troubles respiratoires, thoraciques et médiastinaux — Fréquent: dyspnée
Troubles de la peau et des tissus sous-cutanés— Fréquent: sueurs nocturnes; Peu fréquent: acné, hyperhidrose, réaction de photosensibilité
Troubles vasculaires— Peu fréquent: bouffées vasomotrices
Expérience post-commercialisation
Rapports spontanés concernant le chlorhydrate de trazodone reçus de l'expérience post-commercialisation sont les suivants: rêves anormaux , agitation, alopécie, anxiété, aphasie, apnée, ataxie, hypertrophie mammaire ou engorgement, cardiospasme, accident vasculaire cérébral, frissons, cholestase , clitorisme, insuffisance cardiaque congestive, diplopie, œdème, symptômes extrapyramidaux , convulsions de grand mal, hallucinations, anémie hémolytique, hirsutisme , hyperbilirubinémie, augmentation de l'amylase, augmentation de la salivation, insomnie , leucocytose, leuconychie, jaunisse, lactation, altérations des enzymes hépatiques , méthémoglobinémie, nausées / vomissements (le plus souvent), paresthésie, paranoïaque réaction, priapisme, prurit, psoriasis, psychose, éruption cutanée, stupeur , syndrome de la SDA inapproprié, dyskinésie tardive, mort inexpliquée, urinaire incontinence, rétention urinaire, urticaire, vasodilatation, vertiges, et faiblesse.
Effets sur le système cardiovasculaire qui ont été signalés inclure les éléments suivants: bloc de conduction, hypotension orthostatique et syncope, palpitations, bradycardie, fibrillation auriculaire, infarctus du myocarde, cardiaque arrêt, arythmie, activité ectopique ventriculaire, y compris ventriculaire tachycardie et allongement de l'intervalle QT. Dans la surveillance post-commercialisation, QT prolongé intervalle, torsades de pointes et tachycardie ventriculaire ont été rapportés avec la forme de trazodone à libération immédiate à des doses de 100 mg par jour ou moins .

Expérience humaine
Il est prévu que les risques pour la santé associés un surdosage d'Oleptro est très probablement similaire à celui de la trazodone formulations à libération immédiate.
La mort d'un surdosage est survenue chez des patients ingérant trazodone et autres médicaments dépresseurs du SNC simultanément (alcool; alcool et hydrate de chloral et diazépam; amobarbital; chlordiazépoxyde; ou méprobamate).
Les réactions les plus graves qui se sont produites se sont produites une surdose de trazodone seule a été un priapisme, un arrêt respiratoire, des convulsions et les changements ECG, y compris l'allongement de l'intervalle QT. Les réactions ont été les plus rapportées ont souvent été somnolence et vomissements. Un surdosage peut entraîner une augmentation dans l'incidence ou la gravité de l'un des effets indésirables signalés.
Gestion des surdoses
Il n'y a pas d'antidote spécifique pour un surdosage d'Oleptro.
Le traitement devrait consister en ces mesures générales employé dans la gestion des surdosages avec tout médicament efficace dans le traitement du trouble dépressif majeur. Assurer une voie aérienne adéquate, l'oxygénation et ventilation. Surveillez le rythme cardiaque et les signes vitaux.
Des mesures générales de soutien et symptomatiques le sont également recommandé. L'induction des vomissements n'est pas recommandée. Lavage gastrique avec a tube orogastrique à gros alésage avec protection appropriée des voies respiratoires, si nécessaire, peut être indiqué s'il est effectué peu de temps après l'ingestion ou chez les patients symptomatiques. Le charbon activé doit être administré. La diurèse forcée peut être utile faciliter l'élimination du médicament.
Dans la gestion du surdosage, envisagez la possibilité de implication multiple de médicaments. Le médecin devrait envisager de contacter un poison centre de contrôle pour des informations supplémentaires sur le traitement de tout surdosage.

Des études précliniques ont montré que la trazodone de manière sélective inhibe le recaptage neuronal de la sérotonine et agit comme un antagoniste au 5-HT-2A / 2C récepteurs de la sérotonine.
La trazodone n'est pas un inhibiteur de la monoamine oxydase et, contrairement aux médicaments de type amphétamine, ne stimule pas le système nerveux central.
La trazodone antagonise les récepteurs alpha 1-adrénergiques, a propriété pouvant être associée à une hypotension orthostatique.

L'ASC à l'état d'équilibre de Trazodone est équivalente après administration de Trazodone 100 mg à libération immédiate (IR) trois (3) fois par jour (moyenne ± ET AUCss = 33058 ± 8006 ng * h / ml) et Oleptro 300 mg une fois par jour (moyenne ± SD AUCss = 29131 ± 9931 ng * h / mL) pendant une semaine. Cmax et Cmin de l'état d'équilibre la trazodone n'était pas équivalente après l'administration de trazodone 100 mg IR 3 fois par jour (moyenne ± ET Cmax, ss = 3118 ± 758 ng / mL, Cmin, ss = 843 ± 274 ng / mL) et Oleptro 300 mg une fois par jour (moyenne ± ET Cmax, ss = 1812 ± 621 ng / mL, Cmin, ss = 674 ± 355 ng / ml) pendant une semaine.
Absorption
La trazodone est bien absorbée après administration orale sans localisation sélective dans aucun tissu. Après une dose unique administration de comprimés d'Oleptro 300 mg dans des conditions de jeûne, un pic moyen une concentration plasmatique de trazodone (Cmax) de 1188 ± 362 ng / ml a été rapportée à a Tmax médian de 9 heures après l'administration. Lorsque les comprimés d'Oleptro 300 mg sont pris sous peu après ingestion d'un repas riche en graisses, la Cmax augmente d'environ 86% par rapport à le prendre dans des conditions de jeûne. Cependant, AUC0-∞ et Tmax ne le sont pas significativement affecté par la nourriture.
Les comprimés d'Oleptro sont proportionnels à la dose administration à dose unique de doses allant de 75 mg à 375 mg intactes ou comprimés bisectés.
Métabolisme
In vitro des études sur les microsomes hépatiques humains montrent que la trazodone est métabolisée, par clivage oxydatif, en un métabolite actif m-chlorophénylpipérazine (mCPP) par CYP3A4. Autres voies métaboliques qui peuvent être impliqués dans le métabolisme de la trazodone n'ont pas été bien caractérisés. La trazodone est largement métabolisée; moins de 1% d'une dose orale est excrétée inchangé dans l'urine.
Élimination
L'élimination est principalement rénale, avec 70 à 75% d'an dose orale récupérée dans l'urine au cours des 72 premières heures d'ingestion. Après administration d'une dose unique de comprimés d'Oleptro 300 mg, une moyenne apparente une demi-vie terminale de 10 heures a été signalée.
Liaison aux protéines
La trazodone est liée à 89 à 95% aux protéines in vitro à concentrations atteintes avec des doses thérapeutiques chez l'homme.
However, we will provide data for each active ingredient


