Komposition:
Anwendung:
Medizinisch geprüft von Oliinyk Elizabeth Ivanovna, Apotheke Zuletzt aktualisiert am 10.04.2022

Achtung! Die Informationen auf der Seite sind nur für medizinisches Fachpersonal! Die Informationen werden in öffentlichen Quellen gesammelt und können aussagekräftige Fehler enthalten! Seien Sie vorsichtig und überprüfen Sie alle Informationen auf dieser Seite!
Top 20 Medikamente mit den gleichen Inhaltsstoffen:

Comtan

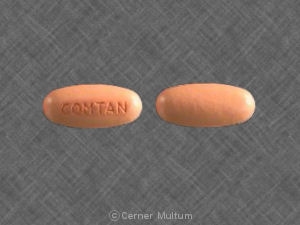
Comtan (entacapone) wird als 200 mg Filmtabletten zur oralen Verabreichung geliefert. Die ovalen Tabletten sind bräunlich-orange, unscored und geprägt "Comtan" auf einer Seite. Tabletten werden in HDPE-Behältern wie folgt bereitgestellt:
Flaschen von 100 UNZUSTELLBARKEITSBERICHT 0078-0327-05
Lagern Sie bei 25°C( 77°F), von 10 bis 15°C bis 30°C (59°F bis 86°F).
Hergestellt von: Orion Corporation, Orion Pharma (Espoo, Finnland). Überarbeitet: Feb 2016

Comtan ist als Ergänzung zu Levodopa und Carbidopa zur Behandlung des "Abnutzens" am Ende der Dosis bei Patienten mit Parkinson-Krankheit indiziert (siehe KLINISCHE PHARMAKOLOGIE, Klinische Studien).
Die Wirksamkeit von Comtan wurde bei Patienten mit Parkinson-Krankheit, bei denen kein "Abnutzen am Ende der Dosis"auftritt, nicht systematisch bewertet.

Die empfohlene Dosis von Comtan (Entacapon) beträgt eine 200-mg-Tablette, die gleichzeitig mit jeder Levodopa-und Carbidopa-Dosis maximal 8-mal täglich verabreicht wird (200 mg x 8 = 1,600 mg pro Tag). Die klinische Erfahrung mit täglichen Dosen über 1.600 mg ist begrenzt.
Comtan sollte immer in Verbindung mit Levodopa und Carbidopa verabreicht werden. Entacapon hat keine eigene antiparkinsonische Wirkung.
In klinischen Studien erforderte die Mehrheit der Patienten eine Abnahme der täglichen Levodopa-Dosis, wenn ihre tägliche Levodopa-Dosis größer oder gleich 800 mg war oder wenn die Patienten vor Beginn der Behandlung eine mittelschwere oder schwere Dyskinesie hatten.
Um die Reaktion eines einzelnen Patienten zu optimieren, kann eine Verringerung der täglichen Levodopa-Dosis oder eine Verlängerung des Intervalls zwischen den Dosen erforderlich sein. In klinischen Studien betrug die durchschnittliche Verringerung der täglichen Levodopa-Dosis bei Patienten, die eine Levodopa-Dosisreduktion benötigten, etwa 25%. (Mehr als 58% der Patienten mit Levodopa-Dosen über 800 mg täglich erforderten eine solche Reduktion.)
Comtan kann sowohl mit den Sofort-als auch mit den Retardformulierungen von Levodopa und Carbidopa kombiniert werden.
Comtan kann mit oder ohne Nahrung eingenommen werden (siehe KLINISCHE PHARMAKOLOGIE).
Patienten Mit eingeschränkter Leberfunktion
Patienten mit Leberfunktionsstörungen sollten mit Vorsicht behandelt werden. Die AUC und Cmax von Entacapon haben sich bei Patienten mit dokumentierter Lebererkrankung im Vergleich zu Kontrollen ungefähr verdoppelt. Diese Studien wurden jedoch mit Einzeldosis-Entacapon ohne Levodopa-und Dopa-Decarboxylase-Inhibitor-Coadministration durchgeführt, und daher wurden die Auswirkungen von Lebererkrankungen auf die Kinetik chronisch verabreichter Entacapon nicht bewertet (siehe KLINISCHE PHARMAKOLOGIE, Pharmakokinetik Von Entacapon).
Patienten aus Comtan zurückziehen
Ein schneller Entzug oder eine abrupte Verringerung der Comtan-Dosis kann zum Auftreten von Anzeichen und Symptomen der Parkinson-Krankheit führen (siehe KLINISCHE PHARMAKOLOGIE, Klinische Studien), und kann zu Hyperpyrexie und Verwirrung führen, einem Symptomkomplex, der NMS ähnelt (siehe VORKEHRUNG, Andere Ereignisse, die mit dopaminerger Therapie berichtet wurden). Dieses Syndrom sollte in der Differentialdiagnose für jeden Patienten in Betracht gezogen werden, der hohes Fieber oder schwere Starrheit entwickelt. Wenn entschieden wird, die Behandlung mit Comtan abzubrechen, sollten die Patienten genau überwacht und andere dopaminerge Behandlungen nach Bedarf angepasst werden. Obwohl Tapering Comtan nicht systematisch untersucht wurde, scheint es ratsam, Patienten langsam zurückzuziehen, wenn die Entscheidung getroffen wird, die Behandlung abzubrechen.

Comtan ist bei Patienten kontraindiziert, die eine Überempfindlichkeit gegen das Arzneimittel oder seine Inhaltsstoffe gezeigt haben.

UNWETTERWARNUNGEN
Monoaminoxidase (MAO) und COMT sind die beiden wichtigsten Enzyme systeme, die am Stoffwechsel von Katecholaminen beteiligt sind. Es ist theoretisch möglich ist daher, dass die Kombination von Comtan (Entacapon) und a nicht selektiver MAO-Inhibitor (z. B. Phenelzin und Tranylcypromin) würde zur Folge haben in Hemmung der Mehrheit der Wege, die für normal verantwortlich sind Katecholamin-Stoffwechsel. Aus diesem Grund sollten Patienten normalerweise nicht sein gleichzeitig mit Comtan und einem nicht selektiven MAO-Inhibitor behandelt.
Entacapon kann gleichzeitig mit einem selektiven eingenommen werden MAO-B-Inhibitor (z. B. Selegilin).
Arzneimittel, Die Durch Catechol-O-Methyltransferase (COMT) Metabolisiert werden)
Wenn eine einzelne 400 mg Dosis Entacapon gegeben wurde mit intravenöse isoprenalin (isoproterenol) und Adrenalin verabreicht, ohne levodopa und Dopa Decarboxylase-Inhibitor, die Gesamtmittel maximale Veränderungen in die Herzfrequenz während der Infusion war etwa 50% und 80% höher als bei Placebo, für isoprenalin und Adrenalin, beziehungsweise.
Daher sind Medikamente bekannt, die durch COMT metabolisiert werden, wie zum Beispiel isoproterenol, Adrenalin, Noradrenalin, Dopamin, Dobutamin, alpha-methyldopa, Apomorphin, isoetherine und bitolterol sollten sein verabreicht mit Vorsicht bei Patienten, die Entacapon unabhängig von der verabreichungsweg (einschließlich Inhalation), da ihre Wechselwirkung zur Folge haben kann bei erhöhten Herzfrequenzen, möglichen Arrhythmien und übermäßigen Blutdruckänderungen.
Ventrikuläre Tachykardie wurde bei einem 32-Jährigen festgestellt gesunder männlicher Freiwilliger in einer Interaktionsstudie nach Adrenalininfusion und orale Verabreichung von Entacapon. Die Behandlung mit Propranolol war erforderlich. Ein kausaler Zusammenhang zur Entacapon-Verabreichung erscheint wahrscheinlich, kann aber nicht sein mit Sicherheit zugeschrieben.
Einschlafen bei Aktivitäten des täglichen Lebens und der Schläfrigkeit
Patienten mit Parkinson-Krankheit mit Comtan behandelt, die Plasma-Levodopa-Spiegel erhöht, oder mit Levodopa berichtet haben. einschlafen ohne vorherige Warnung vor Schläfrigkeit während Aktivitäten des täglichen Lebens (einschließlich des Betriebs von Kraftfahrzeugen). Einige von diesen episoden führten zu Unfällen. Obwohl viele dieser Patienten berichteten somnolence während auf Comtan, einige nicht wahrnehmen, Warnzeichen, wie übermäßige Schläfrigkeit und glaubte, dass sie unmittelbar vor Veranstaltung. Einige dieser Ereignisse wurden erst ein Jahr später gemeldet beginn der Behandlung.
Das Risiko von Somnolenz war erhöht (Comtan 2% und placebo 0%) in kontrollierten Studien. Es wurde berichtet, dass einschlafen während in Aktivitäten des täglichen Lebens engagiert tritt immer in einer Umgebung von bereits existierenden somnolenz, obwohl Patienten eine solche Geschichte nicht geben können. Deshalb, verschreibende Ärzte sollten Patienten auf Schläfrigkeit oder Schläfrigkeit neu bewerten. da einige der Ereignisse weit nach Beginn der Behandlung auftreten. Prescriber sollte sich auch bewusst sein, dass Patienten Schläfrigkeit oder Schläfrigkeit möglicherweise nicht anerkennen bis direkt über Schläfrigkeit oder Schläfrigkeit während der Schwangerschaft befragt Aktivitäten. Den Patienten sollte geraten werden, während der Fahrt Vorsicht walten zu lassen, bedienen von Maschinen oder Arbeiten in Höhen während der Behandlung mit Comtan. Patienten, die bereits Somnolenz und/oder eine plötzliche Episode erlebt haben schlafstörungen sollten während der Behandlung nicht an diesen Aktivitäten teilnehmen mit Comtan
Beraten Sie die Patienten vor Beginn der Behandlung mit Comtan des Potenzials, Schläfrigkeit zu entwickeln und speziell nach Faktoren zu fragen, die kann dieses Risiko erhöhen, wie die gleichzeitige Anwendung von sedierenden Medikamenten und die vorhandensein von Schlafstörungen. Wenn ein Patient tagsüber Schläfrigkeit entwickelt oder episoden des Einschlafens bei Aktivitäten, die eine aktive Teilnahme erfordern (z. B. Gespräche, Essen usw.), Comtan sollte normalerweise eingestellt werden (sehen DOSIERUNG UND VERWERTUNG hinweise zur Einstellung von Comtan). Wenn die Entscheidung wird getroffen, Comtan fortzusetzen, Patienten sollten davon abgeraten werden fahren und andere potenziell gefährliche Aktivitäten zu vermeiden. Es gibt unzureichende Informationen, um festzustellen, ob die Dosisreduktion beseitigt wird episoden des Einschlafens bei Aktivitäten des täglichen Lebens.
VORKEHRUNG
Hypotonie, Orthostatische Hypotonie Und Synkope
Dopaminerge Therapie bei Parkinson-Patienten hat wurde mit orthostatischer Hypotonie assoziiert. Entacapon erhöht die levodopa Bioverfügbarkeit und daher könnte erwartet werden, dass das Auftreten von orthostatische Hypotonie. In kontrollierten Studien, etwa 1,2% und 0,8% 200 mg Entacapon-bzw. Placebo-Patienten berichteten über mindestens einen episode von Synkope. Berichte über Synkope waren im Allgemeinen häufiger bei Patienten in beiden Behandlungsgruppen, die eine Episode von dokumentierter Hypotonie hatten.
Halluzinationen und psychotisch-ähnliches Verhalten
Dopaminerge Therapie bei Patienten mit Parkinson-Krankheit wurde mit Halluzinationen in Verbindung gebracht. In klinischen Studien, Halluzinationen führte zu Drogenabbruch und vorzeitigem Entzug bei 0,8% und 0% der Patienten behandelt mit 200 mg Comtan bzw. Placebo. Halluzinationen führten zu krankenhausaufenthalt in 1,0% und 0,3% der Patienten in der 200 mg Comtan und Placebo gruppen, beziehungsweise. Agitation trat bei 1% der mit COMTAN behandelten Patienten auf und 0% mit placebo behandelten.
Postmarketing-Berichte zeigen, dass Patienten erleben Sie neue oder sich verschlechternde psychische Status - und Verhaltensänderungen, die sein können schweres, einschließlich psychotisch-ähnliches Verhalten während der Comtan-Behandlung oder danach starten oder Erhöhen der Dosis von Comtan. Andere Medikamente verschrieben, um zu verbessern die Symptome der Parkinson-Krankheit können ähnliche Auswirkungen auf das Denken und Verhalten. Abnormales Denken und Verhalten können paranoide Ideen verursachen, wahnvorstellungen, Halluzinationen, Verwirrung, Desorientierung, aggressives Verhalten, agitation und Delirium. Psychotisch-ähnliche Verhaltensweisen wurden auch beobachtet, während der die klinische Entwicklung von Comtan.
Patienten mit einer schweren psychotischen Störung sollten normalerweise nicht mit Comtan wegen der Gefahr einer Verschlimmerung behandelt werden psychose. Darüber hinaus können bestimmte Medikamente zur Behandlung von Psychosen verschlimmern die Symptome der Parkinson-Krankheit und kann die Wirksamkeit von Comtan.
Impulskontrolle und zwanghaftes Verhalten
Postmarketing-Berichte legen nahe, dass Patienten behandelt mit anti-Parkinson-Medikamente können intensive Triebe erleben zu spielen, erhöht sexueller Drang, intensiver Drang, unkontrollierbar Geld auszugeben, und andere intensive fordern. Patienten können diese Triebe möglicherweise nicht kontrollieren, während sie einen oder mehrere einnehmen von den Medikamenten, die zur Behandlung der Parkinson-Krankheit verwendet werden und das erhöht den zentralen dopaminergen Tonus, einschließlich Comtan, das mit Levodopa eingenommen wird und carbidopa. In einigen Fällen, wenn auch nicht alle, wurden diese Dränge gemeldet haben aufgehört, wenn die Dosis von Anti-Parkinson-Medikamenten reduziert wurde oder abgesetzt. Weil Patienten diese Verhaltensweisen möglicherweise nicht als abnormal erkennen. ist wichtig für verschreibende Ärzte, Patienten oder deren Betreuer gezielt zu fragen über die Entwicklung neuer oder erhöhter Glücksspieldrang, sexueller Drang, unkontrollierte Ausgaben oder andere Triebe während der Behandlung mit Entacapon. Ärzte sollten eine Dosisreduktion oder ein Absetzen von Comtan in Betracht ziehen, wenn ein Patient entwickelt solche Triebe während der Einnahme von Comtan
Durchfall Und Kolitis
In klinischen Studien entwickelte sich Durchfall bei 60 von 603 (10%) und 16 von 400 (4%) der mit 200 mg Comtan und Placebo behandelten Patienten, jeweils. Bei Patienten, die mit Comtan behandelt wurden, war der Durchfall im Allgemeinen mild bis mäßiger Schweregrad (8.6%), wurde aber in 1 als schwerwiegend angesehen.3%. Durchfall führte zum Rückzug in 10 von 603 (1.7%) Patienten, 7 (1.2%) mit mildem und mäßiger Durchfall und 3 (0.5%) mit schwerem Durchfall. Durchfall im Allgemeinen behoben nach Absetzen von Comtan. Zwei Patienten mit Durchfall waren eingeliefert. Typischerweise tritt Durchfall innerhalb von 4 Wochen bis 12 Wochen nach entacapone wird begonnen, aber es kann so früh wie die erste Woche und so spät erscheinen so viele Monate nach Beginn der Behandlung. Durchfall kann assoziiert sein mit Gewichtsverlust, dehydration und Hypokaliämie
Postmarketing-Erfahrung hat gezeigt, dass Durchfall ein zeichen einer medikamenteninduzierten mikroskopischen Kolitis, hauptsächlich lymphozytäre Kolitis. In diese Fälle Durchfall war in der Regel mittelschwer bis schwer, wässrig und nicht blutig, manchmal verbunden mit Austrocknung, Bauchschmerzen, Gewichtsverlust, und Hypokaliämie. In den meisten Fällen Durchfall und andere Colitis-bedingte die Symptome lösten sich auf oder verbesserten sich signifikant, wenn die Comtan-Behandlung abgebrochen wurde. Bei einigen Patienten mit Biopsie bestätigte Colitis, Durchfall aufgelöst hatte oder signifikant verbessert nach Absetzen von Comtan, aber wieder aufgetreten nach erneute Behandlung mit Comtan.
Wenn längerer Durchfall vermutet wird Comtan, sollte das Medikament abgesetzt werden und geeignete medizinische Therapie betrachten. Wenn die Ursache für anhaltenden Durchfall unklar bleibt oder anhält nach dem Absetzen von Entacapon, dann weitere diagnostische Untersuchungen einschließlich Koloskopie und Biopsien sollten berücksichtigt werden.
Dyskinesie
Comtan kann die dopaminergen Nebenwirkungen von potenzieren levodopa und kann bereits vorhandene Dyskinesien verursachen oder verschlimmern. Obwohl eine Verringerung der Levodopa-Dosis kann diese Nebenwirkung bei vielen Patienten verbessern in kontrollierten Studien weiterhin häufige Dyskinesie trotz einer verringerung ihrer Levodopa-Dosis. Die Inzidenz von Dyskinesien betrug 25% für die Behandlung mit Comtan und 15% für placebo. Die Inzidenz der Studie Widerrufsrecht für Dyskinesie war 1,5% für 200 mg Comtan und 0,8% für Placebo.
Andere Ereignisse, die mit dopaminerger Therapie berichtet wurden
Die unten aufgeführten Ereignisse sind Ereignisse, die mit dem verwendung von Medikamenten, die die dopaminerge Aktivität erhöhen.
Rhabdomyolyse
Fälle von schwerer Rhabdomyolyse wurden berichtet nach der Genehmigung von Comtan. Obwohl die Reaktionen typischerweise auftraten während Patienten mit Comtan behandelt wurden, ist die komplizierte Natur dieser Fälle macht es schwierig zu bestimmen, welche Rolle, wenn überhaupt, Comtan spielte in ihrem pathogenese. Schwere verlängerte motorische Aktivität einschließlich Dyskinesie kann auftreten für Rhabdomyolyse. Anzeichen und Symptome sind Fieber, Veränderung von bewusstsein, Myalgie, erhöhte Werte der Kreatinphosphokinase (CPK) und myoglobin (siehe VORKEHRUNG, Andere mit dopaminergen gemeldete Ereignisse Therapie).
Hyperpyrexie und Verwirrung
Fälle eines Symptomkomplexes, der neuroleptisch ähnelt malignes Syndrom (NMS) gekennzeichnet durch erhöhte Temperatur, muskulös starrheit, verändertes Bewusstsein und erhöhte CPK wurden berichtet in assoziation mit der schnellen Dosisreduktion oder Entzug anderer dopaminergen Droge. In den meisten dieser Fälle begannen die Symptome nach abruptem Absetzen von behandlung mit Entacapon oder Verringerung seiner Dosis oder nach Beginn der behandlung mit Entacapon. Die komplizierte Natur dieser Fälle macht es schwierig zu bestimmen, welche Rolle, wenn überhaupt, Comtan in ihrem gespielt haben pathogenese. Nach dem abrupten Rückzug wurden keine Fälle gemeldet oder dosisreduktion der Entacapon-Behandlung während klinischer Studien
Verschreibende Ärzte sollten beim Absetzen Vorsicht walten lassen entacapon-Behandlung. Wenn dies als notwendig erachtet wird, sollte der Rückzug fortgesetzt werden langsam. Wenn die Entscheidung getroffen wird, die Behandlung mit Comtan abzubrechen, empfehlungen umfassen die genaue Überwachung des Patienten und die Anpassung anderer dopaminerge Behandlungen nach Bedarf. Dieses Syndrom sollte in der Differentialdiagnose für jeden Patienten, der hohes Fieber oder schwere entwickelt Steifigkeit. Tapering Comtan wurde nicht systematisch bewertet.
Fibrotische Komplikationen
Fälle von retroperitonealer Fibrose, Lungeninfiltraten, Pleuraerguss und Pleuraverdickung wurden bei einigen Patienten berichtet behandlung mit dopaminergen Wirkstoffen aus Mutterkorn. Diese Komplikationen können sich auflösen wenn das Medikament abgesetzt wird, tritt jedoch nicht immer eine vollständige Auflösung auf. Obwohl angenommen wird, dass diese unerwünschten Ereignisse mit dem Ergolin zusammenhängen struktur dieser Verbindungen, unabhängig davon, ob andere, von nonergot abgeleitete Arzneimittel (e.g., entacapon), die dopaminerge Aktivität erhöhen, kann sie verursachen, ist unbekannt. Es sollte beachtet werden, dass die erwartete Inzidenz von fibrotischen Komplikationen so gering ist das, selbst wenn Entacapon diese Komplikationen mit ähnlichen Raten verursachte aufgrund anderer dopaminerger Therapien ist es unwahrscheinlich, dass es wurde in einer Kohorte der Entacapon exponierten Größe nachgewiesen. Vier Fälle von Lungenfibrose wurde während der klinischen Entwicklung von Entacapon berichtet, drei dieser Patienten wurden ebenfalls mit Pergolid und einer mit bromocriptin. Die Behandlungsdauer mit Entacapon lag zwischen 7 Monaten 17 Monate
Melanom
Epidemiologische Studien haben gezeigt, dass Patienten mit Parkinson-Krankheit haben ein höheres Risiko (2-bis etwa 6-fach höher) von entwicklung von Melanomen als die allgemeine Bevölkerung. Ob das erhöhte Risiko beobachtet wurde aufgrund der Parkinson-Krankheit oder anderen Faktoren, wie Drogen verwendet, um behandeln Parkinson-Krankheit, ist unklar.
Aus den oben genannten Gründen sind Patienten und Anbieter empfohlen, bei der Anwendung häufig und regelmäßig auf Melanome zu überwachen Comtan für jede Indikation. Idealerweise sollten regelmäßige Hautuntersuchungen sein durchgeführt von entsprechend qualifizierten Personen (z. B. Dermatologen).
Renale Toxizität
In einer einjährigen Toxizitätsstudie Entacapon (Plasmaexposition 20 mal so hoch wie beim Menschen, der die maximal empfohlene Tagesdosis von 1,600 erhält mg) verursachte eine erhöhte Inzidenz von Nephrotoxizität bei männlichen Ratten, die gekennzeichnet durch regenerative Tubuli, Verdickung der Basalmembranen, infiltration von mononukleären Zellen und tubulären Proteinabgüssen. Diese Effekte wurden nicht mit Änderungen der klinischen Chemieparameter in Verbindung gebracht, und es gibt keine etablierte Methode zur Überwachung des möglichen Auftretens dieser läsionen beim Menschen. Obwohl diese Toxizität eine artspezifische es gibt jedoch noch keine Beweise dafür.
Leberfunktionsstörung
Patienten mit Leberfunktionsstörungen sollten behandelt werden mit Vorsicht. Die AUC und Cmax von Entacapon haben sich bei Patienten mit dokumentierte Lebererkrankung im Vergleich zu Kontrollen (siehe KLINISCHE PHARMAKOLOGIE, Pharmakokinetik von Entacapon und DOSIERUNG UND VERWERTUNG).
Laboruntersuchungen
Comtan ist ein Chelator von Eisen. Die Auswirkungen von Entacapon auf die Eisenspeicher des Körpers sind unbekannt, jedoch eine Tendenz zur Abnahme des Serums eisen-Konzentrationen wurde in klinischen Studien festgestellt. In einer kontrollierten klinischen studie Serum Ferritinspiegel (als Marker für Eisenmangel und subklinische anämie) wurden mit Entacapon im Vergleich zu Placebo nach einem Jahr von behandlung und es gab keinen Unterschied in den Raten der Anämie oder verringert Hämoglobinspiegel.
Besondere Populationen
Patienten mit Leberfunktionsstörungen sollten behandelt werden mit vorsicht (siehe INDIKATION, DOSIERUNG UND VERWERTUNG).
Karzinogenese
Zweijährige Karzinogenitätsstudien von Entacapon waren durchgeführt bei Mäusen und Ratten. Ratten wurden einmal täglich durch orale Gavage behandelt mit entacapon-Dosen von 20, 90 oder 400 mg/kg. Eine erhöhte Inzidenz von Nieren tubuläre Adenome und Karzinome wurden bei männlichen Ratten gefunden, die mit den höchsten dosis von Entacapon. Plasma-Exposition (AUC) im Zusammenhang mit dieser Dosis wurden etwa 20-mal höher als die geschätzten Plasmabelastungen des Menschen empfangen der maximalen empfohlenen Tagesdosis (MRDD) von Entacapon (1.600 mg). Mäuse wurden einmal täglich durch orale Gabe mit Dosen von 20, 100 oder 600 mg/kg behandelt von entacapon (0.05, 0.3 und 2 mal die MRDD für den Menschen auf mg / m2 Basis). Wegen einer hohen Inzidenz vorzeitiger Mortalität bei Mäusen, die die höchste Dosis von Entacapon, die Maus-Studie ist keine angemessene Beurteilung der karzinogenitätsstudien. Obwohl keine behandlungsbedingten Tumoren bei Tieren beobachtet wurden empfangen der niedrigeren Dosen hat das krebserregende Potenzial von Entacapon nicht vollständig ausgewertet. Das kanzerogene Potenzial von Entacapon verabreicht in die Kombination mit Levodopa und Carbidopa wurde nicht bewertet
Mutagenese
Entacapone war mutagen und clastogenic in der in-vitro - - Maus lymphom tk-Assay in Gegenwart und Abwesenheit von metabolischer Aktivierung, und war clastogen in kultivierten menschlichen Lymphozyten in Gegenwart von metabolischen Aktivierung. Entacapon allein oder in Kombination mit levodopa und carbidopa, war in der in vivo maus-Mikronukleustest oder erbgutverändernd in bacterial reverse mutation assay (Ames test).
Beeinträchtigung der Fruchtbarkeit
Entacapone hat Fruchtbarkeit oder allgemein nicht beeinträchtigt reproduktionsleistung bei Ratten behandelt, die mit bis zu 700 mg/kg/Tag (plasma AUCs 28 mal die bei Menschen, die die MRDD von 1.600 mg erhalten). Verzögerte Paarung, aber keine Fruchtbarkeitsstörung, war bei weiblichen Ratten, die mit 700 mg/kg/Tag behandelt wurden, offensichtlich von Entacapon.
Schwangerschaft
Schwangerschaft Kategorie C
In embryofetalen Entwicklungsstudien war Entacapon verabreichung an schwangere Tiere während der gesamten Organogenese in Dosen von bis zu 1.000 mg/kg/Tag bei Ratten und 300 mg/kg/Tag bei Kaninchen. Erhöhte Inzidenz von fetale Variationen zeigten sich bei Würfen von Ratten, die mit den höchsten dosis, in Abwesenheit von offensichtlichen Anzeichen von mütterlicher Toxizität. Das mütterliche Plasma die Arzneimittelexposition (AUC) im Zusammenhang mit dieser Dosis betrug ungefähr das 34-fache der geschätzte Plasmaexposition beim Menschen, der die maximal empfohlene Tagesdosis erhält dosis (MRDD) von 1.600 mg. Erhöhte Häufigkeit von Abtreibungen, spät und insgesamt Resorptionen und verminderte fetale Gewichte wurden in den Würfen von beobachtet kaninchen, die mit mütterlich toxischen Dosen von 100 mg/kg/Tag (Plasma AUCs 0) behandelt wurden.4 mal diejenigen bei Menschen, die die MRDD erhalten) oder höher. Es gab keine Beweise für Teratogenität in diesen Studien
Wenn Entacapon jedoch weiblichen Ratten verabreicht wurde vor der Paarung und während der frühen Schwangerschaft, eine erhöhte Inzidenz von fetalen Augen anomalien (Makrophthalmie, Mikrophthalmie, Anophthalmie) wurden in der würfe von Dämmen, die mit Dosen von 160 mg/kg/Tag behandelt wurden (Plasma-AUCs 7-mal) bei Menschen, die die MRDD erhalten) oder höher, in Abwesenheit von mütterlicher Toxizität. Verabreichung von bis zu 700 mg / kg / Tag (Plasmaaucs 28-mal so hoch wie beim Menschen empfangen der MRDD) an weibliche Ratten während der letzten Schwangerschaftswoche und während der gesamten Laktation keine Hinweise auf Entwicklungsstörungen in der Nachkommen.
Entacapon wird immer gleichzeitig mit Levodopa verabreicht und Carbidopa, das bekanntermaßen viszerale und skelettale Missbildungen bei Kaninchen. Das teratogene Potenzial von entacapon in Kombination mit levodopa und Carbidopa wurde bei Tieren nicht bewertet.
Es gibt keine Erfahrung aus klinischen Studien in Bezug auf die Verwendung von Comtan bei schwangeren Frauen. Daher sollte Comtan verwendet werden während schwangerschaft nur, wenn der potenzielle Nutzen das potenzielle Risiko für den Fötus rechtfertigt.
Pflegende Frauen
In Tierversuchen wurde Entacapon in mütterliche rattenmilch.
Es ist nicht bekannt, ob Entacapon beim Menschen ausgeschieden wird Milch. Da viele Medikamente in die Muttermilch ausgeschieden werden, sollte Vorsicht geboten sein ausgeübt, wenn Entacapon einer stillenden Frau verabreicht wird.
Pädiatrische Verwendung
Sicherheit und Wirksamkeit bei pädiatrischen Patienten haben nicht gegründet worden.

Sehen WECHSELWIRKUNGEN MIT MEDIKAMENTEN.

Schwangerschaft Kategorie C
In embryofetalen Entwicklungsstudien war Entacapon verabreichung an schwangere Tiere während der gesamten Organogenese in Dosen von bis zu 1.000 mg/kg/Tag bei Ratten und 300 mg/kg/Tag bei Kaninchen. Erhöhte Inzidenz von fetale Variationen zeigten sich bei Würfen von Ratten, die mit den höchsten dosis, in Abwesenheit von offensichtlichen Anzeichen von mütterlicher Toxizität. Das mütterliche Plasma die Arzneimittelexposition (AUC) im Zusammenhang mit dieser Dosis betrug ungefähr das 34-fache der geschätzte Plasmaexposition beim Menschen, der die maximal empfohlene Tagesdosis erhält dosis (MRDD) von 1.600 mg. Erhöhte Häufigkeit von Abtreibungen, spät und insgesamt Resorptionen und verminderte fetale Gewichte wurden in den Würfen von beobachtet kaninchen, die mit mütterlich toxischen Dosen von 100 mg/kg/Tag (Plasma AUCs 0) behandelt wurden.4 mal diejenigen bei Menschen, die die MRDD erhalten) oder höher. Es gab keine Beweise für Teratogenität in diesen Studien
Wenn Entacapon jedoch weiblichen Ratten verabreicht wurde vor der Paarung und während der frühen Schwangerschaft, eine erhöhte Inzidenz von fetalen Augen anomalien (Makrophthalmie, Mikrophthalmie, Anophthalmie) wurden in der würfe von Dämmen, die mit Dosen von 160 mg/kg/Tag behandelt wurden (Plasma-AUCs 7-mal) bei Menschen, die die MRDD erhalten) oder höher, in Abwesenheit von mütterlicher Toxizität. Verabreichung von bis zu 700 mg / kg / Tag (Plasmaaucs 28-mal so hoch wie beim Menschen empfangen der MRDD) an weibliche Ratten während der letzten Schwangerschaftswoche und während der gesamten Laktation keine Hinweise auf Entwicklungsstörungen in der Nachkommen.
Entacapon wird immer gleichzeitig mit Levodopa verabreicht und Carbidopa, das bekanntermaßen viszerale und skelettale Missbildungen bei Kaninchen. Das teratogene Potenzial von entacapon in Kombination mit levodopa und Carbidopa wurde bei Tieren nicht bewertet.
Es gibt keine Erfahrung aus klinischen Studien in Bezug auf die Verwendung von Comtan bei schwangeren Frauen. Daher sollte Comtan verwendet werden während schwangerschaft nur, wenn der potenzielle Nutzen das potenzielle Risiko für den Fötus rechtfertigt.

Da klinische Studien unter sehr unterschiedlichen Bedingungen durchgeführt werden, kann die in den klinischen Studien eines Arzneimittels beobachtete Inzidenz von Nebenwirkungen (Anzahl einzigartiger Patienten, bei denen eine mit der Behandlung verbundene Nebenwirkung auftritt, pro Gesamtzahl der behandelten Patienten) nicht direkt mit der Inzidenz von Nebenwirkungen in den klinischen Studien eines anderen Arzneimittels verglichen werden und spiegelt möglicherweise nicht die Inzidenz von Nebenwirkungen wider, die in der Praxis beobachtet wurden.
Insgesamt wurden 1.450 Patienten mit Parkinson-Krankheit in klinischen Premarketing-Studien mit Comtan behandelt. Eingeschlossen waren Patienten mit schwankenden Symptomen sowie Patienten mit stabilen Reaktionen auf die Levodopa-Therapie. Alle Patienten erhielten jedoch eine gleichzeitige Behandlung mit Levodopa-Präparaten und waren in anderen klinischen Aspekten ähnlich.
Die am häufigsten beobachteten Nebenwirkungen (Inzidenz mindestens 3% höher als Placebo) in doppelblinden, placebokontrollierten Studien (N=1,003) im Zusammenhang mit der Anwendung von Comtan waren: Dyskinesie, Verfärbung des Urins, Durchfall, Übelkeit, Hyperkinesie, Bauchschmerzen, Erbrechen und Mundtrockenheit. Ungefähr 14% der 603 Patienten, denen Entacapon in den doppelblinden, placebokontrollierten Studien verabreicht wurde, haben die Behandlung aufgrund von Nebenwirkungen abgebrochen, verglichen mit 9% der 400 Patienten, die Placebo erhielten. Die häufigsten Ursachen für das Absetzen in abnehmender Reihenfolge waren: psychiatrische Störungen (2% vs. 1%), Durchfall (2%). 0%), Dyskinesie und hyperkinesie (2% vs. 1%), Übelkeit (2%). 1%) und Bauchschmerzen (1% vs. 0%)
Inzidenz unerwünschter Ereignisse in kontrollierten klinischen Studien
Tabelle 4 listet behandlungsbedingte unerwünschte Ereignisse auf, die bei mindestens 1% der mit Entacapon behandelten Patienten auftraten, die an den doppelblinden, placebokontrollierten Studien teilnahmen und in der Comtan-Gruppe zahlenmäßig häufiger auftraten als Placebo. In diesen Studien wurde Levodopa und Carbidopa (oder Levodopa und Benserazid) entweder Comtan oder Placebo zugesetzt.
Tabelle 4: Zusammenfassung der Patienten mit unerwünschten Ereignissen nach Beginn der Verabreichung des Arzneimittels in der Comtan-Gruppe von mindestens 1% und mehr als Placebo
| SYSTEM-ORGANKLASSE Bevorzugter Begriff | Comtan | Placebo |
| (n = 603) | (n = 400)) | |
| % der Patienten | % der Patienten | |
| ERKRANKUNGEN DER HAUT UND DER GLIEDMAßEN | ||
| Schwitzen erhöht | 2 | 1 |
| ERKRANKUNGEN DES BEWEGUNGSAPPARATES | ||
| Rückenschmerz | 2 | 1 |
| STÖRUNGEN DES ZENTRALEN UND PERIPHEREN NERVENSYSTEMS | ||
| Dyskinesie | 25 | 15 |
| Hyperkinesie | 10 | 5 |
| Hypokinesie | 9 | 8 |
| Schwindel | 8 | 6 |
| BESONDERE SINNE, ANDERE STÖRUNGEN | ||
| Geschmacksstörungen | 1 | 0 |
| PSYCHIATRISCHEN STÖRUNGEN | ||
| Angst | 2 | 1 |
| Somnolenz | 2 | 0 |
| Agitation | 1 | 0 |
| STÖRUNGEN DES GASTROINTESTINALEN SYSTEMS | ||
| Übelkeit | 14 | 8 |
| Durchfall | 10 | 4 |
| Bauchschmerzen | 8 | 4 |
| Verstopfung | 6 | 4 |
| Erbrechen | 4 | 1 |
| Mund trocken | 3 | 0 |
| Dyspepsie | 2 | 1 |
| Blähungen | 2 | 0 |
| Gastritis | 1 | 0 |
| Gastrointestinale Störungen | 1 | 0 |
| ERKRANKUNGEN DES ATMUNGSSYSTEMS | ||
| Dyspnoe | 3 | 1 |
| THROMBOZYTEN -, BLUTUNGS-UND GERINNUNGSSTÖRUNGEN | ||
| Purpura | 2 | 1 |
| STÖRUNGEN DES HARNSYSTEMS | ||
| Verfärbung des Urins | 10 | 0 |
| KÖRPER ALS GANZES-ALLGEMEINE STÖRUNGEN | ||
| Rückenschmerz | 4 | 2 |
| Müdigkeit | 6 | 4 |
| Asthenie | 2 | 1 |
| WIDERSTANDSMECHANISMUS STÖRUNGEN | ||
| Infektion bakteriell | 1 | 0 |
Auswirkungen von Geschlecht und Alter auf Nebenwirkungen
Es wurden keine Unterschiede in der Rate unerwünschter Ereignisse festgestellt, die Entacapon nach Alter oder Geschlecht zuzuschreiben sind.
Postmarketing-Berichte
Die folgenden spontanen Berichte über Nebenwirkungen, die zeitlich mit Comtan einhergehen, wurden seit Markteinführung identifiziert und sind in Tabelle 4 nicht aufgeführt. Da diese Reaktionen freiwillig aus einer Population unbekannter Größe gemeldet werden, ist es nicht immer möglich, ihre Häufigkeit zuverlässig abzuschätzen oder einen kausalen Zusammenhang zur Komtanexposition herzustellen.
Hepatitis mit hauptsächlich cholestatischen Merkmalen wurde berichtet.

Die Postmarketing-Daten umfassen mehrere Fälle von Überdosierung. Die höchste berichtete Dosis von Entacapon betrug mindestens 40.000 mg. Zu den akuten Symptomen und Anzeichen, die in diesen Fällen häufig auftreten, gehörten Schläfrigkeit und verminderte Aktivität, Zustände im Zusammenhang mit einem depressiven Bewusstseinsniveau (z. B. Koma, Verwirrung und Desorientierung) und Verfärbungen von Haut, Zunge und Urin sowie Unruhe, Unruhe und Aggression.
Die COMT-Hemmung durch Entacapon-Behandlung ist dosisabhängig. Eine massive Überdosierung von Comtan (Entacapon) kann theoretisch eine 100% ige Hemmung des COMT-Enzyms beim Menschen bewirken und dadurch den Metabolismus von endogenen und exogenen Katecholen verhindern.
Die höchste Tagesdosis, die dem Menschen verabreicht wurde, betrug 2.400 mg, die in einer Studie 14 Tage lang mit Levodopa und Carbidopa sechsmal täglich mit 400 mg bei 15 Parkinson-Patienten und in einer anderen Studie mit 800 mg dreimal täglich für 7 Tage bei 8 gesunden Probanden verabreicht wurde. Bei dieser Tagesdosis betrug die maximale Plasmakonzentration von Entacapon durchschnittlich 2.0 mcg pro ml (nach 45 Minuten im Vergleich zu 1.0 mcg pro mL und 1.2 mcg pro ml mit 200 mg Entacapon nach 45 Minuten). Bauchschmerzen und weicher Stuhl waren die am häufigsten beobachteten unerwünschten Ereignisse während dieser Studie. Tagesdosen bis zu 2.000 mg Comtan wurden 10-mal täglich mit Levodopa und Carbidopa oder Levodopa und Benserazid für mindestens 1 Jahr bei 10 Patienten, für mindestens 2 Jahre bei 8 Patienten und für mindestens 3 Jahre bei 7 Patienten verabreicht. Insgesamt ist die klinische Erfahrung mit täglichen Dosen über 1,600 mg jedoch begrenzt
Der Bereich der tödlichen Plasmakonzentrationen von Entacapon basierend auf Tierdaten betrug 80 mcg pro ml bis 130 mcg pro ml bei Mäusen. Atembeschwerden, Ataxie, Hypoaktivität und Krämpfe wurden bei Mäusen nach hohen oralen Dosen (Gavage) beobachtet.
Management Von Überdosierung
Die Behandlung einer Comtan-Überdosierung ist symptomatisch, es ist kein Gegenmittel gegen Comtan bekannt. Ein Krankenhausaufenthalt wird empfohlen und eine allgemeine unterstützende Versorgung ist angezeigt. Es gibt keine Erfahrung mit Hämodialyse oder Hämoperfusion, aber es ist unwahrscheinlich, dass diese Verfahren von Nutzen sind, da Comtan stark an Plasmaproteine gebunden ist. Eine sofortige Magenspülung und wiederholte Dosen von Holzkohle im Laufe der Zeit können die Beseitigung von Comtan beschleunigen, indem die Absorption und Reabsorption aus dem Gastrointestinaltrakt (GI) verringert wird. Die Angemessenheit des Atmungs - und Kreislaufsystems sollte sorgfältig überwacht und geeignete unterstützende Maßnahmen ergriffen werden. Die Möglichkeit von Arzneimittelwechselwirkungen, insbesondere mit katecholstrukturierten Arzneimitteln, sollte berücksichtigt werden

Feb 2016
However, we will provide data for each active ingredient
Verfügbar in Ländern
 Argentina
Argentina Australia
Australia Austria
Austria Bangladesh
Bangladesh Belgium
Belgium Brazil
Brazil Bulgaria
Bulgaria Canada
Canada China
China Croatia (Hrvatska)
Croatia (Hrvatska) Cyprus
Cyprus Czech Republic
Czech Republic Denmark
Denmark Ecuador
Ecuador Egypt
Egypt Estonia
Estonia Finland
Finland France
France Germany
Germany Greece
Greece Hong Kong
Hong Kong Hungary
Hungary Iceland
Iceland Indonesia
Indonesia Ireland
Ireland Israel
Israel Italy
Italy Japan
Japan Latvia
Latvia Liechtenstein
Liechtenstein Lithuania
Lithuania Luxembourg
Luxembourg Malaysia
Malaysia Malta
Malta Netherlands
Netherlands New Zealand
New Zealand Norway
Norway Peru
Peru Philippines
Philippines Poland
Poland Portugal
Portugal Romania
Romania Serbia
Serbia Slovakia
Slovakia Slovenia
Slovenia South Africa
South Africa Spain
Spain Sweden
Sweden Switzerland
Switzerland Taiwan
Taiwan Thailand
Thailand Tunisia
Tunisia Turkey
Turkey United Kingdom
United Kingdom USA
USA Venezuela
Venezuela
