


Composition:
Application:
Utilisé dans le traitement:
Examiné médicalement par Oliinyk Elizabeth Ivanovna, Pharmacie Dernière mise à jour le 10.04.2022

Attention! Information sur la page est réservée aux professionnels de la santé! Les informations sont collectées dans des sources ouvertes et peuvent contenir des erreurs significatives! Soyez prudent et revérifiez toutes les informations de cette page!
Top 20 des médicaments avec les mêmes ingrédients:


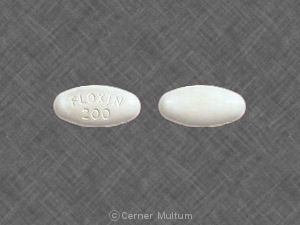
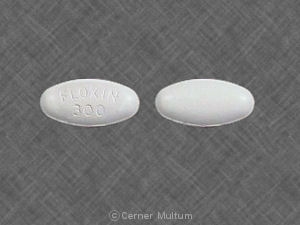
FLOXIN® (comprimés d'ofloxacine) Les comprimés sont fournis en jaune clair à 200 mg Comprimés ovales, à bords droits, enrobés de 300 mg de blanc et 400 mg d'or pâle. Chaque le comprimé se distingue par une empreinte de «FLOXIN (ofloxacine)» et appropriée force. Les comprimés FLOXIN® (ofloxacine) sont emballés dans des bouteilles dans les configurations suivantes:
200 mg comprimés - flacons de 50 (NDC 0062 - 1540-02)
300 mg comprimés - flacons de 50 (NDC 0062 - 1541-02)
400 mg comprimés - flacons de 100 (NDC 0062 - 1542-01)
Les comprimés FLOXIN® (ofloxacine) doivent être stockés dans des conteneurs bien fermés. Conserver à 25 ° C (77 ° F); excursions autorisées à 15-30 ° C (59-86 ° F).
Tenir hors de portée des enfants.
Ortho-McNeil, Division d'Ortho-McNeil-Janssen Pharmaceuticals, Inc. Raritan , NJ USA 08869. Délivré en janvier 2011

Réduire le développement de bactéries résistantes aux médicaments et maintenir l'efficacité de FLOXIN® (comprimés d'ofloxacine) Comprimés et autres médicaments antibactériens, FLOXIN® (comprimés d'ofloxacine) Les comprimés ne doivent être utilisés que pour traiter ou prévenir les infections qui sont prouvés ou fortement suspectés d'être causés par des bactéries sensibles. Lorsque des informations sur la culture et la sensibilité sont disponibles, elles doivent être prises en compte dans la sélection ou la modification du traitement antibactérien. En l'absence de telles données , l'épidémiologie locale et les schémas de sensibilité peuvent contribuer à l'empirique sélection de la thérapie.
FLOXIN® (comprimés d'ofloxacine) Les comprimés sont indiqués pour le traitement de les adultes atteints d'infections légères à modérées (sauf indication contraire) provoquées par des souches sensibles des micro-organismes désignés dans les infections répertoriées au dessous de. S'il vous plaît voir DOSAGE ET ADMINISTRATION pour des recommandations spécifiques.
Exacerbations bactériennes aiguës de bronchite chronique dû à Haemophilus influenzae ou Streptococcus pneumoniae.
Pneumonie d'origine communautaire dû à Haemophilus influenzae ou Streptococcus pneumoniae.
Infections simples de la peau et de la structure cutanée en raison de la méthicilline sensible Staphylococcus aureus, Streptococcus pyogenes, ou Proteus mirabilis.
Gonorrhée urétrale et cervicale aiguë et non compliquée dû à Neisseria gonorrhoeae (Voir. AVERTISSEMENTS.)
Uréthrite nongonococcique et cervicite dû à Chlamydia trachomatis. (Voir AVERTISSEMENTS.)
Infections mixtes de l'urètre et du col de l'utérus dû à Chlamydia trachomatis et Neisseria gonorrhoeae (Voir. AVERTISSEMENTS.)
Maladie inflammatoire pelvienne aiguë (y compris une infection grave) due à Chlamydia trachomatis et / ou Neisseria gonorrhoeae (Voir. AVERTISSEMENTS.)
REMARQUE: Si des micro-organismes anaérobies sont soupçonnés de contribuer au infection, une thérapie appropriée pour les agents pathogènes anaérobies doit être administrée.
Cystite simple dû à Citrobacter diversus, Enterobacter aerogenes, Escherichia coli, Klebsiella pneumoniae, Proteus mirabilis, ou Pseudomonas aeruginosa.
Infections compliquées des voies urinaires dû à Escherichia coli, Klebsiella pneumoniae, Proteus mirabilis, Citrobacter diversus *, ou Pseudomonas aeruginosa *.
Prostatite dû à Escherichia coli.
* = Bien que le traitement des infections dues à cet organisme dans ce système d'organes a démontré un résultat cliniquement significatif, l'efficacité a été étudiée en moins plus de 10 patients.
Des tests de culture et de sensibilité appropriés doivent être effectués avant le traitement afin d'isoler et d'identifier les organismes provoquant l'infection et de déterminer leur sensibilité à l'ofloxacine. Le traitement par l'ofloxacine peut être initié avant les résultats de ces tests sont connus; une fois que les résultats deviennent disponibles, approprié la thérapie doit être poursuivie.
Comme pour les autres médicaments de cette classe, certaines souches de Pseudomonas aeruginosa peuvent développer une résistance assez rapidement pendant le traitement par la ofloxacine. Culture et les tests de sensibilité effectués périodiquement pendant le traitement fourniront des informations non seulement sur l'effet thérapeutique de l'agent antimicrobien mais également sur le émergence possible de la résistance bactérienne.

La dose habituelle de comprimés FLOXIN® (comprimés d'ofloxacine) est de 200 mg à 400 mg par voie orale toutes les 12 h comme décrit dans le tableau d'administration suivant. Ces recommandations s'appliquer aux patients ayant une fonction rénale normale (c.-à-d., clairance de la créatinine> 50 mL / min). Pour les patients dont la fonction rénale a été modifiée (c.-à-d., clairance de la créatinine <50 ml / min), voir le Patients présentant une fonction rénale altérée Sous-section.
| Infection † | Dose unitaire | Fréquence | Durée | Dose quotidienne |
| Exacerbation bactérienne aiguë de la bronchite chronique | 400 mg | q12h | 10 jours | 800 mg |
| Comm. Pneumonie acquise | 400 mg | q12h | 10 jours | 800 mg |
| Infections non compliquées de la structure de la peau et de la peau | 400 mg | q12h | 10 jours | 800 mg |
| Gonorrhée urétrale et cervicale aiguë et non compliquée | 400 mg | dose unique | 1 jour | 400 mg |
| Cervicite / Uréthrite nongonococcique due à C. trachomatis | 300 mg | q12h | 7 jours | 600 mg |
| Infection mixte de l'urètre et du col de l'utérus due à C. trachomatis et N. gonorrhoeae | 300 mg | q12h | 7 jours | 600 mg |
| Maladie inflammatoire pelvienne aiguë | 400 mg | q12h | 10-14 jours | 800 mg |
| Cystite simple due à E. coli ou K. pneumoniae | 200 mg | q12h | 3 jours | 400 mg |
| Cystite non compliquée due à d'autres agents pathogènes approuvés | 200 mg | q12h | 7 jours | 400 mg |
| UTI compliquées | 200 mg | q12h | 10 jours | 400 mg |
| Prostatite due à E.Coli | 300 mg | q12h | 6 semaines | 600 mg |
| † EN RAISON DES PATHOGÈNES DÉSIGNÉS (Voir INDICATIONS ET UTILISATION.) |
Antiacides contenant du calcium, du magnésium ou de l'aluminium; sucralfate; divalent ou cations trivalents tels que le fer; ou multivitamines contenant du zinc; ou Videx® (didanosine) ne doit pas être pris dans le délai de deux heures avant ou à l'intérieur la période de deux heures après la prise d'ofloxacine. (Voir PRÉCAUTIONS.)
Patients présentant une fonction rénale altérée: La posologie doit être ajustée pour les patients avec une clairance de la créatinine <50 ml / min. Après une dose initiale normale, posologie doit être ajusté comme suit:
| Clairance de la créatinine | Dose de maintenance | Fréquence |
| 20-50 ml / min | la dose unitaire habituelle recommandée | q24h |
| <20 ml / min | ½ la dose unitaire habituelle recommandée | q24h |
Lorsque seule la créatinine sérique est connue, la formule suivante peut être utilisée pour estimer la clairance de la créatinine.
| Hommes: | Clairance de la créatinine (mL / min) = | (140 - âge) x (corps réel en kg) |
| 72 x (créatinine sérique) |
Femmes: 0,85 x la valeur calculée pour les hommes
La créatinine sérique doit représenter un état d'équilibre de la fonction rénale.
Patients atteints de cirrhose :
L'excrétion de l'ofloxacine peut être réduite chez les patients présentant une fonction hépatique sévère troubles (par ex., cirrhose avec ou sans ascite). Une dose maximale de 400 mg de l'ofloxacine par jour ne doit donc pas être dépassée.

FLOXIN® (comprimés d'ofloxacine) Les comprimés sont contre-indiqués chez les personnes atteintes des antécédents d'hypersensibilité associés à l'utilisation de l'ofloxacine ou de tout membre du groupe quinolone d'agents antimicrobiens.

AVERTISSEMENTS
Tendinopathie et rupture de Tendon
Les fluoroquinolones, y compris FLOXIN® (ofloxacine), sont associées à un risque accru de tendinite et de rupture tendineuse à tous les âges. Cette réaction indésirable le plus souvent implique le tendon d'Achille, et la rupture du tendon d'Achille peut nécessiter réparation chirurgicale. Tendinite et rupture du tendon dans la coiffe des rotateurs (l'épaule) la main, les biceps, le pouce et d'autres tendons ont également été signalés. Risque de développer une tendinite associée à la fluoroquinolone et une rupture du tendon est encore augmenté chez les patients plus âgés, généralement âgés de plus de 60 ans, chez ceux-ci prendre des corticostéroïdes et chez les patients atteints de transplantation rénale, cardiaque ou pulmonaire. Facteurs, en plus de l'âge et de l'utilisation des corticostéroïdes, qui peuvent augmenter indépendamment le risque de rupture du tendon comprend une activité physique intense, une insuffisance rénale et les troubles tendineux antérieurs tels que la polyarthrite rhumatoïde. Tendinite et tendon une rupture a été rapportée chez des patients prenant des fluoroquinolones qui n'en ont pas les facteurs de risque ci-dessus. La rupture du tendon peut se produire pendant ou après la fin de thérapie; cas survenus jusqu'à plusieurs mois après la fin du traitement ont été signalés. FLOXIN® (ofloxacine) doit être arrêté si le patient présente une douleur, un gonflement, une inflammation ou une rupture d'un tendon. Les patients doivent être informés se reposer au premier signe de tendinite ou de rupture tendineuse, et contacter leur fournisseur de soins de santé concernant le passage à un médicament antimicrobien non quinolone.
LA SÉCURITÉ ET L'EFFICACITÉ DE L'OflOXACINE DANS LES PATIENTS ET ADOLESCENTS PÉDIATRIQUES (SOUS L'ÂGE DE 18 ANS), LES FEMMES ENCEINTES ET LES FEMMES EN LACTE N'ONT PAS ÉTÉ ÉTABLI . (Voir PRÉCAUTIONS: Utilisation pédiatrique, Grossesse, et Sous-sections mères allaitantes.)
Chez le rat immature, l'administration orale d'ofloxacine à 5 à 16 fois la dose humaine maximale recommandée basée sur mg / kg ou 1 à 3 fois sur mg / m² a augmenté l'incidence et la gravité de l'ostéochondrose. Les lésions ne l'ont pas fait régresser après 13 semaines de sevrage. D'autres quinolones produisent également des produits similaires érosions dans les articulations portantes et autres signes d'arthropathie immatures animaux de diverses espèces. (Voir Pharmacologie animale.)
Exacerbation de Myasthenia Gravis
Les fluoroquinolones, y compris FLOXIN® (ofloxacine), ont une activité de blocage neuromusculaire et peut exacerber la faiblesse musculaire chez les personnes atteintes de myasthénie grave. Postmarketing événements indésirables graves, y compris les décès et les besoins en soutien ventilatoire ont été associés à l'utilisation de la fluoroquinolone chez les personnes atteintes de myasthénie grave. Évitez FLOXIN® (ofloxacine) chez les patients ayant des antécédents connus de myasthénie grave. (Voir INFORMATIONS PATIENTES et RÉACTIONS INDÉSIRABLES: Événements indésirables post-commercialisation.)
Effets sur le système nerveux central
Des convulsions, une augmentation de la pression intracrânienne et une psychose toxique l'ont été signalé chez des patients recevant des quinolones, y compris de l'ofloxacine. Quinolones , y compris la ofloxacine, peut également provoquer une stimulation du système nerveux central qui peut conduire à: tremblements, agitation / agitation, nervosité / anxiété, vertiges, confusion, hallucinations, paranoïa et dépression, cauchemars, insomnie, et pensées ou actes rarement suicidaires. Ces réactions peuvent survenir après la première dose. Si ces réactions surviennent chez des patients recevant de l'ofloxacine, le médicament doit être interrompue et des mesures appropriées instituées. L'insomnie peut être plus fréquente avec de l'ofloxacine que certains autres produits de la classe quinolone. Comme pour tous les quinolones, l'ofloxacine doit être utilisée avec prudence chez les patients connus ou suspicion de trouble du SNC qui peut prédisposer à des convulsions ou à une diminution de la crise seuil (par ex., artériosclérose cérébrale sévère, épilepsie) ou en présence d'autres facteurs de risque qui peuvent prédisposer à des saisies ou abaisser le seuil de saisie (par ex., certaines thérapies médicamenteuses, dysfonction rénale). (Voir PRÉCAUTIONS: Général, INFORMATIONS PATIENTES, INTERACTIONS DE DROGUES et RÉACTIONS INDÉSIRABLES.)
Réactions d'hypersensibilité
Hypersensibilité et / ou réactions anaphylactiques graves et parfois mortelles ont été rapportés chez des patients recevant un traitement par quinolones, y compris ofloxacine. Ces réactions surviennent souvent après la première dose. Quelques réactions ont été accompagnés d'un effondrement cardiovasculaire, d'une hypotension / choc, d'une crise , perte de conscience, picotements, œdème de Quincke (y compris la langue, le larynx, la gorge, ou œdème facial / gonflement), obstruction des voies respiratoires (y compris bronchospasme, brièveté de respiration et de détresse respiratoire aiguë), dyspnée, urticaire, démangeaisons, et autres réactions cutanées graves. Ce médicament doit être arrêté immédiatement à la première apparition d'une éruption cutanée ou tout autre signe d'hypersensibilité. Sérieux des réactions d'hypersensibilité aiguë peuvent nécessiter un traitement par l'épinéphrine et d'autres mesures réanimation, y compris l'oxygène, les fluides intraveineux, les antihistaminiques corticostéroïdes, amines sous-traitantes et gestion des voies respiratoires, comme indiqué cliniquement. (Voir PRÉCAUTIONS et RÉACTIONS INDÉSIRABLES.)
Autres événements graves et parfois mortels, certains dus à l'hypersensibilité, et certains en raison d'une étiologie incertaine, ont été rarement rapportés chez les patients recevant thérapie avec les quinolones, y compris l'ofloxacine. Ces événements peuvent être graves et se produisent généralement après l'administration de doses multiples. Manifestations cliniques peut inclure un ou plusieurs des éléments suivants:
- fièvre, éruption cutanée ou réactions dermatologiques sévères (par ex., nécrolyse épidermique toxique, Syndrome de Stevens-Johnson) ;
- vascularite; arthralgie; myalgie; maladie sérique;
- pneumonite allergique;
- néphrite interstitielle; insuffisance ou insuffisance rénale aiguë ;
- hépatite; jaunisse; nécrose hépatique aiguë ou échec ;
- anémie, y compris hémolytique et aplastique; thrombocytopénie, y compris thrombotique purpura thrombocytopénique; leucopénie; agranulocytose; pancytopénie; et / ou autres anomalies hématologiques.
Le médicament doit être arrêté immédiatement lors de la première apparition de la peau éruption cutanée, jaunisse ou tout autre signe d'hypersensibilité et mesures de soutien institué (voir INFORMATIONS PATIENTES et PUBLICITÉ RÉACTIONS).
Neuropathie périphérique
Rares cas de polyneuropathie axonale sensorielle ou sensorimotrice affectant les petits et / ou grands axones entraînant des paresthésies, des hypoesthésies, des dysesthésies et une faiblesse a été rapportée chez des patients recevant des quinolones, y compris de l'ofloxacine. L'ofloxacine doit être interrompue si le patient présente des symptômes de neuropathie y compris la douleur, la brûlure, les picotements, l'engourdissement et / ou la faiblesse ou d'autres altérations de sensation, y compris toucher léger, douleur, température, sens de position et vibratoire sensation afin d'empêcher le développement d'une condition irréversible.
Clostridium difficile une diarrhée associée (CDAD) a été rapportée utilisation de presque tous les agents antibactériens, y compris FLOXIN® (ofloxacine), et peut varier en gravité de diarrhée légère à colite mortelle. Traitement avec antibactérien les agents modifie la flore normale du côlon conduisant à une prolifération de C. difficile.
C. difficile produit des toxines A et B qui contribuent au développement de CDAD. Hypertoxine produisant des souches de C. difficile cause augmentée morbidité et mortalité, car ces infections peuvent être réfractaires à antimicrobiennes thérapie et peut nécessiter une colectomie. Le CDAD doit être pris en compte chez tous les patients qui présent avec diarrhée après utilisation d'antibiotiques. Des antécédents médicaux minutieux sont nécessaires depuis que le CDAD aurait eu lieu plus de deux mois après l'administration d'agents antibactériens.
Si le CDAD est suspecté ou confirmé, l'utilisation continue d'antibiotiques n'est pas dirigée contre C. difficile peut devoir être interrompu. Liquide et électrolyte appropriés gestion, supplémentation en protéines, traitement antibiotique de C. difficile, et une évaluation chirurgicale doit être instituée comme indiqué cliniquement. (Voir PUBLICITÉ RÉACTIONS.)
L'ofloxacine ne s'est pas révélée efficace dans le traitement de la syphilis.
Agents antimicrobiens utilisés à fortes doses pendant de courtes périodes de traitement la gonorrhée peut masquer ou retarder les symptômes de la syphilis incubante. Tous les patients avec la gonorrhée doit avoir un test sérologique pour la syphilis au moment du diagnostic. Les patients traités par l'ofloxacine pour la gonorrhée doivent avoir un sérologique de suivi tester la syphilis après trois mois et, si elle est positive, un traitement approprié antimicrobien doit être institué.
PRÉCAUTIONS
Général
Prescription des comprimés FLOXIN® (comprimés d'ofloxacine) en l'absence de preuve ou une infection bactérienne fortement suspectée ou une indication prophylactique est peu probable apporter des bénéfices au patient et augmenter le risque de développement de bactéries résistantes aux médicaments.
Une hydratation adéquate des patients recevant de l'ofloxacine doit être maintenue empêcher la formation d'une urine hautement concentrée.
Administrer l'ofloxacine avec prudence en présence d'insuffisance / altération rénale ou hépatique. Chez les patients présentant une insuffisance / altération rénale ou hépatique connue ou suspectée une observation clinique minutieuse et des études de laboratoire appropriées doivent être effectuées avant et pendant le traitement, car l'élimination de l'ofloxacine peut être réduite. Dans patients présentant une insuffisance rénale (clairance de la créatinine <50 mg / ml), altération du schéma posologique est nécessaire. (Voir PHARMACOLOGIE CLINIQUE et DOSAGE ET ADMINISTRATION.)
Réactions de photosensibilité / phototoxicité modérées à sévères, ces dernières qui peut se manifester par des réactions exagérées de coup de soleil (par ex., brûlant, érythème, exsudation, vésicules, cloques, œdème) impliquant des zones exposées à la lumière (généralement le visage, la zone «V» du cou, les surfaces d'extenseur des avant-bras dorsa des mains), peut être associé à l'utilisation de quinolones après le soleil ou exposition à la lumière UV. Par conséquent, exposition excessive à ces sources de lumière doit être évité. Le traitement médicamenteux doit être interrompu en cas de photosensibilité / phototoxicité se produit (voir RÉACTIONS INDÉSIRABLES/Événements indésirables post-commercialisation).
Comme pour les autres quinolones, l'ofloxacine doit être utilisée avec prudence chez tout patient avec un trouble du SNC connu ou suspecté qui peut prédisposer à des convulsions ou à une baisse le seuil de saisie (par ex., artériosclérose cérébrale sévère, épilepsie) ou en présence d'autres facteurs de risque qui peuvent prédisposer à des saisies ou à une baisse le seuil de saisie (par ex., certaines thérapies médicamenteuses, dysfonction rénale). (Voir AVERTISSEMENTS et INTERACTIONS DE DROGUES.)
Une interaction possible entre les hypoglycémiants oraux (par ex., glyburide / glibenclamide) ou avec de l'insuline et des agents antimicrobiens fluoroquinolones ont été rapportés entraînant une potentialisation de l'action hypoglycémique de ces médicaments. Le mécanisme car cette interaction n'est pas connue. Si une réaction hypoglycémique se produit chez un patient traité avec de l'ofloxacine, arrêter immédiatement l'ofloxacine et consulter un médecin. (Voir INTERACTIONS DE DROGUES et RÉACTIONS INDÉSIRABLES.)
Comme pour tout médicament puissant, évaluation périodique des fonctions du système d'organes, y compris rénal, hépatique et hématopoïétique, est conseillé pendant un traitement prolongé. (Voir AVERTISSEMENTS et RÉACTIONS INDÉSIRABLES.)
Torsades de pointes
Certaines quinolones, dont la ofloxacine, ont été associées à un allongement de l'intervalle QT sur l'électrocardiogramme et les cas peu fréquents d'arythmie. De rares cas de torsades de pointes ont été spontanément signalés lors de la post-commercialisation surveillance chez les patients recevant des quinolones, y compris de l'ofloxacine. Ofloxacine doit être évité chez les patients présentant une prolongation connue de l'intervalle QT, les patients avec hypokaliémie non corrigée et patients recevant la classe IA (quinidine, procaïnamide) ou agents antiarythmiques de classe III (amiodarone, sotalol).
Informations pour les patients
Les patients doivent être informés
- contacter leur professionnel de la santé s'ils ressentent de la douleur, un gonflement ou inflammation d'un tendon, ou faiblesse ou incapacité à utiliser l'une de leurs articulations; se reposer et s'abstenir de faire de l'exercice; et interrompre le traitement par FLOXIN® (ofloxacine). Le le risque de troubles tendineux sévères avec les fluoroquinolones est plus élevé chez les patients plus âgés généralement plus de 60 ans, chez les patients prenant des corticostéroïdes, et chez les patients atteints de transplantation rénale, cardiaque ou pulmonaire;
- que des fluoroquinolones comme FLOXIN® (ofloxacine) peuvent provoquer une aggravation de la myasthénie les symptômes du gravis, y compris la faiblesse musculaire et les problèmes respiratoires. Les patients devrait appeler immédiatement leur professionnel de la santé si vous avez une aggravation faiblesse musculaire ou problèmes respiratoires;
- que les médicaments antibactériens, y compris les comprimés FLOXIN® (comprimés d'ofloxacine) ne doit être utilisé que pour traiter les infections bactériennes. Ils ne traitent pas le virus infections (par ex., le rhume). Lorsque FLOXIN® (comprimés d'ofloxacine) Comprimés sont prescrits pour traiter une infection bactérienne, les patients doivent être informés de cela bien qu'il soit courant de se sentir mieux au début du traitement, le médicament doit être pris exactement comme indiqué. Sauter des doses ou ne pas terminer le le traitement complet peut (1) diminuer l'efficacité de l'immédiat le traitement et (2) augmenter la probabilité que les bactéries développent une résistance et ne sera pas traitable par les comprimés FLOXIN® (comprimés d'ofloxacine) ou autres médicaments antibactériens à l'avenir.
- que des neuropathies périphériques ont été associées à l'utilisation de l'ofloxacine. Si symptômes de neuropathie périphérique, y compris douleur, brûlure, picotements, engourdissement et / ou une faiblesse se développe, ils doivent interrompre le traitement et contacter leur médecins;
- boire généreusement des fluides ;
- que les suppléments minéraux, vitamines avec du fer ou des minéraux, calcium, aluminium- ou des antiacides à base de magnésium, du sucralfate ou du Videx® (didanosine) devraient ne pas être pris dans la période de deux heures avant ou dans la période de deux heures après la prise d'ofloxacine (voir INTERACTIONS DE DROGUES);
- que l'ofloxacine peut être prise sans égard aux repas;
- cette ofloxacine peut provoquer des effets indésirables neurologiques (par ex., étourdissements, vertiges) et que les patients doivent savoir comment ils réagissent à l'ofloxacine avant de fonctionner une automobile ou une machine ou se livrer à des activités nécessitant une vigilance mentale et coordination (voir AVERTISSEMENTS et RÉACTIONS INDÉSIRABLES);
- cette ofloxacine peut être associée à des réactions d'hypersensibilité, même suivantes la première dose, pour arrêter le médicament au premier signe d'une éruption cutanée, urticaire ou autres réactions cutanées, rythme cardiaque rapide, difficulté à avaler ou respirer, tout gonflement suggérant un œdème de Quincke (par ex., gonflement des lèvres, langue, visage; oppression de la gorge, enrouement) ou tout autre symptôme de une réaction allergique (voir AVERTISSEMENTS et RÉACTIONS INDÉSIRABLES);
- que la photosensibilité / phototoxicité a été rapportée chez des patients recevant antibiotiques quinolones. Les patients doivent minimiser ou éviter l'exposition au naturel ou lumière du soleil artificielle (lits de bronzage ou traitement UVA / B) lors de la prise de quinolones. Si les patients doivent être à l'extérieur lors de l'utilisation de quinolones, ils doivent porter des vêtements amples des vêtements qui protègent la peau contre l'exposition au soleil et discutent d'autres protections solaires mesure avec leur médecin. Si une réaction semblable à un coup de soleil ou une éruption cutanée survient, les patients doivent contacter leur médecin;
- que s'ils sont diabétiques et sont traités avec de l'insuline ou une voie orale médicament hypoglycémique, pour arrêter immédiatement l'ofloxacine si elle est hypoglycémique la réaction se produit et consultez un médecin (voir PRÉCAUTIONS: Général et INTERACTIONS DE DROGUES);
- que des convulsions ont été rapportées chez des patients prenant des quinolones, y compris l'ofloxacine et d'aviser leur médecin avant de prendre ce médicament s'il y en a est une histoire de cette condition;
- cette diarrhée est un problème courant causé par des antibiotiques qui se terminent généralement lorsque l'antibiotique est arrêté. Parfois après avoir commencé le traitement avec antibiotiques, les patients peuvent développer des selles aqueuses et sanglantes (avec ou sans crampes d'estomac et fièvre) même jusqu'à deux mois ou plus après l'avoir fait pris la dernière dose de l'antibiotique. Si cela se produit, les patients doivent contacter leur médecin dès que possible ;
- informer leur médecin de tout antécédent personnel ou familial de prolongation de la QTc ou des conditions proarythmiques telles que l'hypokaliémie, la bradycardie ou le myocarde récent ischémie; s'ils prennent une classe IA (quinidine, procaïnamide) ou classe III (amiodarone, sotalol) agents antiarythmiques. Les patients doivent en informer leur les médecins s'ils présentent des symptômes de prolongation de l'intervalle QTc, y compris palpitations cardiaques prolongées ou perte de conscience.
Cancérogenèse, mutagenèse, altération de la fertilité
Études à long terme pour déterminer le potentiel cancérogène de l'ofloxacine pas été menée.
L'ofloxacine n'était pas mutagène dans le test bactérien d'Ames in vitro et test cytogénétique in vivo, échange de chromatides sœurs (jambon chinois et lignes de cellules humaines), réparation d'ADN imprévue (UDS) à l'aide de fibroblastes humains, tests létaux dominants ou test de micronoyaux de souris. L'ofloxacine était positive dans l'UDS tester à l'aide d'hépatocytes de rat et de dosage du lymphome de souris.
Grossesse
Effets tératogènes - Catégorie de grossesse C
Il n'a pas été démontré que l'ofloxacine présente des effets tératogènes à des doses orales jusqu'à 810 mg / kg / jour (11 fois la dose humaine maximale recommandée en fonction en mg / m² ou 50 fois à base de mg / kg) et 160 mg / kg / jour (4 fois le recommandé dose humaine maximale basée sur mg / m² ou 10 fois sur la base de mg / kg) lorsqu'elle est administrée aux rates et lapines gravides, respectivement. Études supplémentaires chez le rat avec doses orales jusqu'à 360 mg / kg / jour (5 fois la dose humaine maximale recommandée en fonction en mg / m² ou 23 fois sur la base de mg / kg) n'a démontré aucun effet indésirable sur développement fœtal tardif, travail, accouchement, lactation, viabilité néonatale ou croissance du nouveau-né. Doses équivalentes à 50 et 10 fois le maximum recommandé la dose humaine d'ofloxacine (sur la base de mg / kg) était fétotoxique (c.-à-d., diminution du fœtus poids corporel et mortalité fœtale accrue) chez le rat et le lapin, respectivement. Des variations mineures du squelette ont été rapportées chez des rats recevant des doses de 810 mg / kg / jour qui est plus de 10 fois supérieure à la dose humaine maximale recommandée sur mg / m².
Il n'y a cependant pas d'études adéquates et bien contrôlées chez la femme enceinte. L'ofloxacine ne doit être utilisée pendant la grossesse que si le bénéfice potentiel le justifie le risque potentiel pour le fœtus. (Voir AVERTISSEMENTS.)
Mères infirmières
Chez les femelles allaitantes, une dose orale unique de 200 mg de de loxacine a entraîné des concentrations de l'ofloxacine dans le lait qui étaient similaires à ceux trouvés dans le plasma. À cause de le potentiel d'effets indésirables graves de l'ofloxacine chez les nourrissons allaités , il convient de décider d'interrompre l'allaitement ou d'interrompre le médicament, compte tenu de l'importance du médicament pour la mère. (Voir AVERTISSEMENTS et RÉACTIONS INDÉSIRABLES.)
Utilisation pédiatrique
Sécurité et efficacité chez les patients pédiatriques et les adolescents de moins de l'âge de 18 ans n'ont pas été établis. L'ofloxacine provoque une arthropathie (arthrose) et ostéochondrose chez les animaux juvéniles de plusieurs espèces. (Voir AVERTISSEMENTS.)
Utilisation gériatrique
Les patients gériatriques courent un risque accru de développer des troubles tendineux sévères y compris la rupture du tendon lors du traitement avec une fluoroquinolone telle que FLOXIN® (ofloxacine). Ce risque est encore accru chez les patients recevant un corticostéroïde concomitant thérapie. La tendinite ou la rupture du tendon peut impliquer l'Achille, la main, l'épaule ou d'autres sites de tendons et peuvent survenir pendant ou après la fin du traitement; cas survenant jusqu'à plusieurs mois après le traitement par la fluoroquinolone. La prudence est de mise lors de la prescription de FLOXIN® (ofloxacine) aux patients âgés en particulier ceux sous corticostéroïdes. Les patients doivent être informés de ce côté potentiel effet et conseillé d'arrêter FLOXIN® (ofloxacine) et de contacter leur professionnel de la santé en cas de symptômes de tendinite ou de rupture du tendon (voir AVERTISSEMENT EN BOÎTE, AVERTISSEMENTS, et RÉACTIONS INDÉSIRABLES/Événement indésirable post-commercialisation Rapports).
Dans les essais cliniques de phase 2/3 avec l'ofloxacine, 688 patients (14,2%) étaient ≥ 65 ans. Sur ce nombre, 436 patients (9,0%) avaient entre 65 ans et 74 et 252 patients (5,2%) avaient 75 ans ou plus. Il n'y avait aucune différence apparente dans la fréquence ou la gravité des effets indésirables chez les personnes âgées comparée avec des adultes plus jeunes. Les propriétés pharmacocinétiques de l'ofloxacine chez les personnes âgées les sujets sont similaires à ceux des sujets plus jeunes. L'absorption des médicaments semble ne pas être affecté par l'âge. Un ajustement posologique est nécessaire pour les patients âgés insuffisance rénale (taux de clairance de la créatinine ≤ 50 ml / min) due à une réduction clairance de l'ofloxacine. Dans les études comparatives, la fréquence et la gravité de la plupart des événements liés au système nerveux liés à la drogue chez les patients ≥ 65 ans l'étaient comparable pour l'ofloxacine et les médicaments témoins. Les seules différences identifiées étaient une augmentation des rapports d'insomnie (3,9% contre 1,5%) et de maux de tête (4,7% contre 1,8%) avec de l'ofloxacine. Il est important de noter que ces données de sécurité gériatriques sont extraits de 44 études comparatives où les informations sur les effets indésirables à partir de 20 témoins différents (autres antibiotiques ou placebo) ont été regroupés pour comparaison avec de l'ofloxacine. La signification clinique d'une telle comparaison n'est pas claire. (Voir PHARMACOLOGIE CLINIQUE et DOSAGE ET ADMINISTRATION.)
Les patients âgés peuvent être plus sensibles aux effets associés au médicament sur le QT intervalle. Par conséquent, des précautions doivent être prises lors de l'utilisation de l'ofloxacine avec concomitant médicaments pouvant entraîner une prolongation de l'intervalle QT (par ex. Classe IA ou Classe III antiarythmiques) ou chez les patients présentant des facteurs de risque de torsade de pointes (par ex. allongement connu de l'intervalle QT, hypokaliémie non corrigée). (Voir PRÉCAUTIONS: Général: Torsades de pointes)

EFFETS CÔTÉ
Ce qui suit est une compilation des données pour l'ofloxacine sur la base de la clinique expérience des formulations orales et intraveineuses. L'incidence de effets indésirables liés au médicament chez les patients au cours des essais cliniques de phase 2 et 3 était de 11%. Parmi les patients recevant un traitement à doses multiples, 4% ont arrêté l'ofloxacine en raison d'expériences indésirables.
Dans les essais cliniques, les événements suivants étaient considérés comme probablement liés au médicament chez les patients recevant plusieurs doses d'ofloxacine :
nausées 3%, insomnie 3%, maux de tête 1%, étourdissements 1%, diarrhée 1%, vomissements 1% éruption cutanée 1%, prurit 1%, prurit génital externe chez la femme 1%, vaginite 1%, dysgueusie 1%.
Dans les essais cliniques, les événements indésirables les plus fréquemment rapportés, peu importe de relation avec la drogue, étaient:
nausées 10%, maux de tête 9%, insomnie 7%, prurit génital externe chez la femme 6% étourdissements 5%, vaginite 5%, diarrhée 4%, vomissements 4%.
Dans les essais cliniques, les événements suivants, quelle que soit la relation avec le médicament, survenu chez 1 à 3% des patients:
Douleurs et crampes abdominales, douleurs thoraciques, diminution de l'appétit, sécheresse de la bouche, dysgueusie , fatigue, flatulences, détresse gastro-intestinale, nervosité, pharyngite, prurit, fièvre, éruption cutanée, troubles du sommeil, somnolence, douleur thoracique, écoulement vaginal, visuel troubles et constipation.
Événements supplémentaires, survenus dans des essais cliniques à un taux inférieur à 1% quelle que soit la relation avec la drogue, étaient:
Corps dans son ensemble : asthénie, frissons, malaise, douleur aux extrémités, douleur, épistaxis
Système cardiovasculaire: arrêt cardiaque, œdème, hypertension, hypotension , palpitations, vasodilatation
Système gastro-intestinal: Dyspepsie
Système génital / reproducteur: brûlure, irritation, douleur et éruption cutanée du organes génitaux féminins; dysménorrhée; ménorragie; métrorragie
Système musculo-squelettique: Arthralgie, myalgie
Système nerveux: convulsions, anxiété, changement cognitif, dépression, rêve anomalie, euphorie, hallucinations, paresthésie, syncope, vertige, tremblements confusion
Nutritionnel / Métabolique: soif, perte de poids
Système respiratoire: arrêt respiratoire, toux, rhinorrhée
Peau / hypersensibilité: œdème de Quincke, diaphorèse, urticaire, vascularite
Sens spéciaux: diminution de l'acuité auditive, acouphènes, photophobie
Système urinaire: dysurie, fréquence urinaire, rétention urinaire
Les anomalies biologiques suivantes sont apparues chez ≥ 1,0% des patients recevant doses multiples d'ofloxacine. On ne sait pas si ces anomalies l'ont été causée par le médicament ou les conditions sous-jacentes traitées.
Hématopoïétique: anémie, leucopénie, leucocytose, neutropénie, neutrophilie, augmentation des formes des bandes, lymphocytopénie, éosinophilie, lymphocytose, thrombocytopénie , thrombocytose, ESR élevé
Hépatique: élevé: phosphatase alcaline, AST (SGOT), ALT (SGPT) Sérum chimie: hyperglycémie, hypoglycémie, créatinine élevée, BUN élevé urinaire: glucosurie, protéinurie, alcalinurie, hyposthénurie, hématurie, pyurie
Événements indésirables post-commercialisation
Événements indésirables supplémentaires, quelle que soit la relation avec le médicament, signalés expérience marketing mondiale avec les quinolones, y compris l'ofloxacine :
Clinique
Système cardiovasculaire: thrombose cérébrale, œdème pulmonaire, tachycardie , hypotension / choc, syncope, torsades de pointes
Endocrinien / Métabolique: hyper- ou hypoglycémie, en particulier chez les patients diabétiques sous forme d'insuline ou d'agents hypoglycémiques oraux (voir PRÉCAUTIONS: Général et INTERACTIONS DE DROGUES.)
Système gastro-intestinal: dysfonctionnement hépatique, y compris: nécrose hépatique , jaunisse (cholestatique ou hépatocellulaire), hépatite; perforation intestinale ; insuffisance hépatique (y compris les cas mortels); colite pseudomembraneuse (le début des symptômes de colite pseudomembraneuse peuvent survenir pendant ou après l'antimicrobien traitement), hémorragie gastro-intestinale; hoquet, muqueuse orale douloureuse, pyrose (voir AVERTISSEMENTS.)
Système génital / reproducteur: candidose vaginale
Hématopoïétique: anémie, y compris hémolytique et aplastique; hémorragie, pancytopénie, agranulocytose, leucopénie, dépression réversible de la moelle osseuse thrombocytopénie, purpura thrombotique thrombocytopénique, pétéchies, ecchymose / bruissement (Voir AVERTISSEMENTS.)
Musculo-squelettique: tendinite / rupture; faiblesse; rhabdomyolyse (voir AVERTISSEMENTS.)
Système nerveux: cauchemars; pensées ou actes suicidaires, désorientation , réactions psychotiques, paranoïa; phobie, agitation, agitation, agressivité / hostilité, réaction maniaque, labilité émotionnelle; neuropathie périphérique, ataxie, incoordination; exacerbation de: myasthénie grave et troubles extrapyramidaux; dysphasie, étourdissements (voir AVERTISSEMENTS et PRÉCAUTIONS.)
Système respiratoire: dyspnée, bronchospasme, pneumonite allergique, stridor (Voir AVERTISSEMENTS.)
Peau / hypersensibilité: réactions / choc anaphylactiques (-toid); purpura, maladie sérique, érythème polymorphe / syndrome de Stevens-Johnson, érythème noueux , dermatite exfoliatrice, hyperpigmentation, nécrolyse épidermique toxique, conjonctivite , réaction de photosensibilité / phototoxicité, éruption vésiculobulleuse (voir AVERTISSEMENTS et PRÉCAUTIONS.)
Sens spéciaux: diplopie, nystagmus, vision trouble, perturbations de: goût, odeur, audition et équilibre, généralement réversibles après l'arrêt
Système urinaire: anurie, polyurie, calculs rénaux, insuffisance rénale, interstitielle néphrite, hématurie (voir AVERTISSEMENTS et PRÉCAUTIONS.)
Laboratoire
Hématopoïétique: prolongation du temps de prothrombine
Chimie sérique: acidose, élévation de: triglycérides sériques, sérum cholestérol, potassium sérique, tests de la fonction hépatique, y compris: GGTP, LDH, bilirubine
Urinaire: albuminurie, candidurie
Dans les essais cliniques utilisant un traitement à doses multiples, des anomalies ophtalmologiques y compris des cataractes et de multiples opacités lenticulaires ponctuées, ont été notées chez les patients sous traitement avec d'autres quinolones. La relation de les médicaments à ces événements ne sont pas actuellement établis.
LA CRYSTALLURIE et la CYLINDRURIE ONT ÉTÉ SIGNALÉES avec d'autres quinolones.
INTERACTIONS DE DROGUES
Antiacides, Sucralfate, Cations métalliques, Multivitamines
Les quinolones forment des chélates avec de la terre alcaline et des cations métalliques de transition. Administration de quinolones avec des antiacides contenant du calcium, du magnésium ou aluminium, avec sucralfate, avec des cations divalents ou trivalents tels que le fer, ou avec des multivitamines contenant du zinc ou avec Videx® (didanosine) peut considérablement interférer avec l'absorption des quinolones entraînant des niveaux systémiques considérablement inférieur à ce que vous souhaitez. Ces agents ne doivent pas être pris dans le délai de deux heures avant ou dans la période de deux heures après l'administration d'ofloxacine. (Voir DOSAGE ET ADMINISTRATION.)
Caféine
Aucune interaction entre l'ofloxacine et la caféine n'a été détectée.
Cimétidine
La cimétidine a démontré une interférence avec l'élimination de certaines quinolones. Cette interférence a entraîné une augmentation significative de la demi-vie et de l'ASC de quelques quinolones. Le potentiel d'interaction entre l'ofloxacine et la cimétidine n'a pas été étudié.
Cyclosporine
Des taux sériques élevés de cyclosporine ont été rapportés avec une utilisation concomitante de cyclosporine avec quelques autres quinolones. Le potentiel d'interaction entre l'ofloxacine et la cyclosporine n'ont pas été étudiées.
Médicaments métabolisés par les enzymes du cytochrome P450
La plupart des médicaments antimicrobiens quinolones inhibent l'activité enzymatique du cytochrome P450. Cela peut entraîner une demi-vie prolongée pour certains médicaments qui sont également métabolisés par ce système (par ex., cyclosporine, théophylline / méthylxanthines, warfarine) en cas de co-administration avec des quinolones. L'étendue de cette inhibition varie entre les deux différentes quinolones. (Voir autres interactions médicamenteuses.)
Anti-inflammatoires non stéroïdiens
L'administration concomitante d'un anti-inflammatoire non stéroïdien avec une quinolone, y compris l'ofloxacine, peut augmenter le risque de stimulation du SNC et convulsions convulsives. (Voir AVERTISSEMENTS et PRÉCAUTIONS: Général.)
Probénécide
L'utilisation concomitante de probénécide avec certaines autres quinolones a été rapportée affecter la sécrétion tubulaire rénale. L'effet du probénécide sur l'élimination de l'ofloxacine n'a pas été étudié.
Théophylline
Les taux de théophylline à l'état d'équilibre peuvent augmenter lorsque l'ofloxacine et la théophylline sont administrés simultanément. Comme pour les autres quinolones, administration concomitante de l'ofloxacine peut prolonger la demi-vie de la théophylline, élever la théophylline sérique et augmenter le risque d'effets indésirables liés à la théophylline. Théophylline les niveaux doivent être étroitement surveillés et les ajustements posologiques de la théophylline doivent être effectués le cas échéant, lorsque l'ofloxacine est co-administrée. Effets indésirables (y compris convulsions) peuvent survenir avec ou sans élévation du taux de théophylline sérique. (Voir AVERTISSEMENTS et PRÉCAUTIONS: Général.)
Warfarine
Certaines quinolones auraient amélioré les effets de l'anticoagulant oral warfarine ou ses dérivés. Par conséquent, si un antimicrobien quinolone est administré en concomitance avec la warfarine ou ses dérivés, le temps de prothrombine ou autre un test de coagulation approprié doit être étroitement surveillé.
Agents antidiabétiques (par ex., insuline, glyburide / glibenclamide)
Depuis les perturbations de la glycémie, y compris l'hyperglycémie et l'hypoglycémie ont été rapportés chez des patients traités simultanément avec des quinolones et un antidiabétique agent, une surveillance attentive de la glycémie est recommandée lorsque ces agents sont utilisés en concomitance. (Voir PRÉCAUTIONS: Général et INFORMATIONS PATIENTES.)
Interaction avec les tests de laboratoire ou de diagnostic
Certaines quinolones, y compris l'ofloxacine, peuvent produire un dépistage urinaire faussement positif résultats pour les opiacés utilisant des kits d'immunodosage disponibles dans le commerce. Confirmation des écrans opiacés positifs par des méthodes plus spécifiques peuvent être nécessaires.

Effets tératogènes - Catégorie de grossesse C
Il n'a pas été démontré que l'ofloxacine présente des effets tératogènes à des doses orales jusqu'à 810 mg / kg / jour (11 fois la dose humaine maximale recommandée en fonction en mg / m² ou 50 fois à base de mg / kg) et 160 mg / kg / jour (4 fois le recommandé dose humaine maximale basée sur mg / m² ou 10 fois sur la base de mg / kg) lorsqu'elle est administrée aux rates et lapines gravides, respectivement. Études supplémentaires chez le rat avec doses orales jusqu'à 360 mg / kg / jour (5 fois la dose humaine maximale recommandée en fonction en mg / m² ou 23 fois sur la base de mg / kg) n'a démontré aucun effet indésirable sur développement fœtal tardif, travail, accouchement, lactation, viabilité néonatale ou croissance du nouveau-né. Doses équivalentes à 50 et 10 fois le maximum recommandé la dose humaine d'ofloxacine (sur la base de mg / kg) était fétotoxique (c.-à-d., diminution du fœtus poids corporel et mortalité fœtale accrue) chez le rat et le lapin, respectivement. Des variations mineures du squelette ont été rapportées chez des rats recevant des doses de 810 mg / kg / jour qui est plus de 10 fois supérieure à la dose humaine maximale recommandée sur mg / m².
Il n'y a cependant pas d'études adéquates et bien contrôlées chez la femme enceinte. L'ofloxacine ne doit être utilisée pendant la grossesse que si le bénéfice potentiel le justifie le risque potentiel pour le fœtus. (Voir AVERTISSEMENTS.)

Ce qui suit est une compilation des données pour l'ofloxacine sur la base de la clinique expérience des formulations orales et intraveineuses. L'incidence de effets indésirables liés au médicament chez les patients au cours des essais cliniques de phase 2 et 3 était de 11%. Parmi les patients recevant un traitement à doses multiples, 4% ont arrêté l'ofloxacine en raison d'expériences indésirables.
Dans les essais cliniques, les événements suivants étaient considérés comme probablement liés au médicament chez les patients recevant plusieurs doses d'ofloxacine :
nausées 3%, insomnie 3%, maux de tête 1%, étourdissements 1%, diarrhée 1%, vomissements 1% éruption cutanée 1%, prurit 1%, prurit génital externe chez la femme 1%, vaginite 1%, dysgueusie 1%.
Dans les essais cliniques, les événements indésirables les plus fréquemment rapportés, peu importe de relation avec la drogue, étaient:
nausées 10%, maux de tête 9%, insomnie 7%, prurit génital externe chez la femme 6% étourdissements 5%, vaginite 5%, diarrhée 4%, vomissements 4%.
Dans les essais cliniques, les événements suivants, quelle que soit la relation avec le médicament, survenu chez 1 à 3% des patients:
Douleurs et crampes abdominales, douleurs thoraciques, diminution de l'appétit, sécheresse de la bouche, dysgueusie , fatigue, flatulences, détresse gastro-intestinale, nervosité, pharyngite, prurit, fièvre, éruption cutanée, troubles du sommeil, somnolence, douleur thoracique, écoulement vaginal, visuel troubles et constipation.
Événements supplémentaires, survenus dans des essais cliniques à un taux inférieur à 1% quelle que soit la relation avec la drogue, étaient:
Corps dans son ensemble : asthénie, frissons, malaise, douleur aux extrémités, douleur, épistaxis
Système cardiovasculaire: arrêt cardiaque, œdème, hypertension, hypotension , palpitations, vasodilatation
Système gastro-intestinal: Dyspepsie
Système génital / reproducteur: brûlure, irritation, douleur et éruption cutanée du organes génitaux féminins; dysménorrhée; ménorragie; métrorragie
Système musculo-squelettique: Arthralgie, myalgie
Système nerveux: convulsions, anxiété, changement cognitif, dépression, rêve anomalie, euphorie, hallucinations, paresthésie, syncope, vertige, tremblements confusion
Nutritionnel / Métabolique: soif, perte de poids
Système respiratoire: arrêt respiratoire, toux, rhinorrhée
Peau / hypersensibilité: œdème de Quincke, diaphorèse, urticaire, vascularite
Sens spéciaux: diminution de l'acuité auditive, acouphènes, photophobie
Système urinaire: dysurie, fréquence urinaire, rétention urinaire
Les anomalies biologiques suivantes sont apparues chez ≥ 1,0% des patients recevant doses multiples d'ofloxacine. On ne sait pas si ces anomalies l'ont été causée par le médicament ou les conditions sous-jacentes traitées.
Hématopoïétique: anémie, leucopénie, leucocytose, neutropénie, neutrophilie, augmentation des formes des bandes, lymphocytopénie, éosinophilie, lymphocytose, thrombocytopénie , thrombocytose, ESR élevé
Hépatique: élevé: phosphatase alcaline, AST (SGOT), ALT (SGPT) Sérum chimie: hyperglycémie, hypoglycémie, créatinine élevée, BUN élevé urinaire: glucosurie, protéinurie, alcalinurie, hyposthénurie, hématurie, pyurie
Événements indésirables post-commercialisation
Événements indésirables supplémentaires, quelle que soit la relation avec le médicament, signalés expérience marketing mondiale avec les quinolones, y compris l'ofloxacine :
Clinique
Système cardiovasculaire: thrombose cérébrale, œdème pulmonaire, tachycardie , hypotension / choc, syncope, torsades de pointes
Endocrinien / Métabolique: hyper- ou hypoglycémie, en particulier chez les patients diabétiques sous forme d'insuline ou d'agents hypoglycémiques oraux (voir PRÉCAUTIONS: Général et INTERACTIONS DE DROGUES.)
Système gastro-intestinal: dysfonctionnement hépatique, y compris: nécrose hépatique , jaunisse (cholestatique ou hépatocellulaire), hépatite; perforation intestinale ; insuffisance hépatique (y compris les cas mortels); colite pseudomembraneuse (le début des symptômes de colite pseudomembraneuse peuvent survenir pendant ou après l'antimicrobien traitement), hémorragie gastro-intestinale; hoquet, muqueuse orale douloureuse, pyrose (voir AVERTISSEMENTS.)
Système génital / reproducteur: candidose vaginale
Hématopoïétique: anémie, y compris hémolytique et aplastique; hémorragie, pancytopénie, agranulocytose, leucopénie, dépression réversible de la moelle osseuse thrombocytopénie, purpura thrombotique thrombocytopénique, pétéchies, ecchymose / bruissement (Voir AVERTISSEMENTS.)
Musculo-squelettique: tendinite / rupture; faiblesse; rhabdomyolyse (voir AVERTISSEMENTS.)
Système nerveux: cauchemars; pensées ou actes suicidaires, désorientation , réactions psychotiques, paranoïa; phobie, agitation, agitation, agressivité / hostilité, réaction maniaque, labilité émotionnelle; neuropathie périphérique, ataxie, incoordination; exacerbation de: myasthénie grave et troubles extrapyramidaux; dysphasie, étourdissements (voir AVERTISSEMENTS et PRÉCAUTIONS.)
Système respiratoire: dyspnée, bronchospasme, pneumonite allergique, stridor (Voir AVERTISSEMENTS.)
Peau / hypersensibilité: réactions / choc anaphylactiques (-toid); purpura, maladie sérique, érythème polymorphe / syndrome de Stevens-Johnson, érythème noueux , dermatite exfoliatrice, hyperpigmentation, nécrolyse épidermique toxique, conjonctivite , réaction de photosensibilité / phototoxicité, éruption vésiculobulleuse (voir AVERTISSEMENTS et PRÉCAUTIONS.)
Sens spéciaux: diplopie, nystagmus, vision trouble, perturbations de: goût, odeur, audition et équilibre, généralement réversibles après l'arrêt
Système urinaire: anurie, polyurie, calculs rénaux, insuffisance rénale, interstitielle néphrite, hématurie (voir AVERTISSEMENTS et PRÉCAUTIONS.)
Laboratoire
Hématopoïétique: prolongation du temps de prothrombine
Chimie sérique: acidose, élévation de: triglycérides sériques, sérum cholestérol, potassium sérique, tests de la fonction hépatique, y compris: GGTP, LDH, bilirubine
Urinaire: albuminurie, candidurie
Dans les essais cliniques utilisant un traitement à doses multiples, des anomalies ophtalmologiques y compris des cataractes et de multiples opacités lenticulaires ponctuées, ont été notées chez les patients sous traitement avec d'autres quinolones. La relation de les médicaments à ces événements ne sont pas actuellement établis.
LA CRYSTALLURIE et la CYLINDRURIE ONT ÉTÉ SIGNALÉES avec d'autres quinolones.

Les informations sur le surdosage avec l'ofloxacine sont limitées. Un incident accidentel un surdosage a été signalé. Dans ce cas, une femelle adulte a reçu 3 grammes d'ofloxacine par voie intraveineuse sur 45 minutes. Un échantillon de sang a obtenu 15 minutes après la fin de la perfusion a révélé un taux d'ofloxacine de 39,3 μg / ml En 7 h, le niveau était tombé à 16,2 μg / ml et de 24 h à 2,7 μg / ml Pendant la perfusion, le patient a développé une somnolence, des nausées, des étourdissements, chauds et bouffées de chaleur, gonflement subjectif du visage et engourdissement, insultes à la parole, et désorientation légère à modérée. Toutes les plaintes, à l'exception des étourdissements, se sont apaisées dans les 1 h après l'arrêt de la perfusion. Les étourdissements, les plus gênants en position debout, résolu en environ 9 h. Des tests de laboratoire auraient été effectués n'a révélé aucun changement cliniquement significatif des paramètres de routine chez ce patient.
En cas de surdosage aigu, l'estomac doit être vidé. Le patient doit être observée et une hydratation appropriée doit être maintenue. L'ofloxacine n'est pas efficace retiré par hémodialyse ou dialyse péritonéale.
However, we will provide data for each active ingredient


